- Update zum Screening auf Präeklampsie
Die Präeklampsie ist eine gefürchtete Schwangerschaftskomplikation ohne Therapieoption ausser der Entbindung. Entsprechend sind Screening und präventive Massnahmen von grosser Bedeutung. Bekannt sind das Screening nach anamnestischen Risikofaktoren sowie das kombinierte Screening der FMF London. Zunehmend wird das Screening im ersten Trimenon und die Verordnung von Aspirin bei Risikoschwangerschaften in die Schwangerenvorsorge integriert, jedoch bleibt die Präeklampsie am Termin ein ungelöstes Problem. Neue Studien zeigen, dass ein Screening in der 35-36. SSW mit gezielter Einleitung ab 37. SSW das Risiko der Termin-Präeklampsie signifikant reduzieren könnte.
Pre-eclampsia is a dreaded pregnancy complication with no treatment options other than delivery. Accordingly, screening and preventive measures are of great importance. Screening for anamnestic risk factors and combined screening of the FMF London are well known. Increasingly, screening in the first trimester and the prescription of aspirin for high-risk pregnancies are being integrated into antenatal care, but pre-eclampsia at term remains an unresolved problem. New studies show that screening at 35-36 weeks’ gestation with targeted induction from 37 weeks’ gestation could significantly reduce the risk of pre-eclampsia at term.
Key Words: Pre-eclampsia screening, prevention, therapy
Einleitung
Weltweit liegt die Inzidenz der Präeklampsie (PE) bei 2-8% aller Schwangerschaften. Ca. 1% aller Schwangerschaften werden wegen einer frühgeburtlichen PE (preterm PE, pPE) vor der 37 Schwangerschaftswoche (SSW) entbunden (1). Nebst der unmittelbaren Gefährdung von Mutter und Kind, haben Frauen nach einer PE ein zwei- bis fünffach erhöhtes Risiko kardiovaskuläre Langzeitfolgen zu entwickeln. Fetal ist das Risiko von intrauterinen Wachstumsretardierung, Frühgeburt und intrauterinen Fruchttodes erhöht; Im späteren Leben hat das Kind ein höheres Risiko kardiovaskuläre Langzeitfolgen oder ein metabolisches Syndrom zu entwickeln (2). PE definiert sich als Hypertonie (systolischer Blutdruck ≥140mmHg und/oder diastolischer Blutdruck ≥90mmHg nach 20 SSW) kombiniert mit mindestens einem der folgenden Kriterien: Proteinurie, maternale Organdysfunktion (Niere, Leber, Lunge, hämatologische oder neurologische Beteiligung) und/oder fetale Wachstumsrestriktion (1). Da es keine Therapie für die PE gibt und nur die Entbindung die akute Problematik für Mutter und Kind löst, sind präventive Strategien essenziell. Die Prävention mit niedrig dosiertem Aspirin (low dose aspirin, LDA), begonnen vor der 16 SSW ist die einzig effektive Massnahme zur Verhinderung der pPE (3). Wichtig ist das Screening auf pPE im ersten Trimenon mittels kombiniertem Ersttrimesterscreening. Während die schwerste Morbidität mit der pPE assoziiert ist, sind deutlich mehr Schwangerschaften von einer Termin-PE (tPE) betroffen. Präventive Massnahmen mit LDA oder auch mit Statinen sind gemäss heutiger Studienlage ineffektiv, so dass mittels rechtzeitiger Entbindung die tPE zu verhindern ist (3, 4).
Ersttrimester-Screeningmethoden im Vergleich
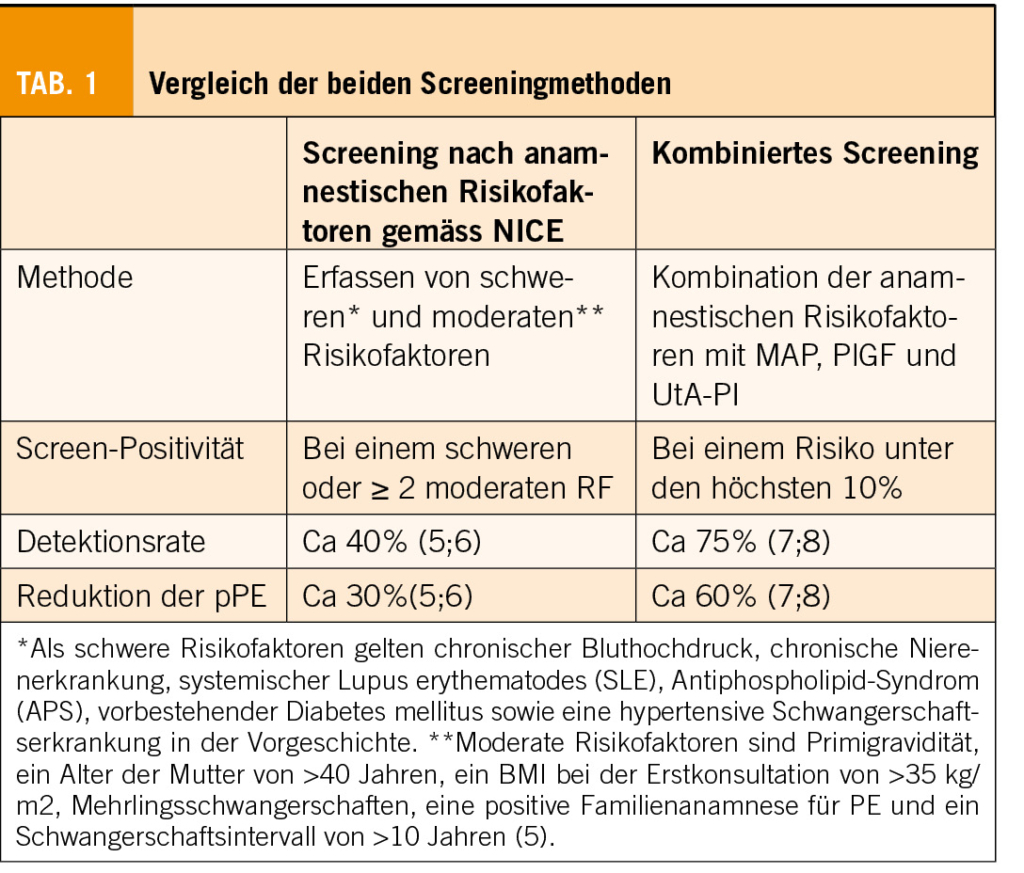
Beim Screening nach NICE (National Institute of clinical excellence) und ACOG (American College of Obstetrics and Gynaecology) wird eine Risikoschwangerschaft definiert, wenn mindestens ein schwerer oder mindestens zwei moderate Risikofaktoren (RF) vorliegen (5). Als schwere RF zählen chronischer Bluthochdruck, chronische Nierenerkrankung, systemischer Lupus erythematodes, Antiphospholipid-Syndrom, vorbestehender Diabetes mellitus sowie eine hypertensive Schwangerschaftserkrankung in der Vorgeschichte; Primigravidität, Alter der Mutter >40 Jahren, ein BMI bei der Erstkonsultation >35 kg/m2, Mehrlingsschwangerschaften, eine positive Familienanamnese für PE und ein Schwangerschaftsintervall von >10 Jahren gelten als moderate RF (5;6). Beim kombinierten Screening werden anamnestische Risikofaktoren mit dem mittleren arteriellen Druck (MAP), dem mittleren Pulsatilitätsindex (PI) der Arteria uterinae sowie dem Biomarker placental growth factor (PlGF) zwischen 11+0 und 14+0 SSW kombiniert (7). Tabelle 1 zeigt die Screeningmethoden im Vergleich. Die ASPRE-Studie bewies, dass LDA bei guter Compliance das pPE-Risiko um 62-75% reduziert, wenn LDA vor 16 SSW und in einer Dosierung von 150mg eingenommen wird (9). Eine letzte Metaanalyse bestätigt, dass nur diese Art der LDA-Verschreibung, 150mg begonnen vor 16 SSW, das pPE-Risiko senkt (10). Während ACOG und NICE an einem Screening mit anamnestischen RF festhalten, empfehlen die FIGO (International Federation of Gynecology and Obstetrics) und die ISSHP (International Societey for Study of Hypertension in Pregnancy) das kombinierte Ersttrimesterscreening, mit der Option, bei limitierten Ressourcen ein zweizeitiges Screening anzubieten (1;2;8;11). Der Expertenbrief der SGGG empfiehlt weiterhin beide Screeningmethoden (2).
Zur Frage vom Cut-Off
Die ASPRE-Studie benutzte einen Cut-Off von >1:100 um eine Risikoschwangerschaft zu definieren. An diesen halten sich Guidelines und der SGGG-Expertenbrief (2;9). Allgemein akzeptiert ist, dass ein Screeningtest eine Falsch-positiv-Rate (FPR) von 10% nicht überschreiten sollte. Die Detektionsrate (DR) hängt direkt von der FPR ab. In den meisten Studien der FMF London findet sich eine FPR aber eher bei einem Cut-Off von >1:70 (12;13;14). Auch die Daten aus der Schweiz zeigen bisher, dass der Cut-off >1:100 zu einer zu hohen FPR führt. Zudem konnte in einer Berner Studie gezeigt werden, dass nicht mehr pPEs auftreten, wenn man den Cut-off auf 1:70 senkt (16;17). Nach Abschluss der aktuellen IPSISS-Studie, ist anzunehmen, dass der Expertenbrief bezüglich des geltenden Cut-Offs für die Schweiz angepasst wird.
Neuere Screeningmarker
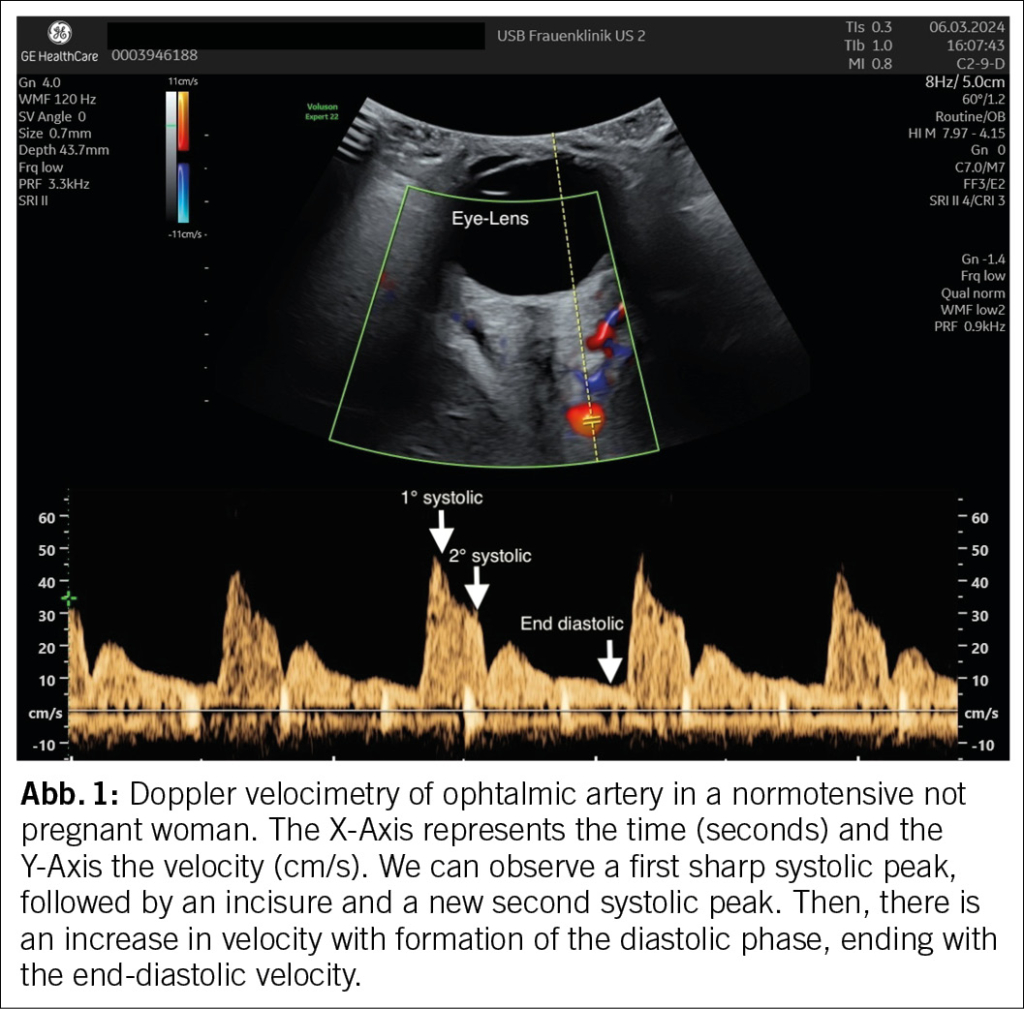
Die A. ophthalmica (Abbildung 1) wird am besten mit einer 7.5 MHz-Linearsonde gedopplert. Das Flussmuster weist zwei systolische Peaks auf. Im zweiten und dritten Trimenon zeigte sich, dass die Ratio dieser beiden PSV (peak systolic velocity, Maximalgeschwindigkeit) ein nützlicher PE-Marker ist (18;19). Kleinere Studien zeigten auch einen prädiktiven Wert in der alleinigen Messung der PSV des zweiten Peaks, dies konnte aber im grösseren Kollektiv nicht bestätigt werden (20). Der Doppler der A. ophthalmica wurde auch im ersten Trimenon untersucht und es wurde fest-gestellt, dass die PSV-Ratio beim Screening auf pPE ein guter prädiktiver Wert ist (21). Die Resultate sind noch von einem grösseren Kollektiv zu bestätigen (19). Während der direkte Zusammenhang zwischen einer gestörten Plazentaimplantation und einem erhöhten Widerstand in den A. uterinae einleuchtet, weist ein verändertes Flussmuster in der A. ophthalmica eher auf eine kardiovaskuläre Grundproblematik hin (22). Das glykosylierte Fibronectin (GlyFn) ist ein anderer vielversprechender Marker, der bei präeklamptischen Patientinnen erhöht ist (23;24). Eine Studie zeigte, dass die Vorhersagekraft für eine PE innerhalb von 2 Wochen nach der GlyFn-Untersuchung ähnlich hoch war wie die von PlGF und dem sFLT-1 / PlGF-Ratio, mit einer Entdeckungsrate von etwa 75 %, bei einer FPR von 42 % (25). Allerdings dürften weder GlyFn noch angiogene Faktoren die Behandlung von Frauen mit chronischem Bluthochdruck verbessern, da ihre Vorhersagekraft für eine überlagernde PE gering sind (25;26).
Risikobewertung bei Zwillingsschwangerschaft
Die Gesamtinzidenz von PE bei Zwillingsschwangerschaften ist mit 9% etwa dreimal so hoch wie bei Einlingsschwangerschaften (27;28). Unklar ist, ob LDA bei Gemini-Schwangerschaften denselben Nutzen in der Prävention der pPE aufweist wie bei Einlingsschwangerschaften. Es gibt Hinweise, dass auch hier der Nutzen Dosis-abhängig ist (28; 29; 30). Wie auch bei Einlingsschwangerschaften erzielt man im Screening bei Zwillingsschwangerschaften die besten Resultate mit der Kombination aus anamnestischen Risikofaktoren, MAP, UtA-PI und PlGF, ohne zusätzlichen Benefit durch die Bestimmung von PAPP-A (pregnancy-associated plasma protein A) (27;28). Die Performance des Screenings ist aber deutlich schlechter: um eine DR von 75% zu erzielen muss die FPR von 40% anstatt 10% akzeptiert werden (28;29). Das PE-Screening von Zwillingsschwangerschaften und der Nutzen von LDA ist individuell mit der Patientin zu diskutieren.
Prävention der PE am Termin
Die DR der PE am Termin (tPE) im kombinierten Ersttrimesterscreening liegt bei nur ca. 50% und die Einnahme von LDA reduziert das Risiko der tPE nicht (31;32;33). Ebenso wie im ersten besteht auch im zweiten und dritten Trimenon die Möglichkeit des kombinierten Screenings auf PE (34;35;36). Die einzige Prävention der tPE bleibt die zeitgerechte Entbindung und wird bei anamnestischen Risiken, mit 38 SSW empfohlen (38;39). Entsprechend besteht heute die Überlegung, dass ein generelles Screening in der Spätschwangerschaft Risiken für eine tPE besser erfasst als ein Screening nach anamnestischen RF und dass mit einer Einleitung ab 37 SSW das Risiko der tPE reduziert werden kann (40,41). Während noch keine randomisierten Studien vorliegen, weisen Ergebnisse aus Sekundäranalysen darauf hin, dass sich mit dieser Strategie bis zu 60% anstatt knapp 40% der tPEs verhindern lassen (40).
Copyright bei Aerzteverlag medinfo AG
Assistenzärztin Gynäkologie und Geburtshilfe
Universitätsspital Basel
Spitalstrasse 21
4031 Basel
valeria.filippi@usb.ch
Oberärztin Gynäkologie und Geburtshilfe
Universitätsspital Basel
Spitalstrasse 21
4031 Basel
Chefärztin für Geburtshilfe und Pränatalmedizin
Universitätsspital Basel
Spitalstrasse 21
4031 Basel
Die Autoren haben keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
◆ Die effizienteste Methode für das PE-Screening ist das kombinierte Ersttrimester-Screening der FMF London.
◆ Neuere erfolgversprechende Marker sind der Doppler der A. ophtalmica und das GlyFn .
◆ Das Screening von Zwillingsschwangerschaften und der Nutzen von LDA müssen individuell besprochen werden.
◆ Statine zeigten keine präventive Wirkung für eine tPE.
◆ Die zeitgerechte Entbindung bleibt die einzige Präventionsmassnahme der tPE. Neuere Daten zeigen, dass ein PE-Screening in der Spätschwangerschaft und eine gezielte Einleitung ab 37 SSW das Risiko der tPE signifikant reduzieren können.
1. Laura A Magee, Mark A. et al. The 2021 International Society for the Study of Hypertension in Pregnancy classification, diagnosis & management recommendations for international practice, Pregnancy Hypertension, Volume 27, 2022, Pages 148-169, ISSN 2210-7789. doi.org/10.1016/j.preghy.2021.09.008
2. Expert Letter No 80 SGGG First trimester screening for preeclampsia
3. Bujold E, Roberge S, Lacasse Y, et al. Prevention of Preeclampsia and Intrauterine Growth Restriction With Aspirin Started in Early Pregnancy: A Meta-Analysis. Obstetrics & Gynecology 116(2 Part 1):p 402-414, August 2010. | DOI: 10.1097/AOG. 0b013e3181e9322a
4. Dobert M, Varouxaki AN, Mu AC, Syngelaki A, et al. Pravastatin Versus Placebo in Pregnancies at High Risk of Term Preeclampsia. Circulation. 2021 Aug 31;144(9): 670-679. doi: 10.1161/CIRCULATIONAHA.121.053963. Epub 2021 Jun 24. PMID: 34162218.
5. NICE Hypertension in pregnancy. 2013
6. ACOG Committee Opinion Nr 743. O+G 2018; 132:e44-52.
7. Wright D, Syngelaki A, Akolekar R, Poon LC, Nicolaides KH. Competing risks model in screening for preeclampsia by maternal characteristics and medical history. Am J Obstet Gynecol. 2015 Jul;213(1):62.e1-62.e10. doi: 10.1016/j.ajog.2015.02.018. Epub 2015 Feb 25. PMID: 25724400.
8. Tan MY, Wright D, Syngelaki A, et al. Comparison of diagnostic accuracy of early screening for pre-eclampsia by NICE guidelines and a method combining maternal factors and biomarkers: results of SPREE. Ultrasound Obstet Gynecol. 2018 Jun;51(6):743-750. doi: 10.1002/uog.19039. Epub 2018 Mar 14. PMID: 29536574.
9. Rolnik DL, Wright D, Poon LCY, et al. ASPRE trial: performance of screening for preterm pre-eclampsia. Ultrasound Obstet Gynecol 2017;50:492-5.
10. Ghesquiere L, Guerby P, Marchant I, et al. Comparing aspirin 75 to 81 mg vs 150 to 162 mg for prevention of preterm preeclampsia: systematic review and metaanalysis. Am J Obstet Gynecol MFM 2023;5:101000.
11. Poon LC, Shennan A, Hyett JA et al. The International Federation of Gynecology and Obstetrics (FIGO) initiative on pre-eclampsia: A pragmatic guide for first-trimester screening and prevention. Int J Gynaecol Obstet. 2019 May;145 Suppl 1(Suppl 1):1-33. doi: 10.1002/ijgo.12802. Erratum in: Int J Gynaecol Obstet. 2019 Sep;146(3):390-391. PMID: 31111484; PMCID: PMC6944283.
12. Akolekar R, Syngelaki A, Poon L, et al. Competing risks model in early screening for preeclampsia by biophysical and biochemical markers. Fetal Diagn Ther. 2013;33(1): 8-15. doi: 10.1159/000341264. Epub 2012 Aug 16. Erratum in: Fetal Diagn Ther. 2013;34(1):43. PMID: 22906914.
13. Tan, M.Y., Syngelaki, A., Poon, L.C., et al. (2018), Screening for pre-eclampsia by maternal factors and biomarkers at 11–13 weeks’ gestation. Ultrasound Obstet Gynecol, 52: 186-195. doi.org/10.1002/uog.19112
14. Poon LC, Nicolaides KH. Early prediction of preeclampsia. Obstet Gynecol Int. 2014; 2014:297397. doi: 10.1155/2014/297397. Epub 2014 Jul 17. PMID: 25136369; PMCID: PMC4127237.
15. Mosimann B, Amylidi-Mohr SK, Surbek D, et al. FIRST TRIMESTER SCREENING FOR PREECLAMPSIA – A SYSTEMATIC REVIEW. Hypertens Pregnancy. 2020 Feb;39 (1):1-11. doi: 10.1080/10641955.2019.1682009. Epub 2019 Oct 31. PMID: 31670986.
16. Trottmann et al. IPSISS: Implementing PE-Screening Fetal Diagn Ther DOI: 10.1159/ 000533201
17. Amylidi-Mohr S, Kubias J, Neumann S, Surbek D, Risch L, Raio L, Mosimann B. Reducing the Risk of Preterm Preeclampsia: Comparison of Two First Trimester Screening and Treatment Strategies in a Single Centre in Switzerland. Geburtshilfe Frauenheilkd. 2021 Jul 15;81(12):1354-1361. doi: 10.1055/a-1332-1437. PMID: 34899048; PMCID: PMC8654509.
18. Sapantzoglou I, Wright A, Gallardo Arozena M, et al. Ophthalmic artery Doppler in combination with other biomarkers in the prediction of pre-eclampsia at 19–23weeks’ gestation. Ultrasound Obstet Gynecol 2021; 57: 75–83.
19. Sarno M, Wright A, Vieira N, et al. Ophthalmic artery Doppler in combination with other biomarkers in prediction of pre-eclampsia at 35–37weeks’ gestation. Ultrasound Obstet Gynecol 2021; 57:600–606.
20. Gurgel Alves JA, Praciano de Sousa PC, Bezerra Maia e Holanda Moura et al. First trimester maternal ophthalmic artery Doppler analysis for prediction of pre-eclampsia. Ultrasound Obstet Gynecol 2014; 44: 411–418.
21. Gana N, Sarno M, Vieira N, Wright A, Charakida M, Nicolaides KH. Ophthalmic artery Doppler at 11-13 weeks’ gestation in prediction of pre-eclampsia. Ultrasound Obstet Gynecol. 2022 Jun;59(6):731-736. doi: 10.1002/uog.24914. PMID: 35642909
22. Kalafat E, Laoreti A, Khalil A, Da Silva Costa F, Thilaganathan B. Ophthalmic artery Doppler for prediction of pre-eclampsia: systematic review and meta-analysis. Ultrasound Obstet Gynecol. 2018 Jun;51(6):731-737. doi: 10.1002/uog.19002. Epub 2018 May 3. PMID: 29330892.
23. Huhn EA, Hoffmann I, Martinez De Tejada B, et al. Maternal serum glycosylated fibronectin as a short-term predictor of preeclampsia: a prospective cohort study. BMC Pregnancy Childbirth. 2020 Feb 24;20(1):128. doi: 10.1186/s12884-020-2809-2. PMID: 32093623; PMCID: PMC7041257.
24. Rasanen J, Quinn MJ, Laurie A, et al. Maternal serum glycosylated fibronectin as a point-of-care biomarker for assessment of preeclampsia. Am J Obstet Gynecol. 2015 Jan;212(1):82.e1-9. doi: 10.1016/j.ajog.2014.07.052. Epub 2014 Jul 31. PMID: 25086276.
25. Sokratous N, Bednorz M, Syngelaki A, Wright A, Nicolaides KH, Kametas NA. Prediction using serum glycosylated fibronectin and angiogenic factors of superimposed pre-eclampsia in women with chronic hypertension. Ultrasound Obstet Gynecol. 2023 Dec;62(6):836-842. doi: 10.1002/uog.27475. PMID: 37675881.
26. Nagalla SR, Janaki V, Vijayalakshmi AR, Chayadevi K, Pratibha D, Rao PV, Sage KM, Nair-Schaef D, Bean E, Roberts CT Jr, Gravett MG. Glycosylated fibronectin point-of-care test for diagnosis of pre-eclampsia in a low-resource setting: a prospective Southeast Asian population study. BJOG 2020; 127: 1687-1694.
27. Benkő, Z. et al. (2021), Prediction of pre-eclampsia in twin pregnancy by maternal factors and biomarkers at 11–13 weeks’ gestation: data from EVENTS trial. Ultrasound Obstet Gynecol, 57: 257-265. https://doi.org/10.1002/uog.23531
28. Francisco C, Gamito M, Reddy M, Rolnik DL. Screening for preeclampsia in twin pregnancies. Best Pract Res Clin Obstet Gynaecol. 2022 Nov;84:55-65. doi: 10.1016/j.bpobgyn.2022.03.008. Epub 2022 Mar 31. PMID: 35450774.
29. Kalafat E, Shirazi A, Thilaganathan B et al.The role of aspirin in prevention of preeclampsia in twin pregnancies: does the dose matter? American Journal of Obstetrics & Gynecology, Volume 223, Issue 3, 457 – 458
30. Bergeron TS, Roberge S, Carpentier C, et al. Prevention of Preeclampsia with Aspirin in Multiple Gestations: A Systematic Review and Meta-analysis. Am J Perinatol. 2016 May;33(6):605-10. doi: 10.1055/s-0035-1570381. Epub 2016 Jan 5. PMID: 26731178.
31. Roberge S, Villa P, Nicolaides K, et al.; Early Administration of Low-Dose Aspirin for the Prevention of Preterm and Term Preeclampsia: A Systematic Review and Meta-Analysis. Fetal Diagn Ther 1 April 2012; 31 (3): 141-146. doi.org/10.1159/000336662
32. Askie, Lisa M et al. Antiplatelet agents for prevention of pre-eclampsia: a meta-analysis of individual patient data. The Lancet, Volume 369, Issue 9575, 1791 – 1798
33. Villa, P., Kajantie, E., Räikkönen, et al. (2013), Aspirin in the prevention of pre-eclampsia in high-risk women: a randomised placebo-controlled PREDO Trial and a meta-analysis of randomised trials. BJOG: An International Journal of Obstetrics & Gynaecology, 120: 64-74. https://doi.org/10.1111/j.1471-0528.2012.03493.x
34. O’Gorman N, Wright D, Syngelaki A, et al. Competing risks model in screening for preeclampsia by maternal factors and biomarkers at 11-13 weeks gestation. Am J Obstet Gynecol. 2016 Jan;214(1):103.e1-103.e12. doi: 10.1016/j.ajog.2015.08.034. Epub 2015 Aug 19. PMID: 26297382.
35. Gallo DM, Wright D, Casanova C, et al. Competing risks model in screening for preeclampsia by maternal factors and biomarkers at 19-24 weeks’ gestation. Am J Obstet Gynecol. 2016 May;214(5):619.e1-619.e17. doi: 10.1016/j.ajog.2015.11.016. Epub 2015 Nov 25. PMID: 26627730.
36. Panaitescu A, Ciobanu A, Syngelaki A, Wright A, Wright D, Nicolaides KH. Screening for pre-eclampsia at 35-37 weeks’ gestation. Ultrasound Obstet Gynecol. 2018 Oct;52(4):501-506. doi: 10.1002/uog.19111. Epub 2018 Aug 27. PMID: 29896778.
37. Dobert M, Varouxaki AN, Mu AC, Syngelaki A, et al. Pravastatin Versus Placebo in Pregnancies at High Risk of Term Preeclampsia. Circulation. 2021 Aug 31;144(9):670-679. doi: 10.1161/CIRCULATIONAHA.121.053963. Epub 2021 Jun 24. PMID: 34162218.
38. Hutcheon JA, Lisonkova S, Magee LA, Von Dadelszen P, Woo HL, Liu S, Joseph KS. Optimal timing of delivery in pregnancies with pre-existing hypertension. BJOG. 2011;118:49–54. doi: 10.1111/j.1471-0528.2010.02754.x
39. Cruz MO, Gao W, Hibbard JU. What is the optimal time for delivery in women with gestational hypertension?. Am J Obstet Gynecol. 2012;207:214.e1–214.e6. doi: 10.1016/j.ajog.2012.06.009
40. Magee LA, Wright D, Syngelaki A, von Dadelszen P, et al. Preeclampsia Prevention by Timed Birth at Term. Hypertension. 2023 May;80(5):969-978. doi: 10.1161/HYPERTENSIONAHA.122.20565. Epub 2023 Apr 10. PMID: 37035913; PMCID: PMC10112937
41. von Dadelszen P, Syngelaki A, Wright A, Akolekar R, Magee LA, Wright D, Nicolaides KH. The implications of the Fetal Medicine Foundation 35- to 36-week preeclampsia prediction competing-risk model on timing of birth. Am J Obstet Gynecol. 2023 Apr;228(4):457.e1-457.e7. doi: 10.1016/j.ajog.2022.09.047. Epub 2022 Oct 4. PMID: 36206987.
info@gynäkologie
- Vol. 14
- Ausgabe 2
- April 2024