- Vitamin-D-Serumkonzentration und Knochengesundheit
Vor 111 Jahren prägte der polnische Biochemiker Kazimierz Funk den Begriff «Vital-Amine» oder kurz «Vitamine» für Nahrungsmittelbestandteile, die für das Leben wichtig sind (1). Diese erhielten Buchstaben in der Reihenfolge ihrer Entdeckung; als viertes Vitamin wurde 1922 von Elmer McCollum das Vitamin D beschrieben, eine Substanz, welche die Rachitis bekämpfen konnte (2). Seit dieser ersten Publikation wird über Vitamin D geforscht und publiziert, es werden Thesen zu Wirkungen erhoben und wieder verworfen, Richtlinien aufgestellt und wieder geändert. Die Zahl der Artikel zu Vitamin D, die in PubMed gelistet sind, ist in den letzten 100 Jahren von einer einzigen Publikation im Jahr 1922 auf über 5500 im Jahr 2022 gestiegen. Im nachfolgenden Artikel wird versucht, aus der Fülle der Informationen einige in der Praxis relevante Punkte herauszugreifen.
111 years ago, the Polish biochemist Kazimierz Funk coined the term «vital amines» or «vitamins» for food components that are important for life (1). These were given letters in the order of their discovery; the fourth vitamin to be described was vitamin D, a substance that could combat rickets, by Elmer McCollum in 1922 (2). Since this first publication, vitamin D has been researched and published, theses on effects have been raised and rejected, guidelines have been established and changed again. The number of articles on vitamin D listed in PubMed has increased over the past 100 years from a single publication in 1922 to over 5500 in 2022. The following article attempts to pick out some points relevant in practice from the wealth of information.
Key Words: Vitamine D, bone health, serum concentration
Wofür brauchen wir Vitamin D?
Unbestritten ist die Rolle des Vitamin D für die Knochengesundheit. Vereinfacht gesagt, fördert Vitamin D, bzw. seine aktive Form, das 1,25-Dihydroxy-Vitamin D (1,25 (OH)2 D) die Kalziumresorption im Darm und erhöht damit den Kalzium-Serumspiegel. Zur Verhinderung einer Hyperkalzämie kommt es zu einer verminderten Ausschüttung von Parathormon (PTH), was die Verschiebung von Kalzium in den Knochen und damit seine Mineralisierung bewirkt. Umgekehrt führt ein zu tiefer 1,25 (OH)2 D-Spiegel über eine verminderte Kalziumresorption zu einem erniedrigten Kalzium-Serumspiegel, dadurch zu einer vermehrten Sekretion von Parathormon und in der Folge zur Mobilisierung von Kalzium aus dem Knochen ins Serum. Die damit erreichte lebenswichtige Stabilität des Kalziumblutspiegels wird über eine Schwächung des Knochens erreicht.
Da die meisten Gewebe Vitamin-D-Rezeptoren aufweisen und damit Vitamin D potentiell auf diese Gewebe wirken kann, wird seit Jahren spekuliert, welche Einflüsse Vitamin D auf andere Erkrankungen haben könnte: Das Spektrum umfasst u.a. Haut- und Muskelerkrankungen, Malignome, Autoimmunerkrankungen, Allergien und Infektionen bis hin zu neuropsychiatrischen Erkrankungen. Obwohl es bei vielen dieser Erkrankungen eine Assoziation zu niedrigen Vitamin-D-Spiegeln gibt, konnte bisher nicht bewiesen werden, dass Vitamin D tatsächlich präventiv wirken kann (3,4).
Wieviel Vitamin D brauchen wir für einen gesunden Knochen?
Da die Kalziumverschiebung aus dem Knochen vorwiegend von PTH gesteuert wird, kann der PTH-Spiegel theoretisch indirekt als Mass für die Knochenmineralisierung dienen. Demnach würde der Knochen umso weniger Kalzium verlieren, je tiefer der PTH-Spiegel ist. Diese maximale Unterdrückung des PTH-Spiegels wird bei einem 25-OH-Vitamin-D-Spiegel von ca. 30ug/L (75nmol/L) erreicht (5). Ist es deshalb sinnvoll, allen Personen soviel Vitamin D zu geben, dass ein Vitamin-D-Spiegel von 30ug/L erreicht wird? Und wenn dies der Fall ist, welche Dosis ist notwendig, um dieses Ziel zu erreichen und welches ist das optimale Dosierungsintervall?
Zu diesen Themen wurden viele Studien durchgeführt und diese wiederum in Metaanalysen untersucht. Bis heute bleiben aber die meisten Punkte unklar und werden weiterhin kontrovers diskutiert: Höchstwahrscheinlich führt eine Vitamin-D-Supplementation bei gesunden Personen nicht zur Frakturrisikoreduktion oder Verbesserung der Knochendichte. Gemäss einer Cochrane Review 2023 konnte bei prämenopausalen gesunden Frauen weder ein Effekt auf die Knochendichte noch auf das Frakturrisiko gezeigt werden (6). Ebenso fand sich kein Effekt bei gesunden Personen über 70 Jahren (7). Andererseits wurde in einer Metaanalyse von 2012 gezeigt, dass eine Supplementation mit 800IU pro Tag das Hüftfrakturrisiko bei Personen über 65 Jahren senken konnte (8).
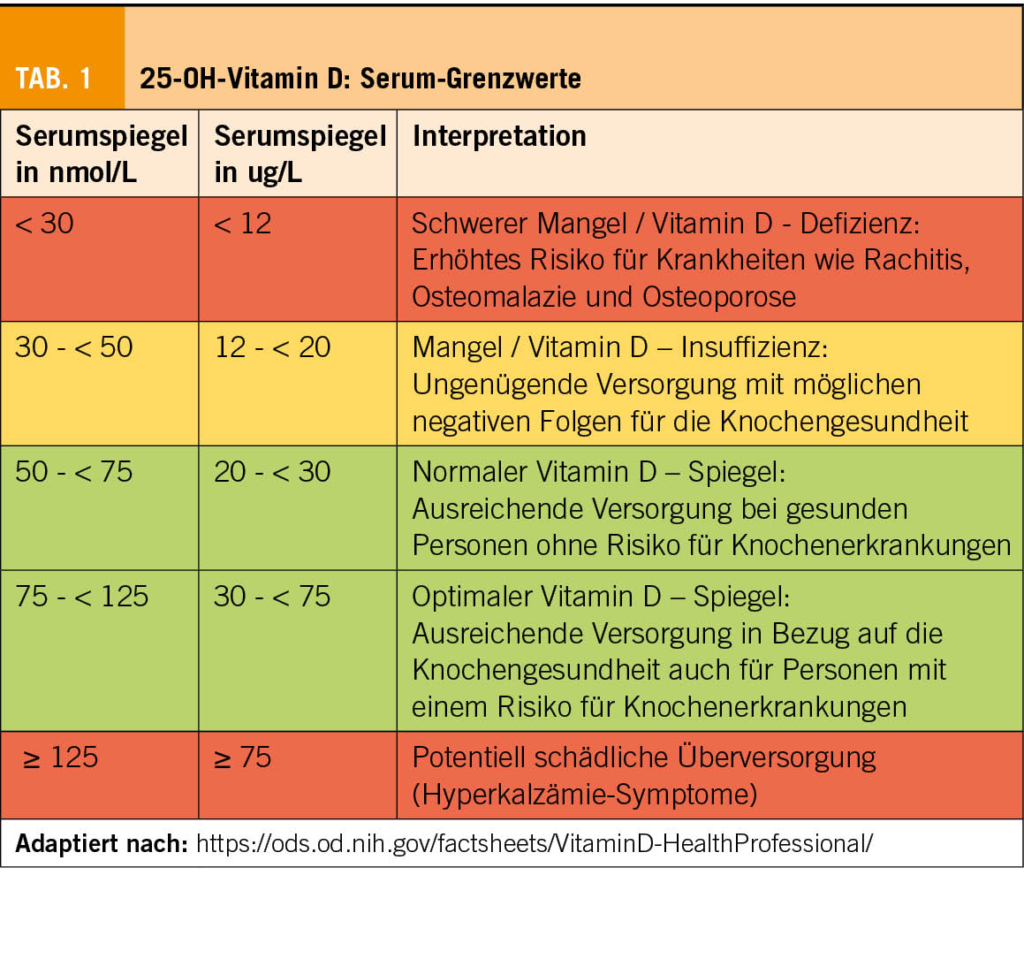
Trotz dieser Unklarheiten sind sich alle Osteologie-Gesellschaften einig, dass eine Vitamin-D-Supplementation bei gewissen Personengruppen (ältere oder gebrechliche Personen, Personen mit erhöhtem Sturz- und Frakturrisiko, Personen mit einem Risiko für einen Vitamin-D-Mangel) sinnvoll ist. Ein Vitamin-D-Spiegel von >20ug/L (>50nmol/L) gilt als genügend, zur Frakturprävention sollte ein Spiegel von 30ug/L (75nmol/L) angestrebt werden (Tab. 1).
Die International Osteoporosis Foundation empfiehlt eine Supplementation mit 800 - 1000 IU täglich, bzw. einen Serumspiegel von 20ug/L (50nmol/L) (9). Das Bundesamt für Lebensmittelsicherheit und Veterinärwesen empfiehlt für gesunde Erwachsene zwischen 18-65 Jahren eine Zufuhr von 600 IU täglich und für Personen ab 66 Jahren 800IU. Ab dem 60. Lebensjahr sollte die Zufuhr zudem ganzjährig mittels Supplementen erfolgen, während jüngere Personen im Sommer den Bedarf durch regelmässigen Aufenthalt im Freien decken können. Für Schwangere wird eine Zufuhr von mindestens 600 IU täglich empfohlen (10).
Muss der Vitamin-D-Spiegel gemessen werden?
Zur Messung der Serumkonzentration von 25-OH-Vitamin D können verschiedene Assays verwendet werden, deren Ergebnisse aber um 10 bis 15% variieren. Dies erschwert die Diagnose einer Hypovitaminose D, bzw. die Angabe des effektiven Serumspiegels. Zudem sind Verlaufskontrollen nicht aussagekräftig, wenn die Analysen in unterschiedlichen Labors mit verschiedenen Assays durchgeführt werden. Seit 2010 koordiniert deshalb das Vitamin D Standardization Program (VDSP) Aktivitäten zur Standardisierung der Vitamin-D-Messungen (11). Nichtsdestotrotz dürften auch in der Schweiz unterschiedliche Messmethoden angewendet werden, welche unterschiedliche Resultate ergeben. Falls Vitamin-D-Spiegel gemessen werden – und insbesondere für Verlaufsbeurteilungen – ist es deshalb wichtig, jeweils immer dasselbe Labor mit der Analyse zu beauftragen.
Die Kosten einer 25-OH-Vitamin-D-Bestimmung betragen aktuell (März 2023) gemäss Analysenliste CHF 47.70 (12). Dazu kommen Kosten für die Blutentnahme sowie die Auftragstaxe für das Labor. Die Gesamtkosten einer einzigen Vitamin-D-Bestimmung dürften deshalb bei CHF 60.00 - 70.00 liegen. Eine Supplementation mit 800 IU Vitamin D/Tag kostet zwischen CHF 30.00 und 40.00 pro Jahr. In Anbetracht dessen, dass eine Dosierung von 800 - 1000 IU Vitamin D täglich als sicher gilt, ist es kostengünstiger und medizinisch vertretbar, bei gesunden Personen eine Supplementation durchzuführen ohne den Vitamin-D-Spiegel zu bestimmen. Bei Patienten mit einem Risiko für einen Vitamin-D-Mangel oder mit einer Osteoporose ist es jedoch sinnvoll, vor Beginn einer Supplementation den Vitamin-D-Spiegel zu bestimmen und auf dieser Basis eine individuelle Vitamin-D-Supplementation zu verschreiben.
Wird eine Verlaufskontrolle durchgeführt, sollte diese frühestens 12 Wochen nach Dosisänderung erfolgen, da erst dann wieder ein steady state erreicht ist (13, 14). Seit Juli 2023 vergüten die Krankenkassen Vitamin-D-Bestimmungen zudem nur für bestimmte Erkrankungen und nur alle 3 Monate (Tab. 2) (12).
Welche Dosis soll gegeben werden?
Die Dosis, die notwendig ist, um einen bestimmten Vitamin-D-Spiegel zu erreichen, ist von verschiedenen Faktoren abhängig: Ausgangswert des Vitamin-D-Spiegels, Body-Mass-Index, begleitende Kalziumsupplementation und Art des zugeführten Vitamin D (Vitamin D2 oder D3). In Studien wurde ein Anstieg des Vitamin-D-Spiegels um 0.5 - 3.5ug/L pro zusätzlich eingenommene 100 IU Vitamin D beobachtet (13, 14). Als Faustregel kann deshalb angenommen werden, dass pro 100 IU zusätzliches Vitamin D pro Tag der Serumspiegel um 1ug/L (2.5nmol/L) ansteigt. So würde beispielsweise eine Patientin, die unter einer bestehenden Vitamin D-Supplementation von 800 IU täglich einen Vitamin-D-Spiegel von 18 ug/L aufweist, zusätzlich 1200IU Vitamin D täglich benötigen, um einen steady state von 30ug/L zu erreichen. Die totale tägliche Dosis müsste in diesem Fall 2000 IU pro Tag betragen und dauerhaft eingenommen werden, um den erwünschten Blutspiegel zu erhalten.
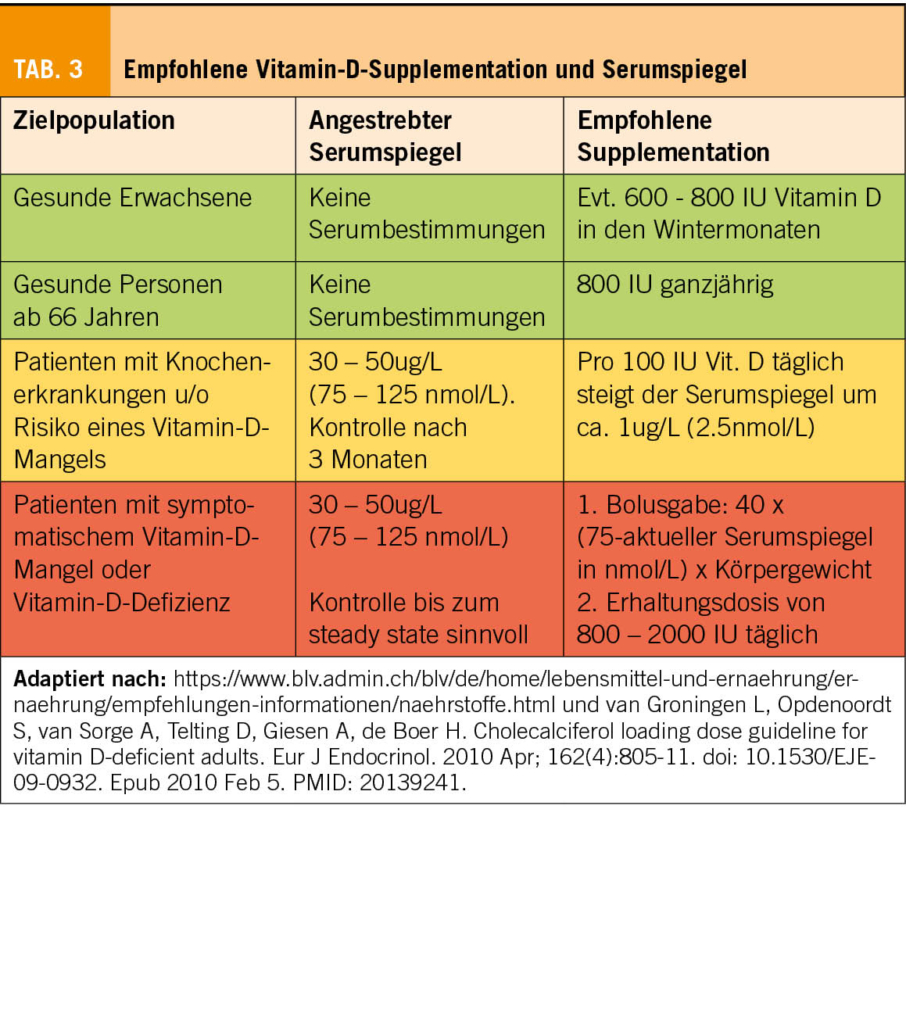
Um einen sehr tiefen Vitamin-D-Spiegel rasch anzuheben (z.B. bei Patienten mit einem schweren Vitamin-D-Mangel, bzw. einer symptomatischen Osteomalazie) kann eine initiale Ladedosis Vitamin D verabreicht werden. Danach muss mit einer Erhaltungsdosis weiter behandelt werden. Verschiedene Empfehlungen existieren bezüglich der geeigneten Ladedosis: so empfiehlt das NIH eine individuelle Ladedosis gemäss Körpergewicht und angestrebter Erhöhung des Vitamin-D-Spiegels, während andere Gesellschaften eine mehr oder weniger fixe Ladedosis verabreichen. Ob eine Ladedosis einen therapeutischen Effekt hat, ist allerdings umstritten (Tab. 3) (15, 16, 17).
Viel hilft nicht immer viel
Um die Vitamin-D-Versorgung zu vereinfachen, wurden bereits vor Jahren verschiedene Dosierungsschemata evaluiert – tägliche, wöchentliche, monatliche oder sogar jährliche Verabreichungen von kleinen bis sehr hohen Dosen. Dabei zeigte es sich, dass jährliche hohe Dosen das Sturz- und Frakturrisiko sogar erhöhen (18). Auch monatliche hohe Dosen scheinen einen eher negativen Effekt zu haben. Ein Dosisregime einer täglichen oder maximal wöchentlichen Einnahme einer geringen Dosis scheint den höheren Dosen in längeren Abständen überlegen zu sein (19). Eine Ladedosis bei sehr tiefen Vitamin-D-Spiegeln sollte deshalb immer von einer täglichen oder wöchentlichen Erhaltungsdosis gefolgt sein.
Copyright bei Aerzteverlag medinfo AG
Leiterin OsteoporoseZentrum
Klinik für Rheumatologie
UniversitätsSpital Zürich
Rämistrasse 100
8091 Zürich
diana.frey@usz.ch
Die Autorin hat keine Interessenkonflikte im Zusammenhang mit diesem Artikel deklariert.
◆ Vitamin D ist für die Knochengesundheit essentiell.
◆ Es ist umstritten, ob Vitamin D andere Erkrankungen vermindern kann
◆ Eine tägliche Dosis von 800 IU Vitamin D ist für Personen ohne wesentliche Erkrankungen ausreichend
◆ Der Vitamin D – Spiegel sollte bei Personen ohne Risikofaktoren für einen Vitamin D – Mangel nicht routinemässig gemessen werden
◆ Vitamin D – Spiegel-Bestimmungen werden von den Krankenkassen nur bei bestimmten Risikosituationen und maximal alle 3 Monate
vergütet
◆ Eine tägliche oder wöchentliche niedrig dosierte Supplementation ist einer hochdosierten Supplementation in grösseren Abständen
(monatlich oder jährlich) überlegen
◆ Bei schwerem und/oder symptomatischem Vitamin D-Mangel kann eine Ladedosis gegeben werden, gefolgt von einer täglichen oder wöchentlichen Erhaltungstherapie
1. Funk Casmir. The journal of State Medicine. Volume XX: 341-368, 1912. The etiology of the deficiency diseases, Beri-beri, polyneuritis in birds, epidemic dropsy, scurvy, experimental scurvy in animals, infantile scurvy, ship beri-beri, pellagra. Nutr Rev. 1975 Jun;33(6):176-7. doi: 10.1111/j.1753-4887.1975.tb05095.x. PMID: 1095967.
2. McCollum EV, Pitz W, Simmonds N, Becker JE, Shipley PG, Bunting RW. The effect of additions of fluorine to the diet of the rat on the quality of the teeth. 1925. Studies on experimental rickets. XXI. An experimental demonstration of the existence of a vitamin which promotes calcium deposition. 1922. The effect of additions of fluorine to the diet of the rat on the quality of the teeth. 1925. J Biol Chem. 2002 May 10;277(19):E8. PMID: 11991957.
3. Manson JE, Cook NR, Lee IM, Christen W, Bassuk SS, Mora S, Gibson H, Gordon D, Copeland T, D’Agostino D, Friedenberg G, Ridge C, Bubes V, Giovannucci EL, Willett WC, Buring JE; VITAL Research Group. Vitamin D Supplements and Prevention of Cancer and Cardiovascular Disease. N Engl J Med. 2019 Jan 3;380(1):33-44. doi: 10.1056/NEJMoa1809944. Epub 2018 Nov 10. PMID: 30415629; PMCID: PMC6425757.
4. Institute of Medicine (US) Committee to Review Dietary Reference Intakes for Vitamin D and Calcium. Dietary Reference Intakes for Calcium and Vitamin D. Ross AC, Taylor CL, Yaktine AL, Del Valle HB, editors. Washington (DC): National Academies Press (US); 2011. PMID: 21796828.
5. Durazo-Arvizu RA, Dawson-Hughes B, Sempos CT, Yetley EA, Looker AC, Cao G, Harris SS, Burt VL, Carriquiry AL, Picciano MF. Three-phase model harmonizes estimates of the maximal suppression of parathyroid hormone by 25-hydroxyvitamin D in persons 65 years of age and older. J Nutr. 2010 Mar;140(3):595-9. doi: 10.3945/jn.109.116681. Epub 2010 Jan 20. PMID: 20089790; PMCID: PMC2821888.
6. Méndez-Sánchez L, Clark P, Winzenberg TM, Tugwell P, Correa-Burrows P, Costello R. Calcium and vitamin D for increasing bone mineral density in premenopausal women. Cochrane Database Syst Rev. 2023 Jan 27;1(1):CD012664. doi: 10.1002/14651858.CD012664.pub2. PMID: 36705288; PMCID: PMC9881395.
7. Bischoff-Ferrari HA, Vellas B, Rizzoli R, Kressig RW, da Silva JAP, Blauth M, Felson DT, McCloskey EV, Watzl B, Hofbauer LC, Felsenberg D, Willett WC, Dawson-Hughes B, Manson JE, Siebert U, Theiler R, Staehelin HB, de Godoi Rezende Costa Molino C, Chocano-Bedoya PO, Abderhalden LA, Egli A, Kanis JA, Orav EJ; DO-HEALTH Research Group. Effect of Vitamin D Supplementation, Omega-3 Fatty Acid Supplementation, or a Strength-Training Exercise Program on Clinical Outcomes in Older Adults: The DO-HEALTH Randomized Clinical Trial. JAMA. 2020 Nov 10;324(18):1855-1868. doi: 10.1001/jama.2020.16909. PMID: 33170239; PMCID: PMC7656284.
8. Bischoff-Ferrari HA, Willett WC, Orav EJ, Lips P, Meunier PJ, Lyons RA, Flicker L, Wark J, Jackson RD, Cauley JA, Meyer HE, Pfeifer M, Sanders KM, Stähelin HB, Theiler R, Dawson-Hughes B. A pooled analysis of vitamin D dose requirements for fracture prevention. N Engl J Med. 2012 Jul 5;367(1):40-9. doi: 10.1056/NEJMoa1109617. Erratum in: N Engl J Med. 2012 Aug 2;367(5):481. Oray, Endel J [corrected to Orav, Endel J]. PMID: 22762317.
9. https://www.osteoporosis.foundation/vitamin-d-recommendations – aufgerufen 12.3.2023
10. https://www.blv.admin.ch/blv/de/home/lebensmittel-und-ernaehrung/ernaehrung/empfehlungen-informationen/naehrstoffe.html – aufgerufen 12.3.2023
11. Wise SA, Camara JE, Sempos CT, Lukas P, Le Goff C, Peeters S, Burdette CQ, Nalin F, Hahm G, Durazo-Arvizu RA, Kuszak AJ, Merkel J, Cavalier É. Vitamin D Standardization Program (VDSP) intralaboratory study for the assessment of 25-hydroxyvitamin D assay variability and bias. J Steroid Biochem Mol Biol. 2021 Sep;212:105917. doi: 10.1016/j.jsbmb.2021.105917. Epub 2021 May 16. PMID: 34010687; PMCID: PMC8403635.
12. www.bag.admin.ch/bag/de/home/versicherungen/krankenversicherung/krankenversicherung-leistungen-tarife/Analysenliste.html – aufgerufen 12.3.2023
13. Ramasamy I. Vitamin D Metabolism and Guidelines for Vitamin D Supplementation. Clin Biochem Rev. 2020 Dec;41(3):103-126. doi: 10.33176/AACB-20-00006. PMID: 33343045; PMCID: PMC7731935.
14. Pilz S, Zittermann A, Trummer C, Theiler-Schwetz V, Lerchbaum E, Keppel MH, Grübler MR, März W, Pandis M. Vitamin D testing and treatment: a narrative review of current evidence. Endocr Connect. 2019 Feb 1;8(2):R27-R43. doi: 10.1530/EC-18-0432. PMID: 30650061; PMCID: PMC6365669.
15. van Groningen L, Opdenoordt S, van Sorge A, Telting D, Giesen A, de Boer H. Cholecalciferol loading dose guideline for vitamin D-deficient adults. Eur J Endocrinol. 2010 Apr;162(4):805-11. doi: 10.1530/EJE-09-0932. Epub 2010 Feb 5. PMID: 20139241.
16. Bertoldo F, Cianferotti L, Di Monaco M, Falchetti A, Fassio A, Gatti D, Gennari L, Giannini S, Girasole G, Gonnelli S, Malavolta N, Minisola S, Pedrazzoni M, Rendina D, Rossini M, Chiodini I. Definition, Assessment, and Management of Vitamin D Inadequacy: Suggestions, Recommendations, and Warnings from the Italian Society for Osteoporosis, Mineral Metabolism and Bone Diseases (SIOMMMS). Nutrients. 2022 Oct 6;14(19):4148. doi: 10.3390/nu14194148. PMID: 36235800; PMCID: PMC9573415.
17. Berger MM, Shenkin A, Schweinlin A, Amrein K, Augsburger M, Biesalski HK, Bischoff SC, Casaer MP, Gundogan K, Lepp HL, de Man AME, Muscogiuri G, Pietka M, Pironi L, Rezzi S, Cuerda C. ESPEN micronutrient guideline. Clin Nutr. 2022 Jun;41(6):1357-1424. doi: 10.1016/j.clnu.2022.02.015. Epub 2022 Feb 26. PMID: 35365361.
18. Sanders KM, Stuart AL, Williamson EJ, Simpson JA, Kotowicz MA, Young D, Nicholson GC. Annual high-dose oral vitamin D and falls and fractures in older women: a randomized controlled trial. JAMA. 2010 May 12;303(18):1815-22. doi: 10.1001/jama.2010.594. Erratum in: JAMA. 2010 Jun 16;303(23):2357. PMID: 20460620.
19. Bischoff-Ferrari HA, Dawson-Hughes B, Orav EJ, Staehelin HB, Meyer OW, Theiler R, Dick W, Willett WC, Egli A. Monthly High-Dose Vitamin D Treatment for the Prevention of Functional Decline: A Randomized Clinical Trial. JAMA Intern Med. 2016 Feb;176(2):175-83. doi: 10.1001/jamainternmed.2015.7148. PMID: 26747333. Amrein, K., Scherkl, M., Hoffmann, M. et al. Vitamin D deficiency 2.0: an update on the current status worldwide. Eur J Clin Nutr 74, 1498–1513 (2020). https://doi.org/10.1038/s41430-020-0558-y
info@gynäkologie
- Vol. 13
- Ausgabe 2
- April 2023