- 19. Cardio Update 2024 – Teil 1
Auch dieses Jahr berichten wir über einige Highlights des alljährlichen, zweitägigen, ausgezeichneten Kongresses der Deutschen Gesellschaft für Kardiologie in Berlin resp. Mainz. In diversen Vorträgen wurden am 16./17. bzw. am 23./24. Februar die neuesten relevanten Fachpublikationen aus dem Jahre 2023 von Experten besprochen und gewertet. Wir geben einige praktische Schlaglichter aus einigen Vorträgen resp. aus dem Handbuch wieder.
Prähospitale Reanimation:
In Deutschland wurde 2022 von 60’000 ausserklinischen Herzkreislaufstillständen (OHCA) bei 51,3% (+10%) eine Laienreanimation durchgeführt; in Skandinavien liegt diese Zahl bei 80%. In 30% wurde eine Telefonreanimation unterstützend eingesetzt. Die Häufigkeit einer Telefonreanimation ist weiterhin unzureichend. Nur bei jedem vierten rettungsdienstlich begleiteten Herz-Kreislauf-Stillstand führte ein Disponent diese hocheffektive und lebensrettende Massnahme durch. In 70% erfolgt hierdurch eine Laienreanimation. Der überwiegende Teil der Reanimationen wurde im häuslichen Umfeld durchgeführt. 58% hatten eine kardiale Ursache.
In der Schweiz haben wir 2022 bei 6854 ausserklinischen Herzkreislaufstillständen eine REA-Rate von 44 auf 100 000 Einwohnern, 31% First Responder vor Ort (Swissreca Register 2022). Nur in 27% zeigte das primäre EKG einen defibrillierbaren Rhythmus. In beiden Ländern erreichten 30% nach der REA mit einem Spontanrhythmus die Klinik. 11% in DL und 13% in der Schweiz konnten bei einer OHCA die Klinik verlassen, teils mit eingeschränktem neurologischem Outcome. Der Kreislaufstillstand wurde beobachtet und
► die vermutete Ursache war medizinisch (z.B. durch einen Herzinfarkt verursacht)
► die Beobachtenden des Ereignisses haben bereits mit der Wiederbelebung gestartet
► der erste erkannte Herzrhythmus konnte defibrilliert werden
So betrug in der CH die Überlebensrate 29%, davon hatten 84% ein gutes neurologisches Outcome.
5 wichtige Kernaussagen bei den Reanimationsmassnahmen für Erwachsene (ALS):
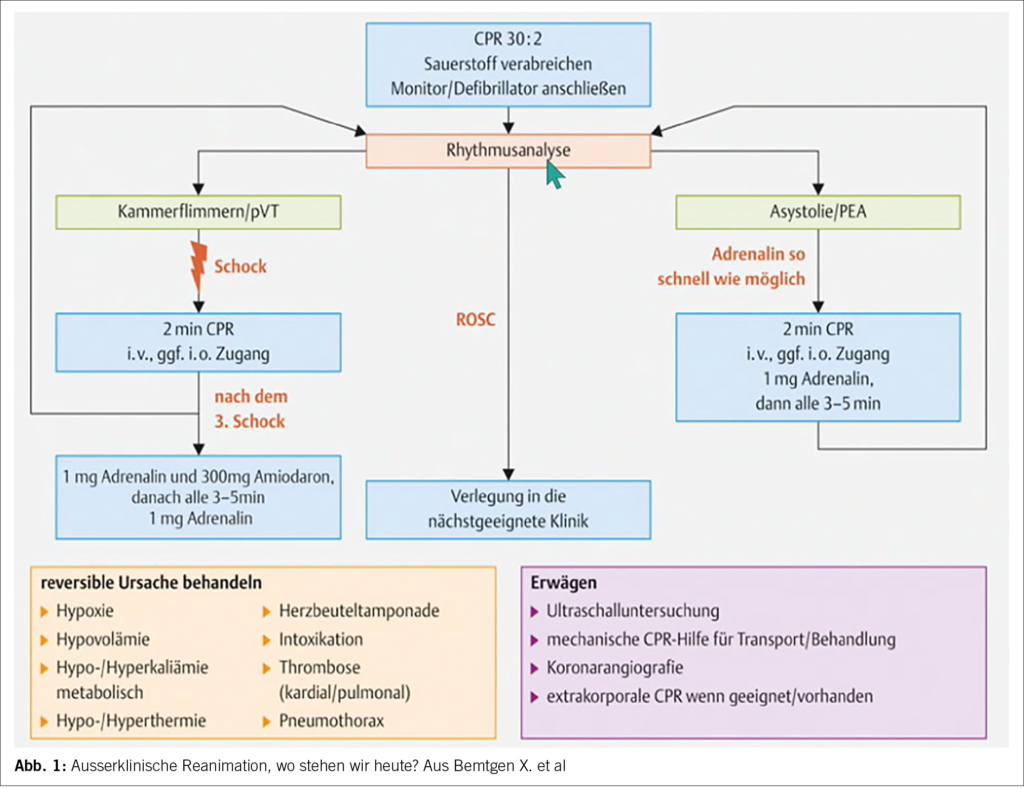
1. Priorität haben qualitativ hochwertige Thoraxkompressionen mit minimalen Unterbrechungen, frühzeitiger Defibrillation und Therapie von reversiblen Ursachen – vgl. Abbildung 1.
2. Vor dem innerklinischen wie präklinischen Kreislaufstillstand treten oft Frühwarnsymptome auf.
Der Kreislaufstillstand ist bei vielen Patienten vermeidbar.
3. Sichern Sie die Atmung durch Basis- und erweitertes Atemwegsmanagement – nur Anwender mit hoher Erfolgsrate sollen endotracheal intubieren.
4. Geben Sie bei nicht-schockbaren Rhythmen frühzeitig Adrenalin.
5. Erwägen Sie, wenn die konventionelle Reanimation erfolglos bleibt, bei ausgewählten Patienten – (beobachteter HK-Stillstand, kardiale Genese, initial defibrillierbarer Rhythmus, <70 Jahre, keine sign. Komorbiditäten, durchgehende hochwertige REA, reversible Ursache, Patientenwille) sofern möglich – die extrakorporale CPR (eCPR) als Rescue-Therapie.
Insgesamt stützen die Daten weiterhin den Einsatz von Adrenalin bei Patienten mit OHCA, auch wenn bisher keine der Studien einen Vorteil für ein gutes neurologisches Ergebnis bei Krankenhausentlassung zeigen konnte.
FAZIT für die Praxis zur Adrenalingabe bei der Reanimation:
► Geben Sie Erwachsenen im Kreislaufstillstand mit einem nicht-defibrillierbaren Rhythmus so bald wie möglich 1 mg Adrenalin i. v. (i. o.).
► Geben Sie bei erwachsenen Patienten mit Kreislaufstillstand, mit einem defibrillierbaren Rhythmus nach dem 3. Schock 1 mg Adrenalin i. v. (i. o.).
► Wiederholen Sie die Gabe von 1 mg Adrenalin i. v. (i. o.) alle 3–5 min, solange die ALS-Massnahmen fortgeführt werden.
Nach wie vor wird beim erwachsenen Patienten für ausgebildete Helfer ein Verhältnis von 30 Thoraxkompressionen zu 2 Beatmungen empfohlen. Allerdings wird die Atemspende von vielen Menschen als unangenehm oder unhygienisch empfunden. Eine alleinige Herzdruckmassage ist auf jeden Fall besser als keine Herzdruckmassage oder eine zu häufig unterbrochene Herzdruckmassage. In jedem Fall sollte die «No-Flow-Zeit» so kurz wie möglich sein.
FAZIT für die Praxis zum Atemwegsmanagement bei Reanimation:
► Sofern erweiterte Atemwegstechniken (z. B. Intubation) erforderlich sind, sollen diese nur Ersthelfer mit grosser Intubationserfahrung durchführen.
► Streben Sie an, die Thoraxkompression für eine endotracheale Intubation für weniger als 5 s zu unterbrechen.
► Verwenden Sie Video- oder direkte Laryngoskopie für die endotracheale Intubation, je nach den lokalen Behandlungsprotokollen und der Erfahrung der Ersthelfer.
► Verwenden Sie die Kapnographie, um die Position des Endotrachealtubus zu bestätigen.
► Geben Sie bei der CPR die höchstmögliche Konzentration inspiratorischen Sauerstoffs.
► Lassen Sie bei jeder Beatmung mehr als 1 s Zeit, bis sich der Brustkorb sichtbar hebt.
► Sobald ein Endotrachealtubus oder ein supraglottischer Atemweg (SGA) eingeführt wurde, beatmen Sie die Lunge mit einer Frequenz von 10/min und setzen die Thoraxkompressionen ohne Beatmungspausen fort. Wenn bei einem SGA eine Leckage zu einer unzureichenden Beatmung führt, unterbrechen Sie die Kompressionen für die Beatmung wieder (Kompressions-Beatmungs-Verhältnis 30:2). Vgl. Abbildung 1: aus Bemtgen X. et al, Ausserklinische Reanimation, wo stehen wir heute? DMW 2023;148 (14):921-933
Mithilfe der Notfallechokardiographie können bereits unmittelbar verschiedene, potenziell reversible Ursachen des Herz-Kreislauf-Stillstands evaluiert werden. Hierzu gehört insbesondere die Diagnose der Perikardtamponade oder einer akuten Rechtsherzbelastung. Weiterhin kann die Einschätzung des Volumenstatus, der linksventrikulären Pumpfunktion und ggf. relevanter Herz-klappenvitien erfolgen.
Post-REA: Notfallecho sehr hilfreich; sofortiges Koro nur bei einer ST-Hebung im EKG. Überwachung Kerntemperatur, Vermeidung von Fieber (>37.7 Grad); evt. erweiterte Bildgebung (Ganzkörper-CT); Abschätzung der Prognose nach dem ERC-ESICM 2021 Algorithmus Score von Sandroni.
Die BIG-FIVE-Überlebensstrategien nach Kreislaufstillstand, also fünf Strategien, mit denen die grösste Verbesserung des Überlebens erreicht werden kann umfassen folgende Punkte:
1. Programme zur Erhöhung der Laienreanimationsrate
2. Leitstellen-angeleitete Telefon-Reanimation: Verdoppelung des Überlebens erwartet
3. First-Responder-Programme mit öffentlich zugänglichen Defibrillatoren
4. Qualitativ hochwertige CPR durch erfahrene Rettungsteams und First-Responder
5. Spezialisierte Postreanimationsbehandlung in Cardiac-Arrest-Zentren
Herz-Niere-Hypertonie
Nach Erstdiagnose einer kardiovaskulären Erkrankung sollte die Nierenfunktion regelmässig kontrolliert werden, da das Risiko für eine Verschlechterung der GFR in den ersten 3 Jahren 3-5-fach erhöht ist. Das Risiko ist insbesondere in den ersten 3 Monaten stark erhöht (Faktor 106). Dies gilt vor allem für Patienten mit Herzinsuffizienz, gefolgt von Herzinfarkt, Vorhofflimmern und Stroke.
SGLT2-Inhibitoren gehören zur Standardtherapie der Herz- und Niereninsuffizienz. Es konnte gezeigt werden, dass Patienten mit einer Abnahme der eGFR <25 ml/min/1,73 m² ein deutlich erhöhtes kardiovaskuläres Risiko haben. Dapagliflozin verringerte im Vergleich zu Placebo das Risiko für kardiovaskulären Tod oder HI-Verschlechterung, unabhängig davon, ob eine Verschlechterung der eGFR <25 ml/min/1,73 m² auftrat oder nicht. Das Nutzen-Risiko-Verhältnis spricht für eine fortgesetzte Behandlung mit Dapagliflozin bei Patienten mit HI, selbst wenn die Nierenfunktion auf <25 ml/min/1,73 m² abfällt.
Bei Patienten mit CKD die eine invasive Untersuchung mit Kontrastmittel (KM) erhalten, besteht ein relevantes Risiko für ein akutes KM-assoziiertes Nierenversagen. Zur Vermeidung dieser NW empfehlen die Fachgesellschaften eine angemessene intravenöse Flüssigkeitszufuhr, die in der Regel 12 Stunden vor dem Eingriff initiiert werden sollte und bis 12 h nach der Intervention aufrecht-erhalten wird. Eine Studie zeigt, dass ein neues vereinfachtes Hydrations-Protokoll (mit einer kürzeren Hydrationsdauer von 1 Stunde vor bis 4 Stunden nach der Herzkatheteruntersuchung mit einer Rate von 3 ml/kg/h) der Standardhydration mit 1ml/kg/h in der Prävention eines KM-assoziierten Nierenversagens nicht unterlegen ist und sicher zur Anwendung gebracht werden kann.
Möglicherweise wirkt auch Kaliumnitrat, eingenommen in Form von 20ml Rote Beete Saft Konzentrat über 5 Tage vor einer KM-Gabe via eine NO-Freisetzung, bei einer CKD zusätzlich nephroprotektiv. Auch reduzierte die Gabe von anorganischen Nitraten die Rate an kardiovaskulären und renalen Ereignissen.
Die American Heart Association (AHA) hat in einem Positionspapier vorgeschlagen, die häufige und prognostisch wichtige Schnittmenge aus Diabetes, Niereninsuffizienz und Adipositas als Cardiovascular-Kidney-Metabolic-Syndrom (CKM) zu bezeichnen und in 4 Stadien einzuteilen.
Stad.1: Adipositas u. gestörte Glucosetoleranz, Stad.2: Metabol. RF u. CKD, Stad.3: subklin. CVD, Stad. 4: klinische CVD: CCS, HI, VHFli, Stroke, PAVK. 29% der Todesfälle in USA sind auf ein CKM-Syndrom zurückzuführen. Pathophysiologisch spielen neben den bekannten Interaktionen des metabolischen und kardiorenalen Syndroms Mediatoren des abdominellen Fettgewebes (Adipokine) eine Rolle, welche zu den Teufelskreisen aus Inflammation, oxidativem Stress, Insulinresistenz und vaskulärer Dysfunktion beitragen. Diese neue Bezeichnung kann dazu beitragen, die neuen Therapieoptionen an der klinisch relevanten Schnittstelle zwischen Adipositas und Typ II Diabetes und Nierenerkrankungen in den Fokus zu rücken.
Bei der steatotischen Lebererkrankung (SLD) wurden 2023 die Nomenklaturen geändert: Neben 5 metabolischen Risikofaktoren, wovon einer vorhanden sein muss, spricht man bei einer Lebersteatose heute anstelle der Ausdrücke NAFL und NASH von MASLD und MASH (metabolic dysfunction associated steatotic liver disease resp. metabolic dysfunction associated steatohepatitis). Der neue Begriff MASLD zeigt die enge Vernetzung hepatischer und metabolischer Faktoren der Erkrankung auf.
Bei einer SLD besteht ein deutlich erhöhtes cv Risiko, insbesondere bei einem zusätzlichen T2DM.
Die neuen Europäischen Hypertonie Leitlinien Empfehlungen von 2023 sind lesenswert. So ist auch die Durchführung einer korrekten BD-Messung im Sitzen und die Auswahl einer passenden Manschettengrösse von erheblicher Relevanz für die Erhebung einer validen Blutdruckmessung. Die Studie von Ishigami zeigt, dass es keine einheitliche BD-Manschette für Alle gibt. Die Verwendung einer zu kleinen Standardmanschette kann dazu führen, dass fälschlich eine Hypertonie diagnostiziert und behandelt wird. Die Auswirkung einer falschen Manschettengrösse war umso ausgeprägter, je massiger der Oberarm war. Insbesondere wenn die Manschette zu klein für den Oberarmumfang ist, war die Abweichung der Messung besonders gross (bis zu 20 mmHg systolisch und 7 mmHg diastolisch zu hoch).
Die Behandlungsindikation bei Hypertonie besteht bei den meisten Patienten bei Praxisblutdruckwerten ≥140/90 mmHg, bei über 80-Jährigen bei ≥160/90 mmHg, bzw. ≥130/80 mmHg im Gesamtmittelwert bzw. ≥135/85 mmHg im Tagesmittelwert. In der Diagnosestellung nehmen praxisunabhängige Messungen (Langzeit- und häusliche Blutdruckmessungen) eine wichtige Rolle ein.
Der Langzeitblutdruck ist prognostisch wichtiger als der Praxisblutdruck. Es besteht eine Assoziation zwischen einem 24-h-BD-Profil und dem cv Outcome. So ist das cv Risiko bei einer nächtlichen Hypertonie deutlich erhöht, ebenso bei einer maskierten Hypertonie, nicht aber bei einer Weisskittelhypertonie.
Fixkombinationen sind heute zu bevorzugen. Es besteht eine bessere Adhärenz, eine stärkere BD-Senkung und weniger NW.
Durch ein neues Therapiekonzept (Phase 1) mit einer RNA-Interferenz (siRNA) (Zilebesiran-Injektion 1x s.c.) kann die hepatische Produktion von Angiotensinogen verhindert werden und dadurch der erhöhte systolische und diastolische BD über 24 Wochen dosisabhängig konstant gesenkt werden. Es wurden keine systemischen NW beobachtet. Unklar sind noch die Konsequenzen bei einer akuten Aktivierung des RAAS-Systems z.B. bei einem Schock resp. Hypovolämie. Das Problem der Nicht-Adhärenz könnte so mit 2 Injektionen/Jahr gelöst werden.
Ein weiteres neues erfolgreiches orales Medikament (Phase2) ist ein Aldosteronsynthase-Hemmer (Baxdrostat) bei Patienten mit einer resistenten Hypertonie.
Bei einer Therapieresistenz ist die renale Denervation wieder in den Leitlinien. Diese kann auch bei einer Medikamentenunverträglichkeit/Nicht-Adhärenz diskutiert werden.
Zelglistrasse 17
8127 Forch
u.n.duerst@ggaweb.ch
Diese kann beim Verfasser angefordert werden.
info@herz+gefäss
- Vol. 14
- Ausgabe 2
- April 2024