- Arterielle Hypertonie und Hirnschlag
Hirnschläge haben in unseren Breitengraden eine hohe Inzidenz. Arterielle Hypertonie ist ein häufiger und der wichtigste behandelbare Risikofaktor für erstmalige sowie wiederholte Hirnschläge. Der vorliegende Artikel erläutert epidemiologische und pathophysiologische Aspekte und thematisiert die aktuellen Richtlinien betreffs Akutphase, Primär- und Sekundärprävention der arteriellen Hypertonie in Patienten mit Hirnschlag.
Les accidents vasculaires cérébraux (AVC) ont une incidence élevée à nos latitudes. L’ hypertension artérielle est un facteur de risque courant et le plus important que l’on puisse traiter pour les premiers AVC et les AVC répétés. Cet article explique les aspects épidémiologiques et physiopathologiques et discute des directives actuelles concernant la phase aiguë, la prévention primaire et secondaire de l’hypertension artérielle chez les patients ayant subi un AVC.
In unseren Breitengraden ist der Hirnschlag der häufigste Grund für Behinderung und die zweithäufigste Todesursache. In der Schweiz ereigneten sich im Jahr 2016 gemäss schweizerischem Bundesamt für Statistik 15254 Hirnschläge; die Hirnschlag-Inzidenz betrug gemäss schweizerischem Gesundheitsobservatorium 188/100 000 (157/100 000 bei Frauen, 224/100 000 bei Männern) und die Mortalität 16.2% (19.4% für Frauen, 12.9% für Männer) (1, 2). Im Jahr 2017 litten in der Schweiz 19.2% der Männer und 16% der Frauen an arterieller Hypertonie; in der Altersgruppe 65-74 Jahre 43.3% respektive 36% und in der Altersgruppe ≥ 75 Jahre 55.8% respektive 57.2% (1).
Blutdruck in der Primärprävention des Hirnschlags
Die arterielle Hypertonie ist ein häufiger und der wichtigste behandelbare Risikofaktor für Hirnschlag. Dies zeigte unter anderem die INTERSTROKE Fallkontrollstudie, welche 3000 Patienten mit erstmaligem Hirnschlag (78% mit Hirninfarkt, 22% mit Hirnblutung) aus 22 Ländern einschloss. Diese Studie errechnete, dass das Risiko einen Hirnschlag zu erleiden, um 34.6% (respektive 51.8%) niedriger war, bei nicht vorliegender selbstberichteter arterieller Hypertonie (respektive nicht vorliegenden Blutdruckwerten > 160/90 mmHg) (3). Es ist davon auszugehen, dass arterielle Hypertonie weltweit jährlich mit 1.5 Millionen Hirninfarkten und mit 2 Millionen Hirnblutungen assoziiert ist (4). Eine Metaanalyse von 61 prospektiven Beobachtungsstudien mit 958 074 Patienten mit 12 000 Hirnschlägen und einer Beobachtungszeit von über 5000 Patientenjahren zeigte einen unabhängigen annähernd logistisch-linearen Zusammenhang zwischen Blutdruck und Hirnschlag ab Blutdruckwerten von 115/75 mmHg (5). Eine Metaanalyse von 12 prospektiven Kohortenstudien mit 518 520 Patienten und einer Beobachtungszeit von 2.7 bis 23.7 Jahren, fand ein um 22% respektive 79% erhöhtes Hirnschlagrisiko bei Blutdruckwerten von 120-129/80-84 mmHg respektive 130-139/85-89 mmHg (6).
Zunehmendes Alter schwächt den Zusammenhang zwischen arterieller Hypertonie und Hirnschlag ab. Ein um 10 mmHg niedrigerer Blutdruck senkt das Hirnschlagrisiko um 40-50% bei < 60-Jährigen, um 30-40% bei 60-69-Jährigen und um 20-30% bei ≥ 70-Jährigen (5, 7).
Zerebrovaskuläre Pathophysiologie der arteriellen Hypertonie
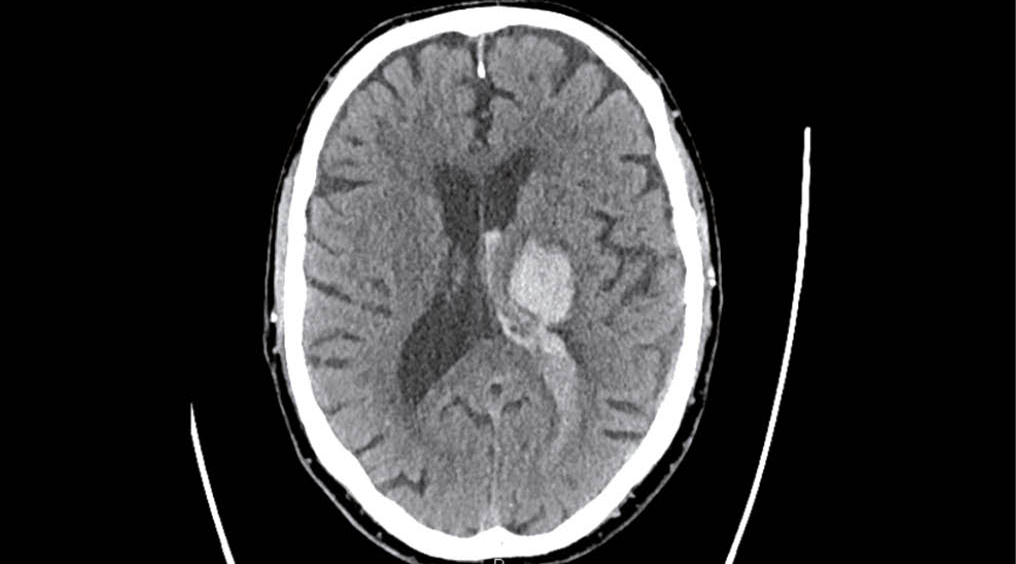
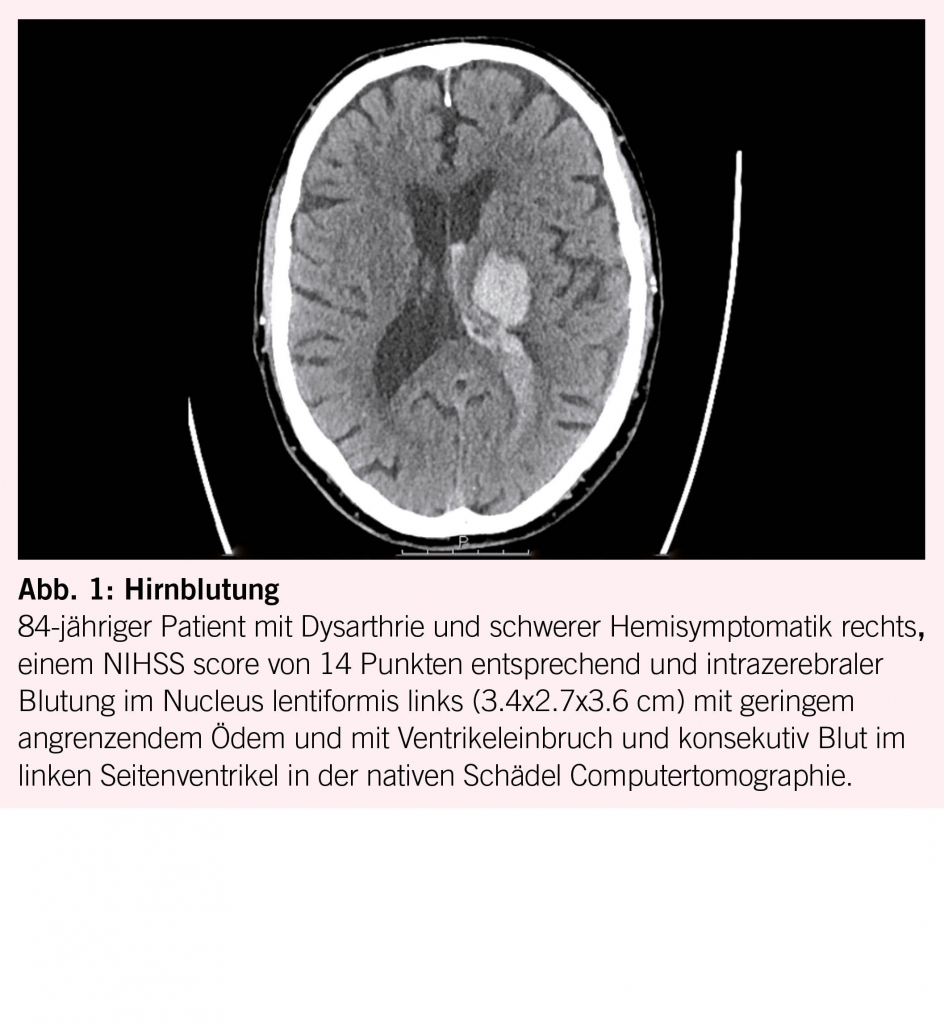
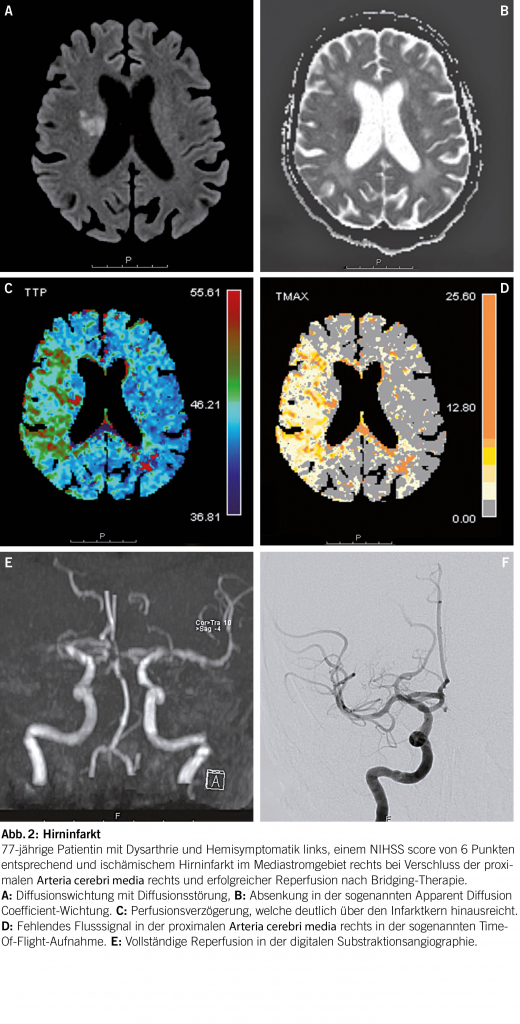
Arterielle Hypertonie verursacht einen Umbau der Gefässwand, fördert Atheromatose und Veränderungen der Endothelfunktion sowie der zerebralen Autoregulation. In der Folge entstehende Gefässrupturen führen zu Hirnblutungen (Abb. 1). Embolien, lokale Thrombusbildung oder seltener eine hämodynamische Insuffizienz verursachen Hirninfarkte (Abb. 2). Durch chronische mikroangiopathische Schäden entstehen Marklagerhyperintensitäten, Mikroinfarkte/-blutungen und neurodegenerative Prozesse wie Hirnatrophie. Es steigt nicht nur das Hirnschlag- aber auch das Demenzrisiko vom vaskulären aber auch vom Alzheimer Typ (8, 9).
Blutdruck in der Akutphase des Hirnschlags
Der Blutdruck ist innert den ersten Tagen nach Hirnschlag in der Mehrzahl der Patienten erhöht, wobei verschiedene Gründe wie Fluktuation oder Erhöhung vorbestehender arterieller Hypertonie, Stress, Schmerzen, Infekt, Harnverhalt, Aktivierung der Sympathikus-, der Renin-Angiotensin- und der ACTH-Cortisol-Achse, Hirndrucksteigerung, etc. zugrunde liegen können (10). In einer Populations-basierten Studie mit 636 Patienten war der Blutdruck in der Akutphase im Vergleich zum mittleren 10-Jahres-Vorwert insbesondere bei Hirnblutungen (im Mittel um 41 mmHg), weniger ausgeprägt bei Hirnischämien (im Mittel um 11 mmHg) erhöht (11). Hypertone Blutdruckwerte in der Akutphase eines Hirnschlages erhöhen das Rezidivrisiko, einer neuen oder progredienten Einblutung, eines Hirnödems und einer hypertensiven Enzephalopathie, können aber auch vor einer weiteren Ausdehnung des Infarktareals bei gestörter zerebraler Autoregulation und Hypoperfusion schützen (12-14). Beobachtungsstudien zeigten ein höheres zerebrales Einblutungsrisiko nach intravenöser Thrombolyse mit Alteplase im Falle höherer Blutdruckwerte. Daher wird empfohlen, dass vor intravenöser Thrombolyse mit Alteplase der Blutdruck vorsichtig auf < 185/110 mmHg gesenkt und die nächsten 24h darunter gehalten wird (Klasse I Evidenz) (15, 16). Dies könnte auch bei endovaskulärer Therapie sinnvoll sein (Klasse IIa Evidenz) (15).
In der Situation eines zusätzlich zum Hirninfarkt vorliegenden akuten koronaren Ereignisses, einer akuten Herzinsuffizienz, einer Aortendissektion, einer postthrombolytischen symptomatischen intrazerebralen Einblutung oder einer Prä-/eklampsie ist ein Senken deutlich hypertoner Blutdruckwerte empfohlen, um hierdurch Sekundärschäden vorzubeugen (Klasse I Evidenz) (15). Ein Senken des Blutdrucks um 15% innert 24 Stunden nach Hirninfarkt ist hierbei wahrscheinlich als sicher anzusehen (15, 16).
In konservativ therapierten Patienten mit Hirninfarkt ohne relevante Komorbiditäten ist ein Wieder-/beginn einer antihypertensiven Therapie innert 24 bis 72 Stunden nicht effektiv hinsichtlich Reduktion von Tod oder Invalidität bei Blutdruckwerten < 220/120 mmHg (Klasse III Evidenz) und der Nutzen unsicher bei Blutdruckwerten ≥ 220/120 mmHg (Klasse IIb Evidenz) (15, 16). Zu beachten ist allerdings, dass eine abrupt abgesetzte oder in der Dosis reduzierte vorbestehende antihypertensive Therapie im Falle von Beta-Blockern mit einer Rebound-Tachykardie und im Falle einer Herzinsuffizienztherapie mit einer kardialen Dekompensation einhergehen kann (17). Auch kann aber eine vermeintlich fortgeführte antihypertensive Therapie bei vorgängiger Malcompliance unerwünschte Nebenwirkungen inklusive übermässige Blutdruckabfälle bedingen (18).
Die INTERACT-2 Studie randomisierte 2793 Patienten mit intensiver (< 140 mmHg) versus moderater Blutdrucksenkung (< 180 mmHg) innert 6 Stunden nach Symptombeginn einer spontanen intrazerebralen Blutung. Der primäre Endpunkt Tod und Behinderung unterschied sich nicht signifikant zwischen den Gruppen. Allerdings fand sich in der Gruppe mit intensiver Blutdrucksenkung ein besseres funktionelles Ergebnis (19). Die nachfolgende ATACH-2 Studie schloss 1000 Patienten ein. Blutdruckwerte wurden rascher, innert 4.5 Stunden nach Symptombeginn auf 140-170 mmHg respektive 100-139 mmHg gesenkt. Hierbei wurden letztlich in der Gruppe der Patienten mit weniger intensiver Blutdrucksenkung Blutdruckwerte erzielt, die in der INTERACT-2-Studie der Gruppe mit intensiverer Blutdrucksenkung entsprachen. Auch in der ATACH-2-Studie unterschieden sich die beiden Gruppen nicht signifikant hinsichtlich Tod und Behinderung, aber im Unterschied zur INTERACT-2 Studie wies die Gruppe mit der intensiveren Blutdrucksenkung kein verbessertes funktionelles Ergebnis und häufiger renale Nebenwirkungen auf (20). Gemäss den aktuellsten Richtlinien ist ein unmittelbares Senken des Blutdrucks bei spontanen intrazerebralen Blutungen bei Werten < 220 mmHg nicht empfohlen, um Tod oder schwere Behinderung zu minimieren respektive kann potenziell schädlich sein (Klasse III Evidenz) (16, 21). Bei Blutdruckwerten ≥ 220 mmHg sollte eine intravenös verabreichte vorsichtige Blutdrucksenkung erwogen werden (Klasse IIa Evidenz) (16, 21).
Antihypertensiva, die nach Abwägen von Nutzen/Risiken in der Akutphase eines Hirnschlages zum Senken des Blutdrucks angewandt werden können, sind vorzugsweise intravenös und wenn möglich kontinuierlich verabreichtes Uradipil, Enalapril, Labetalol, Nicardipin, Clevedipin, Metoprolol und Dihydralazin (15, 17).
Blutdruck in der Sekundärprävention des Hirnschlags
Arterielle Hypertonie ist der wichtigste behandelbare Risikofaktor für wiederholte Hirnschläge.
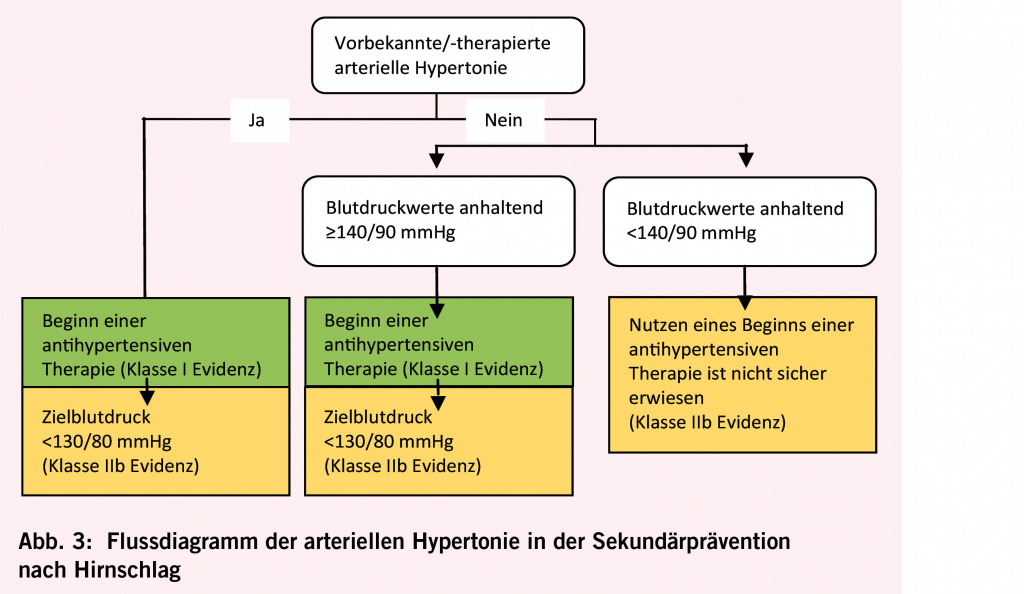
In der Sekundärprävention (Abb. 3) kann eine nach wenigen Tagen wiederbegonnene oder im Falle von Blutdruckwerten anhaltend ≥ 140/90 mmHg neu begonnene antihypertensive Therapie, falls nicht kontraindiziert, das Rezidivrisiko sowie das vaskuläre Risiko senken (Klasse I Evidenz) (15, 16). In TIA-Patienten kann der Wieder-/beginn unmittelbar erfolgen (Klasse I Evidenz) (21). Hierbei erscheint ein Zielblutdruck von < 130/80 mmHg häufig (Vorsicht bei hohem Patientenalter) vernünftig zu sein (Klasse IIb Evidenz) (16); allenfalls kann ein systolischer Zielblutdruck von 120-130 mmHg erwogen werden (Klasse IIa Evidenz) (21), insbesondere zur Sekundärprävention von Hirnblutungen (22). Allerdings muss berücksichtigt werden, dass ein zu tiefer Zielblutdruck schädlich sein kann. Ein solcher kann beispielsweise bei persistierend gestörter zerebraler Autoregulation und Hypoperfusion Hirninfarkte verursachen oder aber Synkopen auslösen. Auch Organdysfunktionen können auftreten. Der Nutzen eines Beginns einer antihypertensiven Therapie bei Blutdruckwerten < 140/90 mmHg ist nicht sicher erwiesen (Klasse IIb Evidenz) (16). Die empfohlenen Substanzklassen der Antihypertensiva in der Sekundärprävention sind Thiaziddiuretika oder ACE-Hemmer (oder Sartane) oder deren Kombination (Klasse I Evidenz) (16). Auch Kalziumantagonisten können von Nutzen sein. Beta-Blocker sind nicht empfohlen, ausser es besteht hierfür eine überzeugende kardiale Indikation (23). Das Verschreiben einer spezifischen Substanzklasse sollte unter Beachten von Komorbiditäten individualisiert erfolgen (Klasse I Evidenz) (16).
Neurologische Universitätsklinik
Institut für Interventionelle und Diagnostische Neuroradiologie
Universitätsspital – Inselspital
Freiburgstrasse 10
3010 Bern
mirjam.heldner@insel.ch
Neurologische Universitätsklinik
Institut für Interventionelle und Diagnostische Neuroradiologie
Universitätsspital – Inselspital
Freiburgstrasse 10
3010 Bern
simon.jung@insel.ch
Neurologische Universitätsklinik
Institut für Interventionelle und Diagnostische Neuroradiologie
Universitätsspital – Inselspital
Freiburgstrasse 10
3010 Bern
pasquale.mordasini@insel.ch
Die Autoren haben keine Interessenskonflikte im Zusammenhang mit diesem Beitrag deklariert.
- In unseren Breitengraden ist der Hirnschlag der häufigste Grund für Behinderung und die zweithäufigste Todesursache.
- Arterielle Hypertonie ist der wichtigste behandelbare Risikofaktor für erstmalige sowie wiederholte Hirnschläge und Demenz.
- In der Akutphase eines Hirnschlages ist der Blutdruck häufig erhöht und dessen optimales Management zu diesem Zeitpunkt nach wie vor insbesondere bei Hirnblutungen erst teilweise klar.
- Vor intravenöser Thrombolyse mit Alteplase sollte der Blutdruck vorsichtig auf < 185/110 mmHg gesenkt werden und die nächsten 24h darunter gehalten werden.
- Die empfohlenen Substanzklassen der Antihypertensiva in der Sekundärprävention sind Thiaziddiuretika oder ACE-Hemmer (oder Sartane) oder deren Kombination.
Messages à retenir
- À nos latitudes, l’AVC est la cause la plus fréquente d’invalidité et la deuxième cause de décès.
- L’hypertension artérielle est le facteur de risque le plus important traitable pour les accidents vasculaires cérébraux initiaux et répétés et la démence.
- Dans la phase aiguë d’un AVC, la tension artérielle est souvent élevée et sa prise en charge optimale à ce stade n’est encore que partiellement claire, surtout en cas d’hémorragies cérébrales.
- Avant une thrombolyse intraveineuse avec l’alteplase, la tension artérielle doit être soigneusement abaissée à <185/110 mmHg et maintenue sous ce niveau pendant les 24 heures suivantes.
- Les classes recommandées d’antihypertenseurs dans la prévention secondaire sont les diurétiques thiazidiques ou les inhibiteurs de l’ECA (ou Sartane) ou une combinaison de ceux-ci.
Literatur
1. Schweizerisches Bundesamt für Statistik: https://www.bfs.admin.ch/bfs/de/home/statistiken/gesundheit/gesundheitszustand/krankheiten/herz-kreislauf-erkrankungen.html
2. Schweizerisches Gesundheitsobservatorium: https://www.obsan.admin.ch//de/indikatoren/hirnschlag
3. O’Donnell MJ et al. INTERSTROKE investigators. Risk factors for ischaemic and intracerebral haemorrhagic stroke in 22 countries (the INTERSTROKE study): a case-control study. Lancet 2010;376:112-23.
4. Forouzanfar MH et al. Global burden of hypertension and systolic blood pressure of at least 110 to 115mmHg, 1990-2015. JAMA 2017;317:165-82.
5. Lewington S et al. Age-specific relevance of usual blood pressure to vascular mortality: a meta-analysis of individual data for one million adults in 61 prospective studies. Lancet 2002;360:1903-13.
6. Lee M et al. Presence of baseline prehypertension and risk of incident stroke: a meta-analysis. Neurology 2011;77:1330-7.
7. Lawes CM et al. Blood pressure and stroke: an overview of published reviews. Stroke 2004;35:1024.
8. Pantoni L et al. Cerebral small vessel disease: from pathogenesis and clinical characteristics to therapeutic challenges. Lancet Neurol 2010;9:689-701.
9. Emdin CA et al. Blood pressure and risk of vascular dementia: evidence from a primary care registry and a cohort study of transient ischemic attack and stroke. Stroke 2016;47:1429-35.
10. Qureshi AI et al. Prevalence of elevated blood pressure in 563’704 adult patients with stroke presenting to the ED in the United States. Am J Emerg Med 2007;25:32-8.
11. Fischer U et al. Acute post-stroke blood pressure relative to premorbid levels in intracerebral haemorrhage versus major ischaemic stroke: a population-based study. Lancet Neurol 2014;13:374-84.
12. Leonardi-Bee J et al. IST Collaborative Group. Blood pressure and clinical outcomes in the International Stroke Trial. Stroke 2002;33:1315-20.
13. Vemmos KN, et al. U-shaped relationship between mortality and admission blood pressure in patients with acute stroke. J Intern Med 2004;255:257-65.
14. Stead LG et al. Impact of acute blood pressure variability on ischemic stroke outcome. Neurology 2006;66:1878-81.
15. Powers WJ et al. American Heart Association Stroke Council. 2018 Guidelines for the Early Management of Patients With Acute Ischemic Stroke. Stroke 2018;49:e46-110.
16. Whelton PK et al. 2017 ACC/AHA/AAPA/ABC/ ACPM/AGS/APhA/ASH/ASPC/NMA/PCNA guideline for the prevention, detection, evaluation, and management of high blood pressure in adults: executive summary: a report of the American College of Cardiology/American Heart Association Task Force on clinical practice guidelines. Hypertension 2018;71:1269-324.
17. Die aktuellen Stroke Richtlinien des Berner Stroke Centers sind kostenlos unter (http://www.neurologie.insel.ch/de/unser-angebot/stroke-center/stroke-richtlinien/) und auch als kostenlose App für Smartphones verfügbar.
18. Woodhouse LJ et al. Continuing or temporarily stopping prestroke antihypertensive medication in acute stroke: an individual patient data meta-analysis. Hypertension 2017;69:933-41.
19. Anderson CS et al. INTERACT 2 Investigators. Rapid blood-pressure lowering in patients with acute intracerebral hemorrhage. N Engl J Med 2013;368:2355-65.
20. Qureshi AI et al. Intensive blood-pressure lowering in patients with acute cerebral hemorrhage. N Engl J Med 2016;375:1033-43.
21. Williams B et al. European Society of Cardiology (ESC) and the European Society of Hypertension (ESH). 2018 ESC/ESH Guidelines for the management of arterial hypertension. European Heart Journal. 2018;39:3021-104.
22. Benavente OR et al. SPS3 Study Group. Blood-pressure targets in patients with recent lacunar stroke: the SPS3 randomised trial. Lancet 2013;382:507-15.
23. Vickrey BG et al. Occurrence of secondary ischemic events among persons with atherosclerotic vascular disease. Stroke 2002;33:901-6.
info@herz+gefäss
- Vol. 9
- Ausgabe 1
- Januar 2019