- Behandlung des kardiogenen Schocks
Der kardiogene Schock verbleibt auch mit den heute verfügbaren diagnostischen und therapeutischen Möglichkeiten eine schwer zu behandelnde Erkrankung. Patienten mit diesem Krankheitsbild widerspiegeln eine heterogene Population mit unterschiedlichen Schockursachen, Schockstadien und Komorbiditäten, welche zusammen die Gesamtprognose bestimmen. Die hohe Mortalität von circa 50% konnte in den vergangenen zwei Jahrzehnten trotz grossem Aufwand zur Generierung von Evidenz nicht merklich reduziert werden und die Therapie richtet sich weiterhin vorwiegend nach pathophysiologischen Gesichtspunkten und ist dazu zeitsensibel. Dies macht die Therapie für das behandelnde Team herausfordernd, aber auch spannend.
Even with the diagnostic and therapeutic options that are available nowadays, treatment of cardiogenic shock remains difficult to handle. Patients present with different causes and stages of shock and various comorbidities, which together determine the overall prognosis. The high mortality of around 50% could not be reduced in a significant manner over the past two decades, despite a great effort to generate evidence. Treatment strategies of such patients continue to be based primarily on pathophysiological considerations and are additionally time-sensitive. This leads to a challenge but also excitement for the whole team involved in the treatment of such patients.
Key Words: cardiogenic shock, vasoactive therapy, temporary mechanical circulatory support, advanced heart failure
Schock-Klassifikation
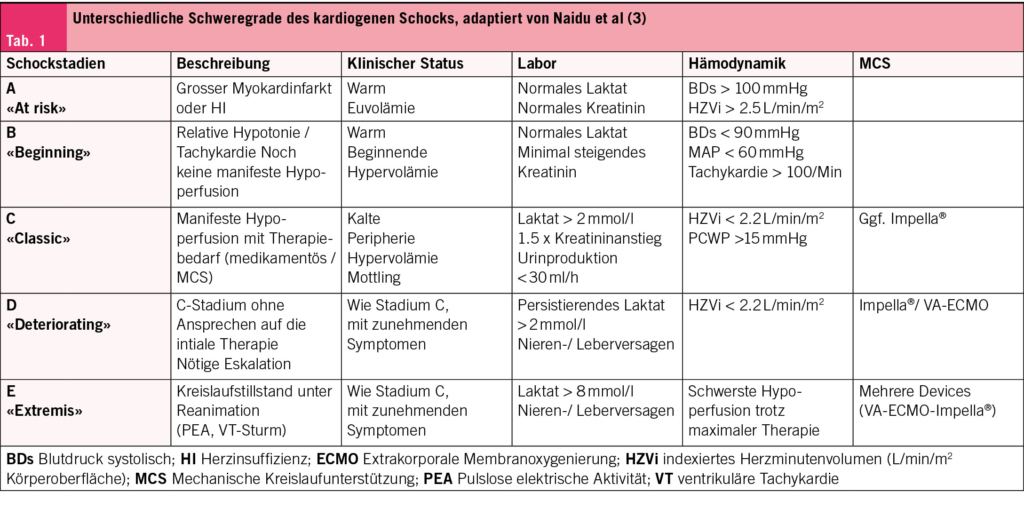
In der Klassifikation des Schweregrades des Schocks herrschte lange Zeit Uneinigkeit. Im Jahr 2019 wurde schliesslich von der amerikanischen Gesellschaft für kardiovaskuläre Angiographie und Interventionen (SCAI) ein mittlerweile international anerkanntes, auf dem Konsens von Experten basierendes Dokument veröffentlicht, welches den kardiogenen Schock in unterschiedliche Schweregrade unterteilt (1). Es wurden insgesamt fünf Stadien, von A bis E, anhand von klinischen, laborchemischen und hämodynamischen Kriterien definiert (Tab. 1).
In einer grossen Kohorte mit > 10 000 Patienten einer kardiologischen Intensivstation wurde die Klassifikation validiert: Es zeigte sich eine starke Assoziation zwischen den SCAI-Schockstadien und der Mortalität (2).
Die Einteilung der Patienten in eines dieser Schockstadien ist ohne komplizierte Berechnungen und rasch möglich und erlaubt, therapeutische Schritte (beispielsweise eine Eskalation der Therapie) frühzeitig in die Wege zu leiten.
Ein weiteres Ziel der Klassifikation ist es, eine einheitliche Definition für künftige Studien zu kreieren, um die Patientenpopulation möglichst homogen zu halten und die Aussagekraft der Studienergebnisse zu erhöhen.
Nachträgliche Analysen von publizierten Studien haben ergeben, dass die Schockstadien und –verteilung in den verschiedenen Studien beträchtlich variiert 3. Diese heterogenen Studienpopulationen mit unterschiedlichen Schock-Schweregraden sind sicherlich miterklärend für die diskrepanten Ergebnisse der verschiedenen Studien.
Behandlungsstrategien
Nach dem prompten Erkennen des kardiogenen Schocks geht es darum, die fortschreitende Schockspirale möglichst rasch zu durchbrechen. Dazu müssen folgende Massnahmen getroffen werden:
1. Rasche Identifikation und- wenn möglich- Behandlung der Ursache
2. Kreislaufstabilisierung zur Wiederherstellung einer genügenden Gewebeperfusion sowie kardioprotektive Massnahmen zum Schutz des Myokards
Ursachen
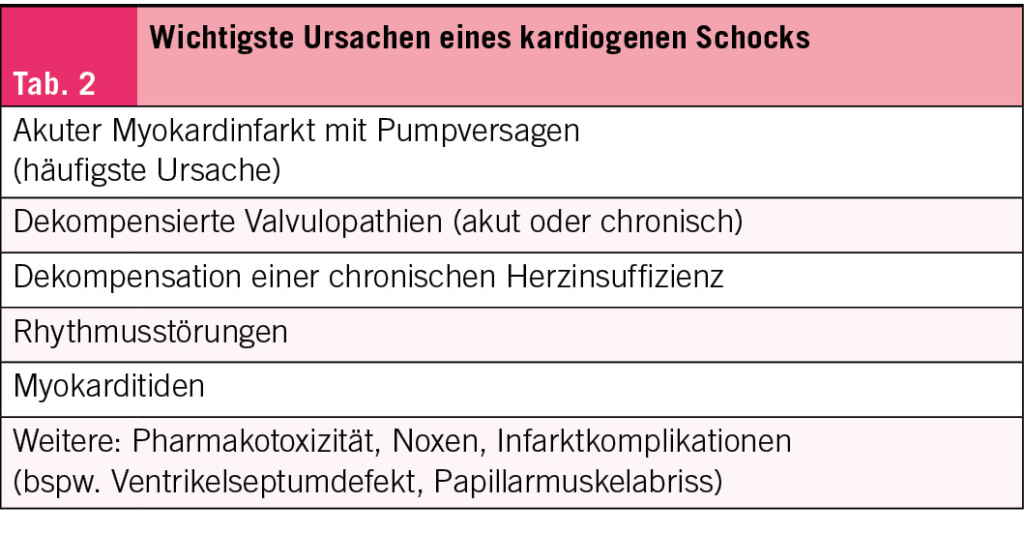
Die Ätiologie des kardiogenen Schocks ist vielfältig (Tab. 2) und die Diagnose kann gerade bei seltenen, schwer diagnostizierbaren Ätiologien verspätet oder gar nie gestellt werden, was zu Verzögerungen oder gar einer Unmöglichkeit der kausalen Behandlung führt.
Exkurs: Kardiogener Schock im Rahmen eines akuten Myokardinfarkts
Die häufigste Ursache des kardiogenen Schocks ist der akute Myokardinfarkt mit Pumpversagen aufgrund der Myokardischämie. Der kardiogene Schock kompliziert 5-10% der akuten Myokardinfarkte und ist die häufigste Todesursache bei dieser Patientenpopulation. Die massgebliche Studie «SHould we emergently revascularize Occluded Coronaries for cardiogenic shocK (SHOCK)» wurde noch vor der Jahrtausendwende- im Jahr 1999- publiziert und zeigte einen signifikanten Überlebensvorteil nach 6 Monaten (Mortalität von 50.3% in der Revaskularisationsgruppe, versus 63.1% in der Kontrollgruppe (p = 0.027) (4). Dieser Vorteil hielt auch nach 6 Jahren weiter an (5). Die perkutane Revaskularisation wird heute routinemässig angewendet und ist breit verfügbar.
Die Mortalität bleibt aber trotz Revaskularisation hoch (um die 50%) und verblieb seit Beginn der 2000-er Jahre trotz der routinemässigen Anwendung neuer Technologien und zahlreichen Studien auf diesem Niveau.
Neben der Heterogenität dieser Population ist auch die hohe Rate an mechanisch reanimierten Patienten mit überwiegend neurologischem, und nicht kardial bedingtem Tod ursächlich für die persistierend hohe Mortalität des kardiogenen Schocks. Eine erste nachweisliche Mortalitätsreduktion gelang erst dieses Jahr. Dies nach Jahren an negativen Studien im Bereich der mechanischen Kreislaufunterstützung, auf welche wir weiter unten eingehen.
Andere Schockursachen als der Myokardinfarkt bedürfen zur Ursachenbehandlung beispielsweise:
- Eine notfallmässige herzchirurgische oder ggf perkutane Behandlung (z. B. bei gewissen Klappenvitien)
- Eine Immunsuppression (z. B. bei Riesenzellmyokarditis oder der kardialen Sarkoidose)
- Eine Elektrokonversion (z. B. kreislaufrelevante Kammertachykardie)
Folgende Schocks werden oft fälschlicherweise als kardiogen beurteilt, fallen jedoch in die Kategorie der obstruktiven Schocks und sollten entsprechend primär mittels Desobstruktion behandelt werden:
- Lungenembolie: Aufhebung der Obstruktion mittels Lyse (systemische Lyse oder- bei hämodynamisch zumindest knapp stabilen Patienten- die EKOS-Lyse (ultraschallverstärkte Katheterthrombolyse))oder chirurgische/interventionelle Thrombektomie. Daneben ist stets eine Antikoagulation nötig
- Perikardtamponade: Perikardpunktion zur Entlastung des Perikards und Ermöglichung der Entfaltung der Herzhöhlen
Kreislaufstabilisierung
Die rasche Kreislaufunterstützung ist nebst der Behandlung der Ursache des kardiogenen Schocks wichtig, um ein lebensbedrohliches Multiorganversagen zu verhindern. Grundsätzlich bieten sich in der Akutsituation zwei Optionen, die auch kombiniert werden können:
a) die pharmakologische Therapie
b) die temporäre mechanische Kreislaufunterstützung
Die Kombination dieser beiden Optionen, und in fortgeschrittenen Schockstadien sogar die Kombination von mehreren Vasoaktiva/Inotropika mit mehreren mechanischen Unterstützungssystemen ist möglich, wenn auch (naturgemäss aufgrund der Erkrankungsschwere) mit einer höheren Mortalität vergesellschaftet (6).
A. Pharmakologische Therapie des kardiogenen Schocks
Die pharmakologische Behandlung mittels Vasoaktiva wird in > 90 % der Patienten notwendig. Gleichzeitig gibt es keine Evidenz, welche Wirkstoffklasse in der jeweiligen Situation überlegen ist (7).
Die Therapie richtet sich überwiegend nach pathophysiologischen Überlegungen und in Abwägung mit den Nebenwirkungen.
Grundsätzlich liegt der Zweck einer pharmakologischen Therapie in der Verbesserung der Sauerstoffversorgung des Gewebes. Dies geht- in unterschiedlichem Ausmass je nach Typ und Dosis des Wirkstoffs- auf Kosten eines erhöhten myokardialen Sauerstoffverbrauchs einher. Dies kann zu einem Missverhältnis zwischen Sauerstoffangebot und –bedarf der Kardiomyozyten führen, was die myokardiale Funktion weiter beansprucht und Verletzungen im kontraktilen Apparat verstärken, und die Regeneration aufhalten kann (8).
Vasoaktiva können in folgende vier Kategorien eingeteilt werden:
1. Vasopressoren
Typische Vertreter: Noradrenalin, Phenylephrin, (Vasopressin, Dopamin → kaum mehr angewendet).
Verbessert die Gewebeperfusion durch Steigerung des systemischen Widerstands und damit dem Perfusionsdruck. Nebeneffekt: Nachlasterhöhung für den linken Ventrikel, was je nach Ausmass bei Linksherzinsuffizienz zu einer relevanten Reduktion des Schlagvolumens führen kann und das Remodeling verstärkt.
Anwendungsbereich (Beispiele):
- Vor einer Revaskularisation beim akuten Myokardinfarkt mit Hypotonie, um die Koronarperfusion aufrechtzuerhalten. Dies zu Ungunsten der peripheren Sauerstoffversorgung, was in Anbetracht von Nutzen und Risiken in Kauf genommen wird. Man merke deswegen: Primär Noradrenalingabe bei Hypotonie während des Transports ins Herzkatheterlabor.
- Korrektur bei schwerer Hypotonie im Rahmen einer Therapie mit Inodilatatoren
2. Inotropika
Typische Vertreter: Dobutamin, Adrenalin.
Erhöhen das Herzminutenvolumen durch Steigerung der myokardialen Kontraktilität (= Inotropie) und oft auch der Herzfrequenz.
Grössten Einfluss auf den myokardialen Sauerstoffverbrauch hat die Herzfrequenz; einen geringeren Einfluss haben Kontraktilität und Wandspannung. Dobutamin wird Adrenalin wegen des geringeren Herzfrequenzanstiegs aus diesem Grund oft der Vorzug gegeben.
Anwendungsbereich (Beispiele):
Linksherz-Pumpversagen mit dem Ziel, das Herzminutenvolumen zu steigern (und nicht primär die Hypotonie zu korrigieren).
3. Inodilatatoren
Typische Vertreter: Levosimendan, Phosphodiesterasehemmer (= Milrinon) und in tiefer Dosierung Dobutamin (in hoher Dosierung wirkt Dobutamin vasokonstriktiv).
Weisen eine Kombination von Inotropika und Vasodilatatoren auf. Sie steigern die Kontraktilität und vermindern den systemischen Widerstand durch eine Vasodilatation. Achtung: Milrinon sollte nicht generell beim ischämisch bedingten kardiogenen Schock angewendet werden und ist dort mit einer erhöhten Mortalität assoziiert (9).
Anwendungsbereich (Beispiele):
- Linksherz-Pumpversagen mit dem Ziel, nebst der Inotropie die Nachlast zu senken (kardioprotektiver Effekt)
4. Vasodilatatoren
Typische Vertreter zur intravenösen Gabe: Nitratverbindungen (Nitroprussid, Nitroglyzerin)
Wirken vasodilatierend. Je nach Wirkstoff mit überwiegendem Effekt auf die präkapillären Arteriolen, was vor allem zur Nachlastsenkung führt.
Anwendungsbereich (Beispiele):
Linksherz-Pumpversagen bei arterieller Hypertonie, hypertensives Lungenödem.
Exkurs zum Levosimendan
Levosimendan ist anders als Dobutamin, Noradrenalin oder Adrenalin kein (künstliches oder echtes) Katecholamin, sondern ein Calcium-Sensitizer. Die Inotropie des Herzens wird durch eine Ca2+-Sensibilisierung der kontraktilen Proteine im Zellinneren erreicht, und die Nachlast durch eine K+-Kanal-vermittelte Vasodilatation und Phosphodiesterase-III-Inhibition gesenkt.
Vorteile am Levosimendan sind unter anderem:
- lange Halbwertszeit (Wirkungsdauer 10-14 Tage nach Beendigung der Infusion)
- der myokardiale Sauerstoffverbrach wird nicht erhöht
- die Wirksamkeit ist auch gegeben bei Patienten, die noch unter Betablocker stehen
In der Praxis wird anhand des klinischen Bildes und der verfügbaren Vitalparametern abgeschätzt, was das Therapieziel ist, um dann gezielt eine Therapie einzuleiten.
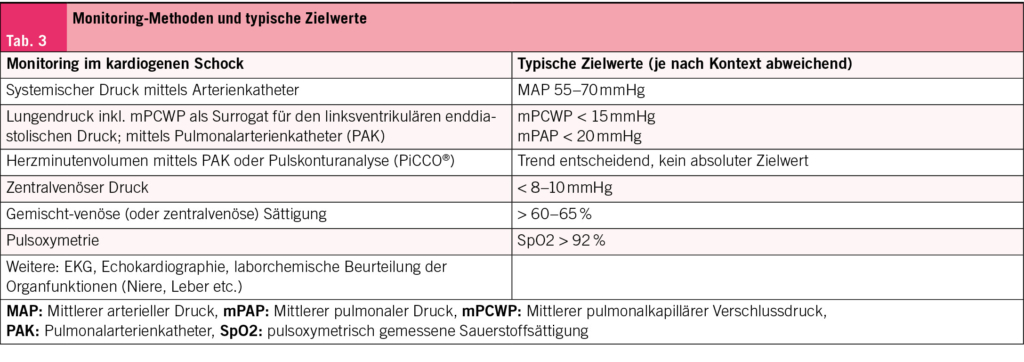
Der Einsatz eines adäquaten Monitorings ist also zentral, auch wenn hierfür die Evidenz fehlt und der Umfang häufig von den Gewohnheiten der jeweiligen Institution abhängt. Tabelle 3 gibt einen Überblick über die verfügbaren und oft angewendeten Methoden sowie einen typischen Zielbereich. Die angestrebten Zielwerte sind im Alltag aber je nach hämodynamischer Situation individuell festzulegen und variieren beträchtlich, wie folgende zwei Beispiele veranschaulichen:
Beispiel 1:
Kardiogener Schock bei akut dekompensierter Mitralinsuffizienz (bspw. flail leaflet bei Sehnenfadenabriss)
Beispiel 2:
Kardiogener Schock bei schwerer dekompensierter Aortenstenose vom Typ high gradient
Während den beiden Beispielen die rasche (chirurgische oder perkutane) Sanierung des Klappenvitiums gemeinsam ist, so sind die hämodynamischen Ziele bis zu dem Zeitpunkt abweichend:
Bei der Mitralinsuffizienz (Beispiel 1) steht die maximale Nachlastsenkung im Vordergrund. Und zwar mit einem Zielwert, der möglichst tief angesetzt wird und durch eine periphere Vasodilatation erreicht wird (das Ziel kann durchaus einem arteriellen Mitteldruck von 55mmHg oder tiefer entsprechen). Dies, um den Vorwärtsfluss zu steigern.
Bei der schweren high gradient Aortenstenose (Beispiel 2) ist die Nachlast weitestgehend fixiert und entspricht im Wesentlichen dem Widerstand durch die Aortenstenose. Eine Senkung des peripheren Widerstands reduziert die Nachlast daher nicht, sondern führt bei systemischer Hypotonie in Verbindung mit einem hohen linksventrikulären Füllungsdruck u.a. zu einer Abnahme des koronaren Perfusionsdrucks bis auf kritische Werte, was zu einer myokardialen Globalischämie führen kann (mit deletären Folgen). Auch eine Hypotonie durch Vorlastsenkung kann durch Abnahme des Schlagvolumens zur kaum reversiblen Kreislaufinsuffizienz führen (Tab. 3).
B. Temporäre mechanische Kreislaufunterstützung
Bei der Behandlung des kardiogenen Schocks geht es einerseits um die Aufrechterhaltung der Endorganfunktionen durch Verbesserung der Gewebeperfusion, und andererseits sollten die Therapien die bereits strapazierte kardiale Funktion nicht weiter belasten.
Genau dies widerspricht sich bei der pharmakologischen Therapie im kardiogenen Schock in aller Regel, wie im vorherigen Abschnitt zur vasoaktiven Therapie dargestellt. Wenn immer möglich soll zur kardialen Protektion die Dauer der Vasoaktivatherapie also nicht länger als absolut nötig verabreicht werden (Ausnahme: whs. Levosimendan). Eine Ergänzung oder Alternative zur pharmakologischen Therapie stellt die mechanische Kreislaufunterstützung dar, welche die Funktion des Herzens – und je nach Wahl des Gerätes – auch der Lunge übernehmen kann.
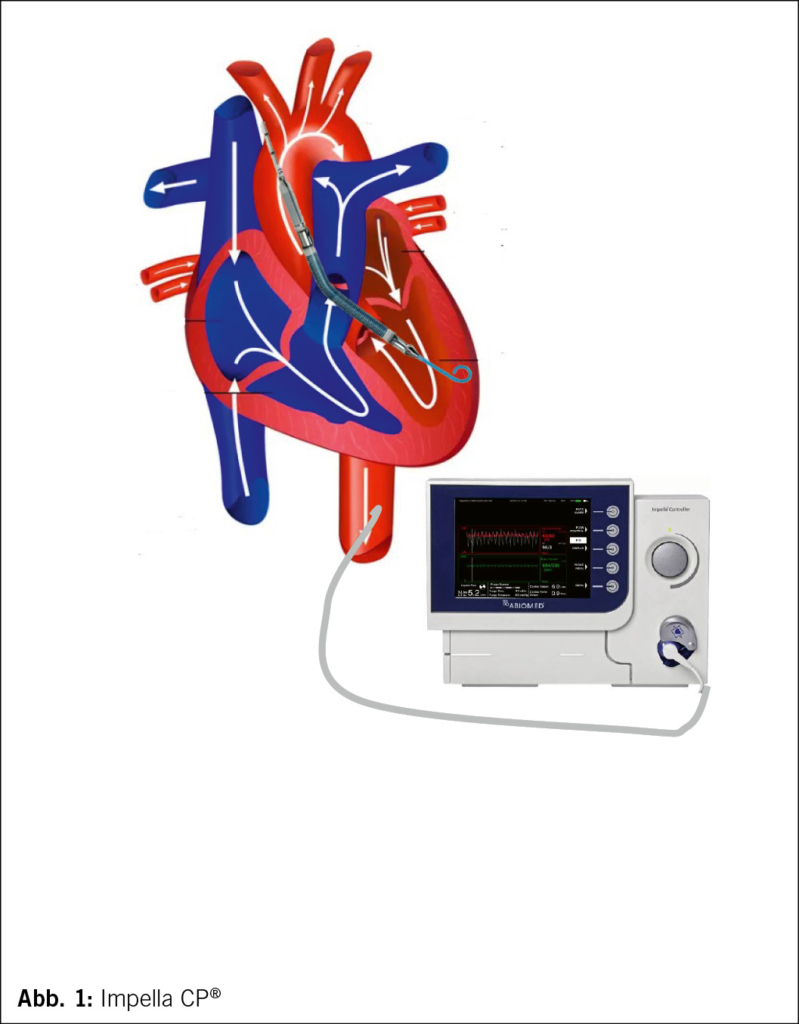
Ob eine solche Kreislaufunterstützung auch eine kardioprotektive Wirkung hat, hängt von der Wahl des Gerätes ab: Das Linksherzunterstützungssystem «Impella®» (schematisch dargestellt in Bild 1) befördert als Mikroaxialpumpe das Blut vom linken Ventrikel in die Aorta ascendens und entlastet somit den linken Ventrikel. So kann der Vasoaktivabedarf gering gehalten werden oder gar unnötig bleiben. Es wird sogar angestrebt, bereits eine konventionelle Herzinsuffizienztherapie unter laufender Kreislaufunterstützung zu beginnen (mittels SGLT-2-Inhibitor, ACE-Inhibitor/AR(N)I, Mineralokortikoidantagonist und verzögert Betablocker).
Bei einem mutmasslich grossen Myokardschaden (wie beispielsweise beim ausgedehnten Vorderwandinfarkt) empfiehlt sich die Gabe von Levosimendan als unterstützende Massnahme. Die lange Wirkungsdauer von bis zu 2 Wochen kann genutzt werden, um auch beim hämodynamisch instabilen Patienten langsam eine Herzinsuffizienztherapie einzuleiten, um die Entwöhnung zu erleichtern (Abb. 1).
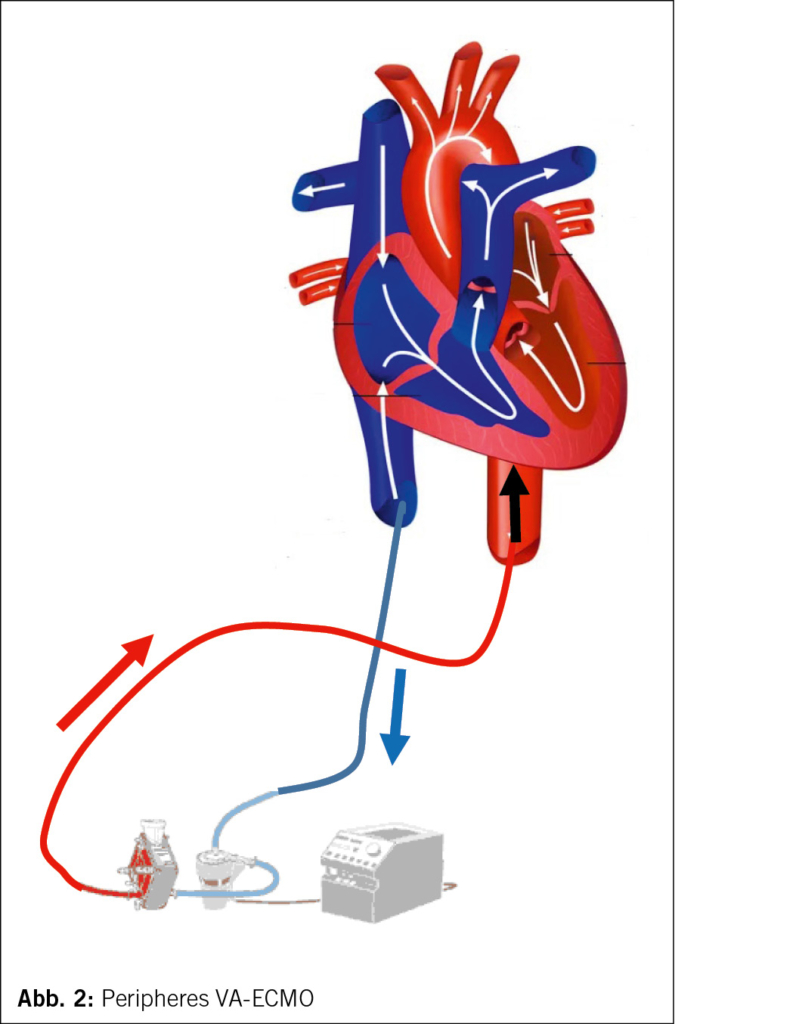
Eine andere hämodynamische Wirkung erzielt die Anwendung der veno-arteriellen ECMO oder ECLS («extrakorporale Membranoxygenierung» oder «extrakorporaler Life Support»), schematisch dargestellt in Bild 2. Das Blut wird über einen venösen Schenkel mittels Zentrifugalpumpe durch einen Membranoxygenator geleitet, wo es zum Gasaustausch kommt. Das sauerstoffreiche Blut wird dann über den arteriellen Schenkel dem Körper zugeführt.
Bei der gängigsten (peripheren) Anlage des VA-ECMO kommen die Schleusen femoral-venös und femoral-arteriell zu liegen. Die drainierende venöse Schleuse ist lang und reicht bis in den rechten Vorhof. Anders die zurückführende arterielle Schleuse: Diese ist kurz und gibt das Blut bereits auf Höhe der Aorta abdominalis ab. Das Blut fliesst entsprechend körperaufwärts und somit in umgekehrter Richtung als dies physiologischerweise der Fall ist.
Das Myokard wird damit, anders als bei der Impella®, nicht entlastet, sondern durch diese Nachlasterhöhung belastet. Bei eingeschränkter Myokardfunktion und hohem Fluss über das VA-ECMO ist der linke Ventrikel oft nicht mehr fähig den Aortendruck zu generieren, womit die Aortenklappe geschlossen bleibt. Dies führt zu einer Blutstase im gesamten Lungengefässbett, im linken Vorhof, linken Ventrikel und in der Aortenwurzel. Bleibt dieser Zustand über Stunden bestehen, sind die Folgen verheerend: Es kommt zu einer kompletten Thrombosierung und die Wiederaufnahme eines physiologischen Flusses wird verunmöglicht (Abb. 2).
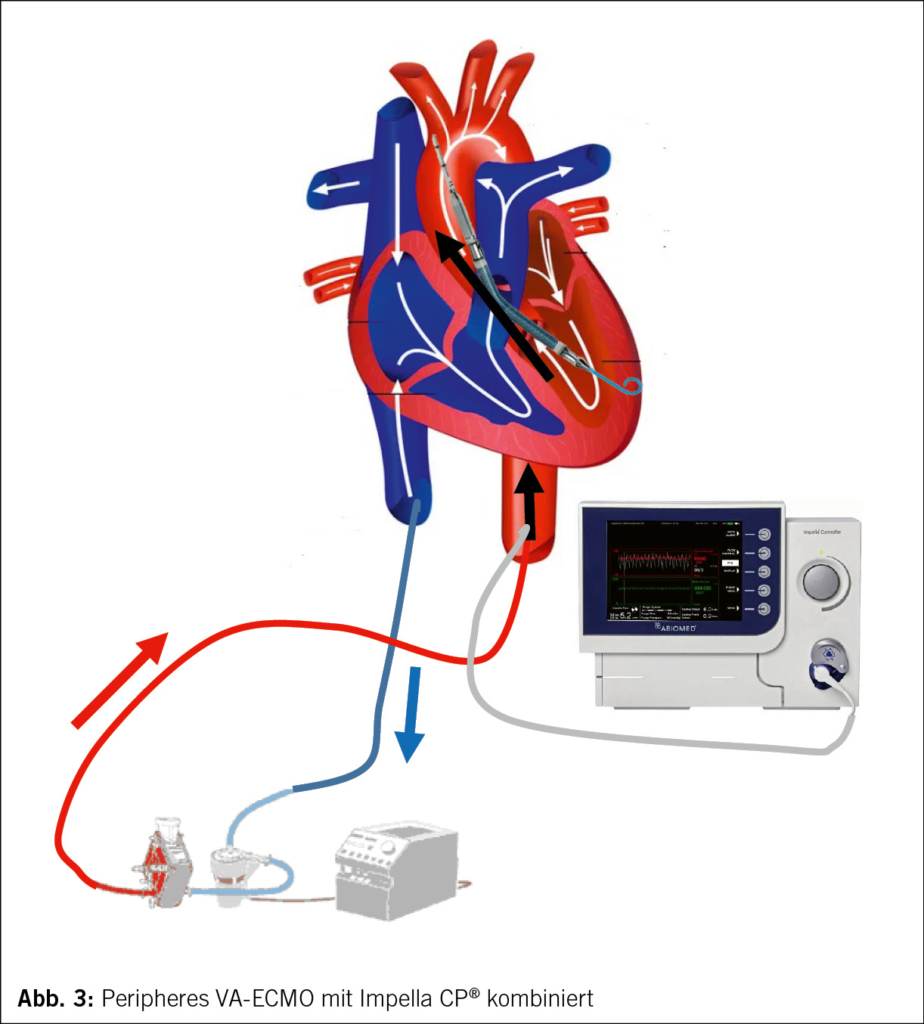
Durch eine Entlastung des linken Ventrikels- typischerweise mittels zusätzlicher Einlage einer Impella®– lässt sich die Stase durch den kontinuierlichen Abfluss des linken Ventrikels und Wiederherstellung eines zumindest minimalen physiologischen Flusses über die Pulmonalgefässe vermeiden (schematisch dargestellt in Abb. 3).
Das Ziel ist auch bei dieser Gerätekombination die sequentielle Entwöhnung. Aus naheliegenden Gründen wird in der Situation des kardiogenen Schocks mit Linksherzinsuffizienz in aller Regel versucht einen physiologischen Zustand zu erreichen, in dem zuerst die v-a- ECMO und in einem zweiten Schritt die Impella entfernt wird.
Wird angenommen, dass eine Linksherzunterstützung (Impella®) über eine längere Zeit nötig sein wird (entweder zur Erholung des Myokards oder zur neurologischen Beurteilung bei komatösen Patienten), so steht mit der «Impella 5.5®» eine axillär implantierbare Pumpe mit grösserer Förderleistung zur Verfügung (maximal 5.5 L/min im Vergleich zur Impella CP® mit maximal 3.8 L/min). Die Einlage erfolgt über einen axillären Zugang und ermöglicht anders als bei femoral eingelegten Systemen die Mobilisation der Patienten.
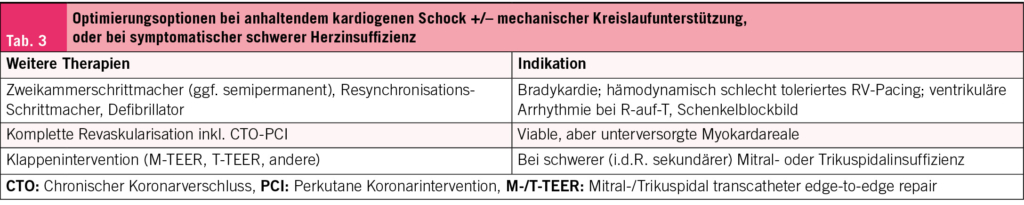
Zusätzliche Therapien können weiters eine Entwöhnung ermöglichen, oder bei schwer herzinsuffizienten Patienten auch ohne temporäre Kreislaufunterstützung zur Optimierung angewendet werden (Tab. 4).
Weitere Therapien, die im kardiogenen Schock häufig angewendet werden, sind die Beatmung (nicht-invasive und mechanische Beatmung), wobei die positive Druckbeatmung zu einer Nachlastsenkung für den linken Ventrikel, und einer Nachlasterhöhung für den rechten Ventrikel führt. Zudem kommen additive Therapien bei Endorganschäden zur Anwendung, wie die Hämodiafiltration beim akuten Nierenversagen.
Lässt sich eine schwere Herzinsuffizienz oder ein kardiogener Schock auch unter den oben beschriebenen Therapien nicht mindestens so weit beheben, dass es zu einer genügenden Endorganperfusion und akzeptablen Lebensqualität kommt, so soll frühzeitig eruiert werden, ob Patienten für eine fortgeschrittene Herzinsuffizienztherapie in Frage kommen. Hierbei kommt als klassische Therapie der «fortgeschrittenen Herzinsuffizienz» ein linksventrikuläres Unterstützungsdevice (LVAD) und/oder die Herztransplantation in Frage.
Es versteht sich von selbst, dass nicht alle Patienten im kardiogenen Schock von diesen fortgeschrittenenen Therapieoptionen profitieren. Sei es wegen der Gesamtsituation mit refraktärem Multiorganversagen, relevanten Nebenerkrankungen oder fortgeschrittenem Alter.
Es empfiehlt sich, in solchen Fällen frühzeitig den Patienten und Angehörigen eine psychologische Unterstützung anzubieten und Palliativgespräche einzuleiten.
Studienlage zur temporären Kreislaufunterstützung
Die Behandlung von Patienten mit Bedarf einer mechanischen Kreislaufunterstützung sind mit einem enormen personellen, monetären und infrastrukturellen Aufwand verbunden und berechtigterweise stellt sich die Frage nach der Evidenz, die dieses Vorgehen rechtfertigt.
Es lohnt sich ein kritischer Blick auf die aktuelle Studienlage, wobei wir uns hier auf die relevantesten beschränken:
Eine erste grosse randomisierte Studie untersuchte den Nutzen der intraaortalen Ballonpumpe (IABP)- der historisch gesehen ersten perkutanen Kreislaufunterstützung:
In der «IABP-Shock II»-Studie wurden 600 Patienten (45% reanimierte Patienten) mit Myokardinfarkt und kardiogenem Schock (AMICS: «acute myocardial infarction complicated by cardiogenic shock») eingeschlossen und 1:1 randomisiert zur Standardtherapie versus IABP plus Standardtherapie: Die Einlage der IABP zusätzlich zur frühen Revaskularisation und optimalen medikamentösen Therapie führte zu keiner Reduktion der Gesamtmortalität (welche sowohl den neurologisch bedingten, als auch den kardialen Tod einschliesst) (10). Diese und weitere kleinere negative Studien führte zu einer Klasse III Empfehlung (= nicht routinemässig empfohlen) der IABP.
Im August 2023 wurden die Ergebnisse der ECLS-SHOCK II Studie veröffentlicht, wo 420 Patienten mit AMICS 1:1 randomisiert wurden zu VA-ECMO-Einlage zusätzlich zur Standardtherapie, oder alleinige Standardtherapie. Die übliche Behandlung- insbesondere die Revaskularisation- wurde bei allen Patienten rasch durchgeführt. Auch diese Studie fiel negativ aus: Es ergab sich kein Vorteil in Bezug auf die Gesamtmortalität nach 30 Tagen (11). Auffallend war auch in dieser Studie der hohe Anteil an Patienten, die reanimiert wurden (knapp 80%, mit einer mittleren Reanimationsdauer von 20 Minuten).
In der rezentesten Studie im Bereich der temporären Kreislaufunterstützung bei AMICS, der im April dieses Jahres publizierten «DanGer Shock» -Studie, wurde im experimentellen Arm eine Impella® implantiert (355 Patienten, 1:1 Randomisierung). Anders als bei den beiden vorgenannten Studien wurden hier sämtliche Patienten, welche nach einer Reanimation keinen Glasgow coma scale von 9 oder höher erreichten, ausgeschlossen. Durch dieses Ausschlusskriterium gelang es, den Störfaktor des neurologisch bedingten Todes weitestgehend zu eliminieren.
Und die routinemässige Anwendung einer Impella® zusätzlich zur Standardbehandlung erwies sich in diesem Patientenkollektiv als nützlich: Das Überleben konnte im Interventionsarm um über 10% erhöht werden (Gesamtmortalität nach 6 Monaten in der «Impella®-Gruppe» 45.8%, versus 58.5% in der Standardgruppe; HR 0.74, P = 0.04). Ein solch klares Zeichen für einen therapeutischen Nutzen einer Therapie bei Patienten mit AMICS gab es seit der «SHOCK»-Studie zur Revaskularisation bei AMICS um die Jahrtausendwende nicht mehr und stimmt zuversichtlich.
Die Anwendung temporärer Kreislaufunterstützungen hat aber – so hoffnungsvoll ihr hämodynamischer Nutzen im korrekt ausgewählten Patientenkollektiv auch sei – auch negative Auswirkungen: so kommt es häufig zu Komplikationen wie Blutungen im Bereich der Punktionsstelle, Beinischämie oder Hämolyse. Die Prävention, rasche Erkennung und Behebung solcher Ereignisse ist von grosser Wichtigkeit und bestimmt mitunter den weiteren Verlauf.
In den Richtlinien der europäischen Gesellschaft für Kardiologie (ESC) wurde die temporäre Kreislaufunterstützung (die klar nicht mehr routinemässig empfohlene IABP ausgenommen) in den 2021 erschienenen Herzinsuffizienzrichtlinien mit einer Klasse IIa Empfehlung versetzt («sollte in Betracht gezogen werden») (12). In den 2023 erschienenen Guidelines für akutes Koronarsyndrom wurde eine IIb-Empfehlung ausgesprochen («kann in Betracht gezogen werden») (13).
Diese Empfehlungen stammen aus einer Zeit vor Veröffentlichung der DanGer-Studie. Damals konnte noch keine Studie einen klaren Nutzen hinsichtlich Mortalitätsreduktion zeigen.
Dies unterstreicht die Tatsache, dass es in der Behandlung des kardiogenen Schocks legitim ist, die Therapie nach pathophysiologischen Überlegungen zu steuern. Die Durchführung von aussagekräftigen Studien in diesem heterogenen, schwer kranken Patientenkollektiv ist derart erschwert, dass dies wohl auch in den kommenden Jahren so bleiben wird.
Copyright Aerzteverlag medinfo AG
Inselspital, Universitätsspital Bern
Universitätsklinik für Kardiologie
Herz Gefäss Zentrum
Freiburgstrasse 20
3010 Bern
Inselspital, Universitätsspital Bern
Universitätsklinik für Kardiologie
Herz Gefäss Zentrum
Freiburgstrasse 20
3010 Bern
Inselspital, Universitätsspital Bern
Universitätsklinik für Kardiologie
Herz Gefäss Zentrum
Freiburgstrasse 20
3010 Bern
Die Autoren haben keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
Die Behandlung des kardiogenen Schocks bleibt auch heutzutage eine Herausforderung. Evidenzbasierte Handlungsanweisungen gibt es weder für die pharmakologische Therapie noch bis vor kurzem für die mechanische Kreislaufunterstützung, was aber nicht mit Sinnlosigkeit der Behandlung gleichzusetzen ist. Vielmehr spielt Erfahrung, interdisziplinäre Zusammenarbeit und vor allem der Einbezug pathophysiologischer Überlegungen eine grosse Rolle zur erfolgreichen Behandlung dieser Patienten.
1. Baran DA, Grines CL, Bailey S, Burkhoff D, Hall SA, Henry TD, Hollenberg SM, Kapur NK, O’Neill W, Ornato JP, Stelling K, Thiele H, Diepen S van, Naidu SS. SCAI clinical expert consensus statement on the classification of cardiogenic shock: This document was endorsed by the American College of Cardiology (ACC), the American Heart Association (AHA), the Society of Critical Care Medicine (SCCM), and the Society of Thoracic Surgeons (STS) in April 2019. Catheter Cardiovasc Interv Off J Soc Card Angiogr Interv 2019.
2. Jentzer JC, Diepen S van, Barsness GW, Henry TD, Menon V, Rihal CS, Naidu SS, Baran DA. Cardiogenic Shock Classification to Predict Mortality in the Cardiac Intensive Care Unit. J Am Coll Cardiol 2019;74:2117–2128.
3. Naidu SS, Baran DA, Jentzer JC, Hollenberg SM, Diepen S van, Basir MB, Grines CL, Diercks DB, Hall S, Kapur NK, Kent W, Rao SV, Samsky MD, Thiele H, Truesdell AG, Henry TD. SCAI SHOCK Stage Classification Expert Consensus Update: A Review and Incorporation of Validation Studies: This statement was endorsed by the American College of Cardiology (ACC), American College of Emergency Physicians (ACEP), American Heart Association (AHA), European Society of Cardiology (ESC) Association for Acute Cardiovascular Care (ACVC), International Society for Heart and Lung Transplantation (ISHLT), Society of Critical Care Medicine (SCCM), and Society of Thoracic Surgeons (STS) in December 2021. J Am Coll Cardiol 2022;79:933–946.
4. Hochman JS, Sleeper LA, Webb JG, Sanborn TA, White HD, Talley JD, Buller CE, Jacobs AK, Slater JN, Col J, McKinlay SM, LeJemtel TH. Early revascularization in acute myocardial infarction complicated by cardiogenic shock. SHOCK Investigators. Should We Emergently Revascularize Occluded Coronaries for Cardiogenic Shock. N Engl J Med 1999;341:625–634.
5. Hochman JS, Sleeper LA, Webb JG, Dzavik V, Buller CE, Aylward P, Col J, White HD, SHOCK Investigators. Early revascularization and long-term survival in cardiogenic shock complicating acute myocardial infarction. JAMA 2006;295:2511–2515.
6. Basir MB, Schreiber TL, Grines CL, Dixon SR, Moses JW, Maini BS, Khandelwal AK, Ohman EM, O’Neill WW. Effect of Early Initiation of Mechanical Circulatory Support on Survival in Cardiogenic Shock. Am J Cardiol 2017;119:845–851.
7. Bloom JE, Chan W, Kaye DM, Stub D. State of Shock: Contemporary Vasopressor and Inotrope Use in Cardiogenic Shock. J Am Heart Assoc 2023;12:e029787.
8. Duncker DJ, Bache RJ. Regulation of coronary blood flow during exercise. Physiol Rev 2008;88:1009–1086.
9. Felker GM, Benza RL, Chandler AB, Leimberger JD, Cuffe MS, Califf RM, Gheorghiade M, O’Connor CM, OPTIME-CHF Investigators. Heart failure etiology and response to milrinone in decompensated heart failure: results from the OPTIME-CHF study. J Am Coll Cardiol 2003;41:997–1003.
10. Thiele H, Zeymer U, Neumann F-J, Ferenc M, Olbrich H-G, Hausleiter J, Waha A de, Richardt G, Hennersdorf M, Empen K, Fuernau G, Desch S, Eitel I, Hambrecht R, Lauer B, Böhm M, Ebelt H, Schneider S, Werdan K, Schuler G, Intraaortic Balloon Pump in cardiogenic shock II (IABP-SHOCK II) trial investigators. Intra-aortic balloon counterpulsation in acute myocardial infarction complicated by cardiogenic shock (IABP-SHOCK II): final 12 month results of a randomised, open-label trial. Lancet Lond Engl 2013;382:1638–1645.
11. Thiele H, Zeymer U, Akin I, Behnes M, Rassaf T, Mahabadi AA, Lehmann R, Eitel I, Graf T, Seidler T, Schuster A, Skurk C, Duerschmied D, Clemmensen P, Hennersdorf M, Fichtlscherer S, Voigt I, Seyfarth M, John S, Ewen S, Linke A, Tigges E, Nordbeck P, Bruch L, Jung C, Franz J, Lauten P, Goslar T, Feistritzer H-J, Pöss J, Kirchhof E, Ouarrak T, Schneider S, Desch S, Freund A, ECLS-SHOCK Investigators. Extracorporeal Life Support in Infarct-Related Cardiogenic Shock. N Engl J Med 2023;389:1286–1297.
12. McDonagh TA, Metra M, Adamo M, Gardner RS, Baumbach A, Böhm M, Burri H, Butler J, Čelutkienė J, Chioncel O, Cleland JGF, Coats AJS, Crespo-Leiro MG, Farmakis D, Gilard M, Heymans S, Hoes AW, Jaarsma T, Jankowska EA, Lainscak M, Lam CSP, Lyon AR, McMurray JJV, Mebazaa A, Mindham R, Muneretto C, Francesco Piepoli M, Price S, Rosano GMC, Ruschitzka F, Kathrine Skibelund A, ESC Scientific Document Group. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J 2021;42:3599–3726.
13. Byrne RA, Rossello X, Coughlan JJ, Barbato E, Berry C, Chieffo A, Claeys MJ, Dan G-A, Dweck MR, Galbraith M, Gilard M, Hinterbuchner L, Jankowska EA, Jüni P, Kimura T, Kunadian V, Leosdottir M, Lorusso R, Pedretti RFE, Rigopoulos AG, Rubini Gimenez M, Thiele H, Vranckx P, Wassmann S, Wenger NK, Ibanez B, ESC Scientific Document Group. [2023 ESC Guidelines for the management of acute coronary syndromes]. G Ital Cardiol 2006 2024;25:e1–e112.
info@herz+gefäss
- Vol. 14
- Ausgabe 5
- November 2024