- Der chronische Koronarverschluss – Wann und wie behandeln?
Der chronische Koronarversschluss wird bei bis zu 20 % der Patienten mit einer koronaren Herzkrankheit diagnostiziert und hat einen negativen Einfluss auf die Lebensqualität und Langzeitprognose. Die rasche Entwicklung der technischen Mittel in Kombination mit neuen Revaskularisationsstrategien in der perkutanen Behandlung von chronisch verschlossenen Herzkranzgefässen hat in erfahrenen Zentren zu einer Wiedereröffnungsrate von über 85 % geführt. Daher sollte sich die Patientenauswahl für eine solche Koronarintervention auf den zu erwartenden Patientennutzen und nicht auf die koronar-anatomische Komplexität konzentrieren.
Chronic coronary occlusion is diagnosed in up to 20 % of patients with coronary artery disease and has a negative impact on quality of life and long-term prognosis. The rapid development of technical means in combination with new revascularization strategies in the percutaneous treatment of chronically occluded coronary arteries has led to a reopening rate of more than 85 % in experienced centers. Therefore, patient selection for such coronary intervention should focus on expected patient benefit rather than coronary anatomic complexity.
Key Words: chronic total occlusion (CTO), revascularization
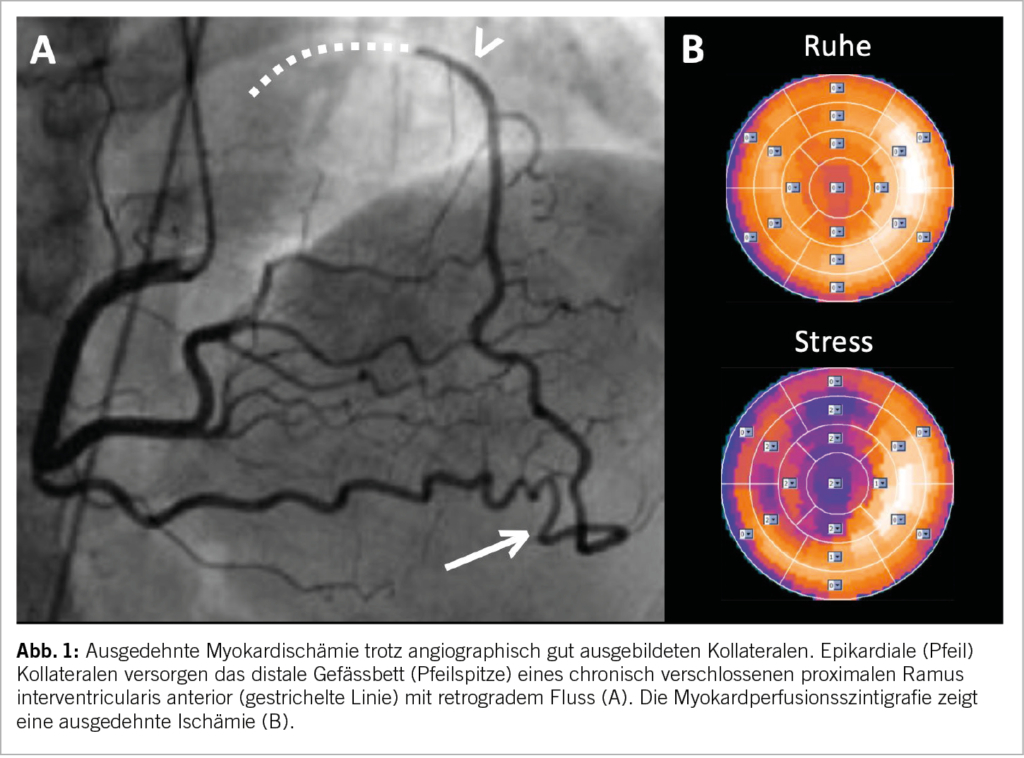
Der chronische totale Koronarverschluss (Chronic Total Occlusion oder CTO) ist definiert als ein vollständiger Verschluss einer Herzkranzarterie von mehr als drei Monaten. Bei der Mehrzahl der Patienten mit einer CTO ist der Verschluss das Ergebnis einer allmählichen Lumeneinengung, die eine Rekrutierung von Kollateralen distal an das verschlossene Gefäss ermöglicht und somit die Viabilität gewährleistet. Nicht-invasive und invasive Studien haben jedoch gezeigt, dass bei der überwiegenden Mehrheit auch angiographisch gut ausgebildete Kollateralen nicht ausreichen, um eine Ischämie zu verhindern (1, 2) (Abb. 1).
Klinische Präsentation des chronischen Koronarverschlusses
Bei symptomatischen CTO-Patienten stehen häufig Dyspnoe oder atypische Symptome wie Einschränkung der körperlichen Leistungsfähigkeit im Vordergrund (3). Angina pectoris ist ein spätes Symptom in der ischämischen Kaskade und kann auch bei ausgedehnter Myokardischämie fehlen. Einer von vier Patienten mit einer CTO ist asymptomatisch. Das Fehlen von Symptomen kann gelegentlich durch eine autonome Neuropathie bei Diabetikern oder durch eine allmähliche Gewöhnung an Beschwerden und Meidung bestimmter Angina pectoris auslösender Tätigkeiten erklärt werden.
Wem nützt die CTO-Revaskularisation?
Mehrere Beobachtungsstudien haben eine signifikante Symptomlinderung sowie eine verbesserte Lebensqualität und Leistungsfähigkeit nach erfolgreicher CTO-Revaskularisation gezeigt (4).
Kürzlich wurden die Ergebnisse der DECISION-CTO-Studie und der EURO-CTO-Studie veröffentlicht, welche als erste randomisierte Studien den klinischen Nutzen einer CTO-Revaskularisation gegenüber der alleinigen medikamentösen Behandlung untersucht haben (5, 6). In der DECISION-CTO-Studie war die 3-Jahres-Rate des kombinierten Endpunkts (Tod, Myokardinfarkt, Schlaganfall und jegliche Revaskularisation) zwischen der interventionell und der konservativ behandelten Gruppe gleich. Aufgrund der langsamen und unvollständigen Rekrutierung, der zusätzlichen Revaskularisation von nicht CTO-Koronarstenosen nach der Randomisierung in beiden Gruppen und der hohen Crossover-Rate in die Interventions-Gruppe (20 %) ist es schwierig, eindeutige Schlussfolgerungen aus dieser Studie zu ziehen. Im Gegensatz dazu zeigte die EURO-CTO-Studie einen signifikant verbesserten Gesundheitsstatus nach einem Jahr in der Interventions-Gruppe, während die Rate an schweren kardiovaskulären Ereignissen vergleichbar war. Gemäss den Leitlinien der Europäischen Gesellschaft für Kardiologie ist eine CTO-Revaskularisation auch bei asymptomatischen Patienten indiziert, sofern die Myokardischämie mehr als 10 % des linken Ventrikels umfasst (7). Letzteres basiert auf Beobachtungsstudien, welche auf einen prognostischen Vorteil der Revaskularisation bei Vorliegen einer allgemeinen Koronaren Herzkrankheit (nicht CTO-spezifisch) und einer grossen Ischämie hinweisen (8). Allerdings fehlen solide, randomisierte Studien, um diese Hypothese zu stützen.
Individuelle Nutzen-Risiko-Analyse der Revaskularisation
Nachdem angiographisch die Diagnose einer CTO gestellt wurde, stellt sich die Frage nach dem Nutzen-Risiko-Verhältnis einer Revaskularisation.
Untersuchungen belegen eine höhere Komplikationsrate durch CTO-Interventionen verglichen mit Nicht-CTO-Interventionen. Schwerwiegende, unerwünschte Ereignisse treten mit einer durchschnittlichen Rate von 3 % auf (9). Die Komplikationsrate nimmt mit dem Grad der anatomischen Komplexität zu und ist auch von der Art der erforderlichen Revaskularisationstechnik abhängig, sodass eine individuelle und kontinuierliche Nutzen-Risiko-Analyse unerlässlich ist. Eine «gute Indikation» zur Revaskularisation einer CTO ist eine therapierefraktäre Angina pectoris, welche den Alltag relevant beeinträchtigt. Bei asymptomatischen Patienten mit einer sogenannten stummen Ischämie, kann sich das Nutzen-Risiko-Verhältnis einer Revaskularisation abhängig von der anatomischen Komplexität in Richtung einer konservativen Behandlung verschieben.
Der Entscheid für eine perkutane oder chirurgische Revaskularisation basiert auf mehreren klinischen und anatomischen Merkmalen. Patienten mit Mehrgefässerkrankung, insbesondere in Kombination mit einem Diabetes mellitus, eingeschränkter Pumpfunktion und vertretbarem Operationsrisiko, sollten sich einer Bypass-Operation unterziehen, was die Langzeitprognose verglichen mit der perkutanen Koronarintervention verbessert (10, 11). Basierend auf den Leitlinien der Europäischen Gesellschaft für Kardiologie und Herzchirurgie empfehlen wir bei Patienten mit einem chronischen Koronarverschluss, speziell bei Vorliegen einer Mehrgefässerkrankung, eine individualisierte Nutzen-Risiko-Analyse durch ein interdisziplinäres Herz-Team durchzuführen. Diese Analyse umfasst klinische und angiographische Überlegungen, auf deren Grundlage schlussendlich die Entscheidung zur Art der Behandlung gefällt wird. Eine anschliessende, umfassende Aufklärung des Patienten in Bezug auf das Nutzen-Risiko-Verhältnis einer CTO-Revaskularisation ist unerlässlich, und somit sollte auch von ad-hoc CTO-Interventionen abgeraten werden.
Perkutane CTO-Intervention: Vorbereitung ist der Schlüssel
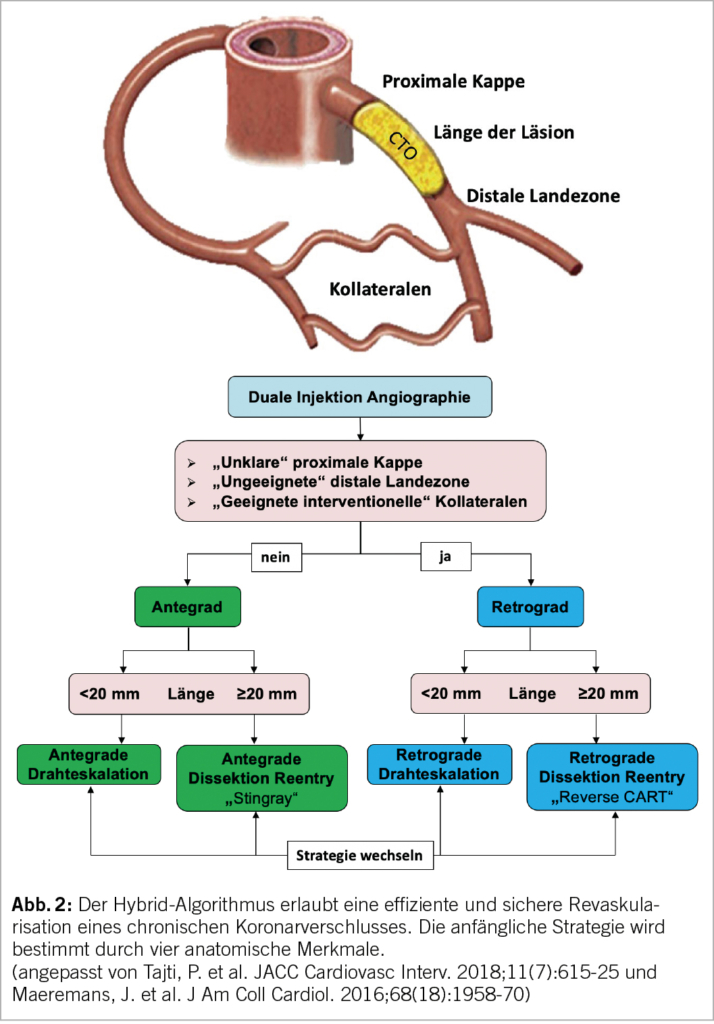
Sobald die Indikation zur CTO-Intervention gestellt wurde, sind die Planung und Vorbereitung des Eingriffs wesentliche Faktoren für den Erfolg der Revaskularisation. Ein doppelter arterieller Zugang wird empfohlen, da er eine duale Kontrastmittelinjektion und einen allfälligen retrograden Zugang ermöglicht (Abb. 2). Die duale Injektion erfolgt durch eine Kontrastmittelgabe in das Spendergefäss, gefolgt von einer zeitlich verzögerten Kontrastmittelinjektion in das CTO-Gefäss. Eine sorgfältige Beurteilung der CTO-Läsion und anderer anatomischer Merkmale ist für eine adäquate Planung des Eingriffs unerlässlich. Im Hybrid-Algorithmus bestimmen die vier folgenden angiographischen Merkmale die anfängliche Strategie: die proximale Kappe, die Länge der CTO-Läsion, die distale Landezone und die interventionelle Eignung der Kollateralen.
Interventionelle Revaskularisationstechnik
Antegrade Drahteskalation
Trotz angiographisch totalem Gefässverschluss zeigen histologische Präpararate oft Mikrokanäle innerhalb des Verschlusses, welche das wahre Lumen proximal und distal von der CTO verbinden.
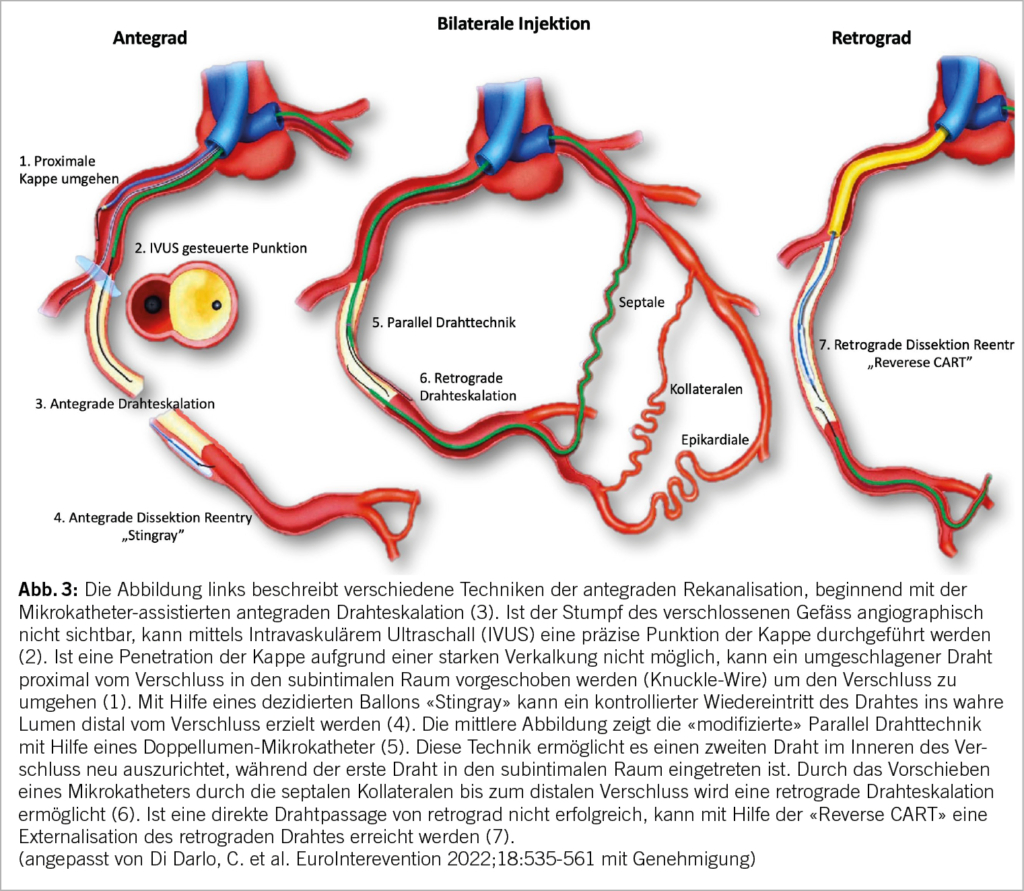
Diese Mikrokanäle finden sich häufig bei jüngeren und kürzeren Verschlüssen (<20mm) mit einer eindeutigen (vorzugsweise konischen) proximalen Kappe und einer guten distalen Landezone. Die Wahrscheinlichkeit, diese Läsion intraluminal passieren zu können, ist hoch und damit ein günstiger angiographischer Befund für eine sogenannte Antegrade Drahteskalations-Technik (Antegrade Wire-Escalation oder AWE, Abb. 3 Punkt 3). Bei der AWE ist die erste Drahtwahl in der Regel ein hydrophiler polymerbeschichteter Draht mit verjüngter Spitze und eher geringer Spitzenlast (<1 g) um die Mikrokanäle zu sondieren. Durch das Vorschieben eines Mikrokatheters bis kurz vor die Drahtspitze kann die Penetrationskraft und Steuerbarkeit des Drahtes entscheidend verbessert werden. Bei mangelndem Fortschritt sollte eine schrittweise Eskalation zu Drähten mit unterschiedlichen Eigenschaften erfolgen, bis eine erfolgreiche Drahtpassage erreicht oder die Strategie gewechselt wird. Bei unklarem, langem oder gewundenem Gefässverlauf wird ein hydrophiler Draht mit mässig hoher Spitzenlast bevorzugt, während im Falle einer kurzen verkalkten Strecke mit einem klaren Ziel ein steifer Draht mit hoher Spitzenlast (bis zu 40 g) für die direkte Penetration effizienter sein wird. Mit der retrograden Kontrastmittelinjektion in das Spendergefäss kann die korrekte intraluminale Drahtlage nach der Passage der CTO gesichert werden.
Rationale für einen retrograden Zugang
Retrograde Zugänge sind komplementäre Techniken zur AWE und haben zu einer deutlichen Steigerung der technischen Erfolgsraten geführt. Im Gegensatz zur distalen ist die proximale Kappe dem arteriellen Blutdruck ausgesetzt, was zu stärkerer Fibrosierung und Verkalkung führt. Somit ist die distale Kappe im Vergleich zur proximalen Kappe leichter zu durchbrechen. Die Okklusion kann mit der Retrograden Drahteskalation (Retrograde-Wire-Escalation oder RWE) Technik passiert werden (Abb. 3.6), ähnlich wie bei der AWE.
Retrograde Zugänge werden häufig bei CTO-Läsionen mit höherer anatomischer Komplexität eingesetzt und sind regelmässig der Schlüssel zur erfolgreichen Rekanalisation nach einem fehlgeschlagenen antegraden Eingriff. Im Allgemeinen führen jedoch retrograde Zugänge zu einer längeren Verfahrensdauer, einem höheren Strahlen- und Kontrastmittelbedarf sowie vermehrten periprozeduralen Komplikationen. Daher ist vor dem Wechsel zu einer retrograden Strategie eine erneute Risiko-Nutzen-Abwägung erforderlich. Septale Kollateralen sind häufig geeignete und sichere Wege, um das CTO-Gefäss von retrograd zu erreichen (Abb. 3). Ein grosser Vorteil der septalen Kollateralen ist, dass eine Perforation nicht zu einer Perikardtamponade führt, da das Blut in eine der Herzkammern auslaufen kann oder es ein meist selbstlimitierendes intraseptales Hämatom zur Folge hat. Die Verwendung einer epikardialen Kollaterale dagegen ist mit einer höheren Inzidenz von perinterventionellen Myokardinfarkten und Perikardtamponaden verbunden und stellt somit ein grösseres Interventionsrisiko dar.
Kontrollierte Gefässdissektion: der subintimale Raum
Mit einer kontrollierten Dissektion wird ein Kanal zwischen Intima und Media (subintimal) geschaffen und anschliessend die Gefässdurchgängigkeit mit einem Stent gewährleistet. Der Stent wird im Verlauf im «falschen Lumen» von Endothel überwachsen und zeigt im Allgemeinen ein gutes Langzeitergebnis. Diese Strategie basiert auf dem Prinzip des unterschiedlichen Widerstands zwischen den Gewebeebenen und nutzt die relative longitudinale Schwäche der subintimalen Ebene. Wenn der Führungsdraht in den subintimalen Raum eindringt, kann eine Dissektion-Reentry-Technik eingeleitet werden. Die hier am häufigsten verwendete Technik ist die reverse CART (kurz für Reverse Controlled-Antegrade-and-retrograde-subintimal-Tracking) Technik (Abb. 3.7). Bei dieser Technik werden sowohl mit einem antegraden als auch mit einem retrograden Führungsdraht benachbarte subintimale Dissektionsebenen um die CTO geschaffen und durch eine Ballondilatation über den antegraden Führungsdraht zu einem Raum verbunden. Anschliessend wird der retrograde Führungsdraht durch die von antegrad geschaffene Höhle geführt, bevor er wieder in das eigentliche Gefässlumen eintritt. Nach erfolgreicher retrograder Passage einer CTO folgt die Drahtexternalisierung, wobei ein geschlossenes System hergestellt wird, was anschliessend eine antegrade Koronarangioplastie ermöglicht.
Die Antegrade Dissektion-Reentry-Technik ist die subintimale Passage einer CTO in antegrader Weise mit Wiedereintritt des Drahtes in das distale wahre Gefässlumen (Abb. 3.1 und 3.4). Der kontrollierte Wiedereintritt wird mit dem Stingray-Ballonkatheter (Boston Scientific, Maple Grove, USA) erreicht, der für die Entfaltung im subintimalen Raum konzipiert ist.
Der Hybridalgorithmus
Der hybride perkutane Behandlungsalgorithmus bietet einen konsistenten und reproduzierbaren Ansatz, welcher einen flexiblen Wechsel von einer Technik zu einer anderen Technik ermöglicht (Abb. 2). Die Anwendung des hybriden Ansatzes in einem erfahrenen CTO-Interventions-Zentrum führt zu einer hohen Erfolgsrate mit vertretbarem Komplikationsrisiko.
Copyright bei Aerzteverlag medinfo AG
Oberarzt Kardiologie
Klinik für Kardiologie
Stadtspital Zürich Triemli
Leitender Arzt Kardiologie
Leiter Koronarinterventionen (spez. Komplexe Koronarinterventionen)
Klinik für Kardiologie
Stadtspital Zürich Triemli
Die Autoren haben keine Interessenkonflikte im Zusammenhang mit diesem Artikel deklariert.
◆ Die Revaskularisation von chronischen Koronarveschlüssen (CTO) führt zu Symptomlinderung und verbessert die Lebensqualität.
◆ Die Indikation für eine CTO-Intervention sollte sich am zu erwarteten klinischen Nutzen und nicht an der koronar-anatomischen Komplexität orientieren.
◆ Die Anwendung des Hybrid-Algorithmus zur Revaskularisation einer CTO erzielt in erfahrenen Zentren eine hohe technische Erfolgsrate mit akzeptabler Komplikationsrate.
with a chronic total occlusion and preserved left ventricular ejection fraction. Eur Heart J Cardiovasc Imaging. 2017;18(9):1025-1033.
- Werner GS, Surber R, Ferrari M, Fritzenwanger M, Figulla HR. The functional reserve of collaterals supplying long-term chronic total coronary occlusions in patients without prior myocardial infarction. Eur Heart J. 2006;27(20):2406-2412.
- Di Marco A, Anguera I, Teruel L, et al. Chronic total occlusion in an infarct-related coronary artery and the risk of appropriate ICD therapies. J Cardiovasc Electrophysiol. 2017;28(10):1169-1178.
- Christakopoulos GE, Christopoulos G, Carlino M, et al. Meta-analysis of clinical outcomes of patients who underwent percutaneous coronary interventions for chronic total occlusions. Am J Cardiol. 2015;115(10):1367-1375.
- Lee SW, Lee PH, Ahn JM, et al. Randomized Trial Evaluating Percutaneous Coronary Intervention for the Treatment of Chronic Total Occlusion. Circulation. 2019;139(14):1674-1683.
- Werner GS, Martin-Yuste V, Hildick-Smith D, et al. A randomized multicentre trial to compare revascularization with optimal medical therapy for the treatment of chronic total coronary occlusions. Eur Heart J. 2018;39(26):2484-2493.
- Neumann FJ, Sousa-Uva M, Ahlsson A, et al. 2018 ESC/EACTS Guidelines on myocardial revascularization. Eur Heart J. 2019;40(2):87-165.
- Hachamovitch R, Hayes SW, Friedman JD, Cohen I, Berman DS. Comparison of the short-term survival benefit associated with revascularization compared with medical therapy in patients with no prior coronary artery disease undergoing stress myocardial perfusion single photon emission computed tomography. Circulation. 2003;107(23):2900-2907.
- Brilakis ES, Mashayekhi K, Tsuchikane E, et al. Guiding Principles for Chronic Total Occlusion Percutaneous Coronary Intervention. Circulation. 2019;140(5):420-433.
- Velazquez EJ, Lee KL, Deja MA, et al. Coronary-artery bypass surgery in patients with left ventricular dysfunction. N Engl J Med. 2011;364(17):1607-1616.
- Farkouh ME, Domanski M, Sleeper LA, et al. Strategies for multivessel revascularization in patients with diabetes. N Engl J Med. 2012;367(25):2375-2384.
info@herz+gefäss
- Vol. 13
- Ausgabe 4
- September 2023