- Die neuen ESC-Guidelines zur Behandlung von akuten Koronarsyndromen
Die neuen Leitlinien der Europäischen Kardiologischen Gesellschaft (ESC) haben die Empfehlungen für Patienten mit ST-Hebungsinfarkten und Nicht-ST-Hebungsinfarkten vereinheitlicht, um den gemeinsamen pathophysiologischen, diagnostischen und therapeutischen Aspekten Rechnung zu tragen. In diesem Review werden ausgewählte praxisrelevante Neuerungen beleuchtet, insbesondere im Hinblick auf antithrombotische Therapien und logistische Gesichtspunkte in der akuten Infarktbehandlung.
The updated guidelines of the European Society of Cardiology (ESC) now combine their recommendations for patients with and without ST-segment elevation myocardial infarction, reflecting the common pathophysiological, diagnostic and therapeutic aspects for the management of acute coronary syndromes. This review seeks to highlight selected updates relevant to everyday clinical practice, particularly with respect to antithrombotic therapies and logistical considerations in the treatment of acute myocardial infarction.
Key words: acute coronary syndromes, acute myocardial infarction, guidelines
Einleitung
Nach der letzten Auflage der Leitlinien der Europäischen Kardiologischen Gesellschaft (ESC) für Patienten mit ST-Hebungsinfarkten (STEMI) im Jahr 2017 und Nicht-ST-Hebungsinfarkten (NSTEMI) im Jahr 2020 entstand nun ein vereinheitlichtes Dokument für Patienten mit akuten Koronarsyndromen (ACS), welches auf der ESC Jahrestagung im August 2023 präsentiert wurde (1-3). Dadurch wurde der gemeinsamen Pathophysiologie und den ähnlichen diagnostischen sowie therapeutischen Behandlungspfaden Rechnung getragen. Naturgemäss fand eine rigorose Evaluation der bisherigen und neu generierten Evidenz statt, insbesondere in Bezug auf antithrombotische Therapien sowie logistische Gesichtspunkte bei Patienten mit NSTEMI (Zeitpunkt der invasiven Abklärung), STEMI (Zeitpunkt der vollständigen Revaskularisierung bei Mehrgefässerkrankung) oder nach Herzkreislaufstillstand («out of hospital cardiac arrest»). Nachfolgend werden ausgewählte, praxisrelevante Neuerungen beleuchtet.
Zeitpunkt für die invasive Abklärung von vermuteten Nicht-ST-Hebungsinfarkten
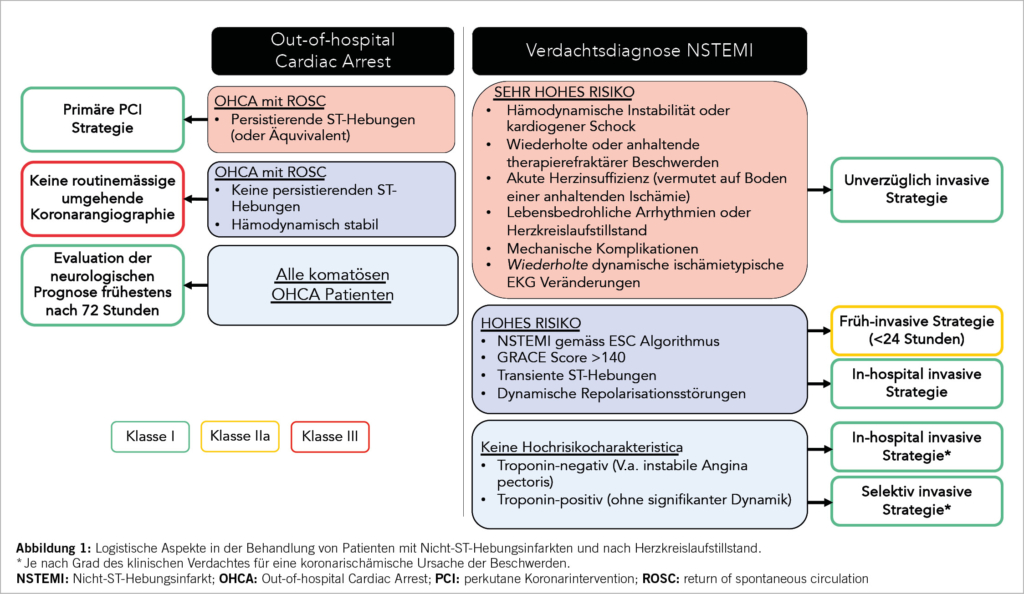
Der Zeitpunkt für invasive Abklärung von Patienten mit vermutetem Myokardinfarkt ohne ST-Streckenhebungen richtet sich weiterhin nach Risikomerkmalen (Abbildung 1). Unverändert zu den Leitlinien aus dem Jahr 2020 sollten «very high risk» Patienten mit Vorliegen von zumindest einem der folgenden Kriterien unverzüglich einer Koronarangiographie zugeführt werden. Die Klasse-I-Empfehlung für eine invasive Abklärung von Hochrisikopatienten («high risk») binnen 24 Stunden wurde auf eine Klasse-IIa-A-Empfehlung zurückgestuft. Weiterhin besteht jedoch eine Klasse-I-Indikation für eine invasive Abklärung dieser Patienten während demselben Krankenhausaufenthalt. Diese Empfehlungen basieren unter anderem auf einer Meta-Analyse mit zwei neuen randomisierten Studien seit 2020 und somit in Summe 17 randomisierten Trials mit 10`209 Patienten. Die gepoolte mediane Zeit bis zur Angiographie waren 3,4 vs. 41,3 Stunden in den jeweiligen Studiengruppen. Eine frühe invasive Strategie war nicht mit einem Unterschied in harten Endpunkten wie Mortalität, Myokardinfarkt (meist definiert anhand von Enzymanstiegen, neuen Q-Zacken oder der universellen Myokardinfarktdefinition), Herzinsuffizienz-Hospitalisation oder schweren Blutungsereignissen assoziiert. Wiederkehrende Ischämien (meist definiert anhand von wiederkehrenden Symptomen von min. 5-10 Minuten Dauer, mit oder ohne begleitende EKG-Veränderungen) traten in der frühen invasiven Gruppe seltener auf (RR: 0.57, 95% CI: 0.40–0.81), die Hospitalisierungsdauer war im Mittel um 22 Stunden kürzer.(4) Für Patienten, welche keine der Hochrisikokriterien erfüllen, ist weiterhin ein selektiver invasiver Approach gemäss Leitlinien für chronische Koronarsyndrome empfohlen, sofern die klinische Einschätzung eine elektive Abklärung erlaubt (1).
Zeitpunkt der invasiven Abklärung nach Out-of-hospital Cardiac Arrest
Während nur ein geringer Prozentsatz von ACS-Patienten mit einem Out-of-hospital Cardiac Arrest (OHCA) präsentiert, ist ein ACS die häufigste Ursache eines OHCA.
Bei Patienten mit ST-Streckenhebungen nach Wiedererlangen des Kreislaufes (ROSC) ist eine primäre PCI-Strategie empfohlen (Klasse I-B). Bei OHCA-Patienten ohne ST-Streckenhebungen sind seit 2019 zumindest fünf neue randomisierte Studien verfügbar, die eine frühe gegenüber einer verzögerten koronarangiographischen Abklärung untersucht haben. In keiner dieser Studien war eine umgehende Koronarangiographie mit einem Überlebensvorteil assoziiert (5-9). Dies war auch bei Patienten mit initial schockbarem Rhythmus der Fall (5, 8). Ursächlich dafür erscheint, dass die neurologische Prognose und intensivmedizinische Komplikationen überwiegend zu der etwa 50-prozentigen Mortalität beitragen und somit selbst durch die Behandlung einer koronarischämischen Ursache das Outcome nicht massgeblich beeinflusst werden kann. Dementsprechend ist eine routinemässige notfallmässige Koronarangiographie bei hämodynamisch stabilen Patienten nach OHCA ohne persistierende ST-Streckenhebungen (oder Äquivalent) nicht empfohlen (Klasse III-A) (1). In der initialen Evaluation dieser Patienten sollten nicht-koronare Ätiologien (z.B. zerebrovaskuläre Ereignisse, respiratorisches Versagen, nicht-kardiogener Schock, Lungenembolie, Intoxikation) untersucht werden, wobei die Echokardiographie einen wesentlichen Beitrag zur Differentialdiagnostik leisten kann. Trotz den neuen Richtlinien kann es in ausgewählten OHCA-Patienten ohne STEMI Sinn machen, ohne Verzug eine Angiographie durchzuführen, nämlich wenn ein Koronarverschluss wahrscheinlich ist und die Aussicht auf neurologische Erholung gut (e.g Patienten mit Thoraxschmerzen vor Herzkreislaufstillstand und kurzer Reanimationsdauer) (10).
Antithrombotische Therapien
«Loading» mit Plättchenaggregationshemmern
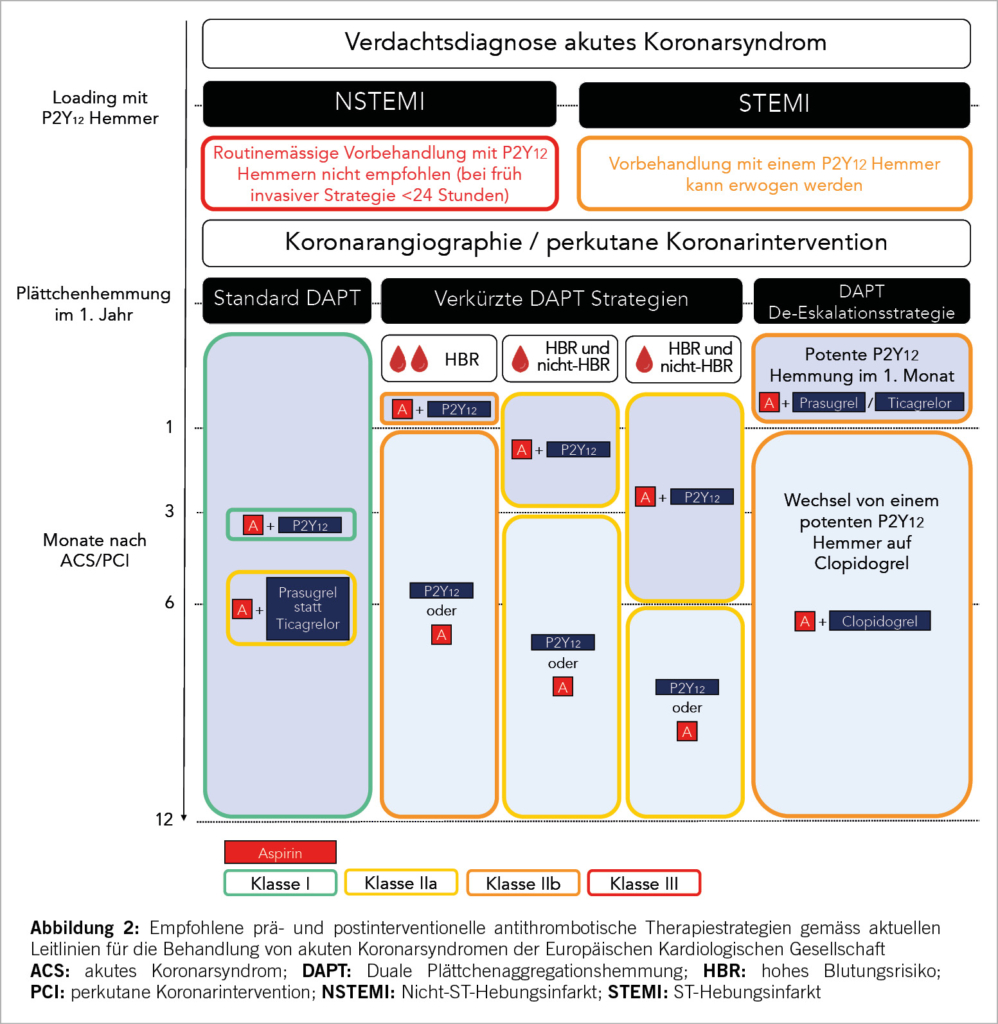
Aktuell empfohlene prä- und postinterventionelle antithrombotische Strategien sind in Abbildung 2 zusammengefasst.
Weiterhin ist bei Patienten mit NSTEMI ohne Kenntnis der Koronaranatomie und zeitnah geplanter Koronarangiographie (<24 Stunden) eine routinemässige Vorbehandlung mit P2Y12 Hemmern nicht empfohlen (Klasse III-A), da ein potenzieller Anstieg von Blutungskomplikationen keinem ischämischen Benefit gegenübersteht. (1, 11) Basierend auf einer verfügbaren randomisierten Studie mit Ticagrelor (ATLANTIC) und Registerstudien ist eine «pre-loading» Strategie bei Patienten mit STEMI weder mit Vorteilen auf der ischämischen Seite, noch mit Nachteilen hinsichtlich Blutungskomplikationen behaftet (12-14). In den aktuellen ESC-Leitlinien wurde die diesbezügliche Empfehlung neu formuliert. Bei Patienten die für eine primäre PCI-Strategie vorgesehen sind, kann eine Vorbehandlung mit P2Y12-Hemmern erwogen werden (Klasse IIb-B), ist aber keine Klasse-I-Indikation mehr.
Das Infarktnetzwerk des Inselspital hat bereits im Jahr 2018 aufgrund von Europäischen Empfehlungen für NSTEMI-Patienten die institutionellen Richtlinien vereinheitlicht und empfahl ab Oktober 2018 sowohl für NSTEMI- als auch STEMI-Patienten kein prä-interventionelles Loading mit P2Y12-Hemmern durchzuführen (15, 16). Dieses Vorgehen wurde kürzlich im Bern-PCI-Register validiert. Eine Strategie mit sofortigem Loading bei Diagnosestellung eines STEMI gegenüber einem verzögerten Loading nach Kenntnis der Koronaranatomie resultierte in einer vergleichbaren Inzidenz von schweren kardiovaskulären Ereignissen, Blutungen und prozedurellen Komplikationen, was die aktuelle Leitlinie mit lokalen Daten unterstützt (17).
Langfristige antithrombotische Therapiestrategien
Die optimale Intensität und Dauer der antithrombotischen Kombinationstherapie ist Gegenstand zahlreicher Studien (18-24). Da die modernen Stent-Plattformen ein Plateau hinsichtlich ihrer Effektivität erreicht haben (25), mittels intrakoronarer Bildgebung das kurz- und langfristige Resultat weiter verbessert werden kann (26-28) und auch basierend auf aggressiveren sekundärprophylaktischen Massnahmen (29) gab es ein Umdenken im Feld der antithrombotischen Therapie in Richtung Vermeidung von Blutungskomplikationen (30, 31).
Es haben sich zwei prädominante Strategien herauskristallisiert, mit denen das Blutungsrisiko ohne apparente «Kosten» auf der ischämischen Seite gesenkt werden kann. Einerseits die Verkürzung der dualen Plättchenaggregationshemmung auf 1-6 Monate nach PCI gefolgt von einer Monotherapie mit einem potenten P2Y12-Hemmer (anstatt Aspirin) – andererseits die De-Eskalation von einem potenten P2Y12-Hemmer auf Clopidogrel frühestens 1 Monat nach PCI mit Aspirin als Hintergrundtherapie (1, 30, 31). Während das standardmässige Vorgehen mit 12 Monate dualer Plättchenaggregationshemmung (DAPT) erneut eine Klasse I-A-Empfehlung erhielt, wurden die oben erwähnten Optionen mit einer Klasse IIa-A (Verkürzung der DAPT auf 3-6 Monate, gefolgt von potenter P2Y12-Hemmer Monotherapie, auch bei niedrigem Blutungsrisiko) und einer Klasse IIb-A-Indikation beurteilt (Verkürzung der DAPT auf 1 Monat bei hohem Blutungsrisiko). Als neue Empfehlung hauptsächlich basierend auf einem Expertenkonsensus, sollte bei Patienten mit ACS und chirurgischer Revaskularisierung postoperativ eine DAPT für mindestens 12 Monate etabliert werden (Klasse 1-C) (1).
Revaskularisierung von Patienten mit akuten Koronarsyndromen und Mehrgefässerkrankung
Die Notwendigkeit einer Behandlung von angiographisch signifikanten nicht-culprit-Läsionen bei Patienten mit akutem Myokardinfarkt ist seit den CULPRIT, DANAMI-3-PRIMULTI- und COMPLETE-Studien bestens etabliert (32-34). Entsprechend wurde der Empfehlungsgrad vorhergehender Leitlinien (eine routinemässige vollständige Revaskularisierung sollte vor Spitalaustritt erwogen werden, Klasse IIa-A) nun hochgestuft. Eine vollständige Revaskularisierung ist entweder während der Index Prozedur oder binnen 45 Tagen empfohlen (Klasse I-A) (1, 3, 15). Der optimale Zeitpunkt, d.h. während der Index-Prozedur, während des Spitalsaufenthaltes oder in einem Folgeaufenthalt, wurde erst in kürzlich publizierten Studien untersucht, die auf die aktuellen Richtlinien noch keinen Einfluss hatten.
Die rezente BIOVASC-Studie randomisierte 1525 Patienten mit STEMI oder NSTEMI zu einer zeitnahen Behandlung (während der Index Prozedur oder während des Index-Aufenthaltes) gegenüber einer «staged» Behandlung aller nicht-culprit-Läsionen binnen 6 Wochen. Der primäre Endpunkt, bestehend aus Gesamtmortalität, Myokardinfarkt, ungeplanter ischämiebedingter Revaskularisierung und zerebrovaskulären Ereignissen nach einem Jahr, war vergleichbar zwischen den Gruppen (HR 0.78, 95% CI 0.55–1.11, p für Überlegenheit 0.17). Myokardinfarkte traten seltener in der zeitnah revaskularisierten Gruppe auf (1.9% vs. 4.5%, HR 0.41, 95% CI 0.22-0.76, p<0.01), jedoch war der Endpunkte durch peri-prozedurale Ereignisse, welche in der zeitnah revaskularisierten Gruppe durch den Index Myokardinfarkt maskiert waren, verzerrt. Die Gesamtsterblichkeit und kardiovaskuläre Mortalität, sowohl nach 30 Tagen als auch nach 12 Monaten war vergleichbar zwischen den Gruppen (numerisch niedriger in der «staged PCI» Gruppe) (35).
Die MULTISTARS-AMI-Studie randomisierte 840 STEMI-Patienten zu einer umgehenden vollständigen Revaskularisierung gegenüber einer «staged PCI» Strategie binnen 19 bis 45 Tagen. Der primäre Endpunkt bestehend aus Gesamtmortalität, Myokardinfarkt, ungeplanter ischämiebedingter Revaskularisierung und Herzinsuffizienz-Hospitalisierung nach 1 Jahr trat seltener in der umgehend vollständig revaskularisierten Gruppe auf (8.5% vs. 16.3%, HR 0.52, 95% CI 0.38-0.72, p<0.01). Wie auch in der BIOVASC-Studie waren nur etwa ein Drittel der ausschlaggebenden Myokardinfarkt-Ereignisse spontane Events der zur Behandlung anstehenden nicht-culprit Läsionen. Ausschlaggebend waren periprozedurale Myokardinfarkte, welche in der frühen Revaskularisationsgruppe im initialen Enzympeak des Indexinfarktes untergehen, aber niederschwellig erkannt werden in der «staged PCI» Gruppe. Die Gesamtsterblichkeit und kardiovaskuläre Sterblichkeit war vergleichbar zwischen den Gruppen (36).
In einer Analyse des Bern-PCI Registers mit 1432 ACS-Patienten fand sich keinerlei Signal dass eine zeitnahe (<4 Wochen) gegenüber einer verzögerten (>4 Wochen) «staged PCI» mit einem Unterschied in schweren kardiovaskulären Ereignissen assoziiert sein könnte (37).
Intrakoronare Bildgebung
Die Bedeutung der intrakoronaren Bildgebung wurde erstmals in den Richtlinien hervorgehoben mit einer Klasse IIa-A-Indikation für die Verwendung von Imaging zur Stentimplantation und einer IIb-C-Indikation zur Klärung von unklaren Angiographiebefunden (mit Präferenz für die optische Kohärenztomographie, OCT) (1).
Sekundärprevention
Zusätzlich zum weiterhin gültigen Motto «the lower the better» gilt es, das Lipidziel nach ACS schnellstmöglich zu erreichen. Bei Patienten mit einem kardiovaskulären Zweitereignis binnen 2 Jahren liegt das LDL-Ziel bei <1.0mmol/L (<40mg/dl).(1, 38) Eine Neueinleitung oder Umstellung auf ein hochpotentes Statin (Atorvastatin, Rosuvastatin) sollte immer Teil der Therapiestrategie sein, wobei gemäss der neuen Empfehlungen zur raschen Zielerreichung eine initiale Kombinationstherapie mit Ezetimib erwogen werden kann (Klasse IIb-B). Gemäss Leitlinien sollte eine erste Kontrolle hinsichtlich Ziel-Erreichung in 4-6 Wochen stattfinden (1). Die Limitatio der PCSK-9 Hemmer verlangt jedoch eine 3-monatige Therapie in maximal verträglicher Dosierung (mit oder ohne Ezetimib, oder Ezetimib als Monotherapie), und erstattet bei LDL-Spiegeln von >1.8mmol/L. Mit einer LDL-Senkung von 50-70% unter einer Statin-/Ezetimib-Kombination fällt ein relevanter Anteil von Patienten in den nicht erstattbaren aber gemäss Leitlinien unzureichend kontrollierten Bereich (d.h. 1.4 – 1.8 mmol/L). Eine praktikable Lösung dieses Problems beinhaltet Ezetimib vorzuenthalten, um eine Therapie mit den etwa 3x so potenten PCSK-9 Hemmern zu ermöglichen (39). Dadurch kann sogar eine Regression von bereits bestehenden Koronarplaques erreicht werden (29, 40).
Die antidiabetische Therapie sollte auf Komorbiditäten wie Herzinsuffizienz, Niereninsuffizienz und Übergewicht abgestimmt werden (Klasse I-A) (1). Die ebenso am ESC präsentierten neuen Leitlinien für das Management von kardiovaskulären Erkrankungen bei Patienten mit Diabetes empfehlen den Einsatz von SGLT-2-Hemmern bei allen Patienten mit Herzinsuffizienz (unabhängig von der systolischen Linksventrikelfunktion, dem HbA1c und der begleitenden antidiabetischen Therapie), und Niereninsuffizienz (Klasse I-A). Bei Patienten mit atherosklerotischer Herzkreislauferkrankung sollte unabhängig von der Blutzuckerkontrolle ein GLP-1-Rezeptor-Antagonist zur Reduktion kardiovaskulärer Ereignisse zum Einsatz kommen (Klasse I-A), speziell wenn eine Gewichtsreduktion angestrebt wird (Klasse IIa-B) (41).
Copyright bei Aerzteverlag medinfo AG
Universitätsklinik für Kardiologie
Inselspital
Freiburgstrasse 20
CH-3010 Bern
Schweiz
miklos.rohla@insel.ch
Leiter Herzkatheterlabor
Universitätsklinik für Kardiologie
Inselspital
Freiburgstrasse 18
3010 Bern
lorenz.raeber@insel.ch
Miklos Rohla erhielt Beratungshonorare von Daiichi Sankyo, Sanofi Aventis, COR2ED, Novartis und Medtronic, sowie Vortragshonorare von Daiichi Sankyo, Biotronik und Takeda Pharma.
Lorenz Räber erhielt Forschungsförderungen an die Institution von Abbott, Biotronik, Heartflow, Sanofi, Regeneron und Beratungs- bzw. Vortragshonorare von Abbott, Amgen, AstraZeneca, Canon, Novo Nordisk, Medtronic, Sanofi, Occlutech, und Vifor.
◆ Bei NSTEMI-Patienten entscheiden weiterhin Risikocharakteristika über die Dringlichkeit der invasiven Abklärung, wobei Patienten mit sehr hohem Risiko («very high risk») wie STEMIs zu behandeln sind. Der anteilsmässig grösste Teil der Patienten fällt in die Hochrisikogruppe («high risk»), bei denen eine Angiographie innerhalb des initialen Krankenhausaufenthaltes Pflicht ist (I B), aber nicht mehr zwingend innerhalb der ersten 24h (IIa B)
◆ OHCA-Patienten ohne ST-Hebungen sollen nicht mehr zwingend unverzüglich angiographiert, wegen fehlendem Einfluss auf die Prognose
◆ Im Hinblick auf antithrombotische Kombinationstherapie rückt die Vermeidung von Blutungskomplikationen und der damit einhergehende netto klinische Benefit vermehrt in den Mittelpunkt der therapeutischen Bemühungen
◆ Ein routinemässiges Pre-loading mit P2Y12 Inhibitoren vor der Angiographie bei STEMI Patienten ist nicht mehr empfohlen
◆ Die vollständige Revaskularisation aller Koronargefässe nach STEMI ist empfohlen (I A), entweder während der Index Angiographie oder während eines geplanten Zweiteingriffes innerhalb von 45 Tagen
◆ Intrakoronares Imaging wird zur Optimierung der PCI empfohlen
(IIa-A)
◆ Für die lipidsenkende Therapie gilt nicht nur «the lower the better» sondern auch «hit hard and early»
1. Byrne RA, Rossello X, Coughlan JJ, Barbato E, Berry C, Chieffo A, et al. 2023 ESC Guidelines for the management of acute coronary syndromes. Eur Heart J. 2023.
2. Collet JP, Thiele H, Barbato E, Barthelemy O, Bauersachs J, Bhatt DL, et al. 2020 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation. Eur Heart J. 2021;42(14):1289-367.
3. Ibanez B, James S, Agewall S, Antunes MJ, Bucciarelli-Ducci C, Bueno H, et al. 2017 ESC Guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevation: The Task Force for the management of acute myocardial infarction in patients presenting with ST-segment elevation of the European Society of Cardiology (ESC). Eur Heart J. 2018;39(2):119-77.
4. Kite TA, Kurmani SA, Bountziouka V, Cooper NJ, Lock ST, Gale CP, et al. Timing of invasive strategy in non-ST-elevation acute coronary syndrome: a meta-analysis of randomized controlled trials. Eur Heart J. 2022;43(33):3148-61.
5. Desch S, Freund A, Akin I, Behnes M, Preusch MR, Zelniker TA, et al. Angiography after Out-of-Hospital Cardiac Arrest without ST-Segment Elevation. N Engl J Med. 2021;385(27):2544-53.
6. Hauw-Berlemont C, Lamhaut L, Diehl JL, Andreotti C, Varenne O, Leroux P, et al. Emergency vs Delayed Coronary Angiogram in Survivors of Out-of-Hospital Cardiac Arrest: Results of the Randomized, Multicentric EMERGE Trial. JAMA Cardiol. 2022;7(7):700-7.
7. Kern KB, Radsel P, Jentzer JC, Seder DB, Lee KS, Lotun K, et al. Randomized Pilot Clinical Trial of Early Coronary Angiography Versus No Early Coronary Angiography After Cardiac Arrest Without ST-Segment Elevation: The PEARL Study. Circulation. 2020;142(21):2002-12.
8. Lemkes JS, Janssens GN, van der Hoeven NW, Jewbali LSD, Dubois EA, Meuwissen M, et al. Coronary Angiography after Cardiac Arrest without ST-Segment Elevation. N Engl J Med. 2019;380(15):1397-407.
9. Viana-Tejedor A, Andrea-Riba R, Scardino C, Ariza-Sole A, Baneras J, Garcia-Garcia C, et al. Coronary angiography in patients without ST-segment elevation following out-of-hospital cardiac arrest. COUPE clinical trial. Rev Esp Cardiol (Engl Ed). 2023;76(2):94-102.
10. Spirito A, Papadis A, Vaisnora L, Iacovelli F, Sardu C, Kavaliauskaite R, et al. Comparative Outcomes After Percutaneous Coronary Intervention in Unconscious and Conscious Patients With Out-of-Hospital Cardiac Arrest. JACC Cardiovasc Interv. 2022;15(13):1338-48.
11. Montalescot G, Bolognese L, Dudek D, Goldstein P, Hamm C, Tanguay JF, et al. Pretreatment with prasugrel in non-ST-segment elevation acute coronary syndromes. N Engl J Med. 2013;369(11):999-1010.
12. Gewehr DM, Carvalho PEP, Dagostin CS, Cardoso R, Kubrusly TBL, Kubrusly FB, et al. Pretreatment with P2Y12 inhibitors in ST-elevation myocardial infarction: A systematic review and meta-analysis. Catheter Cardiovasc Interv. 2023;102(2):200-11.
13. Montalescot G, van ‘t Hof AW, Lapostolle F, Silvain J, Lassen JF, Bolognese L, et al. Prehospital ticagrelor in ST-segment elevation myocardial infarction. N Engl J Med. 2014;371(11):1016-27.
14. Redfors B, Dworeck C, Haraldsson I, Angeras O, Odenstedt J, Ioanes D, et al. Pretreatment with P2Y12 receptor antagonists in ST-elevation myocardial infarction: a report from the Swedish Coronary Angiography and Angioplasty Registry. Eur Heart J. 2019;40(15):1202-10.
15. Neumann FJ, Sousa-Uva M, Ahlsson A, Alfonso F, Banning AP, Benedetto U, et al. 2018 ESC/EACTS Guidelines on myocardial revascularization. Eur Heart J. 2019;40(2):87-165.
16. Valgimigli M, Bueno H, Byrne RA, Collet JP, Costa F, Jeppsson A, et al. 2017 ESC focused update on dual antiplatelet therapy in coronary artery disease developed in collaboration with EACTS: The Task Force for dual antiplatelet therapy in coronary artery disease of the European Society of Cardiology (ESC) and of the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J. 2018;39(3):213-60.
17. Rohla M, Ye SX, Shibutani H, Bruno J, Otsuka T, Häner J, et al. Pretreatment with P2Y12 inhibitors in ST-segment elevation myocardial infarction: Insights from the Bern-PCI registry. JACC Cardiovasc Interv. 2023;accepted, ahead of print.
18. Choi KH, Song YB, Lee JM, Park TK, Yang JH, Choi JH, et al. Clinical Usefulness of PRECISE-DAPT Score for Predicting Bleeding Events in Patients With Acute Coronary Syndrome Undergoing Percutaneous Coronary Intervention: An Analysis From the SMART-DATE Randomized Trial. Circulation Cardiovascular interventions. 2020;13(5):e008530.
19. Hong SJ, Kim JS, Hong SJ, Lim DS, Lee SY, Yun KH, et al. 1-Month Dual-Antiplatelet Therapy Followed by Aspirin Monotherapy After Polymer-Free Drug-Coated Stent Implantation: One-Month DAPT Trial. JACC Cardiovasc Interv. 2021; 14(16):1801-11.
20. Kim BK, Hong SJ, Cho YH, Yun KH, Kim YH, Suh Y, et al. Effect of Ticagrelor Monotherapy vs Ticagrelor With Aspirin on Major Bleeding and Cardiovascular Events in Patients With Acute Coronary Syndrome: The TICO Randomized Clinical Trial. Jama. 2020;323(23):2407-16.
21. Kogame N, Guimaraes PO, Modolo R, De Martino F, Tinoco J, Ribeiro EE, et al. Aspirin-Free Prasugrel Monotherapy Following Coronary Artery Stenting in Patients With Stable CAD: The ASET Pilot Study. JACC Cardiovasc Interv. 2020;13(19):2251-62.
22. Valgimigli M, Frigoli E, Heg D, Tijssen J, Juni P, Vranckx P, et al. Dual Antiplatelet Therapy after PCI in Patients at High Bleeding Risk. N Engl J Med. 2021;385 (18):1643-55.
23. van der Sangen NMR, Claessen B, Kucuk IT, den Hartog AW, Baan J, Beijk MAM, et al. Single antiplatelet therapy directly after percutaneous coronary intervention in non-ST-segment elevation acute coronary syndrome patients: the OPTICA study. EuroIntervention. 2023;19(1):63-72.
24. Vranckx P, Valgimigli M, Odutayo A, Serruys PW, Hamm C, Steg PG, et al. Efficacy and Safety of Ticagrelor Monotherapy by Clinical Presentation: Pre-Specified Analysis of the GLOBAL LEADERS Trial. J Am Heart Assoc. 2021;10(18):e015560.
25. Toyota T, Morimoto T, Kitai T, Park M, Sasaki Y, Kim K, et al. Biodegradable-polymer versus durable-polymer drug eluting stents for coronary artery disease: systematic review and a meta-analysis. European Heart Journal. 2020;41(Supplement_2).
26. Lee JM, Choi KH, Song YB, Lee JY, Lee SJ, Lee SY, et al. Intravascular Imaging-Guided or Angiography-Guided Complex PCI. N Engl J Med. 2023;388(18):1668-79.
27. Kang DY, Ahn JM, Yun SC, Hur SH, Cho YK, Lee CH, et al. Optical Coherence Tomography-Guided or Intravascular Ultrasound Guided Percutaneous Coronary Intervention: The OCTIVUS Randomized Clinical Trial. Circulation. 2023.
28. Holm NR, Andreasen LN, Neghabat O, Laanmets P, Kumsars I, Bennett J, et al. OCT or Angiography Guidance for PCI in Complex Bifurcation Lesions. New England Journal of Medicine. 2023.
29. Raber L, Ueki Y, Otsuka T, Losdat S, Haner JD, Lonborg J, et al. Effect of Alirocumab Added to High-Intensity Statin Therapy on Coronary Atherosclerosis in Patients With Acute Myocardial Infarction: The PACMAN-AMI Randomized Clinical Trial. Jama. 2022;327(18):1771-81.
30. Navarese EP, Landi A, Oliva A, Piccolo R, Aboyans V, Angiolillo D, et al. Within and beyond 12-month efficacy and safety of antithrombotic strategies in patients with established coronary artery disease: two companion network meta-analyses of the 2022 joint clinical consensus statement of the European Association of Percutaneous Cardiovascular Interventions (EAPCI), European Association for Acute CardioVascular Care (ACVC), and European Association of Preventive Cardiology (EAPC). Eur Heart J Cardiovasc Pharmacother. 2023;9(3):271-90.
31. Valgimigli M, Aboyans V, Angiolillo D, Atar D, Capodanno D, Halvorsen S, et al. Antithrombotic treatment strategies in patients with established coronary atherosclerotic disease. Eur Heart J Cardiovasc Pharmacother. 2023;9(5):462-96.
32. Engstrom T, Kelbaek H, Helqvist S, Hofsten DE, Klovgaard L, Holmvang L, et al. Complete revascularisation versus treatment of the culprit lesion only in patients with ST-segment elevation myocardial infarction and multivessel disease (DANAMI-3-PRIMULTI): an open-label, randomised controlled trial. Lancet (London, England). 2015;386(9994):665-71.
33. Gershlick AH, Khan JN, Kelly DJ, Greenwood JP, Sasikaran T, Curzen N, et al. Randomized trial of complete versus lesion-only revascularization in patients undergoing primary percutaneous coronary intervention for STEMI and multivessel disease: the CvLPRIT trial. J Am Coll Cardiol. 2015;65(10):963-72.
34. Mehta SR, Wood DA, Storey RF, Mehran R, Bainey KR, Nguyen H, et al. Complete Revascularization with Multivessel PCI for Myocardial Infarction. N Engl J Med. 2019;381(15):1411-21.
35. Diletti R, den Dekker WK, Bennett J, Schotborgh CE, van der Schaaf R, Sabate M, et al. Immediate versus staged complete revascularisation in patients presenting with acute coronary syndrome and multivessel coronary disease (BIOVASC): a prospective, open-label, non-inferiority, randomised trial. Lancet (London, England). 2023;401(10383):1172-82.
36. Stahli BE, Varbella F, Linke A, Schwarz B, Felix SB, Seiffert M, et al. Timing of Complete Revascularization with Multivessel PCI for Myocardial Infarction. N Engl J Med. 2023;389(15):1368-79.
37. Otsuka T, Bar S, Losdat S, Kavaliauskaite R, Ueki Y, Zanchin C, et al. Effect of Timing of Staged Percutaneous Coronary Intervention on Clinical Outcomes in Patients With Acute Coronary Syndromes. J Am Heart Assoc. 2021;10(23):e023129.
38. Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020;41(1):111-88.
39. Khan SU, Yedlapati SH, Lone AN, Hao Q, Guyatt G, Delvaux N, et al. PCSK9 inhibitors and ezetimibe with or without statin therapy for cardiovascular risk reduction: a systematic review and network meta-analysis. BMJ. 2022;377:e069116.
40. Biccire FG, Haner J, Losdat S, Ueki Y, Shibutani H, Otsuka T, et al. Concomitant Coronary Atheroma Regression and Stabilization in Response to Lipid-Lowering Therapy. J Am Coll Cardiol. 2023;82(18):1737-47.
41. Marx N, Federici M, Schutt K, Muller-Wieland D, Ajjan RA, Antunes MJ, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023;44(39):4043-140.
info@herz+gefäss
- Vol. 13
- Ausgabe 6
- Dezember 2023