- Echokardiographische Diagnose der Pericarditis constrictiva
Fallpräsentation
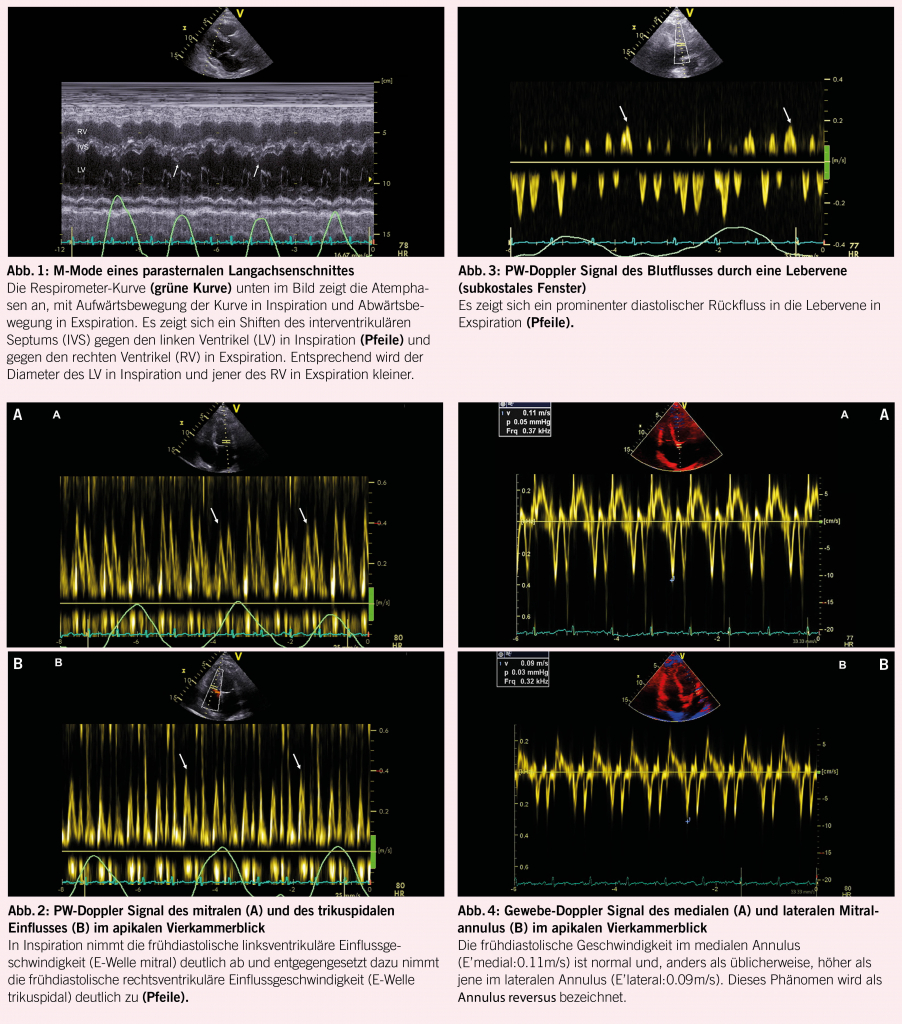
Ein 65-jähriger Patient klagte in den vergangenen Monaten über eine zunehmende Dyspnoe. Diese ging mit einer progredienten Müdigkeit einher. Im Verlauf kam es auch zu zunehmenden Unterschenkelödemen und zu einem Druck im Oberbauch. Im Rahmen der Abklärungen wurde eine transthorakale Echokardiographie durchgeführt. Sowohl die linksventrikuläre, als auch die rechtsventrikuläre systolische Funktion erwiesen sich dabei als normal. Es fiel jedoch eine atemvariable Bewegung des interventrikulären Septums auf, mit einem Shift des Septums gegen den linken Ventrikel in Inspiration und gegen den rechten Ventrikel in Exspiration, was besonders gut im M-Mode des parasternalen Langachsenschnittes dargestellt werden konnte (Abb. 1). Ebenfalls zeigte sich im PW-Doppler eine Atemvariabilität der Einflussmuster durch die AV-Klappen, mit Abnahme der transmitralen E-Welle in Inspiration und Zunahme in Exspiration (Abb. 2A) und entgegengesetztem Verhalten der transtrikuspidalen E-Welle (Abb. 2B). In der PW-Doppler Untersuchung einer Lebervene konnte ein prominentes diastolisches Rückfluss-Signal in Exspiration dargestellt werden (Abb. 3). Im Gewebe-Doppler des medialen und lateralen Mitralklappenannulus zeigten sich erhaltene frühdiastolische Geschwindigkeiten (E’), wobei das me-diale E’ (Abb. 4A) höher war als das laterale E’ (Abb. 4B). Die Doppler-echokardiographisch erhobenen Befunde waren klassisch für das Vorliegen einer Pericarditis constrictiva. Der Patient wurde nach Vervollständigung der Abklärungen einer Perikardektomie unterzogen, was im Verlauf zur deutlichen Reduktion seiner Beschwerden führte.
Kommentar
Die Pericarditis constrictiva ist eine potentiell reversible Ursache einer, typischerweise rechtsbetonten, Herzinsuffizienz. In westlichen Ländern ist die Ursache meistens idiopathisch bzw. viral oder postoperativ nach Herzoperation. Eine seltenere Genese ist eine stattgehabte mediastinale Strahlentherapie (1). Die Tuberkulose als Ursache einer Pericarditis constrictiva ist in Industrieländern mittlerweile sehr selten geworden, wohingegen sie in Entwicklungsländern nach wie vor die häufigste Ätiologie darstellt (2).
Die Diagnose der Pericarditis constrictiva stellt oft eine Herausforderung dar, da sich die Symptomatik schleichend über Jahre entwickeln kann und sich die Erkrankung oft ähnlich präsentiert wie beispielsweise eine restriktive Kardiomyopathie, eine schwere Trikuspidalklappeninsuffizienz oder auch wie einige nicht-kardiale Erkrankungen (3). Die Doppler-Echokardiographie eignet sich dazu, die Pericarditis constrictiva von anderen Herzkrankheiten zu unterscheiden.
Die pathopyhsiologischen Veränderungen bei der Pericarditis constrictiva beruhen auf der Fixation des intrakardialen Volumens infolge des erkrankten, rigiden Perikards, auf der interventrikulären Dependenz sowie auf einer Dissoziation zwischen intrathorakalen und intrakardialen Druckverhältnissen (3). Bei der Inspiration kommt es physiologischerweise zu einem vermehrten venösen Rückstrom von Blut zum rechten Herzen und somit zu vermehrtem Volumen im rechten Ventrikel. Infolge des fixierten kardialen Raumes führt das vermehrte Volumen im rechten Ventrikel bei der Konstriktion zu einer Ausbuchtung des Septums zum linken Ventrikel hin, was wiederum dessen Füllungskapazität in Inspiration vermindert. In Inspiration nehmen ferner der pulmonal-kapilläre Druck und der Druck in den Lungenvenen durch Reduktion des intrathorakalen Druckes ab. Bei der Pericarditis constrictiva wird das linke Herz durch den steifen Perikardraum von den respiratorischen intrathorakalen Druckschwankungen abgeschirmt, wodurch sich der Druckgradient zwischen Lungenvenen und linkem Herzen in der Diastole vermindert. Zusammen mit der Septum-Ausbuchtung nach links, trägt dies zur verminderten Füllung des linken Ventrikels in Inspiration bei. In Exspiration kommt es zu gegenteiligen Effekten, wodurch der linke Ventrikel besser gefüllt wird, das ventrikuläre Septum zur rechten Seite shiftet und die Füllung des rechten Ventrikels abnimmt.
Die Doppler-Echokardiographie ist in der Lage, diese pathophysiologischen Veränderungen aufzuzeigen. Als nützliche und indikative echokardiographische Parameter erweisen sich bei der Pericarditis constrictiva das respiratorische Shiften des ventrikulären Septums, in Inspiration gegen den linken, in Exspiration gegen den rechten Ventrikel (Abb. 1) (4), die Abnahme der transmitralen E-Welle und die Zunahme der transtrikuspidalen E-Welle in Inspiration (Abb. 2A und B) (4, 5), der exspiratorisch betonte diastolische Rückfluss im PW-Doppler Signal der Lebervenen (Abb. 3) (5), die erhaltene oder akzentuierte frühdiastolische Gewebe-Doppler Geschwindigkeit im medialen Mitralannulus (E’ medial; Abb. 4A) (6) und der sogenannte Annulus reversus, d.h. das Vorliegen eines gleich hohen oder höheren E’ im medialen verglichen zum lateralen Annulus (Abb. 4A und B) (7). Letzteres Phänomen kommt durch das Tethering des lateralen Annulus infolge des konstriktiven perikardialen Prozesses zustande.
Gemäss einer Studie der Mayo-Clinic scheinen der respiratorische Shift des interventrikulären Septums, das erhaltene oder erhöhte mediale E’ und das exspiratorisch betonte diastolische Backflow-Signal in den Lebervenen am engsten mit der Diagnose der Pericarditis constrictiva assoziiert zu sein (3).
Stadtspital Triemli
Klinik für Kardiologie
Birmensdorferstrasse 497
8063 Zürich
Alain.Bernheim@triemli.stzh.ch
Der Autor hat keine Interessenskonflikte im Zusammenhang mit diesem Artikel.
Literatur:
1. Bertog SC et al. Constrictive pericarditis: etiology and cause-specific survival after pericardiectomy. J Am Coll Cardiol 2004;43:1445-52.
2. Mutyaba AK et al. Constrictive pericarditis requiring pericardiectomy at Groote Schuur Hospital, Cape Town, South Africa: causes and perioperative outcomes in the HIV era (1990– 2012). J Thorac Cardiovasc Surg 2014;148:3058–65.e1.4.
3. Welch TD et al. Echocardiographic diagnosis of constrictive pericarditis: Mayo Clinic criteria. Circ Cardiovasc Imaging 2014;7:526-34.
4. Hatle LK et al. Differentiation of constrictive pericarditis and restrictive cardiomyopathy by Doppler echocardiography. Circulation 1989;79:357–70.
5. Oh JK et al. Diagnostic role of Doppler echocardiography in constrictive pericarditis. J Am Coll Cardiol 1994;23:154–62.
6. Ha JW et al. Differentiation of constrictive pericarditis from restrictive cardiomyopathy using mitral annular velocity by tissue Doppler echocardiography. Am J Cardiol 2004;94:316–9.
7. Reuss CS et al. Using mitral «annulus reversus» to diagnose constrictive pericarditis. Eur J Echocardiogr 2009;10:372–5.
6. Ha JW et al. Differentiation of constrictive pericarditis from restrictive cardiomyopathy using mitral annular velocity by tissue Doppler echocardiography. Am J Cardiol 2004;94:316–9.
7. Reuss CS et al. Using mitral “annulus reversus” to diagnose constrictive pericarditis. Eur J Echocardiogr 2009;10:372–5.
info@herz+gefäss
- Vol. 9
- Ausgabe 1
- Januar 2019