- Kardiale Resynchronisationstherapie
Obwohl es grosse Fortschritte der medikamentösen Herzinsuffizienz-Therapie in den letzten Jahrzehnten gab, weist diese Erkrankung weiterhin eine hohe Mortalität auf und führt zu einer schwerzen Einschränkung der Lebensqualität der Betroffenen. Bei gut ausgewählten Patienten ist die kardiale Resynchronisationstherapie eine etablierte zusätzliche therapeutische Option, welche eine Chance zur Verbesserung von einerseits Prognose und anderseits Lebensqualität gibt.
Bien qu’il y ait eu de grands progrès dans la pharmacothérapie de l’insuffisance cardiaque au cours des dernières décennies, la maladie continue d’être associée à une mortalité élevée et à une détérioration grave de la qualité de vie. Chez des patients bien sélectionnés, la thérapie de resynchronisation cardiaque est une option thérapeutique supplémentaire établie, qui permet d’améliorer le pronostic d’une part et la qualité de vie d’autre part.
Die Herzinsuffizienz bleibt trotz bemerkenswerter Fortschritte in der Therapie in den letzten Jahrzehnten mit einer hohen Mortalität assoziiert. Darüber hinaus ist die dekompensierte Herzinsuffizienz der häufigste Grund für Hospitalisationen in Europa bei Pateinten älter als 65 Jahre.(1, 2). Pumpversagen und ventrikuläre Arrhythmien sind die häufigsten Ursachen für das Versterben von Patienten mit linskventrikulärer Auswurffraktion (LVEF) ≤ 35% (3). Für gut ausgewählte Patienten, stellt die Device-Therapie eine wertvolle Option dar: eine kardiale Resynchronisationstherapie (CRT) kann zur Verbesserung von Symptomen und Auswurffraktion führen; die Implantation einer CRT mit Defibrillatorfunktion (CRT-D) kann einen plötzlichen Herztod verhindern (1).
Funktionsweise
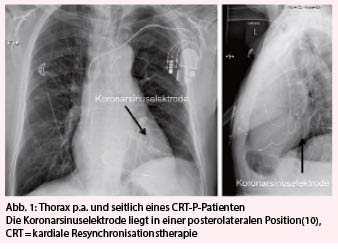
Kardiale Dyssynchronie durch einen Linksschenkelblock (LSB) ist bei Patienten mit Herzinsuffizienz häufig (Prävalenz zwischen 15 und 25%) und geht mit einer schlechten Prognose einher (4, 5). Mechanisch äussert sich die Dyssynchronie bei LSB mit verzögerter Erregung der lateralen Wand des linken Ventrikels. Daraus folgend kontrahiert sie erst zu einem Zeitpunkt, zu dem das Septum bereits wieder relaxiert ist (6–8). Die mechanische Dyssynchronie führt zu Beeinträchtigungen der Funktion des linken Ventrikels: dazu zählen die Verminderung der LVEF, Erhöhung des linksventrikulären Füllungsdruckes, Dilatation des Ventrikels und Zunahme einer Mitralinsuffizienz (8). Elektrisch manifestiert sich die Dyssynchronie als Verbreiterung des QRS-Komplexes im EKG (9). Eine CRT kann die elektrische und somit mechanische Koordination im Herzzyklus wiederherstellen. Dies erfolgt durch simultane elektrische Stimulation des linken und des rechten Ventrikels. Die für die Stimulation des linken Ventrikels notwendige Elektrode wird via Koronarsinus meist in eine posterolaterale Vene implantiert und ist dadurch maximal von der rechts-apikal gelegenen „klassischen“ Elektrode entfernt (Abb. 1). Durch eine entsprechende Programmierung mit einer an sich unphysiologisch kurz gewählten AV-Überleitungszeit können danach entweder beide Ventrikel oder mit komplexen Algorithmen nur der linke Ventrikel bei intrinsischer Überleitung über den rechten Tawaraschenkel rein technisch stimuliert werden (10).
Weil die CRT-Implantation nicht bei allen Patienten den gleichen Erfolg erzielt, ist eine sorgfältige Patientenauswahl entscheidend (7). Im folgenden Abschnitt werden die Evidenz und einige Herausforderungen bei der Indikationsstellung vorgestellt.
Evidenz und Indikationsstellung
Die ersten grossen randomisierten Studien, die das Nutzen einer CRT zeigten, waren Comparison of Medical Therapy, Pacing, and Defibrillation in Heart Failure (COMPANION) und Cardiac Resynchronization – Heart Failure (CARE-HF). In COMPANION wurden 1520 Patienten im Zeitraum zwischen 2000 und 2002 eingeschlossen. Einschlusskriterien waren LVEF ≤ 35% unter optimaler medikamentöser Therapie, NYHA-Stadium III oder IV und QRS-Breite > 120 ms. Die Randomisierung wurde in drei Gruppen durchgeführt: für Placebo, konventionelle CRT (CRT-P) und CRT-D. Den primären Endpunkt, eine Kombination aus Gesamtmortalität oder Hospitalisationen, erreichten signifikant weniger Patienten beider Device-Gruppen. Bemerkenswert ist, dass der Unterschied beim sekundären Endpunkt, Gesamtmortalität alleine, nur zwischen den Placebo- und CRT-D-Gruppen signifikant war (11). In der CARE-HF Studie wurden 813 Patienten mit ähnlichen Einschlusskriterien wie in COMPANION in zwei Gruppen randomisiert: für das Fortführen der optimalen medikamentösen Therapie alleine oder für die zusätzliche Implantation eines CRT-Ps (12). Weil in CARE-HF keine CRT-D implantiert wurden, erklärte sich die beobachtete tiefere Gesamtmortalität in der Device-Gruppe unter anderem auch durch verhinderte Fälle von plötzlichem Herztod aufgrund der Verbesserung der LVEF (8). CARE-HF und COMPANION beeinflussten massgeblich die ursprünglichen Leitlinien zur CRT-Implantation (13).
Spätere randomisierte CRT-Studien schliessen Patienten mit milderer Herzinsuffizienz-Symptomatik ein (hauptsächlich NYHA-Stadium II). In den einzelnen Studien zeigte sich ein Vorteil für die CRT-Patienten hinsichtlich Hospitalisationen (14). Erst in einer Metaanalyse dieser Daten konnte auch ein Überlebensvorteil durch die CRT-Implantation demonstriert werden (14, 15). Die aktuellen Leitlinien beschränken entsprechend die CRT-Indikation nicht nur auf Patienten im NYHA-Stadium III oder IV – diese Intervention kommt auch für diejenigen im NYHA-Stadium II in Frage.
Die Studien nach COMPANION und CARE-HF trugen auch zu weiteren relevanten Veränderungen der Leitlinien mit Betonung auf der QRS-Breite und -Morphologie bei der CRT-Indikationsstellung bei (Abb. 2) (1). Am bedeutendsten unter ihnen ist die Multicenter Automatic Defibrillator Implantation Trial with Cardiac Resynchronization Therapy (MADIT-CRT) Studie. In dieser Studie wurden 1820 NYHA II Patienten mit LVEF ≤ 30% und QRS-Breite > 130 ms eingeschlossen. Der primäre Endpunkt wurde als eine Kombination aus Gesamtmortalität oder Verschlechterung der Herzinsuffizienz festgelegt (16). Dieser wird bei der Interpretation der Ergebnisse kontrovers diskutiert: Obwohl signifikant weniger Patienten der CRT-Gruppe den kombinierten Endpunkt erreichten, konnte kein Unterschied im harten Endpunkt Gesamtmortalität demonstriert werden. Somit trug der ausgewählte weiche Endpunkt Verschlechterung der Herzinsuffizienz, durch gesteigerten Diuretika-Gebrauch definiert, massgeblich zum positiven Studienergebnis bei (17). Eine weitere wichtige Erkenntnis konnte aus den MADIT-CRT Ergebnissen gewonnen werden: In den Subgruppenanalysen zeigte sich, dass nur die Patienten mit einem typischen LSB von der Intervention profitierten (Tab. 2) (6). Hingegen bekamen diejenigen mit RSB oder unspezifischer QRS-Verbreiterung keinerlei Vorteil durch die CRT (1, 10, 16, 17).


Faktoren für ein Ansprechen
Der Einfluss der Device-Implantation auf den natürlichen Verlauf der Herzinsuffizienz wird als Ansprechen auf die CRT bezeichnet. Eine universelle Definition und Quantifizierung diesbezüglich gibt es nicht: in 26 relevanten CRT-Studien wurde die «Response» auf 17 verschiedene Arten festgelegt. Sie umfassen eine Reihe von klinischen und echokardiographischen Parametern wie NYHA-Stadium, Lebensqualität, 6-Minuten-Gehtest oder LVEF-Änderung. Bemerkenswert ist, dass in den CRT-Studien konsistent 25-30% der Patienten die jeweilig definierten Kriterien für Ansprechen nicht erreichen konnten (18).
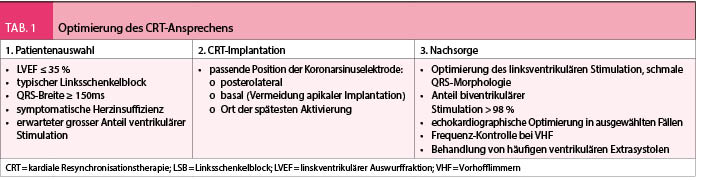
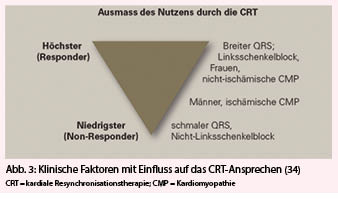
Eine gute Patientenselektion ist somit entscheidend, um ein Ansprechen auf die CRT erzielen zu können und unnötige Interventionen mit den damit verbundenen Kosten und Risiken zu vermeiden. Einer der am besten untersuchten Ansätze dafür ist die Echokardiographie. Aufgrund der jedoch tiefen prädiktiven Werte der ausgewerteten Dyssynchronie-Parameter eignet sich diese Modalität aktuell nicht, um die optimalen Patienten für eine CRT zu identifizieren (abgesehen von der LVEF-Bestimmung) (19). Als hilfreich zeigen sich bei der Patientenselektion Überlegungen zu extrakardialen Faktoren wie Adipositas, COPD oder PAVK, welche eine Verbesserung der körperlichen Leistungsfähigkeit trotz echokardiographischem Ansprechen verunmöglichen. Für das bessere Ansprechen relevante, aber nicht beeinflussbare Faktoren sind das weibliche Geschlecht und die nicht-ischämische Kardiomyopathie. Des Weiteren können technische Schwierigkeiten bei der Implantation oder Device-Programmierung im Follow-Up eine Rolle spielen, wie z.B. die Unmöglichkeit, die Koronarsinuselektrode an einem günstigen Ort zu platzieren (Narbenregion, apikale Position - zu nahe bei der RV-Elektrode), oder weil die Eigenüberleitung wie beim Vorhofflimmern zu rasch erfolgt und somit keine Resynchronisation stattfinden kann (s. Tab. 1 und Abb. 3) (7, 8, 10, 20). Für den positiven Krankheitsverlauf bleibt auch nach der Device-Implantation das Fortführen der optimalen pharmakologischen Therapie im Follow-Up weiterhin notwendig (7, 8).
Patienten mit Vorhofflimmern
Bei Vorhofflimmern kann eine zu schnelle intrinsische Eigenüberleitung in den Ventrikel zum Verringern des Anteils der biventrikulären Stimulation führen. Der Anteil der biventrikulären Simulation sollte über 98% aller Schläge betragen. Somit ist auf der einen Seite diese Rhythmusstörung mit schlechterem Ansprechen auf die CRT assoziiert. Auf der anderen Seite wurden leider nur wenige Patienten mit Vorhofflimmern in den grossen, bereits hier vorgestellten CRT-Studien eingeschlossen (21). Jedoch ist das Vorhofflimmern auch eine häufige Komorbidität in der Herzinsuffizienz und findet sich bei über 25 % der Patienten in NYHA-Stadium III und IV (22). CRT stellt aber auch hier eine IIa Indikation dar sofern bei den Patienten eine biventrikuläre Stimulation entweder durch Ablation des Vorhofflimmers oder des AV-Knotens erreicht werden kann. In randomisierten Studien konnte auch für diese Population eine Verringerung der Hospitalisationsrate (für Herzinsuffizienz) bzw. sogar der Mortalität und Hospitalisationsrate gezeigt werden. Dies wird mit den kürzlich publizierten Ergebnissen der Ablate and Pace in Atrial Fibrillation plus Cardiac Resynchronization Therapy (APAF-CRT) Studie verdeutlicht: In ihr wurden 102 Patienten mit permanentem VHF und QRS-Dauer < 110 ms für medikamentöse Frequenzkontrolle oder CRT-Implantation mit anschliessender AV-Knoten-Ablation 1:1 randomisiert (23). Ebenso wurde ein positives Ergebnis beim selben Endpunkt in der Catheter ablation versus standard conventional treatment in patients with left ventricular dysfunction and atrial fibrillation (CASTLE-AF) Studie demonstriert. In CASTLE-AF wurden 179 VHF-Patienten mit CRT-D oder ICD für medikamentöse Therapie oder VHF-Ablation randomisiert. Die Randomisierung wurde u.a. danach stratifiziert, ob der Patient CRT-Träger ist. Somit konnte gezeigt werden, dass auch diese Subgruppe von der Intervention profitierte (24).
CRT bei Herzinsuffizienz und höhergradigen AV-Blockierungen
Eine bedeutende CRT-Studie, deren Studienpopulation zur Hälfte aus VHF-Patienten bestand, ist Biventricular versus Right Ventricular Pacing in Heart Failure Patients with Atrioventricular Block (BLOCK-HF). In ihr wurden 691 Patienten mit LVEF ≤ 50% und Schrittmacherindikation aufgrund eines AV-Blocks eingeschlossen. Die Randomisierung erfolgte zur CRT- oder konventionellen Schrittmacher-Implantation. Die CRT-Patienten hatten ein besseres Outcome hinsichtlich des kombinierten Endpunktes Gesamtmortalität, Notwendigkeit für intravenöse Diuretika oder ≥ 15% Zunahme des indexierten endsystolischen Volumens. Mit höherem Anteil von biventrikulärer Stimulation profitierten die VHF-Patienten mehr (25). Bei Patienten mit LVEF < 40% und ICD-Indikation konnte in The Dual Chamber and VVI Implantable Defibrillator (DAVID) Studie gezeigt werden, dass mit Zunahme der rechtsventrikulären Stimulation das Sterbe- oder Hospitalisationsrisiko zunehmen (26). Basierend auf den Daten aus BLOCK-HF und DAVID wird der Einsatz von CRT statt konventioneller Schrittmacher empfohlen, wenn bei Patienten mit reduzierter LVEF ein grosser Anteil rechtsventrikulärer Stimulation zu erwarten ist (1, 25).
CRT Implantationen in der Schweiz
Im kürzlich publizierten Vergleich vom CRT Implantationsverhalten in der Schweiz mit Europa zeigte sich, dass die Schweizer Patienten mit 71 Jahren im Schnitt älter waren und geringere Herzinsuffizienzsymptome aber vermehrt eine chronische Niereninsuffizienzsymptome aber vermehrt eine chronische Niereninsuffizienz aufwiesen. In der Schweiz ist mit 37% der Anteil an CRT-Schrtittmachern höher als im europäischen Schnitt. Einen kompletten LSB wiesen zwei Drittel der Patienten auf, 38% hatten Vorhofflimmern und rund ein Viertel höhergradige AV-Blockierungen (27).
Spezielle Aspekte bei der Defibrillator-Indikation bei CRT-Patienten
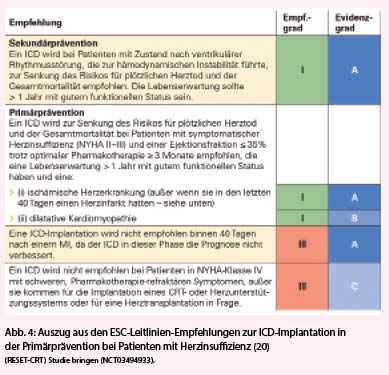
Häufig liegt eine gleichzeitige ICD- und CRT-Indikation vor (Abb. 4) (1, 20, 28, 29). Dies resultiert darin, dass in der Schweiz doppelt so viele CRT-D als CRT-P implantiert werden. Wiederum ist CRT-D im Vergleich zu CRT-P mit höheren Kosten und potenziell belastenden Komplikationen behaftet. Dazu zählen unter anderem Infektionen, Elektrodendysfunktion und inadäquate Schockabgaben (10). Die Entscheidung für oder gegen einen Defibrillator-Back-Up bei der CRT soll ausführlich mit dem Patienten diskutiert werden. Dies ist insbesondere bei der kontroversen Datenlage in der nicht-ischämischen Kardiomyopathie wichtig, gilt aber auch bei den KHK-Patienten (1, 30-32). Ein robuster und vielversprechender prognostischer Faktor für das Nutzen der CRT-D-Implantation erscheint das Loate Gadolinium Enhancement (LGE) im Herz-MRI zu sein (30, 31, 33). Es bedarf weiterer randomisierter Studien, um die Auswahlkriterien für die CRT-D-Indikation zu optimieren – wichtige Erkenntnisse in dieser Hinsicht wird die Re-evaluation of Optimal Re-synchronistion Therapy in Patients With Chronic Heart Failure (RESET-CRT) Studie bringen (NCTO3494933).
Das Ziel des Defibrillator-Back-Ups bei der CRT-D ist es, den plötzlichen Herztod zu verhindern. Mit Fortschreiten der Herzinsuffizienzm^, aber auch dem Auftreten von Komorbiditäten, muss dieser Punkt vom Arzt erneut angesprochen werden. Eine Deaktivierung der Defibrillatorfinktion des CRT-Ds auf Wunsch des Patienten ist möglich.
Kardiologie Universitätsspital Basel
Petersgraben 4
4031 Basel
Prof. Sticherling hat Referentenhonorare von Microport, Medtronic, Biotronik und Boston Scientific erhalten.
Prof. Schär hat Referentenhonorare von Microport und Medtronic erhalten.
Dr. Madaffari und Dr. Kozhuharov haben keine Interessenskonflikte anzugeben.
- Die Device-Therapie ist eine wertvolle Option für gut ausgewählte Patienten mit symptomatischer Herzinsuffizienz, typischem LSB und einer QRS-Breite > 130 ms.
- Die primärprophylaktische CRT-D-Implantation solll auch sorgfältig zusammen mit diesen Patienten evaluiert werden.
- Es besteht solide Evidenz für die Steigerung der Lebensqualität und Lebenserwartung mit dem Einsatz der CRT in dieser vulnerablen Patientenpopulation.
Messages à retenir
- La thérapie par appareil est une option intéressante pour les patients bien sélectionnés souffrant d’insuffisance cardiaque symptomatique, avec une largeur LSB et QRS typique de > 130 ms.
- L’implantation prophylactique primaire d’un CRT-D doit également être soigneusement évaluée avec ces patients.
- Il existe des preuves solides de l’amélioration de la qualité de vie et de l’espérance de vie grâce à l’utilisation de la CRT chez cette population de patients vulnérables.
Literatur:
1. Ponikowski P, Voors AA, Anker SD, et al. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur. Heart J. 2016;37:2129–2200. Available at: http://eurheartj.oxfordjournals.org/lookup/doi/10.1093/eurheartj/ehw128.
2. Miró Ò, Peacock FW, McMurray JJ, et al. European Society of Cardiology – Acute Cardiovascular Care Association position paper on safe discharge of acute heart failure patients from the emergency department. Eur. Hear. J. Acute Cardiovasc. Care 2017;6:311–320. Available at: http://acc.sagepub.com/cgi/content/long/2048872616633853v1.
3. Narang R, Cleland JGF, Erhardt L, et al. Mode of death in chronic heart failure: A request and proposition for more accurate classification. Eur. Heart J. 1996;17:1390–1403. Available at: https://academic.oup.com/eurheartj/article-lookup/doi/10.1093/oxfordjournals.eurheartj.a015074. Accessed May 27, 2018.
4. Khan NK, Goode KM, Cleland JGF, et al. Prevalence of ECG abnormalities in an international survey of patients with suspected or confirmed heart failure at death or discharge. Eur. J. Heart Fail. 2007;9:491–501.
5. Baldasseroni S, Gentile A, Gorini M, et al. Intraventricular conduction defects in patients with congestive heart failure: left but not right bundle branch block is an independent predictor of prognosis. A report from the Italian Network on Congestive Heart Failure (IN-CHF database). Ital. Heart J. 2003;4:607–13. Available at: http://www.ncbi.nlm.nih.gov/pubmed/14635378. Accessed September 23, 2018.
6. Strauss DG, Selvester RH, Wagner GS. Defining Left Bundle Branch Block in the Era of Cardiac Resynchronization Therapy. Am. J. Cardiol. 2011;107:927–934. Available at: https://www.sciencedirect.com/science/article/pii/S0002914910024215. Accessed May 25, 2018.
7. Madhavan M, Mulpuru SK, McLeod CJ, Cha YM, Friedman PA. Advances and Future Directions in Cardiac Pacemakers: Part 2 of a 2-Part Series. J. Am. Coll. Cardiol. 2017;69:211–235.
8. Schaer BA, Sticherling C. Device-Therapie der chronischen Herzinsuffizienz. Ther. Umschau 2011;68:89–93. Available at: http://econtent.hogrefe.com/doi/10.1024/0040-5930/a000125. Accessed May 27, 2018.
9. Iuliano S, Fisher SG, Karasik PE, Fletcher RD, Singh SN. QRS duration and mortality in patients with congestive heart failure. Am Hear. J 2002;143:1085–1091.
10. Schär BA, Sticherling C. CRT in the elderly. Cardiovasc 2016;15:2–5.
11. Bristow MR, Saxon LA, Boehmer J, et al. Cardiac-Resynchronization Therapy with or without an Implantable Defibrillator in Advanced Chronic Heart Failure. N. Engl. J. Med. 2004;350:2140–2150. Available at: http://www.nejm.org/doi/abs/10.1056/NEJMoa032423. Accessed May 25, 2018.
12. Cleland JGF, Daubert J-C, Erdmann E, et al. The Effect of Cardiac Resynchronization on Morbidity and Mortality in Heart Failure. N. Engl. J. Med. 2005;352:1539–1549. Available at: http://www.ncbi.nlm.nih.gov/pubmed/15753115. Accessed May 25, 2018.
13. Vardas PE, Auricchio A, Blanc J-J, et al. Guidelines for cardiac pacing and cardiac resynchronization therapy: The Task Force for Cardiac Pacing and Cardiac Resynchronization Therapy of the European Society of Cardiology. Developed in Collaboration with the European Heart Rhythm Association. Eur. Heart J. 2007;28:2256–2295. Available at: http://www.ncbi.nlm.nih.gov/pubmed/17726042. Accessed September 25, 2018.
14. Amal Muthumala. Overview of devices in advanced heart failure. E-journal-of-cardiology-practice 2017;14. Available at: escardio.org/Journals/E-Journal-of-Cardiology-Practice/Volume-14/Overview-of-devices-in-advanced-heart-failure.
15. Al-Majed NS, McAlister FA, Bakal JA, Ezekowitz JA. Meta-analysis: Cardiac resynchronization therapy for patients with less symptomatic heart failure. Ann. Intern. Med. 2011;154:401–412.
16. Moss AJ, Hall WJ, Cannom DS, et al. Cardiac-Resynchronization Therapy for the Prevention of Heart-Failure Events. N. Engl. J. Med. 2009;361:1329–1338. Available at: http://www.nejm.org/doi/abs/10.1056/NEJMoa0906431. Accessed May 25, 2018.
17. Jessup M. MADIT-CRT — Breathtaking or Time to Catch Our Breath? N. Engl. J. Med. 2009;361:1394–1396. Available at: http://www.nejm.org/doi/abs/10.1056/NEJMe0907335. Accessed May 25, 2018.
18. Fornwalt BK, Sprague WW, Bedell P, et al. Agreement is poor among current criteria used to define response to cardiac resynchronization therapy. Circulation 2010;121:1985–1991. Available at: http://www.ncbi.nlm.nih.gov/pubmed/20421518. Accessed May 25, 2018.
19. Chung ES, Leon AR, Tavazzi L, et al. Results of the Predictors of Response to CRT (PROSPECT) Trial. Circulation 2008;117:2608–2616. Available at: http://www.ncbi.nlm.nih.gov/pubmed/18458170. Accessed May 25, 2018.
20. Laufs U, Anker SD, Baldus S, et al. Deutsche Gesellschaft für Kardiologie – Herz-und Kreislaufforschung e.V. (2017) ESC Pocket Guidelines. Herzinsuffizienz, Version 2016. Börm Bruckmeier Verlag GmbH, Grünwald Kurzfassung der “ESC Guidelines for the Diagnosis and Treatment of Acute and Chron. 2017.
21. Wilton SB, Leung AA, Ghali WA, Faris P, Exner D V. Outcomes of cardiac resynchronization therapy in patients with versus those without atrial fibrillation: A systematic review and meta-analysis. Hear. Rhythm 2011;8:1088–1094. Available at: https://www.sciencedirect.com/science/article/pii/S154752711100172X. Accessed May 27, 2018.
22. Maisel WH, Stevenson LW. Atrial fibrillation in heart failure: epidemiology, pathophysiology, and rationale for therapy. Am. J. Cardiol. 2003;91:2–8. Available at: https://www.sciencedirect.com/science/article/pii/S0002914902033738?via%3Dihub. Accessed May 27, 2018.
23. Brignole M, Pokushalov E, Pentimalli F, et al. A randomized controlled trial of atrioventricular junction ablation and cardiac resynchronization therapy in patients with permanent atrial fibrillation and narrow QRS. Eur. Heart J. 2018:1–10. Available at: https://academic.oup.com/eurheartj/advance-article/doi/10.1093/eurheartj/ehy555/5078460.
24. Marrouche NF, Brachmann J, Andresen D, et al. Catheter Ablation for Atrial Fibrillation with Heart Failure. N. Engl. J. Med. 2018;378:417–427. Available at: http://www.nejm.org/doi/10.1056/NEJMoa1707855.
25. Curtis AB, Worley SJ, Adamson PB, et al. Biventricular Pacing for Atrioventricular Block and Systolic Dysfunction. N. Engl. J. Med. 2013;368:1585–1593. Available at: http://www.nejm.org/doi/10.1056/NEJMoa1210356. Accessed May 27, 2018.
26. Wilkoff BL, Cook JR, Epstein AE, et al. Dual-chamber pacing-or ventricular backup pacing in patients with an implantable defibrillator: The Dual Chamber and VVI Implantable Defibrillator (DAVID) Trial. J. Am. Med. Assoc. 2002;288:3115–3123. Available at: http://www.ncbi.nlm.nih.gov/pubmed/12495391. Accessed May 25, 2018.
27. Zeljkovic I, Burri H, Breitenstein A, et al. Cardiac Resynchronisation Therapy (CRT) Survey II: CRT implantation in Europe and in Switzerland. Swiss Med. Wkly. 2018;148:w14643. Available at: http://www.ncbi.nlm.nih.gov/pubmed/30141519%0Ahttps://doi.emh.ch/smw.2018.14643.
28. Priori SG, Blomström-Lundqvist C, Mazzanti A, et al. 2015 ESC Guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death – Addenda. Eur. Heart J. 2015;36:2793–867. Available at: http://www.ncbi.nlm.nih.gov/pubmed/16935866%5Cnhttp://europace.oxfordjournals.org/cgi/doi/10.1093/europace/eul108%5Cnhttp://www.ncbi.nlm.nih.gov/pubmed/26320108.
29. Brignole M, Auricchio A, Baron-Esquivias G, et al. 2013 ESC Guidelines on cardiac pacing and cardiac resynchronization therapy. Europace 2013;15:1070–1118. Available at: https://watermark.silverchair.com/eht150.pdf?token=AQECAHi208BE49Ooan9kkhW_Ercy7Dm3ZL_9Cf3qfKAc485ysgAAAbAwggGsBgkqhkiG9w0BBwagggGdMIIBmQIBADCCAZIGCSqGSIb3DQEHATAeBglghkgBZQMEAS4wEQQMxoSPZgMLW_BC5RGqAgEQgIIBY6atkz5ggS0K-g3-B2fznEZp_ww3WryCF1ObIaUpOyoT3n1b. Accessed May 25, 2018.
30. Acosta J, Fernández-Armenta J, Borràs R, et al. Scar Characterization to Predict Life-Threatening Arrhythmic Events and Sudden Cardiac Death in Patients With Cardiac Resynchronization Therapy: The GAUDI-CRT Study. JACC Cardiovasc. Imaging 2018;11:561–572.
31. Leyva F, Zegard A, Acquaye E, et al. Outcomes of Cardiac Resynchronization Therapy With or Without Defibrillation in Patients With Nonischemic Cardiomyopathy. J. Am. Coll. Cardiol. 2017;70:1216–1227.
32. Køber L, Thune JJ, Nielsen JC, et al. Defibrillator Implantation in Patients with Nonischemic Systolic Heart Failure. N. Engl. J. Med. 2016;375:1221–1230. Available at: http://www.nejm.org/doi/10.1056/NEJMoa1608029. Accessed May 25, 2018.
33. Kuruvilla S, Adenaw N, Katwal AB, Lipinski MJ, Kramer CM, Salerno M. Late gadolinium enhancement on cardiac magnetic resonance predicts adverse cardiovascular outcomes in nonischemic cardiomyopathy: a systematic review and meta-analysis. Circ. Cardiovasc. Imaging 2014;7:250–258. Available at: http://www.ncbi.nlm.nih.gov/pubmed/24363358. Accessed May 26, 2018.
34. Israel CW, Bänsch D, Breithardt O-A, et al. Deutsche Gesellschaft für Kardiologie – Herz-und Kreislaufforschung e.V. (2015) ESC Pocket Guidelines. Schrittmacher- und kardiale Resynchronisationstherapie, Version 2013. Börm Bruckmeier Verlag GmbH, Grünwald Kurzfassung der “ESC Guidelines on cardiac p.
info@herz+gefäss
- Vol. 8
- Ausgabe 6
- November 2018






