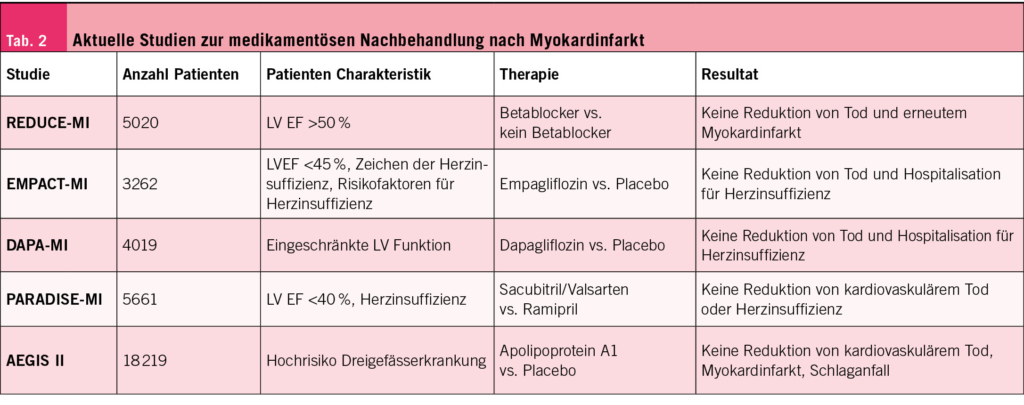
- Medikamentöse Therapie nach Myokardinfarkt
Beta-blocker nach Myokardinfarkt bei Patienten mit erhaltener Pumpfunktion
Studie REDUCE-MI: Der Einsatz von Betablockern als medikamentöse Langzeittherapie nach Myokardinfarkt beruht auf Studien, die vor der aktuellen modernen Behandlung durchgeführt wurden. Ob Betablocker heutzutage nach erfolgreicher Revaskularisation mittels primärer PCI bei erhaltener Pumpfunktion (LV EF >50 %) einen Nutzen bringen, ist nicht klar.
Eine grosse internationale Studie (REDUCE-MI) randomisierte 5020 Patienten mit ST-Hebungsinfarkt (STEMI) und NSTEMI nach erfolgreicher Revaskularisation zu Betablocker oder kein Betablocker in der Nachbehandlung (1). Alle Patienten wurden koronarografiert und über 99 % mittels PCI oder ACBP revaskularisiert. Die verwendeten Betablocker waren 100 mg Metoprolol oder 5 mg Bisoprolol. Die Patienten wurden im Mittel 2 Tage nach Infarkt eingeschlossen und über 3.5 Jahre nachverfolgt. Es zeigt sich kein Unterschied im primären Endpunkt (Gesamtmortalität oder neuer Myokardinfarkt) (Betablocker 7.9 % vs. kein Betablocker 8.3 % (HR 0.96; 95 % Konfidenzintervall 0,79-1,16; P= 0,64). Für alle sekundären Endpunkte, wie kardiovaskulärer Tod, Hospitalisation für Vorhofflimmern, Herzinsuffizienz, AV-Block, Einlage eines Schrittmachers ergab sich ebenfalls kein Unterschied zwischen den beiden Gruppen.
Kommentar: Die Resultate kamen auf dem Hintergrund einer anderweitig exzellenten medikamentösen Sekundärprävention mit anti-thrombotischer und cholesterinsenkender Therapie sowie ACE-Hemmer Therapie zustande. Die tiefer als erwartete Ereignisrate führte zu weiten Konfidenzintervallen. Daher ist die Studie ein Hinweis, dass nach erfolgreicher Revaskularisation der Betablocker bei erhaltener Pumpfunktion wahrscheinlich keinen Zusatznutzen zur sonstigen Therapie bringt, aber der definitive Beweis ist mit dieser Studie noch nicht erbracht.
Empagliflozin nach Myokardinfarkt mit reduzierter Pumpfunktion und Zeichen der Herzinsuffizienz
Studie EMPACT-MI: Ob der frühe Einsatz des SGLT-2 Inhibitors Empagliflozin bei Patienten nach Myokardinfarkt, welche eine eingeschränkte Pumpfunktion, oder Zeichen einer Linksherzinsuffizienz entwickeln, einen Vorteil zusätzlich zur bisherigen medikamentösen Therapie bringen, wurde in EMPACT-MI Studie untersucht (2). Empagliflozin brachte keinen prognostischen Nutzen. Siehe «Cardio Flash» von Professor Otmar Pfister in dieser Ausgabe.
Kommentar: Die Ereignisrate für ein erneutes Ereignis war auch in dieser Studie tiefer als erwartet. Wie bei Patienten mit normaler Pumpfunktion scheint sich auch bei Patienten mit LV Dysfunktion die Prognose durch die gegenwärtig etablierte Myokardinfarktbehandlung gegenüber früheren Studien verbessert zu haben.
Etablierte Therapien müssen neu evaluiert werden!
Die gegenwärtig von den Guidelines der Fachgesellschaften etablierte Behandlung des Myokardinfarktes hat die Sterblichkeit und die kurze und mittelfristige Prognose stark verbessert. Diese Behandlung umfasst die schnelle, vollständige Revaskularisation mittels primärer PCI, gefolgt von einer medikamentösen Therapie mit doppelter Plättchenhemmung, Cholesterinsenkung, einer Hemmung des Renin-Angiotensin-Systems und Betablockade sowie einer rigorosen Kontrolle der kardiovaskulären Risikofaktoren.
Eine Erweiterung der etablierten Therapie mit dem Ziel die Prognose nach dem Herzinfarkt weiter zu verbessern scheint schwierig. So haben die oben vorgestellten und weitere Medikamente (siehe Tabelle) keinen zusätzlichen Nutzen gebracht. Eine stärkere Hemmung des RAAS-Systems als durch einen ACE-Hemmer mittels Sacubitril/Valsartan (3) oder die zusätzliche Cholesterinsenkung mittels Apolipoprotein A1 Infusion (4) zeigten keinen Vorteil. Der fehlende Nutzen des SGLT-2 Inhibitors Empagliflozin überrascht ebenfalls nicht. Hatte doch schon eine frühere Studie bei Patienten mit reduzierter Pumpfunktion mit Dapagliflozin (DAPA-MI) ebenfalls keinen Vorteil dieser Medikamente bei der unmittelbaren Nachbehandlung des Myokardinfarkts bezüglich Tod oder Herzinsuffizienz gebracht (5). Auch bei der DAPA-MI Studie war die Ereignisrate übrigens unerwartet tief, so dass die Investigatoren während der Studie den primären Endpunkt änderten und insgesamt sieben Endpunkte kombinierten. Dabei zeigte sich, wie zu erwarten, zwar eine Verbesserung der metabolischen Parameter, z.B. Abnahme des Körpergewichts, aber kein prognostischer Nutzen.
Deeskalation der Therapie
Angesichts der guten Resultate der Behandlung des akuten Myokardinfarktes, stellt sich viel mehr die Frage nach einer Deeskalation der medikamentösen Nachbehandlung bei gewissen Patientenpopulationen. Die Guidelines der europäischen Gesellschaft für Kardiologie 2023 tragen der sich abzeichnenden Evidenz bereits Rechnung (6). Bei Patienten mit erhaltener Pumpfunktion geben die Guidelines für Betablocker und ACE-Hemmer «nur» eine IIa Empfehlung ab, dh. diese Medikamente sollten in Erwägung gezogen, aber müssen nicht gegeben werden.
Bezüglich der Betablocker stellen sich drei wichtige Fragen: 1. Sollen sie überhaupt eingesetzt werden bei einer Auswurffraktion von >40 %, respektive >50 %? 2. Wenn Betablocker eingesetzt werden, wie lange sollen sie verabreicht werden? Können Betablocker bei fehlender Herzinsuffizienz nach einem Jahr gestoppt werden? Drei grosse laufende Studien (DANBLOCK, BETAMI, REBOOT) untersuchen die erste Frage und drei grosse Studien (SMART DECISION, AβYSS, ABBREVIATE) die anderen Fragen. Die Resultate dieser Studien werden in den nächsten 2-3 Jahren veröffentlicht werden (7). Sie sind wichtig, um Klarheit zu schaffen. Denn gegenwärtig besteht ohne Evidenz aus Studien die – wahrscheinlich berechtigte – Praxis bei erhaltener Auswurffraktion auf den Betablocker zu verzichten.
Ähnlich verhält es sich beim ACE-Hemmer nach Myokardinfarkt und erhaltener Auswurffraktion. Da der ACE-Hemmer das remodeling nach Myokardinfarkt unterstützt, wäre hier eine Klärung dringend. Leider sind gegenwärtig keine grossen Studien am Laufen. Dabei wäre eine Überprüfung der Validität von über 40-jährigen Studienresultaten nicht nur beim Myokardinfarkt dringend. Denn viele veraltete Evidenz fliesst weiterhin in die Guidelines ein. Die Behandlung vieler Krankheiten hat sich in den letzten Jahrzehnten stark verändert und die ehemals etablierten, aber nun vielleicht überflüssigen Therapien, müssen hinterfragt werden.
Stadtspital Zürich Triemli
Klinik für Kardiologie
Birmensdorferstrasse 497
8063 Zürich
franz.eberli@triemli.zuerich.ch
1. Yndigegn T et al. New Engl J Med 2024;390:1372-81. DOI:10.1056/NEJMoa2401479
2. Butler J. et al. New Engl J Med 2024;390:1455-66. DOI:10.1056/NEJMoa2314051
3. Pfeffer MA. et al. New Engl J Med 2021;385:1845-55. DOI:10.1056/NEJMoa2104508
4. Gibson CM. et al. New Engl J Med 2024;390:1560-71. DOI:10.1056/NEJMoa2400969
5. James S. et al. NEJM Evid 2024;3(2) DOI:10.1056/EVIDoa2300286
6. Byrne RA. et al. Eur Heart J 2023;44:3720-3826. doi.org/10.1093/eurheartj/ehad191
7. Steg GP. New Engl J Med 2024;390:1434-36. DOI:10.1056/NEJMoa2402731
info@herz+gefäss
- Vol. 14
- Ausgabe 4
- Juli 2024