- Myokardinfarkte und Myokardischämie nach nichtkardialen Operationen
Perioperative Herzmuskelschädigungen nach nichtkardialen Operationen sind mit einer erhöhten Mortalität assoziiert und werden aufgrund ihrer häufig asymptomatischen Präsentation ohne systematisches Screening leicht übersehen. Das Management von perioperativen Myokardischämien (PMI) richtet sich nach der vermuteten Pathophysiologie, wobei bislang noch zu wenig Daten für klare Therapieempfehlungen vorliegen.
Les lésions périopératoires du muscle cardiaque après une chirurgie non cardiaque sont associées à une mortalité accrue et sont facilement négligées en raison de leur présentation souvent asymptomatique sans dépistage systématique. La prise en charge de l’ infarctus du myocarde périopératoire (IPM) est basée sur la physiopathologie présumée, bien que trop peu de données soient disponibles jusqu’ à présent pour formuler des recommandations thérapeutiques claires.
Wenn nichtkardiale Operationen aufs Herz schlagen
Trotz stetiger Verbesserung der chirurgischen und anästhesiologischen Technik sind nichtkardiale Operationen weiterhin mit einer relevanten Mortalität behaftet (1), welche in Risikopatienten bis 10% beträgt (2, 3). Eine zunehmende Anzahl Studien konnte ischämische Herzmuskelschädigungen als stark assoziiert mit dieser Mortalität zeigen (2–6).
Diagnose und Prognose
Die Prävalenz eines akuten Myokardinfarkts nach nichtkardialen Operationen variiert je nach Art der Operation und Population von 0.2 bis 36% (4, 5). Die Mortalität nach perioperativen akuten Myokardinfarkten (pAMI) ist immer noch hoch (15%), potentiell aufgrund der Schwierigkeit die Diagnose im perioperativen Setting zu stellen (4, 7). Für die Diagnose des Herzinfarkts sind im nichtoperativen Setting Biomarker, insbesondere hochsensitive kardiale Troponintests (hs-cTn), die zentrale diagnostische Komponente (8). Um die Diagnose eines Myokardinfarkt zu stellen braucht es obligat den Nachweis erhöhter und dynamischer cTn-Werte, definiert durch einen akuten Anstieg und/oder Abfall von cTn sowie einem cTn-Wert oberhalb des 99. Perzentile (8). Zusätzlich verlangt die universelle Definition das Vorliegen von ischämischen Symptomen (v.a. Brustschmerzen), ischämische EKG-Veränderungen oder den Nachweis neuer Wandbewegungsstörungen (8). Im perioperativen Setting zeigen jedoch die meisten Patienten (> 50%), am ehesten aufgrund der adäquaten Analgesie oder sogar Sedation, keine typischen ischämischen Symptome wie Brustschmerz. Die Spezifität des EKG ist ebenfalls, wie auch im nichtoperativen Setting, gering (3, 9). Daher wurde vorgeschlagen bei Patienten, welche das zentrale Kriterium eines dynamischen und erhöhten cTn-Werts erfüllen, die Diagnose einer perioperativen Myokardischämie (PMI) zu stellen. Sollte ein weiteres Kriterium für die Definition eines akuten Myokardinfarktes erfüllt sein (z.B. Brustschmerz, EKG-Veränderungen) handelt es sich um einem pAMI. In aktuellen prospektiven Studien war die Prävalenz der PMI 16-17% (2, 3). Diese war mit einer Mortalität von 10% in 30 Tagen und 23% nach einem Jahr assoziiert. Von diesen PMI erfüllten die Minderheit (22-29%) ein zusätzliches Kriterium für die Diagnose eines Myokardinfarkts, dies hatte jedoch keinen Effekt auf die Mortalität nach 30 Tagen, welche 11% bei Patienten mit asymptomatischem PMI und 9% bei Patienten mit pAMI war(3).
Aufgrund der oft asymptomatischen Präsentation im perioperativen Setting und der relevanten Mortalität von PMI empfehlen aktuelle perioperative Guidelines neu ein PMI-Screening mit cTn in Risikopatienten durchzuführen (8, 10–12). Weil die meisten PMI in den ersten drei Tagen nach der Operation auftreten, wird es empfohlen cTn einmal vor der Operation und dann täglich nach der Operation durchzuführen (8, 12). Der präoperative cTn-Wert erscheint aufgrund der zunehmend älteren und kardiovaskulär komorbiden chirurgischen Patienten unerlässlich, da diese immer häufiger chronisch erhöhte cTn-Werte aufweisen. In einer Studie mit Risikopatienten hatten bereits 51% der Patienten präoperativ erhöhte cTn-Werte (3). Entsprechend scheint eine Blutabnahme vor der Operation wesentlich, um postoperative akute Erhöhungen mit Interventionsbedarf sicher von chronischen Erhöhungen ohne akuten Krankheitswert unterscheiden zu können.
Pathophysiologie von PMI
Aktuell gibt es noch Unklarheiten zur Pathophysiologie von PMI, insbesondere der Frage nach der Häufigkeit von Typ I Infarkten (mit Ruptur eines atherosklerotischen Plaques) vs der von Typ II Infarkten (aufgrund einer Dysbalance von koronarer Blutversorgung und myokardialem Sauerstoffverbrauch) und Herzmuskelschädigungen durch andere Erkrankungen wie Sepsis, Tachyarrhythmien oder Herzinsuffizienz (3, 13). Initiale Studien, in welche nur symptomatische, zur Koronarangiographie zugewiesene Patienten eingeschlossen wurden, zeigten in nur 50% der Patienten mit PMI einen Hinweis auf Plaqueruptur als Korrelat für einen Typ I Infarkt(7). Aufgrund der Häufung von mit Typ II-Infarkten assoziierten Faktoren direkt postoperativ (Hypotonie, Blutung, Hypoxie, Inflammation) erscheinen Typ II Mechanismen als wahrscheinliche Auslöser für die Mehrheit von PMI.
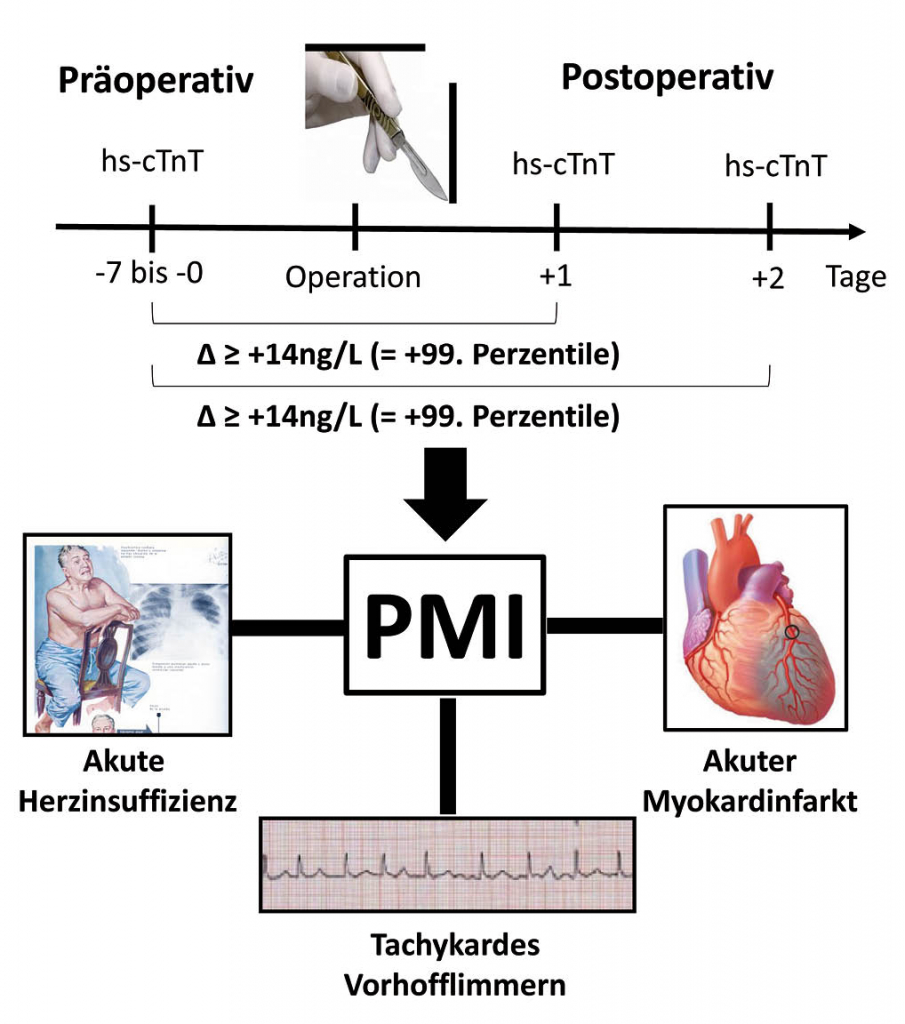
Oberer Abschnitt: Schematische Darstellung des Ablaufs des Routinescreenings für perioperative Myokardischämien (PMI) nach nichtkardialen Operationen in Risikopatienten inkl. Diagnosekriterium für PMI auf Basis von hochsensitivem kardialen Troponin T (hs-cTnT). Unterer Abschnitt: wichtige kardiale Ursachen für PMI
Management von PMI
Systematisches Screening von Risikopatienten ermöglicht es, Erst massnahmen bei Erkennung einer PMI durchzuführen um potentiell das Überleben zu verbessern. Eine Pilotstudie konnte positive Effekte zeigen: In einer retrospektiven Analyse führte die Diagnose einer PMI durch Screening zu einer Intensivierung der medikamentösen Therapie in 65% der Patienten, was mit einem Trend Richtung Reduktion kardiovaskulärer Komplikationen oder Tod einherging (HR 0.63 CI, 0.10–1.19; P = 0.45) (14). In einer retrospektiven Analyse zeigten Sandoval et al, dass auch in einer Population mit vorbestehender schwerer kardiovaskulärer Erkrankung noch eine Optimierung der Medikation möglich war in Patienten mit entdeckter PMI (15).
Aktuell gibt es noch wenig Daten zur Behandlung von PMI, sodass die Therapie aktuell für jeden Patienten individuell festgelegt werden muss. Es existieren jedoch bereits erste Daten zu möglichen Strategien.
Medikamentöse Optionen
Sekundärprophylaktische Medikation
Statine und Acetylsalicylsäure (ASS) mit erwiesenem Nutzen nach akutem Myokardinfarkt scheinen auch nach PMI mit einer verbesserten Prognose assoziiert zu sein, wie eine Subanalyse der POISE-Studie zeigte (multivariable OR von 0.26, 95%CI 0.13-0.54 für Statin und 0.54, 95%CI 0.29-0.99 für ASS)(16). Während Statine im perioperativen Setting unproblematisch erscheinen, muss die Empfehlung zur ASS zusammen mit dem behandelnden Chirurgen getroffen werden aufgrund des erhöhten Blutungsrisikos. Prophylaktisch gegebenes ASS hingegen zeigte keinen Hinweis für einen positiven Effekt auf das Auftreten von Herzinfarkten bei nichtkardialen Operationen, jedoch ein erhöhtes Blutungsrisiko (17).
Unklar sind die Effekte anderer sekundärprophylaktisch eingesetzter Medikamente wie ACE-Hemmer, dualer Antiplättchenhemmung oder Betablocker auf die Prognose nach PMI. In der ersten randomisiert-kontrollierten Studie in Patienten mit PMI zeigte der Einsatz von Dabigatran 110 mg einen leicht positiven Effekt auf kardiovaskuläre Komplikationen nach PMI(18). Aufgrund des erhöhten Blutungsrisikos in der perioperativen Periode wurde jedoch selbst in der Studie Dabigatran erst durchschnittlich sieben Tage nach Auftreten der PMI begonnen, entsprechend erscheint eine interdisziplinäre Besprechung bzgl. des Risiko-Nutzen-Profils zentral.
Koronarinterventionen
Aufgrund der vermuteten Pathophysiologie mit grossteils Typ II Infarkten sowie dem verschlechterten Risiko-Nutzen-Verhältnis einer dualen Antiplättchentherapie postoperativ sollte eine Koronarangiographie nur bei klinischem Verdacht auf Typ I Infarkt durchgeführt werden. Hinweisend können ST-Hebungen, stark erhöhte Troponinwerte oder Thoraxschmerzen ohne Besserung angesehen werden.
Screening und Management von PMI: Erfahrungen aus einem Tertiärspital
In unserer Institution wird seit 2014 Erfahrung mit einem systematischen Screening für Risikopatienten mit nichtkardialen Operationen gesammelt. Gescreent werden Patienten mit erhöhtem kardiovaskulärem Risiko (≥ 65 Jahre ODER ≥ 45 Jahren mit vorbekannter koronarer/peripherer/zerebrovaskulärer Gefässerkrankung) die postoperativ zumindest 24 Stunden im Spital bleiben müssen. Das Screening besteht wie von Guidelines empfohlen aus einer präoperativen und zwei postoperativen Messungen von hs-cTnT. Die präoperative Messung wird idealerweise am Tag vor oder am Tag der Operation abgenommen, bei stabilen Patienten auch früher im Rahmen der präoperativen anästhesiologischen Planungssprechstunde. Die postoperativen Messungen werden am ersten und zweiten Tag morgens im Rahmen der Routineblutmessungen bestimmt (Abb. 1). Eine PMI wird diagnostiziert, wenn es zu einer absoluten Steigerung von prä- zu postoperativen hs-cTnT-Werten um ≥ 14 ng/L (abgeleitet von der 99. Perzentile dieses spezifischen hs-cTnT-Assays) kommt. Im Fall einer PMI kommt es zur elektronischen Auslösung eines Kardiologiekonsils durch ein vom Labor-IT-System generiertes Email. In Vorbereitung auf das Konsil wird ein EKG auf der chirurgischen Bettenstation geschrieben.
Mit der klinischen Untersuchung und EKG wird eine erste Triage durchgeführt zur Identifikation von ST-Hebungsinfarkten, Tachyarrhythmie oder akuter Herzinsuffizienz. Diese werden lt. entsprechender Guidelines im nichtoperativen Setting behandelt. Weiter wird das Vorliegen einer (beginnenden) Sepsis als extrakardiales Problem sowie perioperative Blutungen als potentielle Typ II Auslöser geprüft. Bei stabilen asymptomatischen Patienten ohne vorhergenannte definierte Faktoren beginnen wir eine Therapie mit Statin und führen eine, meist ambulante, Abklärung über das Vorliegen einer oder das Ausmass der KHK durch und passen nachfolgend die medikamentöse Therapie an.
Cardiovascular Research Institute Basel, Department für Kardiologie,
Department für Innere Medizin
Department für Anästhesiologie
Universitätsspital Basel
Universität Basel
Spitalstrasse 2
4056 Basel
christian.puelacher@usb.ch
Cardiovascular Research Institute Basel, Department für Kardiologie
Department für Kardiologie, INCOR Universitätsspital Sao Paulo
Sao Paulo, Brasilien
Universitätsspital Basel
Cardiovascular Research Institute Basel, Department für Kardiologie
Spitalstrasse 2
4056 Basel
Dr. Puelacher hat Unterstützung von der Schweizerischen Herzstiftung, Roche Diagnostics und der Universität Basel erhalten. Dr. Gualandro hat Unterstützung von dem FAPESP (Sao Paulo Nationalfond) erhalten. Prof. Müller hat Unterstützung vom Schweizerischen Nationalfond, der Schweizerischen Herzstiftung, der Europäischen Union, Roche Diagnostics und Abbott für Arbeit im perioperativen Bereich sowie von diversen Diagnostikfirmen für Arbeiten in anderen Gebieten erhalten.
- Perioperative Myokardischämien sind häufiger als angenommen und präsentieren sich meist asymptomatisch im klinischen Setting
- Perioperative Myokardischämien können durch verschiedene Pathologien bedingt sein wie zB koronare Plaquerupturen, akute Herzinusffizienz oder Vorhofflimmern, am häufigsten jedoch durch eine Dys-
balance von koronarer Blutversorgung und myokardialem Sauerstoffverbrauch - Systematisches Screening von Hochrisikopatienten mittels kardialem Troponin ermöglicht das Erkennen von gefährdeten Patienten und die Einleitung von potentiell prognoseverbessernden Interventionen
Messages à retenir
- Les ischémies myocardiques périopératoires sont plus fréquentes que prévu et sont généralement asymptomatiques en milieu clinique.
- L’ischémie myocardique périopératoire peut être causée par diverses pathologies telles que les ruptures de plaques coronaires, l’insuffisance cardiaque aiguë ou la fibrillation auriculaire, mais le plus souvent par un déséquilibre de l’apport sanguin coronarien et de la consommation myocardique en oxygène.
- Le dépistage systématique de la troponine cardiaque chez les patients à risque élevé permet d’identifier les patients à risque et d’amorcer des interventions susceptibles d’améliorer le pronostic.
1. Pearse RM, Moreno RP, Bauer P, et al. Mortality after surgery in Europe: a 7 day cohort study. Lancet 2012;380:1059–65.
2. Devereaux PJ, Biccard BM, Sigamani A, et al. Association of Postoperative High-Sensitivity Troponin Levels With Myocardial Injury and 30-Day Mortality Among Patients Undergoing Noncardiac Surgery. Jama 2017;317:1642.
3. Puelacher C, Lurati Buse G, Seeberger D, et al. Perioperative Myocardial Injury After Noncardiac Surgery: Incidence, Mortality, and Characterization. Circulation 2018;137:1221–1232.
4. Smilowitz NR, Beckman JA, Sherman SE, Berge JS. Hospital Readmission Following Perioperative Acute Myocardial Infarction Associated with Non-Cardiac Surgery. Circulation 2018;ePub.
5. Pedersen TF, Budtz-Lilly J, Petersen CN, et al. Randomized clinical trial of remote ischaemic preconditioning versus no preconditioning in the prevention of perioperative myocardial infarction during open surgery for ruptured abdominal aortic aneurysm. BJS open 2018;2:112–118.
6. van Waes J a R, Nathoe HM, de Graaff JC, et al. Myocardial injury after noncardiac surgery and its association with short-term mortality. Circulation 2013;127:2264–71.
7. Gualandro DM, Campos CA, Calderaro D, et al. Coronary plaque rupture in patients with myocardial infarction after noncardiac surgery: frequent and dangerous. Atherosclerosis 2012;222:191–5.
8. Thygesen K, Alpert JS, Jaffe AS, et al. Fourth universal definition of myocardial infarction (2018). Eur. Heart J. 2018.
9. Botto F, Alonso-Coello P, Chan MT V, et al. Myocardial Injury after Noncardiac Surgery: A Large, International, Prospective Cohort Study Establishing Dia-gnostic Criteria, Characteristics, Predictors, and 30-day Outcomes. Anesthesio-
logy 2014;120:564–78.
10. Duceppe E, Parlow J, MacDonald P, et al. Canadian Cardiovascular Society Guidelines on Perioperative Cardiac Risk Assessment and Management for Patients Who Undergo Noncardiac Surgery. Can. J. Cardiol. 2017;33:17–32.
11. Gualandro DM, Yu PC, Caramelli B, et al. III Guidelines for Perioperative Cardiovascular Evaluation of the Brazilian Society of Cardiology. 2017.
12. Kristensen SD, Knuuti J, Saraste A, et al. 2014 ESC/ESA Guidelines on non-cardiac surgery: cardiovascular assessment and management: The Joint Task Force on non-cardiac surgery: cardiovascular assessment and management of the European Society of Cardiology (ESC) and the European Society of Anaesth. Eur. Heart J. 2014;35:2383–2431.
13. Landesberg G, Beattie WS, Mosseri M, Jaffe AS, Alpert JS. Perioperative myocardial infarction. Circulation 2009;119:2936–44.
14. Foucrier A, Rodseth R, Aissaoui M, et al. The long-term impact of early cardiovascular therapy intensification for postoperative troponin elevation after major vascular surgery. Anesth. Analg. 2014;119:1053–63.
15. Sandoval Y, Zakharova M, Rector TS, et al. Frequency of Increase in Cardiac Troponin Levels After Peripheral Arterial Operations (Carotid Endarterectomy, Abdominal Aorta Procedure, Distal Bypass) and Their Effect on Medical Management. Am. J. Cardiol. 2016;118:1929–1934.
16. Devereaux PJ, Xavier D, Pogue J, et al. Characteristics and short-term prognosis of perioperative myocardial infarction in patients undergoing noncardiac surgery: a cohort study. Ann. Intern. Med. 2011;154:523–8.
17. Devereaux PJ, Sessler DI, Leslie K, et al. Aspirin in patients undergoing noncardiac surgery. N. Engl. J. Med. 2014;370:1494–503.
18. Devereaux PJ, Duceppe E, Guyatt G, et al. Dabigatran in patients with myocardial injury after non-cardiac surgery (MANAGE): an international, randomised, placebo-controlled trial. Lancet 2018;391:2325–2334.
info@herz+gefäss
- Vol. 9
- Ausgabe 2
- März 2019








