- Myokarditis heutzutage – Covid-19 geht uns zu Herzen
Das neue SARS-CoV-2 verursacht zusätzlich zur viralen Pneumonie und zum ARDS eine systemische Inflammation mit Multiorganbeteiligung. Eine seltene Manifestation ist die akute Myokarditis, die vom Myokardschaden mit Troponinerhöhung multifaktorieller Ursache noch nicht klar zu differenzieren ist. Noch mehr als die akute Myokarditis bei Covid-19 beschäftigt uns die akute Myokarditis, welche nach Impfung mit einem mRNA-Vakzin gegen SARS-CoV-2 auftreten kann. Diese seltene Nebenwirkung verläuft zumeist mild, ist weniger besorgniserregend als Covid-assoziierte Komplikationen generell sind und sollte die Motivation zur Impfung nicht mindern.
Abstract: In addition to viral pneumonia and ARDS, the new SARS-CoV-2 causes systemic inflammation with multi-organ involvement. Acute Myocarditis is a rare manifestation and it cannot yet be clearly differentiated from myocardial damage with troponin elevation of multifactorial origin. More so than acute myocarditis with Covid-19, we are concerned with acute myocarditis, which can occur after vaccination with mRNA vaccine against SARS-CoV-2. This rare side effect usually has a mild course, and is of less concern than other Covid-associated complications generally are, so it should not reduce motivation to vaccinate. Key Words: Myocarditis, SARS-CoV-2, ARDS, mRNA vaccine
Keywords: Myokarditis, SARS-CoV-2, ARDS, mRNA-Vakzin
Das neue SARS-CoV-2 (severe acute respiratory distress syndrome coronavius-2) verursacht eine virale Pneumonie und bei schweren Verläufen ein ARDS (acute respiratory distress syndrome). Bald nach Ausrufen der Pandemie durch die WHO (world health organization) im März 2020 wurde klar, dass auch eine Beteiligung des kardiovaskulären Systems auftreten kann. Primär zeigt sich ein Myokardschaden mit Troponinerhöhung, wobei die pathophysiologischen Zusammenhänge bisher nur teilweise verstanden sind. Die möglichen Mechanismen und daraus resultierende Folgen, wie Covid-19 das Herz schädigt, können überlappen und sind zum Beispiel: erhöhte Thrombogenität, endotheliale Dysfunktion, Endothelialitis, mikrovaskuläre Thrombenbildung, ein epikardialer Gefässverschluss (akutes Koronarsyndrom), Lungenembolie, Hypoxie bei ARDS, Sepsis mit Hypotonie, direkte Myokardschädigung durch das Virus via ACE-2 Rezeptor, schwere systemische Inflammation mit Zytokinsturm (1). Ein direkter Myokardschaden durch Virusinvasion und -replikation sowie die Hyperinflammation mit indirekter Myokardschädigung beschreiben 2 ursächliche Vorgänge einer akuten Myokarditis. Die Differenzierung der genannten Ursachen ist nicht trivial und gelingt mitunter nicht, zumal häufig von einem multifaktoriellen Geschehen auszugehen ist.
Akute Myokarditis
Zu der Schwierigkeit der Differentialdiagnostik bei einer Troponinerhöhung im Rahmen von Covid-19 kommt hinzu, dass die Diagnosestellung einer akuten Myokarditis bereits vor Covid-19 eine Herausforderung war. Dies nicht zuletzt, weil der Phänotyp der Erkrankung von asymptomatischen Fällen über eine ACS ähnliche Präsentation mit Thoraxschmerzen, eine chronische oder akute Herzinsuffizienz bis hin zum fulminanten Verlauf mit kardiogenem Schock, Arrhyhtmien und plötzlichem Herztod reichen kann. Die Ursachen sind vielfältig. Im Vordergrund steht das Virus als Auslöser für eine akute Myokarditis mit vornehmlich mildem, selbstlimitierendem Verlauf und guter Prognose. Daneben kann es aber auch zu einem chronischen Verlauf mit Inflammation mit oder ohne Viruspersistenz und Entwicklung einer dilatativen Kardiomyopathie (DCM) in bis zu 30% der Fälle, je nach Quelle, kommen (2). Auch andere Trigger oder Medikamente können direkt durch Toxizität oder indirekt durch Autoinflammation eine Myokarditis verursachen. Spezielle Fälle sind die Riesenzellmyokarditis oder die eosinophile Myokarditis, die einer spezifischen Behandlung mittels Immunsuppression bedürfen.
In Anlehnung an die Vorgaben der Working Group on Myocardial and Pericardial Diseases of the European Society of Cardiology (ESC) (3) unterscheidet man zwischen klinisch vermuteter Myokarditis und definitiver Myokarditis. Der klinische Verdacht basiert auf den Symptomen des Patienten, erhöhten Herzenzymen und der Bildgebung. Die Echokardiographie ist immer noch ein zentrales diagnostisches Mittel, wenn auch weiterführende kardiale Bildgebung mehr an Bedeutung gewinnen. Das kardiale MRI ist der Echokardiographie unter anderem darin überlegen, auch bei fehlender Reduktion der linksventrikulären Ejektionsfraktion (LVEF) den Nachweis einer akuten oder abgelaufenen Myokarditis zu erbringen. Erst kürzlich wurden die MR-Kriterien revidiert. Diese neuen Lake Louise Kriterien beinhalten die Koexistenz von T1- und T2- bezogenen Kriterien, zusätzlich zum extrazellulären Volumen (EZV) und dem late gadolinum enhancement (LGE) für myokardiale Inflammation, Nekrose und Fibrose (4). Fundamental ist daneben der Ausschluss einer koronaren Obstruktion, was bei Patienten mit höchstens mittlerem kardiovaskulärem Risiko mittels Koronar-CT geschehen kann. Trotz aller untersuchungstechnischen Fortschritte wird für die definitive Diagnose die Endomyokardbiopsie (EMB) mit Erfüllung der sogenannten Dallas Kriterien gefordert und gilt weiterhin als Goldstandard (3). In der Realität des Klinikalltages wird die EMB insbesondere bei schwerwiegenden Fällen durchgeführt, wenn sich daraus eine therapeutische Konsequenz ergibt, wie es auch von der amerikanischen Gesellschaft für Kardiologie (ACC) empfohlen wird.
Akute Myokarditis nach mRNA Impfung gegen SARS-CoV-2
Das Auftreten von Myokarditiden nach Impfungen ist ein bekanntes Phänomen und wurde in der Vergangenheit insbesondere nach der Verabreichung von Vakzinen gegen Pocken oder Influenza beobachtet.
Mehr als die akute Myokarditis im Rahmen einer SARS-CoV-2 Infektion erhält momentan die Myokarditis als Nebenwirkung der mRNA Impfung gegen das Virus die allgemeine Aufmerksamkeit. Einer der ersten Berichte über eine vermutete impfassoziierte Myokarditis nach mRNA Impfung wurde im April 2021 publiziert. Zwei Studien aus Israel bestätigten den Zusammenhang früh (5, 6). Die zeitliche Latenz zwischen der Verabreichung des Vakzins und ersten Symptomen beträgt im Mittel 3 Tage, es sind zumeist junge Männer im Alter von weniger als 30 Jahren betroffen, mehrheitlich nach Verabreichung der zweiten Impfdosis. Die Ursache ist weitgehend unklar.
Die Verabreichung von mRNA Impfstoffen führt zur Produktion von SARS-CoV-2 Spikeproteinen, welche das Ziel der gebildeten neutralisierenden Antikörper sind. Dies ist die beabsichtigte Immunantwort, welche zur Immunität gegen das Virus führt. Es wird vermutet, dass es bei entsprechender genetischer Prädisposition zu einer über die eigene adäquate Immunantwort hinausgehende Autoinflammation kommen kann. Dies kann durch die Bindung der Antikörper an körpereigene Zelloberflächenantigene zur Zerstörung von Myokardzellen führen (molekulare Mimikry). Andererseits kann es durch eine ausgelöste zytokingesteuerte Hyperinflammation zur Bildung von zirkulierenden Autoantikörpern gegen das Myokard kommen (7). Eine direkte T-Zell vermittelte Impfung-getriggerte Immunantwort gegen Kardiomyozyten wie es zum Beispiel gegen alpha-Myosin beschrieben wurde, ist eine weitere Möglichkeit. Als Trigger ist am ehesten das SARS-CoV-2 Spikeprotein verantwortlich, weniger wahrscheinlich auch eine immunologische Reaktion gegen die mRNA selbst. Zur Vermeidung einer überschiessenden Immunreaktion auf RNA Moleküle sind die Nukleoside im mRNA Impfstoff modifiziert. Ein Wechsel auf ein anderes mRNA Vakzin ist somit nur bedingt sinnvoll.
Die Verläufe sind erfreulicherweise eher mild und selbstlimitierend, wobei Daten über Prognose oder Langzeitverlauf noch nicht bestehen. In jedem Fall sollte nach einer Impfung bei Auftreten von Symptomen, die mit einer Myokarditis vereinbar sind (Tab. 1) (3), ein EKG und eine Blutentnahme mit Bestimmung der Herzenzyme sowie Entzündungsparameter und bei Auffälligkeiten eine kardiologische Beurteilung erfolgen.
Covid-19 und akute Myokarditis
Die Beschreibung von Viren als Ursache einer Myokarditis reicht in die 50er Jahre zurück und seither konnten mehrere direkt oder indirekt myokardschädigende Viren beschrieben werden.
Die klare Abgrenzung einer Myokarditis von einem Myokardschaden mit Troponinerhöhung anderer Ursache im Rahmen einer SARS-CoV-2 Infektion ist nicht trivial. Unter Berücksichtigung anderer Ursachen für den Myokardschaden ist die akute Myokarditis bei Covid-19 klinisch-epidemiologischen Daten zufolge selten respektive wird selten festgestellt. Einerseits ist die Differentialdiagnostik ohnehin schwierig, andererseits kommt es häufig überhaupt nicht erst zur Durchführung der notwendigen Untersuchungen. Grund hierfür ist meist, dass der begleitende Myokardschaden für die Therapie eines generell schwerwiegenden Verlaufes im Rahmen von Covid-19 kaum eine Rolle spielt, weder für die Therapie noch für die Prognose der Erkrankung.
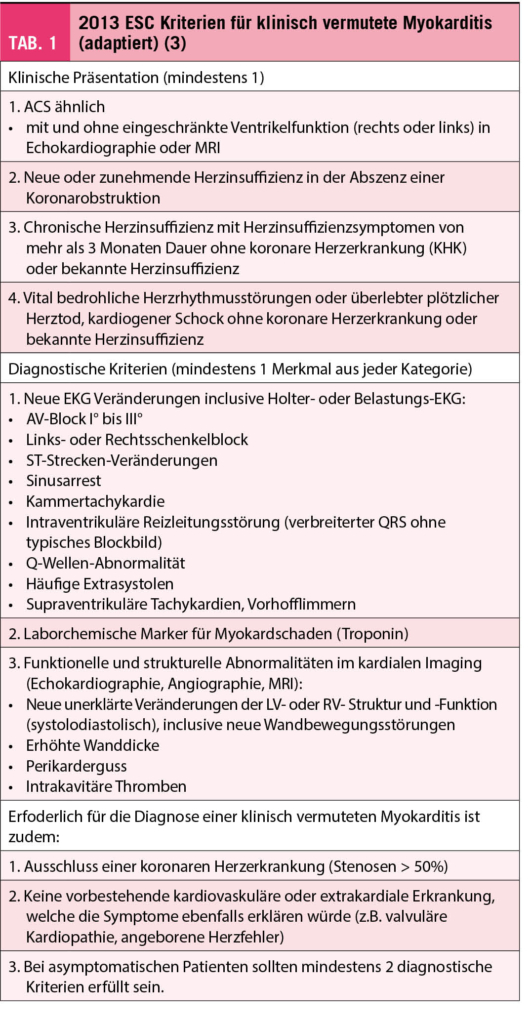
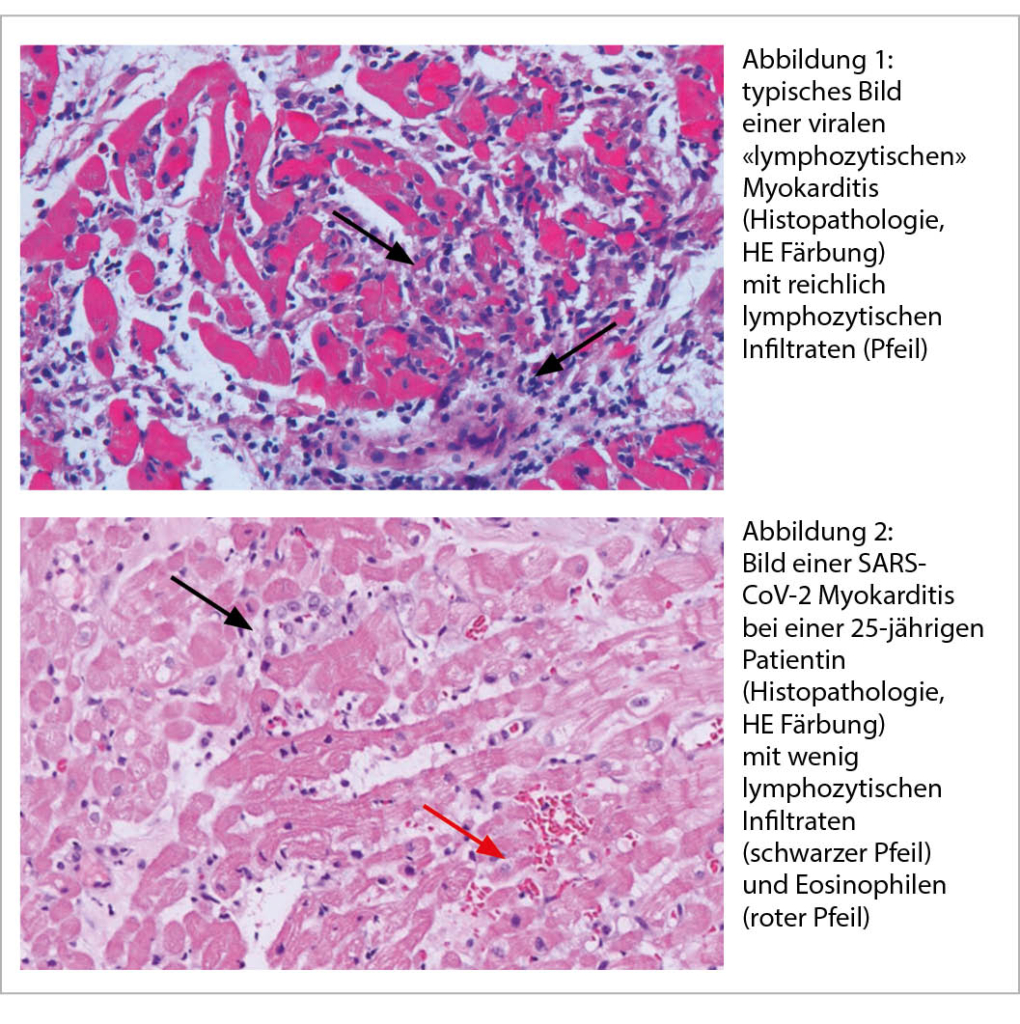
Die Kenntnisse über die akute Myokarditis bei Covid-19 sind daher wenige, beschränken sich auf Fallberichte und über die Richtigkeit von Ursache und Therapie überwiegen Vermutungen. Hinzu kommt, dass wir bei den bisher durchgeführten Untersuchungen auf Diskrepanzen stossen. Zwar ist bekannt, dass SARS-CoV-2 via ACE-2 Rezeptor in die Kardiomyozyten eintreten kann, doch wurde bisher kein definitiver Virusnachweis in einer Endomyokardbiopsie (EMB) bei vermuteter Covid-19 assoziierter Myokarditis erbracht noch in Autopsien nach Tod durch Covid-19. Daher wird postuliert, dass es sich um einen immunologisch getriggerten Prozess handelt. Allerdings konnte in entsprechenden klinischen Verdachtsfällen mittels EMB nie ein typisches lymphozytäres Infiltrat (Abb. 1) oder Myokardnekrosen gefunden werden (7, 8). So auch nicht in dem Fall aus unserer Klinik, einer 25jährige Patientin mit kardiogenem Schock bei fulminanter Myokarditis bei SARS-CoV-2 Infektion, in deren histopathologischen Präparaten aus 7 Myokardstücken nur vereinzelt Lymphozyten, wenige Eosinophile und ebensowenig Nekrosen nachweisbar waren (Abb. 2). Somit erscheint die akute Myokarditis bei Covid-19 nicht einer Myokarditis wie bisher bekannt zu entsprechen, sondern vielmehr einem myokarditisähnlichem Bild mit noch unklarem Pathomechanismus. Aus diesem Grund bleibt die Prognose, insbesondere im Langzeitverlauf, noch unklar und die Therapieansätze sind rein empirisch. Glucokortikoide gelten vorläufig als Mittel der Wahl. Daneben sind bisher NSAR, Immunglobuline und die antivirale Therapie zusätzlich zur klassischen Herzinsuffizienztherapie bis hin zur mechanischen Kreislaufunterstützung und antiarrhythmischen Behandlung zum Einsatz gekommen.
Wie weiter mit der Impfung
Die primäre Sorge vor einer impfassoziierten Myokarditis ist bei Patienten und Ärzten aufgrund der vorliegenden Fallberichte gross. Es muss hier wiederholt und betont werden, dass es sich um eine insgesamt seltene unerwünschte Nebenwirkung handelt und das Risiko für schwere Verläufe einer Myokarditis nach Impfung viel geringer einzuschätzen ist als schwere Verläufe einer Covid-19 vermittelten kardialen Beteiligung zu erwarten sind. Der Nutzen der Impfung überwiegt also bei weitem gegenüber dem leichtgradigen Risiko einer mehrheitlich mild verlaufenden Myokarditis.
Es stellt sich die Frage nach dem weiteren Vorgehen bezüglich der mRNA Impfung nach einer durchgemachten Myokarditis nach Impfung mit einem SARS-CoV-2 mRNA Impfstoff.
Grundsätzlich gibt es nur wenige Ausnahmen für Einschränkungen bezüglich der Verabreichung von mRNA Impfstoff. Eine ehemals durchgemachte Myokarditis gehört nicht dazu, im Gegenteil sollte der betroffene Patient vor einer SARS-CoV-2 in Zukunft geschützt sein. Eine Ausnahme betrifft aktuell die Boosterimpfung nach akuter Myokarditis nach mRNA Impfung, die zumeist nach der zweiten Dosis auftritt. Hier wird vom Bundesamt für Gesundheit ein expektatives Vorgehen in Erwartung neuer Empfehlungen im folgenden Jahr empfohlen (9).
Konklusion
Die Diagnose der akuten Myokarditis stellt grundsätzlich eine Herausforderung dar. Im Rahmen von Covid-19 ist die Troponinerhöhung zu differenzieren von einem Myokardschaden anderer Ursache und zumeist multifaktoriell bedingt. Die akute Myokarditis bei SARS-CoV-2 Infektion wie nach mRNA Impfung ist immunologisch verursacht. Beide Formen der Myokarditis sind selten und betreffen vor allem junge Männer. Der Nutzen des Schutzes vor einer Coronainfektion mit allen Komplikationen inklusive eines schwerwiegenden Verlaufes einer möglichen Myokarditis und Long-Covid Verläufen überwiegt das Risiko einer seltenen impfassoziierten Myokarditis mit zumeist mildem Verlauf bei Weitem.
Bei diesem Artikel handelt es sich um einen Zweitabdruck des in «der informierte arzt» 01-2022 erschienenen Originalartikels.
Copyright bei Aerzteverlag medinfo AG
Inselspital, Universitätsspital Bern
Universitätsklinik für Kardiologie
Herz Gefäss Zentrum
Freiburgstrasse 20
3010 Bern
Die Autorin hat keinen Interessenskonflikt in Zusammenhang mit diesem Artikel.
◆ Myokarditis nach Covid-19 und mRNA Impfung gegen SARS-CoV-2 ist selten, Verläufe zumeist mild und die Impfung wird allen empfohlen.
◆ Zumeist betroffen von einer akuten Myokarditis sind junge Männer, nach Impfung mit einer Latenz von 3 Tagen und höchster Rate nach der zweiten Impfdosis. Dann empfiehlt das Bundesamt für Gesundheit vorerst ein Zuwarten mit der Boosterimpfung.
◆ Die Ursache ist am ehesten eine autoinflammatorische Immunantwort als Reaktion auf die SARS-CoV-2 Spikeproteine.
◆ Bei Thoraxschmerzen, EKG-Veränderungen, Troponinerhöhung
auch an Myokarditis denken und für weiterführende Untersuchungen kardiologisch zuweisen.
1. Fajgenbaum DC, June CH. Cytokine Storm. NEJM 2020; 383: 225-73.
2. Caforio et al. A prospective study of biopsy-proven myocarditis: prognostic relevance of clinical and aetiopathogenetic features at diagnosis. Eur Heart J 2007;28:1326–1333.
3. Caforio et al. Current state of knowledge on aetiology, diagnosis, management, and therapy of myocarditis: a position statement of the European Society of Cardiology Working Group on Myocardial and Pericardial Diseases. Eur Heart J 2013; 34:2636-48.
4. Ferreira et al. Cardiovascular Magnetic Resonance in Nonischemic Myocardial Inflammation. JACC 2018; 3158-76.
5. Witberg et al. Myocarditis after Covid-19 Vaccination in a Large Health Care Organization. NEJM 2021; 385: 2139-9.
6. Barda et al. Safety of the BNT162b2 mRNA Covid-19 Vaccine in a Nationwide Setting. NEJM 2021; 385: 1078-90.
7. Bozkurt et al. Myocarditis with Covid-19 mRNA Vaccines. Circulation 2021; 44: 471-484.
8. Caforio et al. Clinically Suspected and Biopsy-Proven Myocarditis Temporally Associated with SARS-CoV-2 Infection. Annu Rev Med 2022. 73: 10.1-10.18.
9. Bundesamt für Gesundheit und Eidgenössische Komission für Impffragen EKIF. Impfempfehlung für mRNA-Impfstoffe gegen Covid-19 (Stand 21.12.2021).
info@herz+gefäss
- Vol. 12
- Ausgabe 1
- Februar 2022