- Neue Trends der Antikoagulation bei Vorhofflimmern
Der Beitrag beschreibt die Etablierung der direkten oralen Antikoagulantien (DOACs) als Standard zur Schlaganfallsprävention in medizinischen Richtlinien. Er betont ihre Wirksamkeit und verbesserte Sicherheit im Vergleich zu Vitamin K Antagonisten. Er erwähnt auch die Empfehlungen für den klinischen Einsatz von DOACs in verschiedenen Situationen und gibt einen Ausblick auf zukünftige Entwicklungen in diesem Bereich.
The article describes the establishment of direct oral anticoagulants (DOACs) as the standard for stroke prevention in medical guidelines. It emphasises their efficacy and improved safety compared to vitamin K antagonists. It also mentions the recommendations for the clinical use of DOACs in different situations and gives an outlook on future developments in this field.
Key Words: Anticoagulants, DOACs, stroke prevention, subclinical atrial fibrillation, dialysis
Seit Präsentation und Publikation der ersten Studie mit einem der dazumal neuen oralen Antikoagulantien (NOAC) – inzwischen treffender als ‘direkte orale Antikoagulantien’ (DOAC) bezeichnet – sind diese als Standard zur Schlaganfallsprävention in allen grösseren Richtlinien etabliert (1), basierend auf der mindestens gleich effektiven (wenn nicht besseren) Wirksamkeit sowie der deutlich verbesserten Sicherheit, insbesondere hinsichtlich der schwersten Blutungen verglichen mit Vitamin K Antagonisten (2–5). Zahlreiche Richtlinien und Positionspapiere wie der «European Heart Rhythm Association (EHRA) Practical Guide» geben darüber hinaus Tipps und Empfehlungen zum optimalen Einsatz dieser Substanzen im klinischen Alltag, inkl. Patienten mit Niereninsuffizienz, akuten Koronarsyndrom / Stenting, Kardioversion oder nach einem Schlaganfall (6, 7). In manchen Situationen ist hingegen einiges im Fluss; die vorliegende Übersichtsarbeit soll eine Übersicht über die klinisch relevantesten und im Alltag nicht selten vorkommenden Situationen geben, sowie über die weiteren in nächster Zeit zu erwartenden Entwicklungen.
Subklinisches Vorhofflimmern / Device-detektiertes Vorhofflimmern
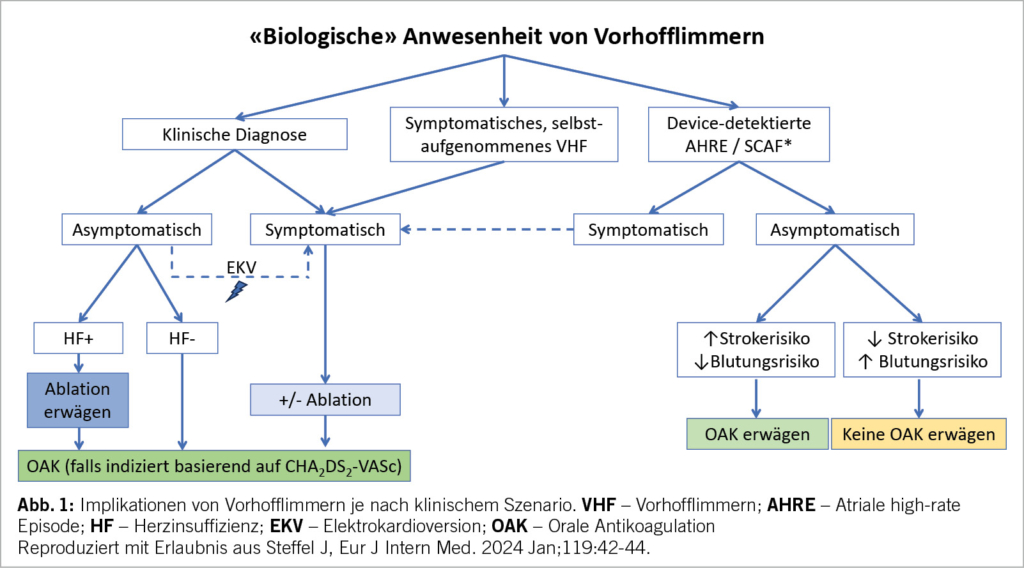
Noch vor wenigen Jahren war die Diagnose des Vorhofflimmerns verhältnismässig einfach: Ein unregelmässig unregelmässiger Herzschlag, keine erkennbaren P-Wellen zwischen den QRS, idealerweise Nachweis von Flimmerwellen. Dies hat sich in letzter Zeit deutlich geändert, nicht zuletzt aufgrund der Versorgung von mehr und mehr Patienten mit implantierbaren kardialen Devices, sowie Smartwatches etc. Und auch wenn es kontra-intuitiv erscheint: Patienten mit asymptomatischem «Device-detektiertem» Vorhofflimmern auf ihren Schrittmachern oder ICDs haben ein tieferes Risiko eines Schlaganfalls als solche mit einer klinischen Vorhofflimmern-Diagnose. Zwei kürzlich erschienene Publikationen (NOAH und ARTESiA) konnten zeigen, dass bei diesen Patienten zwar das Risiko eines Schlaganfalls durch eine OAK (Orale Antikoagulation) verringert werden kann, das Risiko von Blutungen jedoch anstieg. Praktisch bedeutet dies, dass eine gute Risikostratifizierung – beispielsweise mittels CHADS-VASc Score – zu erfolgen hat: Nur bei Patienten mit hohem Schlaganfallsrisiko (und idealerweise niedrigem Blutungsrisiko) erscheint eine OAK bei Device-detektiertem Vorhofflimmern einen Netto-Nutzen zu bringen; ansonsten scheint das Risiko der Blutung zu überwiegen (Abbildung 1). Ab welchem «Burden» des Vorhofflimmerns, und ab welchem Risiko für einen Schlaganfall eine OAK sicher indiziert ist, bleibt aktuell unklar und ist Gegenstand weiterer Studien.
Gleichzeitig ist es sehr wichtig, von diesen asymptomatischen Zufallsdiagnosen das symptomatische Vorhofflimmern, welches ebenfalls auf einem Device festgehalten wurde, zu unterscheiden. Die meisten dieser durch einen Kardiologen oder Elektrophysiologen als Vorhofflimmern bestätigten Episoden würden auf einem zu diesem Zeitpunkt geschriebenen EKG ebenfalls einem Vorhofflimmern entsprechen. Das heisst, dass in diesen Fällen die klinische Diagnose ausschliesslich aufgrund logistischer Limitationen (kein EKG zur Verfügung) nicht gestellt wurde. Entsprechend erscheint die Behandlung dieser Patienten im Sinne eines klinischen Vorhofflimmerns gerechtfertigt – inkl. OAK und Rhythmuskontrolle, falls indiziert.
Jedoch muss bei den zunehmend beobachteten «Diagnosen» eines Vorhofflimmerns mittels Smartwatch genau zwischen der «Screening» Funktion (häufig mittels Plethysmographie) und der Diagnose eines symptomatischen Vorhofflimmerns mittels eigenständig aufgezeichnetem EKG unterschieden werden. Während die Implikationen von ersteren aktuell unklar ist (abgesehen vielleicht von einer erhöhten Vigilanz für eine allfällige klinische Rhythmusstörung), entspricht die Situation bei letzteren Patienten – wie oben erwähnt – de facto der eines klinischen Vorhofflimmerns. Bei der Diagnose eines VHF mittels Smartwatch oder anderen Patienten-aktivierten EKGs ist jedoch zu beachten, dass aufgrund der variablen und zum Teil markanten Filterung andere Massstäbe an die EKG Diagnose anzulegen sind. Gleichwohl ist die Diagnose durch erfahrene Kardiologen / Elektrophysiologen in aller Regel gut möglich.
Schwere Niereninsuffizienz / Dialyse
Das Risiko eines Schlaganfalls ist bei schwerer Niereninsuffizienz sowie an der Dialyse deutlich erhöht. Da die gegenwärtig verfügbaren DOACs in dieser Situation bisher nicht randomisiert untersucht worden waren, werden die meisten dieser Patienten mittels VKA behandelt. Hierbei wird jedoch nicht selten vergessen, dass auch für VKA nie eine adäquat gepowerte randomisierte Studie durchgeführt wurde, die einen Nettonutzen gegenüber Placebo hätte zeigen können. Denn auch das Blutungsrisiko dieser Patienten ist aufgrund verschiedener Mechanismen deutlich erhöht (8). Die Ergebnisse zweier Ende 2022 erschienenen Studien macht die Situation nicht einfacher: Auch für Apixaban – was mangels Alternativen nicht selten «off label» in solchen Situationen eingesetzt wird – konnte in der AXADIA sowie in der RENAL-AF Studie kein Benefit gegenüber VKA gezeigt werden (9, 10). Bedauerlich ist hierbei insbesondere, dass keine der beiden Studien einen Placeboarm hatten, so dass der Nettonutzen einer OAK überhaupt auch hier nicht untersucht werden konnte. Ebenso waren beide Studien underpowered, was insbesondere bei der RENAL-AF Studie auf eine weit unter den Erwartungen zurückbleibenden Rekrutierung zurückzuführen war. Dies ist umso erstaunlicher, als dass in Situationen fehlender klinischer Daten zur Entscheidungsfindung der Einschluss in eine Studie in aller Regel eine hervorragende Gelegenheit bietet, eben solche Daten zu generieren. Leider ist diese Chance erneut ungenutzt geblieben, so dass weiterhin keine Studiendaten existieren, die eine evidenz-basierte Entscheidungsfindung in dieser hoch vulnerablen Patientenpopulation erlauben würde. Dasselbe gilt für die häufig in dieser Situation eingebrachte Option eines perkutanen Vorhofohrverschlusses. In der Tat ist nicht nur die Sicherheit (deutlich erhöhtes Blutungsrisiko), als auch vor allen Dingen die Effizienz einer solchen lokal begrenzten Therapie bei diesen vaskulär und humoral schwer kranken Patienten völlig unklar und bisher nicht randomisiert untersucht. Daher sollte diese Therapie in der Abwesenheit von adäquat gepowerten randomisierten Endpunktstudien nur in Ausnahmefällen und nach ausführlicher Aufklärung (insbesondere der fehlenden Studiendaten) erfolgen.
«Valvuläres» Vorhofflimmern
Patienten mit mechanischen Herzklappen sowie mit mindestens mittelschwerer Mitralstenose sind von den grossen randomisierten Phase III Studien der DOACs aufgrund ihres hohen thromboembolischen Risikos ausgeschlossen gewesen.
Bei Patienten mit mechanischen Herzklappen scheint nunmehr – nach 2 weiteren negativen Studien – die Situation klar zu sein, dass VKA die Therapie der Wahl darstellen und DOACs kontraindiziert bleiben dürften (11, 12).
Bei (in der Regel postrheumatischen) Mitralstenose hingegen war die Situation lange Zeit weniger klar, bis 2022 in der INVICTUS Studie eine signifikant höhere Thromboembolierate sowie eine höhere Mortalität unter Rivaroxaban verglichen mit VKA gezeigt werden konnte (13). Die Daten sind eindeutig – allerdings nur für Patienten, welche prinzipiell in diese Studie eingeschlossen werden konnten. Dies beinhaltete insbesondere die Möglichkeit einer regelmässigen INR Kontrolle, und somit «access to care» – was von entscheidender Bedeutung ist, da es für viele der von post-rheumatischem Vorhofflimmern betroffenen Patienten genau nicht der Fall ist. Ob auch solche Patienten mit ‘unüberwachtem’ und somit fast zwangsläufig schlecht eingestelltem INR Wert eher von einem VKA als von einem DOAC profitieren bleibt auch nach der INVICTUS Studie unklar. Ob weitere Studien in dieser oftmals vernachlässigten, grossen Patientenpopulation durchgeführt werden ist fraglich – nicht zuletzt, da sie zu grossen Teilen in Ländern mit niedrigem bis mittleren Einkommen zu finden sind …
Faktor XIa Hemmer – die nächsten «NOACs»?
Obgleich mithilfe der aktuell eingesetzten DOACs (direkte Thrombin- bzw. Faktor Xa-Hemmer) ein klarer Benefit gegenüber VKA erzielt werden kann, ist insbesondere das Risiko für Blutungen nicht eliminiert. Um dieser Problematik zu begegnen, werden gegenwärtig grosse Phase III Studien der neuen NOACs durchgeführt, welche mittels Inhibition von Faktor XI/XIa die Gerinnung hemmen. Diese Therapie stellt ein prinzipiell hoch attraktives Konzept dar, da FXI/FXIa primär in der pathologischen Thrombusbildung, jedoch weitaus weniger in der physiologischen Hämostase involviert zu sein scheint (14). Daten sowohl aus Tiermodellen, als auch von Patienten mit angeborenem Faktor XI Mangel stützen diese Hypothese (15, 16). Phase II klinische Studien stützen das Konzept und zeigen eine erwartete niedrige Blutungsrate. Allerdings musste das Feld Ende 2023 einen Rückschlag hinnehmen: Eine der grossen Phase III Studien (OCEANIC-AF), in welcher der FXIa-Hemmer Asundexian mit Apixaban verglichen wurde, musste aufgrund unterlegener Effizienz des FXIa-Hemmers vorzeitig terminiert werden. Die Ursachen hierfür sind aktuell noch nicht klar; es kommen grundsätzlich 3 Erklärungen in Frage: Die Substanz, die untersuchte Dosis, oder das ganze Wirkprinzip. Es bleibt abzuwarten, wie die aktuell noch laufenden Studien zu den verbliebenen FXIa-Hemmern herauskommen. Zur Erinnerung: Auch das erste DOAC, der direkte Thrombinhemmer Ximelagatran, musste nach wenigen Wochen auf dem Markt 2006 zurückgezogen werden – wegen eines erhöhten Risikos einer Hepatotoxizität (welches mit den Folgesubstanzen nicht mehr beobachtet werden konnte). Es bleibt abzuwarten, wie sich die Zukunft der FXIa-Hemmer entwickelt.
Copyright
Aerzteverlag medinfo AG
Swiss EP AG
Witellikerstrasse 40
8008 Zürich
J. Steffel hat Beratungs- und / oder Vortragshonorare erhalten von Abbott, Alexion, Astra-Zeneca, Bayer, Berlin-Chemie, Biosense Webster, Biotronik, Boehringer-Ingelheim, Boston Scientific, BMS, Daiichi Sankyo, Medscape, Medtronic, Menarini, Merck/MSD, Organon, Pfizer, Saja, Servier,und WebMD. Er ist Teilhaber der Swiss EP AG und von CorXL.
Dr. Steffel ist Mitglied des Executive Committees der OCEANIC-AF Studie (Asundexian vs. Apixaban zur Schlaganfallsprävention bei Vorhofflimmern).
1. Hindricks G, Potpara T, Dagres N, Arbelo E, Bax JJ, Blomstrom-Lundqvist C, Boriani G, Castella M, Dan GA, Dilaveris PE, Fauchier L, Filippatos G, Kalman JM, La Meir M, Lane DA, Lebeau JP, Lettino M, Lip GYH, Pinto FJ, Thomas GN, Valgimigli M, Van Gelder IC, Van Putte BP, Watkins CL, Group ESCSD. 2020 ESC guidelines for the diagnosis and management of atrial fibrillation developed in collaboration with the european association of cardio-thoracic surgery (EACTS). Eur Heart J. 2021 Feb 1;42(5):373-498. doi: 10.1093/eurheartj/ehaa612t
2. Connolly SJ, Ezekowitz MD, Yusuf S, Eikelboom J, Oldgren J, Parekh A, Pogue J, Reilly PA, Themeles E, Varrone J, Wang S, Alings M, Xavier D, Zhu J, Diaz R, Lewis BS, Darius H, Diener HC, Joyner CD, Wallentin L. Dabigatran versus warfarin in patients with atrial fibrillation. N Engl J Med. 2009;361:1139-1151
3. Patel MR, Mahaffey KW, Garg J, Pan G, Singer DE, Hacke W, Breithardt G, Halperin JL, Hankey GJ, Piccini JP, Becker RC, Nessel CC, Paolini JF, Berkowitz SD, Fox KA, Califf RM. Rivaroxaban versus warfarin in nonvalvular atrial fibrillation. N Engl J Med. 2011;365:883-891
4. Granger CB, Alexander JH, McMurray JJ, Lopes RD, Hylek EM, Hanna M, Al-Khalidi HR, Ansell J, Atar D, Avezum A, Bahit MC, Diaz R, Easton JD, Ezekowitz JA, Flaker G, Garcia D, Geraldes M, Gersh BJ, Golitsyn S, Goto S, Hermosillo AG, Hohnloser SH, Horowitz J, Mohan P, Jansky P, Lewis BS, Lopez-Sendon JL, Pais P, Parkhomenko A, Verheugt FW, Zhu J, Wallentin L. Apixaban versus warfarin in patients with atrial fibrillation. N Engl J Med. 2011;365:981-992
5. Giugliano RP, Ruff CT, Braunwald E, Murphy SA, Wiviott SD, Halperin JL, Waldo AL, Ezekowitz MD, Weitz JI, Spinar J, Ruzyllo W, Ruda M, Koretsune Y, Betcher J, Shi M, Grip LT, Patel SP, Patel I, Hanyok JJ, Mercuri M, Antman EM. Edoxaban versus warfarin in patients with atrial fibrillation. N Engl J Med. 2013;386:2093-2104
6. Steffel J, Verhamme P, Potpara TS, Albaladejo P, Antz M, Desteghe L, Haeusler KG, Oldgren J, Reinecke H, Roldan-Schilling V, Rowell N, Sinnaeve P, Collins R, Camm AJ, Heidbuchel H, Group ESCSD. The 2018 European heart rhythm association practical guide on the use of non-vitamin k antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J. 2018;39:1330-1393
7. Steffel J, Collins R, Antz M, Cornu P, Desteghe L, Haeusler KG, Oldgren J, Reinecke H, Roldan-Schilling V, Rowell N, Sinnaeve P, Vanassche T, Potpara T, Camm AJ, Heidbuchel H. 2021 European heart rhythm association practical guide on the use of non-vitamin k antagonist oral anticoagulants in patients with atrial fibrillation. Europace 2021 Oct 9;23(10):1612-1676. doi: 10.1093/europace/euab065.
8. Steffel J, Hindricks G. Apixaban in renal insufficiency: Successful navigation between the scylla and charybdis. Eur Heart J. 2012;33:2766-2768
9. Reinecke H, Jurgensmeyer S, Engelbertz C, Gerss J, Kirchhof P, Breithardt G, Bauersachs R, Wanner C. Design and rationale of a randomised controlled trial comparing apixaban to phenprocoumon in patients with atrial fibrillation on chronic haemodialysis: The axadia-afnet 8 study. BMJ open. 2018;8:e022690
10. Pokorney SD, Chertow GM, Al-Khalidi HR, Gallup D, Dignacco P, Mussina K, Bansal N, Gadegbeku CA, Garcia DA, Garonzik S, Lopes RD, Mahaffey KW, Matsuda K, Middleton JP, Rymer JA, Sands GH, Thadhani R, Thomas KL, Washam JB, Winkelmayer WC, Granger CB, Investigators R-A. Apixaban for patients with atrial fibrillation on hemodialysis: A multicenter randomized controlled trial. Circulation. 2022;146:1735-1745
11. Eikelboom JW, Connolly SJ, Brueckmann M, Granger CB, Kappetein AP, Mack MJ, Blatchford J, Devenny K, Friedman J, Guiver K, Harper R, Khder Y, Lobmeyer MT, Maas H, Voigt JU, Simoons ML, Van de Werf F, Investigators R-A. Dabigatran versus warfarin in patients with mechanical heart valves. N Engl J Med. 2013;369:1206-1214
12. Jawitz OK, Wang TY, Lopes RD, Chavez A, Boyer B, Kim H, Anstrom KJ, Becker RC, Blackstone E, Ruel M, Thourani VH, Puskas JD, Gerdisch MW, Johnston D, Capps S, Alexander JH, Svensson LG. Rationale and design of proact xa: A randomized, multicenter, open-label, clinical trial to evaluate the efficacy and safety of apixaban versus warfarin in patients with a mechanical on-x aortic heart valve. Am Heart J. 2020;227:91-99
13. Connolly SJ, Karthikeyan G, Ntsekhe M, Haileamlak A, El Sayed A, El Ghamrawy A, Damasceno A, Avezum A, Dans AML, Gitura B, Hu D, Kamanzi ER, Maklady F, Fana G, Gonzalez-Hermosillo JA, Musuku J, Kazmi K, Zuhlke L, Gondwe L, Ma C, Paniagua M, Ogah OS, Molefe-Baikai OJ, Lwabi P, Chillo P, Sharma SK, Cabral TTJ, Tarhuni WM, Benz A, van Eikels M, Krol A, Pattath D, Balasubramanian K, Rangarajan S, Ramasundarahettige C, Mayosi B, Yusuf S, Investigators I. Rivaroxaban in rheumatic heart disease-associated atrial fibrillation. N Engl J Med. 2022;387:978-988
14. Harrington J, Piccini JP, Alexander JH, Granger CB, Patel MR. Clinical evaluation of factor xia inhibitor drugs: Jacc review topic of the week. J Am Coll Cardiol. 2023;81:771-779
15. Preis M, Hirsch J, Kotler A, Zoabi A, Stein N, Rennert G, Saliba W. Factor xi deficiency is associated with lower risk for cardiovascular and venous thromboembolism events. Blood. 2017;129:1210-1215
16. Tucker EI, Marzec UM, White TC, Hurst S, Rugonyi S, McCarty OJ, Gailani D, Gruber A, Hanson SR. Prevention of vascular graft occlusion and thrombus-associated thrombin generation by inhibition of factor xi. Blood. 2009;113:936-944
info@herz+gefäss
- Vol. 14
- Ausgabe 4
- Juli 2024