- Richtiger Umgang mit medikamentöser Dauertherapie
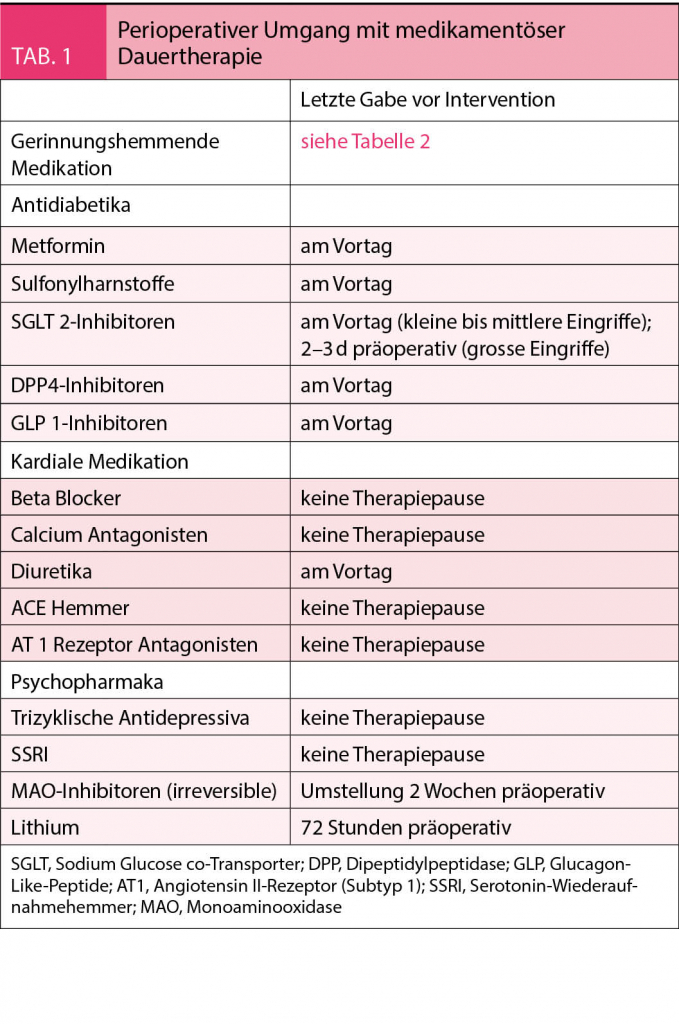
Der richtige Umgang mit medikamentöser Dauertherapie stellt im perioperativen Umfeld eine Herausforderung für die behandelnden Ärzte dar. Ein Grossteil der Dauertherapie kann ohne Unterbrechung fortgeführt werden, wobei vor allem gerinnungshemmende Medikamente häufig von dieser Regel ausgenommen sind. In dieser Arbeit befassen sich die Autoren mit Gerinnungshemmern, Antidiabetika, Antihypertonika und Psychopharmaka und deren Einsatz im perioperativen Umfeld. Eine Übersicht findet sich in Tabelle 1.
Dans un environnement périopératoire, la manipulation correcte de la pharmacothérapie à long terme pose un défi pour les médecins traitants. La plupart des traitements à long terme peuvent être poursuivis sans interruption, bien que les anticoagulants en particulier soient souvent exclus de cette règle. Dans cet article, les auteurs traitent des anticoagulants, des antidiabétiques, des antihypertenseurs et des médicaments psychotropes et de leur utilisation en milieu périopératoire. Une vue d’ensemble peut être trouvée dans le tableau 1.
Die Antikoagulanzien / Thrombozytenaggregationshemmer
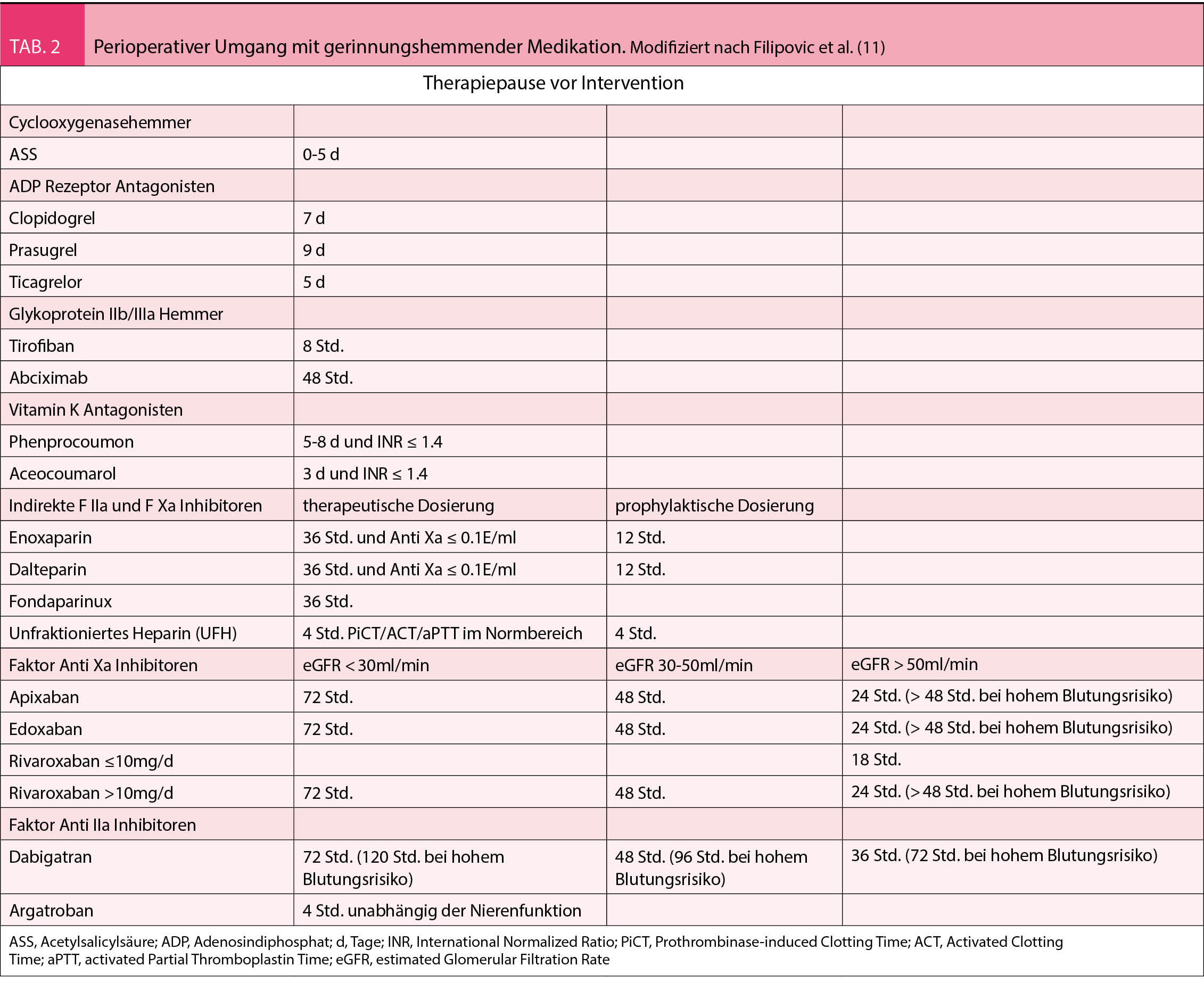
Das perioperative Management von gerinnungshemmenden Substanzen bedarf einer individuellen Risikoabschätzung, welche das chirurgische Blutungsrisiko gegen das thromboembolische Risiko abwägt. Ausmass und Gefährlichkeit möglicher Blutungen bestimmen das Blutungsrisiko. Während dieses bei kleineren Eingriffen an der Körperoberfläche oder an gut komprimierbaren Stellen als gering eingestuft wird, zählen spinale und intrakranielle Operationen zur Hochrisikogruppe. Die überwiegende Anzahl der Eingriffe jedoch weist ein mittleres Blutungsrisiko auf. Das thromboembolische Risiko wird durch die Art und Schwere der kardiovaskulären Grunderkrankung determiniert. Eine Übersicht der Therapiepausen bei gerinnungshemmender Medikation findet sich in Tabelle 2.
Thrombozytenaggregationshemmer
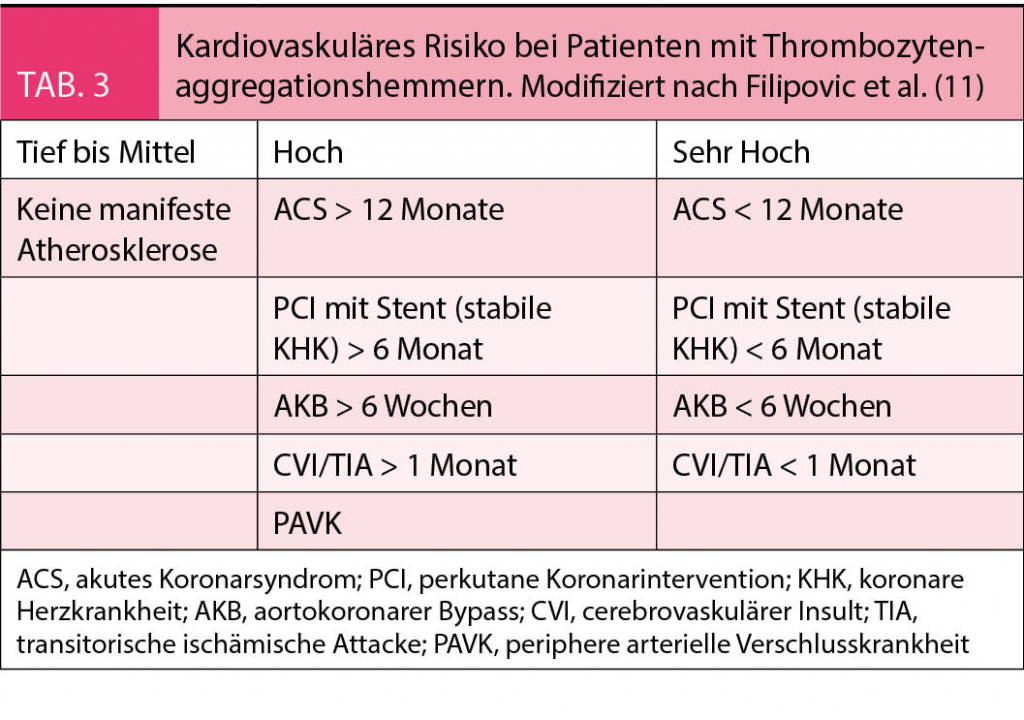
Weit verbreitet sind COX1/2- (Aspirin) sowie P2Y12-Rezeptor-Inhibitoren (Clopidogrel, Prasugrel, Ticagrelor). Das thromboembolische Risiko bei einer allfälligen Therapiepause wird durch die Indikation zur Thrombozytenaggregationshemmung bestimmt (1). Innerhalb des ersten Jahres nach einem akuten Koronarsyndrom (unabhängig der Therapiemodalität) sowie innerhalb der ersten Monate nach einer Koronarintervention (im Rahmen einer chronischen KHK) ist dieses besonders hoch. Nach Ablauf dieser Zeitintervalle sinkt das Risiko auf ein mittleres Niveau. Entsprechend empfehlen die aktuellen Leitlinien der Canadian Cardiovascular Society (CCS), American Heart Association / American College of Cardiology (AHA/ACC) und European Society of Cardiology (ESC) nach einem akuten Koronarsyndrom (ACS) eine doppelte Thrombozytenaggregationshemmung (DAPT) für mindestens zwölf Monate. Nach elektiver Koronarintervention beträgt diese drei bis sechs Monate (2-4).
Von einem niedrigen thromboembolischen Risiko spricht man hingegen beim primärprophylaktischen Einsatz von Thrombozytenaggregationshemmern. Detaillierte Angaben finden sich in Tabelle 3.
Wird die antithrombozytäre Therapie perioperativ weitergeführt, kann dies zu vermehrten Blutungskomplikationen führen (5). Besteht also ein niedriges thromboembolisches Risiko und/oder ein hohes Blutungsrisiko, so soll Aspirin fünf Tage präoperativ abgesetzt werden (1, 6). In allen anderen Situationen soll Aspirin weitergegeben werden (1). In kardialen Hochrisikosituationen sollen elektive Eingriffe verschoben werden. Bei dringlichen, nicht aufschiebbaren Operationen hingegen ist eine interdisziplinäre Absprache notwendig, die Art und Zeitpunkt des Eingriffs, das koronare Risiko sowie die Blutungssituation sind zu berücksichtigen. Je nach der Konstellation wird dann die Therapie unterbrochen oder in Ausnahmefällen ein intravenöses Bridging der DAPT durchgeführt (6). Um ein vollständiges Abklingen der gerinnungshemmenden Wirkung von P2Y12-Rezeptor-Inhibitoren zu erreichen, müssen diese einige Tage vor dem geplanten Eingriff abgesetzt werden. Die in Tabelle 2 aufgeführten Zeitintervalle entsprechen den meisten anästhesiologischen Richtlinien. In den neuesten Richtlinien der European Society of Cardiology (ESC) werden um ein bis zwei Tage kürzere Zeiten angegeben (7). Die dem zugrundeliegenden Daten stammen allerdings von herzchirurgischen Patienten und sind ausserhalb dieser Population nicht validiert. In Einzelfällen kann die Erholung der Thrombozytenfunktion mittels Thrombozytenfunktionstests dokumentiert werden. Generell muss betont werden, dass auch eine fortgesetzte DAPT perioperative kardiale Ereignisse nicht zu verhindern vermag (8).
Vitamin-K-Antagonisten (VKA)
Der Einsatz von VKA erfolgt heutzutage vorwiegend zur Thromboembolieprophylaxe bei Vorhofflimmern oder nach mechanischem Herzklappenersatz und zur Therapie thromboembolischer Ereignisse. Zur Abschätzung des thromboembolischen Risikos eines Vorhofflimmerns wird der CHA2DS2-VASc-Score herangezogen. Dieser wurde jedoch bisher nicht im perioperativen Setting validiert (9).
Liegt ein geringes Blutungsrisiko vor, so sollen die VKA periinterventionell unverändert fortgeführt werden. Bei einem höheren Blutungsrisiko sollte Phenprocoumon (Marcoumar®) rund eine Woche und Acenocoumarol (Sintrom®) drei Tage präoperativ pausiert werden (10). Eine überbrückende Therapie mit anderen gerinnungshemmenden Substanzen («Bridging») ist ausschliesslich bei hohem kardiovaskulären Risiko indiziert (6), da nur dann die Erhöhung des Blutungsrisikos durch eine allfällige Reduktion thromboembolischer Ereignisse wettgemacht wird (11). Ein hohes Risiko liegt in folgenden Situationen vor: CHA2DS2-VASc-Score ≥ 6, Thromboembolie vor < 3 Monaten, St.n. Aortenklappenersatz plus drei Risikofaktoren (mechanische Herzklappe, LVEF < 50%, VHF, Hyperkoagulabilität, St.n. Thromboembolie), St.n. Mitralklappenersatz plus ein Risikofaktor sowie Klappenprothesen alter Bauart (12). Dannzumal wird ab einem INR unter 2 das Bridging nierenfunktionsabhängig mit niedermolekularem oder unfraktioniertem Heparin durchgeführt (6). In allen anderen Situationen reicht die übliche Thromboseprophylaxe aus.
Neue orale Antikoagulanzien (NOAK)
NOAK haben im Vergleich zu VKA ein besseres Risiko-Nutzen-Verhältnis, weshalb sie mittlerweile bei Patienten mit Vorhofflimmern als Therapie der ersten Wahl gelten (10).
Die Dauer der präoperativen Therapiepause richtet sich nach der Nierenfunktion und der Gefährlichkeit allfälliger Blutungskomplikationen und beträgt 24 bis 48 oder gar 72 Stunden. Ein perioperatives Bridging wird aufgrund der aktuellen Datenlage nicht empfohlen (13, 14).
Antidiabetika bei DM Typ II
Ein schlecht kontrollierter Diabetes mellitus gilt unter anderem als Risikofaktor für Wundheilungsstörungen und -infekte (15, 16). Hypoglykämien erhöhen zudem die Morbidität, Mortalität und verlängern den Intensiv- und Krankenhausaufenthalt (17). Dies unterstreicht die Wichtigkeit einer guten Blutzuckereinstellung. In der Regel werden Antidiabetika lediglich am Operationstag pausiert (18), die Datenlage hierfür ist jedoch besonders bei den «neuen» oralen Antidiabetika noch relativ dürftig.
Metformin kann bei Kumulation das Risiko einer Laktatazidose erhöhen, was bei eingeschränkter Nierenfunktion vermehrt auftreten kann. Entsprechend stellt eine GFR unter 30ml/min eine Kontraindikation dar (19). Während gewisse Autoren auch längere Therapiepausen fordern, empfehlen wir, Metformin lediglich am Operationstag zu pausieren, wobei die Nierenfunktion auch im postoperativen Verlauf besonderer Beachtung bedarf. Sulfonylharnstoffe können bei Nüchternheit zu hypoglykämen Entgleisungen führen und sollen präoperativ am Operationstag pausiert werden (20, 21). Sodium-Glukose-Transporter-2(SGLT 2) – Inhibitoren bergen das Risiko einer euglykämen Ketoazidose (22, 23). In der aktuellen Literatur werden präoperativ Therapiepausen von eins (18, 20), drei (24) und bis zu sieben Tagen (25) beschrieben. Wir empfehlen SGLT-2-Inhibitoren vor kleinen bis mittleren Eingriffen am Operationstag und vor grossen Eingriffen zwei bis drei Tage präoperativ zu pausieren. DPP-4-Hemmer sollen gemäss den aktuellen Empfehlungen ebenso am Operationstag pausiert werden (18, 20). Aufgrund des geringen Hypoglykämierisikos ist bei kleinen Eingriffen auch ein perioperatives Fortführen vertretbar (21).
Antihypertensiva
Beta-Rezeptoren-Blocker, Calcium-Antagonisten und Alpha-2-Agonisten sollen gemäss aktueller Datenlage perioperativ fortgeführt werden (26, 27). Hingegen werden Diuretika in der Regel am Operationstag nicht verabreicht (26, 27). Kontrovers diskutiert wird die Therapie mit Renin-Angiotensin-Aldosteron-System-Hemmern. Die Leitlinien der «European Society of Cardiology/European Society of Anesthesiology» empfehlen, die Therapiepause abhängig von der Indikation durchzuführen. Werden ACE-Hemmer oder AT1-Antagonisten zur Therapie der Herzinsuffizienz und/oder linksventrikulären Dysfunktion eingesetzt, so sollen sie lückenlos weitergegeben werden. Erfolgt die Gabe jedoch wegen arterieller Hypertonie, werden sie 24 Stunden präoperativ pausiert (28). Die «CCS» (Canadian Cardiovascular Society) hingegen empfiehlt unabhängig von der Indikation ein perioperatives Absetzen für 24 Stunden (29), wohingegen die «AHA/ACC» ein Fortführen der Medikation als vertretbar erachten (30). In einer rezenten Metaanalyse führte weder perioperatives Pausieren noch Fortführen der Medikation zu einem signifikanten Unterschied beim Auftreten von MACE (major cardiac events) oder der Mortalität (31). Jedoch wurde bestätigt, dass ein Fortführen besagter Medikamente zu einem gehäuften Auftreten intraoperativer Hypotension führte. Weitere Studien zeigten, dass sich intraoperativ erniedrigte Blutdruckwerte negativ auf die renale und kardiale Funktion sowie die Mortalität auswirken können (32, 33).
Ein kausaler Zusammenhang mit ACE-Hemmern/AT1-Antagonisten konnte jedoch bisher nicht gezeigt werden, weshalb wir zusammenfassend kein perioperatives Pausieren der Dauertherapie empfehlen.
Psychopharmaka
Psychiatrische Dauermedikation kann grösstenteils perioperativ unverändert weitergeführt werden (34, 35). Eine Ausnahme bilden hierbei Monoaminooxidase (MAO)-Hemmer und Lithium. MAO-Hemmer können perioperativ in Kombination mit indirekten Sympathomimetika zu exzessiven Blutdruckentgleisungen führen (36). Ausserdem kann es durch eine pharmakokinetische Interaktion mit Opiaten (im Speziellen Pethidin und Tramadol) zu exzitativen Symptomen im Sinne eines Serotonin-Syndroms kommen (27). In der aktuellen Literatur wird für irreversible MAO-Hemmer ein Umstellen der Therapie zwei Wochen vor elektiven Eingriffen empfohlen (27, 34, 35).
Lithium hat eine sehr geringe therapeutische Breite, weshalb engmaschige Spiegelkontrollen notwendig sind (36). Zur Vermeidung von toxischen Nebenwirkungen wird in der aktuellen Literatur ein Absetzen 72 Stunden vor elektiven Eingriffen empfohlen (27,34,35).
Klinik für Anästhesiologie, Intensiv-, Rettungs- und Schmerzmedizin
Kantonsspital St.Gallen
Rorschacher Strasse 95
9007 St. Gallen
widmannjohannes@hotmail.com
Klinik für Anästhesiologie, Intensiv-, Rettungs- und Schmerzmedizin
Kantonsspital St.Gallen
Rorschacher Strasse 95
9007 St. Gallen
miodrag.filipovic@kssg.ch
Die Autoren erklären hiermit, dass kein Interessenskonflikt in Verbindung mit dem vorliegenden Manuskript besteht.
- Eine allfällige perioperative Modifikation der gerinnungshemmenden Medikation bedarf einer sorgfältigen Abschätzung des chirurgischen sowie thromboembolischen Risikos.
- Aspirin im Rahmen einer Primärprophylaxe soll präoperativ pausiert werden.
NOAK bedürfen keiner überbrückenden Gerinnungshemmung. - Antidiabetika haben das Potential, metabolische Veränderungen wie hypoglykäme Zustände, Laktat- und Ketoazidosen zu begünstigen und sollen deshalb mit besonderer Vorsicht gehandhabt werden.
- ACE-Hemmer und AT1-Antagonisten können das perioperative Risiko einer Hypotonie erhöhen, sollen aber in der Regel nicht pausiert werden.
Messages à retenir
- Une éventuelle modification périopératoire de l’anticoagulant nécessite une évaluation attentive du risque chirurgical et thromboembolique.
- L’aspirine doit être interrompue avant l’opération dans le cadre d’une prophylaxie primaire.
- Les NOACs n’ont pas besoin d’un anticoagulant de pontage.
- Les antidiabétiques ont le potentiel de favoriser les changements métaboliques tels que les états hypoglycémiques, les lactatacidoses et les acidocétoses et doivent donc être traités avec une attention particulière.
- Les inhibiteurs de l’ECA et les antagonistes de l’AT1 peuvent augmenter le risque périopératoire d’hypotension, mais ne doivent habituellement pas être interrompus.
1. Yurttas T, Filipovic M. Strategien zum Umgang mit antithrombotischen
Medikamenten im perioperativen Umfeld. Therapeutische Umschau. 2017 Dec;74(7):361–7.
2. Levine GN, Bates ER, Bittl JA, Brindis RG, Fihn SD, Fleisher LA, et al. 2016 ACC/AHA Guideline Focused Update on Duration of Dual Antiplatelet Therapy in Patients With Coronary Artery Disease: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines:
An Update of the 2011 ACCF/AHA/SCAI Guideline for Percutaneous Coronary Intervention, 2011 ACCF/AHA Guideline for Coronary Artery Bypass Graft Surgery, 2012 ACC/AHA/ACP/AATS/PCNA/SCAI/STS Guideline for the Diagnosis and
Management of Patients With Stable Ischemic Heart Disease, 2013 ACCF/AHA Guideline for the Management of ST-Elevation Myocardial Infarction, 2014 AHA/ACC Guideline for the Management of Patients With Non-ST-Elevation Acute
Coronary Syndromes, and 2014 ACC/AHA Guideline on Perioperative Cardiovascular Evaluation and Management of Patients Undergoing Noncardiac Surgery. Circulation. 2016 Sep 6;134(10):e123–55.
3. Roffi M, Patrono C, Collet J-P, Mueller C, Valgimigli M, Andreotti F, et al. 2015 ESC Guidelines for the management of acute coronary syndromes in patients
presenting without persistent ST-segment elevation: Task Force for the Management of Acute Coronary Syndromes in Patients Presenting without Persistent
ST-Segment Elevation of the European Society of Cardiology (ESC). Vol. 37,
European heart journal. 2016. pp. 267–315.
4. Mehta SR, Bainey KR, Cantor WJ, Lordkipanidzé M, Marquis-Gravel G, Robinson SD, et al. 2018 Canadian Cardiovascular Society/Canadian Association of Interventional Cardiology Focused Update of the Guidelines for the Use of Antiplatelet Therapy. Can J Cardiol. 2018 Mar;34(3):214–33.
5. Devereaux PJ, Mrkobrada M, Sessler DI, Leslie K, Alonso-Coello P, Kurz A, et al. Aspirin in Patients Undergoing Noncardiac Surgery. N Engl J Med. 2014 Apr 17;370(16):1494–503.
6. Yurttas T, Wanner PM, Filipovic M. Perioperative management of antithrombotic therapies. Current Opinion in Anaesthesiology. 2017 Aug;30(4):466–73.
7. Valgimigli M, Bueno H, Byrne RA, Collet J-P, Costa F, Jeppsson A, et al. 2017 ESC focused update on dual antiplatelet therapy in coronary artery disease developed in collaboration with EACTS: The Task Force for dual antiplatelet therapy in
coronary artery disease of the European Society of Cardiology (ESC) and of the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J. 2018 Jan 14;39(3):213–60.
8. van Kuijk J-P, Flu W-J, Schouten O, Hoeks SE, Schenkeveld L, de Jaegere PPT,
et al. Timing of noncardiac surgery after coronary artery stenting with bare metal or drug-eluting stents. Am J Cardiol. 2009 Nov 1;104(9):1229–34.
9. Hornor MA, Duane TM, Ehlers AP, Jensen EH, Brown PS, Pohl D, et al. American College of Surgeons’ Guidelines for the Perioperative Management of Antithrombotic Medication. J Am Coll Surg. 2018 Nov;227(5):521–1.
10. Ruff CT, Giugliano RP, Braunwald E, Hoffman EB, Deenadayalu N, Ezekowitz MD, et al. Comparison of the efficacy and safety of new oral anticoagulants with warfarin in patients with atrial fibrillation: a meta-analysis of randomised trials. Lancet. 2014 Mar 15;383(9921):955–62.
11. Douketis JD, Spyropoulos AC, Kaatz S, Becker RC, Caprini JA, Dunn AS, et al. Perioperative Bridging Anticoagulation in Patients with Atrial Fibrillation. N Engl J Med. 2015 Aug 27;373(9):823–33.
12. Filipovic M, Korte W, Rickli H. Thromboseprophylaxe und peri- interventionelle antithrombotische Therapie, 7. Auflage. https://wwwkssgch/kardiologie/fuer-fachpersonen/throm- boseprophylaxe-und-periinterventionelle-antithrombotische 2017. :1–2.
13. Steffel J, Verhamme P, Potpara TS, Albaladejo P, Antz M, Desteghe L, et al. The 2018 European Heart Rhythm Association Practical Guide on the use of non-
vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J. 2nd ed. 2018 Mar 19;39(16):1330–93.
14. Raval AN, Cigarroa JE, Chung MK, Diaz-Sandoval LJ, Diercks D, Piccini JP, et al. Management of Patients on Non-Vitamin K Antagonist Oral Anticoagulants in the Acute Care and Periprocedural Setting: A Scientific Statement From the American Heart Association. Circulation. 2017 Mar 7;135(10):e604–33.
15. Golden SH, Peart-Vigilance C, Kao WH, Brancati FL. Perioperative glycemic
control and the risk of infectious complications in a cohort of adults with diabetes. Diabetes Care. 1999 Sep;22(9):1408–14.
16. Sudhakaran S, Surani SR. Guidelines for Perioperative Management of the
Diabetic Patient. Surg Res Pract. 2015;2015:284063.
17. Turchin A, Matheny ME, Shubina M, Scanlon JV, Greenwood B, Pendergrass ML. Hypoglycemia and clinical outcomes in patients with diabetes hospitalized in the general ward. Diabetes Care. 2009 Jul;32(7):1153–7.
18. Leung V, Ragbir-Toolsie K. Perioperative Management of Patients with Diabetes. Health Serv Insights. 2017;10:1178632917735075.
19. European Medicines Agency (EMA). Use of metformin to treat diabetes now
expanded to patients with moderately reduced kidney function. European
Medicines Agency. 2016 Dec 19;:1–4.
20. Wagner J, Luber V, Lock JF, Dietz UA, Lichthardt S, Matthes N, et al. [Perioperative handling of antidiabetic drugs]. Chirurg. 2018 Feb;89(2):103–7.
21. Membership of the Working Party, Barker P, Creasey PE, Dhatariya K, Levy N, Lipp A, et al. Peri-operative management of the surgical patient with diabetes 2015: Association of Anaesthetists of Great Britain and Ireland. Anaesthesia. 2015 Dec;70(12):1427–40.
22. European Medicines Agency (EMA). EMA confirms recommendations to minimise ketoacidosis risk with SGLT2 inhibitors for diabetes. European Medicines Agency. 2016 May 12;:1–3.
23. Milder DA, Milder TY, Kam PCA. Sodium-glucose co-transporter type-2 inhibitors: pharmacology and peri-operative considerations. Anaesthesia. 2018 Mar 12;73(8):1008–18.
24. Goldenberg RM, Berard LD, Cheng AYY, Gilbert JD, Verma S, Woo VC, et al. SGLT2 Inhibitor. Clinical Therapeutics. Elsevier; 2016 Dec 1;38(12):2654–2664.e1.
25. Pujara S, Ioachimescu A. Prolonged Ketosis in a Patient With Euglycemic Diabetic Ketoacidosis Secondary to Dapagliflozin. J Investig Med High Impact Case Rep. 2017 Apr;5(2):2324709617710040.
26. Pai S-L, Chadha RM, Irizarry-Alvarado JM, Renew JR, Aniskevich S. Pharmacologic and Perioperative Considerations for Antihypertensive Medications. Curr Clin Pharmacol. 2017;12(3):135–40.
27. Gemeinsame Empfehlung der Deutschen Gesellschaft für Anästhesiologie und
Intensivmedizin, der Deutschen Gesellschaft für Chirurgie und der Deutschen
Gesellschaft für Innere Medizin. [Preoperative Evaluation of Adult Patients
Before Elective, Non-Cardiothoracic Surgery]. Anasthesiol Intensivmed Notfallmed Schmerzther. 2017 Jun;52(6):446–62.
28. Kristensen SD, Knuuti J, Saraste A, Anker S, Bøtker HE, Hert SD, et al. 2014 ESC/ESA Guidelines on non-cardiac surgery: cardiovascular assessment and
management: The Joint Task Force on non-cardiac surgery: cardiovascular
assessment and management of the European Society of Cardiology (ESC) and the European Society of Anaesthesiology (ESA). Vol. 35, European heart journal. 2014. pp. 2383–431.
29. Duceppe E, Parlow J, MacDonald P, Lyons K, McMullen M, Srinathan S, et al.
Canadian Cardiovascular Society Guidelines on Perioperative Cardiac Risk Assessment and Management for Patients Who Undergo Noncardiac Surgery. Can J Cardiol. 2017 Jan;33(1):17–32.
30. Fleisher LA, Fleischmann KE, Auerbach AD, Barnason SA, Beckman JA, Bozkurt B, et al. 2014 ACC/AHA guideline on perioperative cardiovascular evaluation and management of patients undergoing noncardiac surgery: executive summary: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. Vol. 130, Circulation. 2014. pp. 2215–45.
31. Hollmann C, Fernandes NL, Biccard BM. A Systematic Review of Outcomes
Associated With Withholding or Continuing Angiotensin-Converting Enzyme Inhibitors and Angiotensin Receptor Blockers Before Noncardiac Surgery. Anesth
Analg. 2018 Sep;127(3):678–87.
32. Walsh M, Devereaux PJ, Garg AX, Kurz A, Turan A, Rodseth RN, et al. Relationship between intraoperative mean arterial pressure and clinical outcomes after noncardiac surgery: toward an empirical definition of hypotension. Anesthesiology. 2013 Sep;119(3):507–15.
33. White SM, Moppett IK, Griffiths R, Johansen A, Wakeman R, Boulton C, et al.
Secondary analysis of outcomes after 11,085 hip fracture operations from the prospective UK Anaesthesia Sprint Audit of Practice (ASAP-2). Anaesthesia. 2016 May;71(5):506–14.
34. De Hert S, Staender S, Fritsch G, Hinkelbein J, Afshari A, Bettelli G, et al. Pre-operative evaluation of adults undergoing elective noncardiac surgery. European Journal of Anaesthesiology. 2018 Jun;35(6):407–65.
35. Redel A, Hommers LG, Kranke P, Schwemmer U, Prasser C. [Modification of perioperative psychiatric drug therapy]. Anasthesiol Intensivmed Notfallmed Schmerzther. 2013 Jan;48(1):10–7.
36. Karow T, Lang-Roth R. Allgemeine und spezielle Pharmakologie und Toxikologie. 2017.
info@herz+gefäss
- Vol. 9
- Ausgabe 2
- März 2019