- Update Chronisch thromboembolische Pulmonale Hypertonie (CTEPH)
Die chronisch thromboembolische pulmonale Hypertonie (CTEPH) gehört zur Gruppe 4 der pulmonalen Hypertonie infolge von Obstruktion der Pulmonalgefässe. Wichtigstes Leitsymptom ist eine progrediente Anstrengungsdyspnoe Monate bis Jahre nach stattgehabter Lungenembolie, obschon die Erkrankung auch ohne erinnerliche akute Embolie auftreten kann. Dieser Artikel berichtet über den aktuellen Wissensstand bezüglich Pathophysiologie, Diagnostik und Therapie der CTEPH und weist auf diese wichtige, zum Teil unterdiagnostizierte Krankheit hin.
Chronic thromboembolic pulmonary hypertension (CTEPH) belongs to group 4 of pulmonary hypertension due to obstruction of the pulmonary vessels. The most important leading symptom is progressive exertional dyspnea months to years after a pulmonary embolism, although the disease can also occur without a previously diagnosed acute embolism. This article reports on the current state of knowledge regarding the pathophysiology, diagnosis and treatment of CTEPH and draws attention to this important, sometimes underdiagnosed disease.
Key Words: pulmonary hypertension, chronic thromboembolic pulmonary hypertension, CTEPH, Exertional dyspnea
Einleitung
Die präkapilläre pulmonale Hypertonie (PH) wird obligatorisch im Rechtsherzkatheter diagnostiziert. Die PH ist seit der Aktualisierung der ESC/ERS Richtlinien für Lungenhochdruck definiert als pulmonal arterieller Mitteldruck (mPAP) >20mmHg (zuvor ≥25mmHg) mit einem pulmonal-vaskulären Widerstand (PVR) >2 WU und einem pulmonal-arteriellen Verschlussdruck (Wedge-Druck) ≤15mmHg (1). Die PH wird in fünf Gruppen eingeteilt, wobei die chronisch thromboembolische PH (CTEPH) der Gruppe 4, der PH assoziiert mit Obstruktion der Pulmonalgefässe, zugeteilt ist. Die CTEPH wird definiert als symptomatische PH mit persistierendem Perfusionsdefizit trotz adäquater Antikoagulation über mehr als 3 Monate (1). Häufig gehen der CTEPH akute Lungenembolien voraus. Bei persistierender Dyspnoe nach akuten Lungenembolien und mindestens 3 Monate suffizienter Antikoagulation sollte daher an eine CTEPH gedacht werden. Da sich nach akuten Lungenembolien noch Monate bis Jahre später auch bei asymptomatischen Personen radiologisch oder pathologisch narbige Residuen in den Lungenarterien finden können (webs and bands), ist die Abklärung bezüglich CTEPH nur bei Patient/-innen mit Dyspnoe empfohlen. Wenn eine persistierende Dyspnoe und entsprechende radiologische Veränderungen vorhanden sind, jedoch keine PH, spricht man von chronisch thromboembolischer Lungenerkrankung (chronic thrombo-embolic lung disease; CTED).
Epidemiologie
Die Inzidenz der CTEPH nach stattgehabter Lungenembolie liegt gemäss Studien zwischen 2.3% und 4% (2-5). Wahrscheinlich besteht eine hohe Dunkelziffer von nicht erkannten Patient/-innen mit CTEPH, aufgrund von Fehldiagnosen aus nicht-spezifischen Symptomen und der zu seltenen Verwendung von Lungenperfusionsszintigrafien (6). Daten aus verschiedenen Registern zeigten zudem, dass 25% – 63% aller Betroffenen keine akute Lungenembolie in der persönlichen Anamnese aufwiesen (7-9).
Pathophysiologie
Die CTEPH beginnt meist mit einer Obstruktion von Lungenarterien im Rahmen einer akuten Lungenembolie. Selbst unter konsequenter Antikoagulation lösen sich bei einem kleinen Teil der Betroffenen nicht sämtliche Emboli auf. In diesem Fall kann es im Verlauf zu einer Organisation und Fibrosierung des residuellen thrombotischen Materials mit meist wandständigen Residuen oder radiologisch zum Teil erkennbaren Strickleitern (webs) kommen. In Fällen ohne erinnerter/stattgehabter akuter Lungenembolie wird ein in-situ Geschehen in den Pulmonalarterien oder okkulte Embolien diskutiert. Dazu können eine Inflammation/Infektion, ein abnormales Fibrinogen, eine eingeschränkte Angiogenese, eine unzureichende Antikoagulation oder biologische und genetische Faktoren, die die Hyperkoagulabilität erhöhen, beitragen (10-12). Passend zur gesteigerten Inzidenz von CTEPH nach erfolgter Splenektomie wird auch ein erhöhter Thrombozytenumsatz als Faktor in der Entstehung beschrieben (13).
Bereits 1993 wurde zusätzlich eine mikrovaskuläre «small vessel» Komponente beschrieben (14). Diese Mikrovaskulopathie verhält sich sehr ähnlich zu derjenigen bei pulmonal-arterieller Hypertonie (PAH) und ist von dieser kaum zu unterscheiden (15). Die Umverteilung des pulmonalen Blutflusses verursacht in den kleinen Gefässen erhöhte Scherkräfte, was über eine endotheliale Dysfunktion und ein Remodelling der Gefässwände zu einem erhöhten Gefässwiderstand und schliesslich Symptomatik der PH führt (11, 16).
Klinische Präsentation
Die Symptomatik der CTEPH ist unspezifisch, da sie durch die Dysfunktion des rechten Ventrikels als Folge der PH verursacht ist, was die Diagnosestellung erschwert. Als erstes Leitsymptom beschreiben die meisten Patient/-innen eine Belastungsdyspnoe, welche unbehandelt progressiv zunimmt (17). Weitere Symptome sind in Tab. 1 zusammengefasst (18). Die klinischen Befunde sind unspezifisch, abgesehen von einer möglichen Akzentuierung der pulmonalen Komponente des zweiten Herztons.
Diagnostik
Die CTEPH sollte sowohl bei persistierenden Beschwerden nach stattgehabter Lungenembolie als auch bei anderweitigen Hinweisen für eine PH differenzialdiagnostisch evaluiert werden. Ein routinemässiges Screening nach überstandener Lungenembolie ist nicht empfohlen. Weitere Untersuchungen sind indiziert bei Befunden passend zu einer vorbestehenden CTEPH, Patient/-innen mit erhöhtem Risiko für CTEPH oder persistierenden Beschwerden nach 3-monatiger Antikoagulation (19, 20). Die entsprechende Diagnostik und Festlegung der Therapie sollte in einem Referenzzentrum im multidisziplinären Team erfolgen (1, 21).
Erste Hinweise für eine pulmonale Hypertonie finden sich oftmals mittels Echokardiografie. Neben dem systolischen pulmonal arteriellen Druck (sPAP) können auch indirekte Hinweise für eine PH vorhanden sein, zum Beispiel ein dilatierter rechter Vorhof/Ventrikel, eine eingeschränkte Kontraktilität des rechten Ventrikels, ein D-shaping des linken Ventrikels oder Fluss-Abnormalitäten im Doppler des Ausflusstrakts des rechten Ventrikels (22, 23).
Zu möglichen EKG-Veränderungen bei der PH zählen das P-pulmonale in Ableitung II, eine Achsenabweichung (QRS-Achse >90°), ein Rechtsschenkelblock oder eine T-Inversion (V1-4 oder II, III, aVF) (24).
In der Spiroergometrie finden sich bei CTEPH typischerweise eine Hyperventilation, ineffiziente Ventilation und erhöhte alveolo-kapilläre O2- und CO2-Gradienten (22). Diese Befunde können auch bei unauffälliger Echokardiografie auf eine pulmonale Hypertonie hinweisen (25).
Spätestens bei auffälligen Ergebnissen obiger Untersuchungen sollte eine Zuweisung ins Referenzzentrum erfolgen. Eine Rechtsherzkatheter-Untersuchung (RHK) ist zwingend nötig zur Bestätigung der PH-Diagnose und kann, gerade in frühen Stadien mit normaler Hämodynamik in Ruhe, auch unter Belastung durchgeführt werden (26). Dabei sollte der Herzauswurf mit der direkten Fick-Methode oder Thermodilution gemessen werden. Nur so ist eine korrekte Bestimmung und Errechnung des Gefässwiderstandes (PVR), der benötigt wird, möglich. Die dazu verwendete metabolische Einheit im RHK-Raum ist nur in spezialisierten Zentren vorhanden. Zudem ist für die Diagnose einer CTED eine dynamische Belastungsuntersuchung mittels Fahrradergometrie im RHK angezeigt. Im Falle der CTEPH ist die korrekte Erfassung des Lungenwiderstandes in Ruhe und unter Belastung diagnostisch wichtig sowie prä- und postoperativ ein prognostischer Marker (27).
Die Lungenperfusionsszintigrafie (V/Q-Scan) ist weiterhin das Mittel der Wahl zum Ausschluss einer CTEPH (1). Bei bestehendem Verdacht auf eine CTEPH ist eine Computertomografie der Pulmonalarterien (CTPA) empfohlen, insbesondere hinsichtlich Einschätzung der Operabilität (19). Wenn vorhanden, können diese beiden Bildgebungsverfahren in spezialisierten Zentren auch direkt durch eine Dual-Energy CT ersetzt werden (Abb. 1). Selten wird in erfahrenen Zentren bei nicht konklusivem Befund, aber ansonsten hochgradigem Verdacht, eine klärende digitale Subtraktionsangiographie (DSA) angewendet (19).
Therapie
Die Lokalisation der Gefässobstruktion ist massgebend für die möglichen Therapieoptionen. Häufig besteht ein Mischbild aus proximalen, distalen und mikrovaskulären Läsionen. Entsprechend kommt ein multimodales Therapiekonzept zum Zug. Therapieempfehlungen werden in multidisziplinären Teams spezialisierter Zentren festgelegt. In der Schweiz gibt es hierfür, organisiert durch die Gesellschaft für pulmonale Hypertonie (SGPH), ein nationales multidisziplinäres CTEPH-Board (cteph@sgph.ch), welches alle beteiligten Disziplinen umfasst (u.a. Pneumologie, Kardiologie, (interventionelle) Radiologie und Thoraxchirurgie).
Antikoagulation
Da eine inkomplette Auflösung von Gerinnseln und rezidivierende Thromboembolien wichtige pathophysiologische Mechanismen in der Entstehung von CTEPH sind, ist eine lebenslängliche Antikoagulation empfohlen (1). Bei 10 % aller Patient/-innen mit CTEPH liegt ein Antiphospholipidsyndrom vor, welches aufgrund der Indikation für eine Antikoagulation mittels eines Vitamin-K-Antagonisten (VKA) aktiv gesucht werden sollte (7, 28). Ansonsten gibt es mangels RCTs keine Empfehlung zur Wahl der Antikoagulation. Eine Meta-Analyse zeigte eine tiefere Mortalität von DOAKs gegenüber VKAs, bei jedoch höherem Rezidivrisiko für thromboembolische Ereignisse (29).
Chirurgisch
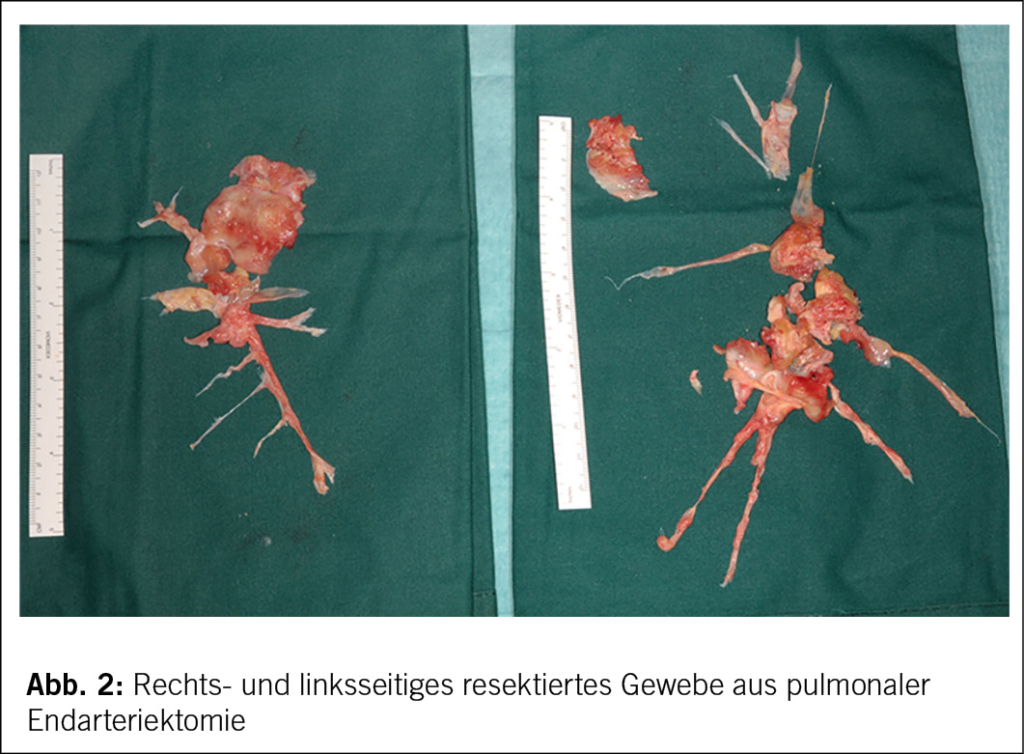
Die pulmonale Endarteriektomie (PEA, siehe Abb. 2) ist der Goldstandard bei zugänglichen Läsionen und kann die pulmonale Hämodynamik deutlich verbessern oder in einem erheblichen Teil normalisieren (1, 30). Dies geschieht durch die Verbesserung des Ventilations-Perfusions-Mismatch, was die rechtsventrikuläre Funktion steigert und sekundären Veränderungen der kleinen Gefässe vorbeugt (31). Durch gewonnene Erfahrung konnte die perioperative Mortalität auf 2 % gesenkt werden, obschon immer mehr Patient/-innen als operabel eingestuft werden (18, 32, 33). Die Mortalität hängt vom Patientenkollektiv und den Risiken ab, beispielsweise vom präoperativen PVR als Zeichen der bestehenden Mikroangiopathie und Komorbiditäten (33-35). Die Überlebensrate nach 3 Jahren von 89% gegenüber 70% bei nicht operierten Patient/-innen unterstreicht die Wichtigkeit der PEA (36).
Der chirurgische Zugang erfolgt via medianer Sternotomie. Wichtig ist eine gute Sicht auf das Operationsfeld, erreicht durch einen kardiopulmonalen Bypass sowie kurzzeitigem hypothermem Kreislaufstillstand (31). Die visuell identifizierte Dissektionsebene in der Gefässwand wird von proximal nach distal verfolgt und die Okklusion bis subsegmental entfernt (37). Dies ist wichtig, da eine Thrombektomie ohne Endarteriektomie den PVR nicht senkt (38). Die postoperativ häufigsten Komplikationen, das Reperfusionsödem der Lunge und eine residuelle PH im Rahmen der konkomittierenden Mikroangiopathie, treten oft gemeinsam auf und werden, wenn nötig, mit einer überbrückenden extrakorporalen Membran-oxygenierung (ECMO) behandelt (39, 40).
Interventionell
Je nach Grundpopulation ist bis zu 1/3 der Erkrankten nicht operabel, sei dies aus morphologisch-technischen Gründen (z.B. zu distale Läsionen), wegen erheblicher Komorbiditäten oder Ablehnung einer Operation durch die Patient/-innen selbst (9). Für diese Patient/-innen, sowie bei Mischformen mit distaler Beteiligung im Sinne eines multimodalen Behandlungskonzeptes, hat die Ballonangioplastie (balloon pulmonary angioplasty; BPA) in den letzten Jahren weltweit an Bedeutung gewonnen, nachdem initial vor allem japanische Studien durch verbesserte Technik eine Reduktion der potenziell lebensgefährlichen Komplikationen zeigten (41). Studien beschreiben ein Komplikationsrisiko von 8% bis 12% mit Lungenverletzung/Hämoptysen als häufigste Folge, was wiederum stark von der Patientenauswahl und Erfahrung der Zentren abhängt (42-44). Neue Daten zeigen zudem, dass in erfahrenen Zentren auch (sub-)segmentale totale Gefässverschlüsse mittels BPA therapiert werden können – mit vergleichbarem Komplikationsrisiko (45).
Die Intervention erfolgt in mehreren Etappen, um das Komplikationsrisiko zu senken. Einerseits sollte eine schrittweise Dilatation das Risiko für allfällige Verletzungen der Gefässe vermindern, andererseits dem Reperfusionsödem vorbeugen. Zudem können Erkrankte mit einem PVR >4 WU von einer vorgängigen medikamentösen Therapie profitieren (43).
Es gibt immer mehr Langzeitdaten zur BPA und diese ist auch im multimodalen Therapiekonzept, das heisst vor, während oder nach einer PEA, im Aufschwung (46-49). In aktuellen Leitlinien ist die BPA neben Patient/-innen, die inoperabel sind oder mit persistierender PH nach PEA (neu Empfehlungsgrad I-B), auch bei operablen Patient/-innen mit ungünstiger Nutzen/Risiko-Abwägung (Empfehlungsgrad IIb-C) in Betracht zu ziehen (1).
Medikamente
Die medikamentöse Therapie wird zur Behandlung der Mikrovaskulopathie bei inoperablen Patient/-innen oder bei persistierender PH nach PEA eingesetzt. Die erste zugelassene und am besten erforschte medikamentöse Therapie für CTEPH ist Riociguat, ein Stimulator der löslichen Guanylatcyclase (sGC). Nach 16 Wochen Therapie zeigte sich eine signifikante Verbesserung im 6-Minuten-Gehtest sowie eine Reduktion des PVR (50). Treprostinil, ein parenterales Prostacyclin-Analogon, erwies sich in einer Phase-3-Studie ebenfalls als sicher und ist sogar zugelassen für Betroffene mit WHO-Funktionsklasse III-IV (1, 51). Ebenso wurde die Wirksamkeit von Macitentan, einem für PAH zugelassener Endothelinrezeptor-Antagonisten, aufgezeigt und kürzlich publiziert (52). Weitere Wirkstoffe aus der PAH-Therapie (z.B. Sildenafil oder Bosentan) werden im klinischen Alltag häufig off-label verwendet, da ihr Nutzen bislang in keinen randomisiert-kontrollierten Studien belegt werden konnte (1).
Ergänzende Therapien
Sowohl operable als auch inoperable Patient/-innen profitieren von kontrolliertem Muskel- und Ausdauertraining (53, 54). Unter gezielter Anleitung konnte eine Verbesserung im 6-Minuten-Gehtest, der Lebensqualität und der Leistungsfähigkeit erzielt werden (54).
Herausforderungen im Alltag und Ausblick
Die Unterscheidung zwischen einer akuten Lungenembolie und einer vorbestehenden CTEPH ist nicht trivial. Guérin et al fanden, dass Patient/-innen mit nachfolgend bestätigter CTEPH bereits zum Diagnosezeitpunkt der Lungenembolie häufiger einen sPAP >60mmHg aufwiesen, hinweisend auf eine vorbestehende Adaptation des rechten Ventrikels. Aufgrund dessen liessen sie die CT-Befunde erneut und verblindet beurteilen, wobei bei allen Betroffenen bereits dort Hinweise für eine CTEPH gefunden werden konnten, gegenüber 20% der nicht erkrankten (55). Auch Barco et al fanden bei 15 % aller Patient/-innen mit akuter Lungenembolie Hinweise für eine CTEPH, die sich in 1.7 % der Ausgangspopulation im Verlauf diagnostizieren liess (56). Eine weitere Studie identifizierte 6 radiologische Parameter als unabhängige Prädiktoren für eine CTEPH (57). Somit sollte bei akuten Lungenembolien bereits an die CTEPH gedacht werden. Ein Mittel zur Früherkennung der CTEPH könnte ein «surveillance program» bei Hochrisikopatient/-innen sein, wobei es hierfür aktuell keine klaren Guidelines gibt (58). Eine verkürzte Zeit bis zur CTEPH-Diagnosestellung wäre jedoch wichtig, da eine spätere Diagnose mit einer schlechteren Prognose einhergeht (59).
Ein weiterer Diskussionspunkt ist die medikamentöse Therapie vor geplanter PEA/BPA. Einerseits sollte, um der fortschreitenden Mikrovaskulopathie vorzubeugen, mit Interventionen nicht unnötig zugewartet werden. Andererseits ist das Komplikationsrisiko grösser, je höher der PVR. Im klinischen Alltag tendieren wir dazu, Patient/-innen mit einem hohen PVR (>6-8 WU) bei Diagnosestellung vorzubehandeln, dies sollte jedoch auf keinen Fall die Operation verzögern. Ein Entscheid für oder gegen eine medikamentöse Therapie vor einer geplanten Intervention wird individuell vom multidisziplinären Gremium gefällt (60).
med. pract. Aldo Kammerlander 1
Prof. Dr. med. Isabelle Opitz 2
PD Dr. med. Mona Lichtblau 1
Prof. Dr. med. Silvia Ulrich 1
1 Klinik für Pneumologie, Universitätsspital Zürich, Rämistrasse 100, 8091 Zürich
2 Klinik für Thoraxchirurgie, Universitätsspital Zürich, Rämistrasse 100, 8091 Zürich
Copyright Aerzteverlag medinfo AG
Klinik für Pneumologie
Universitätsspital Zürich
Rämistrasse 100
8091 Zürich
Klinik für Thoraxchirurgie
Universitätsspital Zürich
Rämistrasse 100
8091 Zürich
Klinik für Pneumologie
Universitätsspital Zürich
Rämistrasse 100
8091 Zürich
silvia.ulrich@usz.ch
Die Autorenschaft hat keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
- Bei ungeklärter anstrengungsinduzierter Dyspnoe, insbesondere nach stattgehabter Lungenembolie, ist PH/CTEPH eine wichtige Differenzialdiagnose, die häufig vergessen geht.
- Sollten sich in Basisuntersuchungen (EKG, Echo, Spiroergometrie) pathologische Befunde zeigen, die vereinbar mit einer pulmonalen Hypertonie sind, ist eine Zuweisung in ein Referenzzentrum empfohlen (www.sgph.ch).
- Die mögliche Normalisierung der Hämodynamik nach PEA macht die Früherkennung von CTEPH umso wichtiger. Auch nicht operable Patient/-innen können deutlich von multimodalen Therapiekonzepten profitieren.
- Eine lebenslängliche Antikoagulation ist empfohlen. Ein Antiphospholipidsyndrom sollte bei vorliegender CTEPH aktiv gesucht werden, insbesondere als Indikation für eine Antikoagulation mittels VKA.
1. Humbert M, Kovacs G, Hoeper MM, Badagliacca R, Berger RMF, Brida M, et al. 2022 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension. Eur Heart J. 2022;43(38):3618-731.
2. Luijten D, Talerico R, Barco S, Cannegieter SC, Delcroix M, Ende-Verhaar YM, et al. Incidence of chronic thromboembolic pulmonary hypertension after acute pulmonary embolism: an updated systematic review and meta-analysis. European Respiratory Journal. 2023;62(1):2300449.
3. Pengo V, Lensing AWA, Prins MH, Marchiori A, Davidson BL, Tiozzo F, et al. Incidence of Chronic Thromboembolic Pulmonary Hypertension after Pulmonary Embolism. New England Journal of Medicine. 2004;350(22):2257-64.
4. Valerio L, Mavromanoli AC, Barco S, Abele C, Becker D, Bruch L, et al. Chronic thromboembolic pulmonary hypertension and impairment after pulmonary embolism: the FOCUS study. European Heart Journal. 2022;43(36):3387-98.
5. Gall H, Hoeper MM, Richter MJ, Cacheris W, Hinzmann B, Mayer E. An epidemiological analysis of the burden of chronic thromboembolic pulmonary hypertension in the USA, Europe and Japan. European Respiratory Review. 2017;26(143):160121.
6. Tapson VF, Platt DM, Xia F, Teal SA, De La Orden M, Divers CH, et al. Monitoring for Pulmonary Hypertension Following Pulmonary Embolism: The INFORM Study. The American Journal of Medicine. 2016;129(9):978-85.e2.
7. Pepke-Zaba J, Delcroix M, Lang I, Mayer E, Jansa P, Ambroz D, et al. Chronic Thromboembolic Pulmonary Hypertension (CTEPH). Circulation. 2011;124(18):1973-81.
8. Lang IM. Chronic Thromboembolic Pulmonary Hypertension — Not So Rare after All. New England Journal of Medicine. 2004;350(22):2236-8.
9. Guth S, D‘Armini AM, Delcroix M, Nakayama K, Fadel E, Hoole SP, et al. Current strategies for managing chronic thromboembolic pulmonary hypertension: results of the worldwide prospective CTEPH Registry. ERJ Open Research. 2021;7(3):00850-2020.
10. Lang IM, Dorfmuller P, Vonk Noordegraaf A. The Pathobiology of Chronic Thromboembolic Pulmonary Hypertension. Ann Am Thorac Soc. 2016;13 Suppl 3:S215-21.
11. Simonneau G, Torbicki A, Dorfmüller P, Kim N. The pathophysiology of chronic thromboembolic pulmonary hypertension. European Respiratory Review. 2017;26(143):160112.
12. Opitz I, Kirschner MB. Molecular Research in Chronic Thromboembolic Pulmonary Hypertension. International Journal of Molecular Sciences. 2019;20(3):784.
13. Zhang L, Yan P, Yang K, Wu S, Bai Y, Zhu X, et al. Association between splenectomy and chronic thromboembolic pulmonary hypertension: a systematic review and meta-analysis. BMJ Open. 2021;11(2):e038385.
14. Moser KM, Bloor CM. Pulmonary vascular lesions occurring in patients with chronic major vessel thromboembolic pulmonary hypertension. Chest. 1993;103(3):685-92.
15. Ulrich S, Fischler M, Speich R, Popov V, Maggiorini M. Chronic thromboembolic and pulmonary arterial hypertension share acute vasoreactivity properties. Chest. 2006;130(3):841-6.
16. Humbert M. Pulmonary arterial hypertension and chronic thromboembolic pulmonary hypertension: pathophysiology. European Respiratory Review. 2010;19(115):59-63.
17. Galiè N, Humbert M, Vachiery J-L, Gibbs S, Lang I, Torbicki A, et al. 2015 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension. European Heart Journal. 2016;37(1):67-119.
18. Kerr KM, Elliott CG, Chin K, Benza RL, Channick RN, Davis RD, et al. Results From the United States Chronic Thromboembolic Pulmonary Hypertension Registry. Chest. 2021;160(5):1822-31.
19. Helmersen D, Provencher S, Hirsch AM, Van Dam A, Dennie C, De Perrot M, et al. Diagnosis of chronic thromboembolic pulmonary hypertension: A Canadian Thoracic Society clinical practice guideline update. Canadian Journal of Respiratory, Critical Care, and Sleep Medicine. 2019;3(4):177-98.
20. Konstantinides SV, Meyer G, Becattini C, Bueno H, Geersing G-J, Harjola V-P, et al. 2019 ESC Guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). European Heart Journal. 2020;41(4):543-603.
21. Cullivan S, Boucly A, Jevnikar M, Lechartier B, Ulrich S, Bertoletti L, et al. ERS International Congress 2023: highlights from the Pulmonary Vascular Diseases Assembly. ERJ Open Res. 2024;10(1).
22. Gopalan D, Delcroix M, Held M. Diagnosis of chronic thromboembolic pulmonary hypertension. European Respiratory Review. 2017;26(143):160108.
23. Brugger N, Lichtblau M, Maeder MT, Müller H, Pellaton C, Yerly P. Two-dimensional transthoracic echocardiography at rest for the diagnosis, screening and management of pulmonary hypertension. Swiss Medical Weekly. 2021;151(2122):w20486.
24. Henkens IR, Mouchaers KT, Vonk-Noordegraaf A, Boonstra A, Swenne CA, Maan AC, et al. Improved ECG detection of presence and severity of right ventricular pressure load validated with cardiac magnetic resonance imaging. Am J Physiol Heart Circ Physiol. 2008;294(5):H2150-7.
25. Held M, Grün M, Holl R, Hübner G, Kaiser R, Karl S, et al. Cardiopulmonary Exercise Testing to Detect Chronic Thromboembolic Pulmonary Hypertension in Patients with Normal Echocardiography. Respiration. 2014;87(5):379-87.
26. Kovacs G, Herve P, Barbera JA, Chaouat A, Chemla D, Condliffe R, et al. An official European Respiratory Society statement: pulmonary haemodynamics during exercise. European Respiratory Journal. 2017;50(5):1700578.
27. Skoro-Sajer N, Marta G, Gerges C, Hlavin G, Nierlich P, Taghavi S, et al. Surgical specimens, haemodynamics and long-term outcomes after pulmonary endarterectomy. Thorax. 2014;69(2):116-22.
28. Pengo V, Denas G, Zoppellaro G, Jose SP, Hoxha A, Ruffatti A, et al. Rivaroxaban vs warfarin in high-risk patients with antiphospholipid syndrome. Blood. 2018;132(13):1365-71.
29. Ishisaka Y, Watanabe A, Takagi H, Steiger D, Kuno T. Anticoagulation in chronic thromboembolic pulmonary hypertension: A systematic review and meta-analysis. Thromb Res. 2023;231:91-8.
30. Hsieh WC, Jansa P, Huang WC, Nižnanský M, Omara M, Lindner J. Residual pulmonary hypertension after pulmonary endarterectomy: A meta-analysis. The Journal of Thoracic and Cardiovascular Surgery. 2018;156(3):1275-87.
31. Madani MM. Surgical Treatment of Chronic Thromboembolic Pulmonary Hypertension: Pulmonary Thromboendarterectomy. Methodist DeBakey Cardiovascular Journal. 2016;12(4):213.
32. Jenkins DP, Tsui SS, Taghavi J, Kaul P, Ali J, Ng C. Pulmonary thromboendarterectomy—the Royal Papworth experience. Annals of Cardiothoracic Surgery. 2022;11(2):128-32.
33. Mayer E, Jenkins D, Lindner J, D’Armini A, Kloek J, Meyns B, et al. Surgical management and outcome of patients with chronic thromboembolic pulmonary hypertension: Results from an international prospective registry. The Journal of Thoracic and Cardiovascular Surgery. 2011;141(3):702-10.
34. Jamieson SW, Kapelanski DP, Sakakibara N, Manecke GR, Thistlethwaite PA, Kerr KM, et al. Pulmonary endarterectomy: experience and lessons learned in 1,500 cases. Ann Thorac Surg. 2003;76(5):1457-62; discussion 62-4.
35. Dartevelle P, Fadel E, Mussot S, Chapelier A, Herve P, De Perrot M, et al. Chronic thromboembolic pulmonary hypertension. European Respiratory Journal. 2004;23(4):637-48.
36. Delcroix M, Lang I, Pepke-Zaba J, Jansa P, D’Armini AM, Snijder R, et al. Long-Term Outcome of Patients With Chronic Thromboembolic Pulmonary Hypertension. Circulation. 2016;133(9):859-71.
37. Delcroix M, de Perrot M, Jais X, Jenkins DP, Lang IM, Matsubara H, et al. Chronic thromboembolic pulmonary hypertension: realising the potential of multimodal management. Lancet Respir Med. 2023;11(9):836-50.
38. Opitz I, De Perrot M. Technique of Pulmonary Thromboendarterectomy. Operative Techniques in Thoracic and Cardiovascular Surgery. 2012;17(3):168-80.
39. Kim NH, Delcroix M, Jenkins DP, Channick R, Dartevelle P, Jansa P, et al. Chronic thromboembolic pulmonary hypertension. J Am Coll Cardiol. 2013;62(25 Suppl):D92-9.
40. Mayer E, Klepetko W. Techniques and outcomes of pulmonary endarterectomy for chronic thromboembolic pulmonary hypertension. Proc Am Thorac Soc. 2006;3(7):589-93.
41. Nakazato K, Sugimoto K, Oikawa M, Takeishi Y. Balloon pulmonary angioplasty for chronic thromboembolic pulmonary hypertension:its history and development, and regional medical cooperation in Fukushima. Fukushima J Med Sci. 2023;69(3):167-76.
42. Kawakami T, Matsubara H, Shinke T, Abe K, Kohsaka S, Hosokawa K, et al. Balloon pulmonary angioplasty versus riociguat in inoperable chronic thromboembolic pulmonary hypertension (MR BPA): an open-label, randomised controlled trial. Lancet Respir Med. 2022;10(10):949-60.
43. Jais X, Brenot P, Bouvaist H, Jevnikar M, Canuet M, Chabanne C, et al. Balloon pulmonary angioplasty versus riociguat for the treatment of inoperable chronic thromboembolic pulmonary hypertension (RACE): a multicentre, phase 3, open-label, randomised controlled trial and ancillary follow-up study. Lancet Respir Med. 2022;10(10):961-71.
44. Brenot P, Jaïs X, Taniguchi Y, Carlos, Gerardin B, Mussot S, et al. French experience of balloon pulmonary angioplasty for chronic thromboembolic pulmonary hypertension. European Respiratory Journal. 2019;53(5):1802095.
45. Suruga K, Shimokawahara H, Miyagi A, Sugiyama Y, Suetomi T, Ogawa A, Matsubara H. Flow Grade-Based Success Rates, Complication Rates, and Balloon Pulmonary Angioplasty Patency for Total Occlusions. Canadian Journal of Cardiology. 2023.
46. Inami T, Kataoka M, Yanagisawa R, Ishiguro H, Shimura N, Fukuda K, et al. Long-Term Outcomes After Percutaneous Transluminal Pulmonary Angioplasty for Chronic Thromboembolic Pulmonary Hypertension. Circulation. 2016;134(24):2030-2.
47. Wiedenroth CB, Liebetrau C, Breithecker A, Guth S, Lautze H-JF, Ortmann E, et al. Combined pulmonary endarterectomy and balloon pulmonary angioplasty in patients with chronic thromboembolic pulmonary hypertension. The Journal of Heart and Lung Transplantation. 2016;35(5):591-6.
48. Araszkiewicz A, Darocha S, Pietrasik A, Pietura R, Jankiewicz S, Banaszkiewicz M, et al. Balloon pulmonary angioplasty for the treatment of residual or recurrent pulmonary hypertension after pulmonary endarterectomy. International Journal of Cardiology. 2019;278:232-7.
49. Shimura N, Kataoka M, Inami T, Yanagisawa R, Ishiguro H, Kawakami T, et al. Additional percutaneous transluminal pulmonary angioplasty for residual or recurrent pulmonary hypertension after pulmonary endarterectomy. Int J Cardiol. 2015;183:138-42.
50. Ghofrani HA, D‘Armini AM, Grimminger F, Hoeper MM, Jansa P, Kim NH, et al. Riociguat for the treatment of chronic thromboembolic pulmonary hypertension. N Engl J Med. 2013;369(4):319-29.
51. Sadushi-Kolici R, Jansa P, Kopec G, Torbicki A, Skoro-Sajer N, Campean IA, et al. Subcutaneous treprostinil for the treatment of severe non-operable chronic thromboembolic pulmonary hypertension (CTREPH): a double-blind, phase 3, randomised controlled trial. Lancet Respir Med. 2019;7(3):239-48.
52. Ghofrani H-A, Simonneau G, D‘Armini AM, Fedullo P, Howard LS, Jaïs X, et al. Macitentan for the treatment of inoperable chronic thromboembolic pulmonary hypertension (MERIT-1): results from the multicentre, phase 2, randomised, double-blind, placebo-controlled study. The Lancet Respiratory Medicine. 2024;12(4):e21-e30.
53. Nagel C, Nasereddin M, Benjamin N, Egenlauf B, Harutyunova S, Christina, et al. Supervised Exercise Training in Patients with Chronic Thromboembolic Pulmonary Hypertension as Early Follow-Up Treatment after Pulmonary Endarterectomy: A Prospective Cohort Study. Respiration. 2020;99(7):577-88.
54. Nagel C, Prange F, Guth S, Herb J, Ehlken N, Fischer C, et al. Exercise Training Improves Exercise Capacity and Quality of Life in Patients with Inoperable or Residual Chronic Thromboembolic Pulmonary Hypertension. PLoS ONE. 2012;7(7):e41603.
55. Guérin L, Couturaud F, Parent F, Revel M-P, Gillaizeau F, Planquette B, et al. Prevalence of chronic thromboembolic pulmonary hypertension after acute pulmonary embolism. Thrombosis and Haemostasis. 2014;112(09):598-605.
56. Barco S, Mavromanoli AC, Kreitner KF, Bunck AC, Gertz RJ, Ley S, et al. Preexisting Chronic Thromboembolic Pulmonary Hypertension in Acute Pulmonary Embolism. Chest. 2023;163(4):923-32.
57. Ende-Verhaar YM, Meijboom LJ, Kroft LJM, Beenen LFM, Boon G, Middeldorp S, et al. Usefulness of standard computed tomography pulmonary angiography performed for acute pulmonary embolism for identification of chronic thromboembolic pulmonary hypertension: results of the InShape III study. J Heart Lung Transplant. 2019;38(7):731-8.
58. Opitz I, Patella M, Lauk O, Inci I, Bettex D, Horisberger T, et al. Acute on Chronic Thromboembolic Pulmonary Hypertension: Case Series and Review of Management. Journal of Clinical Medicine. 2022;11(14):4224.
59. Klok FA, Barco S, Konstantinides SV, Dartevelle P, Fadel E, Jenkins D, et al. Determinants of diagnostic delay in chronic thromboembolic pulmonary hypertension: results from the European CTEPH Registry. European Respiratory Journal. 2018;52(6):1801687.
60. Delcroix M, Torbicki A, Gopalan D, Sitbon O, Klok FA, Lang I, et al. ERS statement on chronic thromboembolic pulmonary hypertension. European Respiratory Journal. 2021;57(6):2002828.
info@herz+gefäss
- Vol. 14
- Ausgabe 5
- November 2024