- Ausgewählte Studien aus der Hämato-Onkologie
Neoantigen T-Cell Receptor Gene Therapy in Pancreatic Cancer
Quelle: Rom Leidner et al. N Engl J Med 2022;386:2112-9
Zelluläre Therapien werden in grosser Zahl entwickelt, bisher vorwiegend für hämatologische Neoplasien, deshalb sei hier erlaubt etwas zum Pankreaskarzinom zu sagen. Wir haben uns soeben an die CAR-T Therapien gewöhnt, d.h. autologe T Lymphozyten des Patienten denen ein Gen eingeschleust wird welches einer Kombination aus einem T-Zell Rezeptor und einem Immunglobulin Gen (darum Chimär) besteht und eine bestimmte Struktur z.B. CD19 auf B Zellen angreift. Dies funktioniert für viele solide Tumoren nicht, weil diese keine Strukturen aufweisen, die eliminiert werden dürfen. Im N Engl J Med im Juni ist nun über einen Fall mit einer alternativen Strategie berichtet worden. Mutiertes K-Ras Protein spezifische T-Zell Rezeptor Gene wurden transfiziert (G12D). Dieser T Zell Rezeptor erkennt nur mutiertes Peptid, die Präsentation ist abhängig vom «richtigen» HLA Molekül, in diesem Fall HLA-C*08:02. K-RAS Mutationen sind häufig, (90% der Pankreaskarzinome), die G12D Mutation in 30%, HLA-C*08:02 in 8-11% je nach Ethnie. Ein gutes partielles Ansprechen nach Cyclophosphamide Tocilizumab Lymphodepletionstherapie und Interleukin-2 zur T-Zell Stimulation wurde in einer Patientin beobachtet. Dies war verbunden mit der Persistenz der transfizierten Zellen in der Zirkulation. Neben CAR-T Zellen und in vitro expandierten tumorinfiltierenden Lymphozyten werden möglicherweise genmodifizierte mutationsspezifische T-Zell Rezeptor T Zellen ein weiterer Baustein in der zellulären Immuntherapie werden.
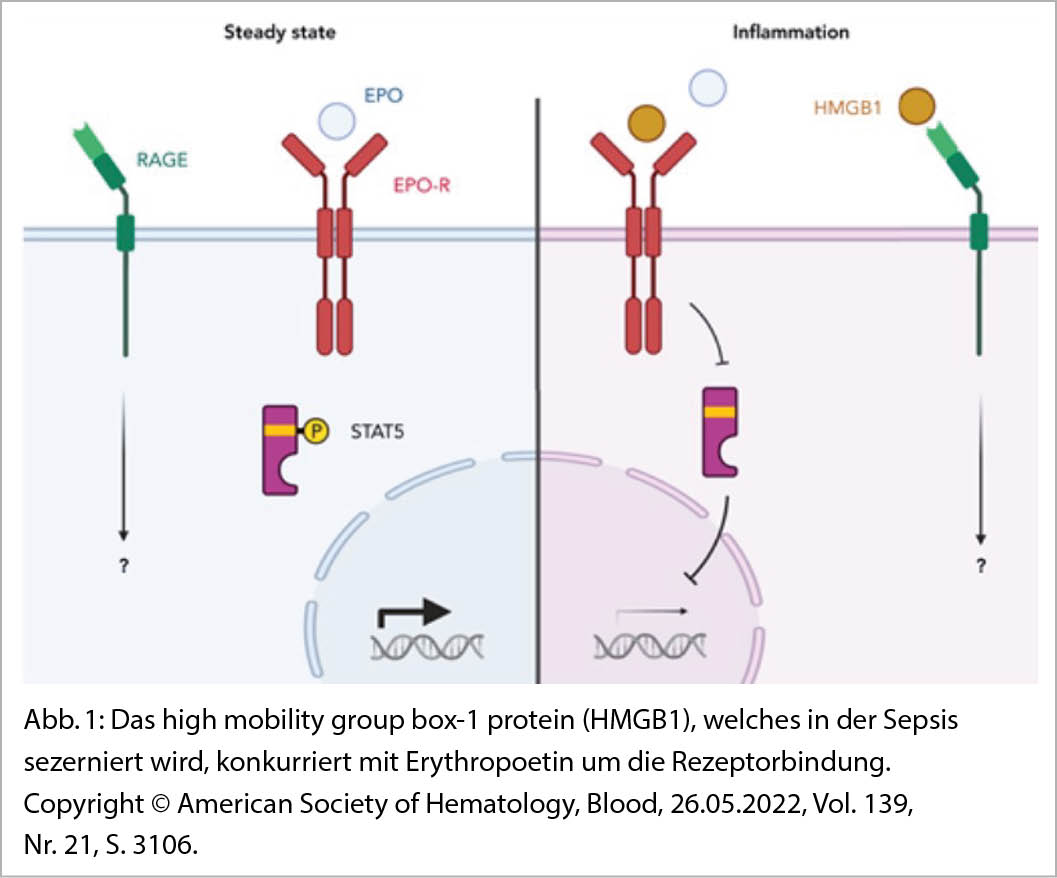
HMGB1-mediated restriction of EPO signaling contributes to anemia of inflammation
Quelle: Dulmovits BM, et al .Blood. 2022 May 26;139(21):3181-3193
Inflammatorische Anämie (Anämie der chronischen Krankheit) ist die zweithäufigste Anämieursache nach Eisenmangel, bei älteren Patienten wahrscheinlich die häufigste. Sie ist gekennzeichnet durch eine Sequestration von Eisen im RES, in den Darmepithelien und dadurch durch eine fehlende Verfügbarkeit von Eisen für die Erythropoese. Die dahinterliegenden Mechanismen sind in den letzten Jahren aufgeklärt worden und sind hauptsächlich durch die Sekretion von Hepcidin bedingt. Ein zweiter Mechanismus ist das ungenügende Ansprechen der Erythropoese auf Erythropoetin. Das Verstecken von Eisen vor den Krankheitserregern in infektiösen Zuständen hat seine gute Erklärung. Die Mechanismen hinter dem Erythropoetin refraktären Zustand waren bisher unklar.
In dieser Arbeit zeigen Dulmovits et al., dass das high mobility group box-1 protein (HMGB1), welches in der Sepsis sezerniert wird mit Erythropoetin um die Rezeptorbindung konkurriert (Abb. 1). Dies reduziert die STAT5 Phosphorylierung und somit die Erythropoetinwirkung. Weitere Mechanismen sind über RAGE den Rezeptor von HMGB1. In verschiedenen Tiermodellen haben die Autoren diese Mechanismen nachgebildet, so führt die Injektion von HMGB1 in Mäusen zu dem besagten Anämiebild.
Ivosidenib and Azacitidine in IDH1-Mutated Acute Myeloid Leukemia
Quelle: P Montesinos et al. N Engl J Med. 2022 Apr 21;386(16):1519-1531
Hypomethylierende Substanzen (HMA) sind zum Standard in der Behandlung von Patienten mit akuter myeloischer Leukämie (AML) geworden, die für eine intensive Chemotherapie nicht in Frage kommen. Da die Wirksamkeit beschränkt ist mit Raten an kompletten Remissionen im tieferen zweistelligen Bereich und seltenen langanhaltenden kompletten Remissionen werden Kombinationspartner gesucht, die synergistisch wirken. Vor kürzerem ist über die Kombination HMA mit dem bcl2 Inhibitor Venetoclax berichtet worden. Bei einem Teil der AML Patienten findet sich eine Mutation in der IDH1 der Isocitrate Dehydrogenase 1, ein onkometabolisches Protein dessen Funktion mit Ivosidenib gehemmt werden kann.
In dieser Phase III Studie wurden Patienten mit neu diagnostizierter AML und IDH1 Mutation zwischen der Kombination Azacytidine + Ivosidenib oder Azacytidine + Placebo randomisiert. Ivosidenib wurde oral kontinuierlich gegeben, Azacytidine s.c. alle 28d für 7 Tage.
Therapieversagen war definiert als Tod, Rezidiv oder fehlende komplette Remission nach 24 Wochen Behandlung. Randomisiert wurden 146 Patienten. Nach median 12.4 Monaten war die Hazard Ratio für Therapieversagen 0.33; (0.16 – 0.69; P = 0.002) für die Kombination.
Das Eventfreie Ueberleben zum Zeitpunkt 12 Monate war 37% vs. 12% in den Armen mit und ohne Ivosidenib und das Gesamtüberleben 24.0 versus 7.9 Monate. Febrile Neutropenien traten in 28% und 34% auf, Blutungen bei 41% und 29% und Infektionen bei 28% versus 49. Ein Differenzierungssyndrom wurde in 14% der mit Ivosidenib behandelten beobachtet versus 8% in der Plazebogruppe.
Die Schlussfolgerung ist, dass die Kombination von Ivosidenib + Azacytidine im Vergleich mit Azacytidine allein einen klaren klinischen Benefit bringt bei Patienten mit AML mit IDH1 Mutation.
Einordnung: HMA + Partner werden zunehmend zum Standard bei Patienten mit AML, die für eine intensive Chemotherapie nicht in Frage kommen. Welches der beste Partner oder die besten Partner sind wird sich in Zukunft weisen.
Measurable Residual Disease Response and Prognosis in Treatment-Naive Acute Myeloid Leukemia with Venetoclax and Azacitidine
Quelle: KW Pratz et al J Clin Oncol J Clin Oncol. 2022 Mar 10;40(8):855-865
Bei Patienten mit AML, die für eine intensive Chemotherapie nicht in Frage kommen, haben in einer randomisierten Studie die Kombination der hypomethylierenden Substanz (HMA) Azacytidine in Kombination mit dem bcl2 Inhbitior Venetoclax interessante Resultate ergeben (Azacitidine and Venetoclax in Previously Untreated Acute Myeloid Leukemia. N Engl J Med. 2020 Aug 13;383(7):617-629) mit Ansprechsraten von 66% vs. 28%.
Die Studie hier untersucht die Wertigkeit der gemessenen minimalen Resterkrankung (MRD) nach Therapie. MRD < 10-3 wurde als MRD Negativität definiert. Die verwendete Methode für die MRD war die Durchflusszytometrie. MRD wurde nach Zyklus 1 und dann alle 3 Zyklen gemessen in Patienten mit einem Ansprechen auf die Kombination von Azacytidine und Venetoclax. 164 Patienten wurden untersucht. MRD < 10-3 wurde bei 41% erreicht, 59% hatten MRD > 10-3. Das mediane Eventfreie Ueberleben war bei Patienten mit MRD < 10-3 nicht erreicht. Das eventfreie Ueberleben (EFS) war bei diesen Patienten nach 12 Monaten 83%, Das mediane EFS und Gesamtüberleben war bei diesen Patienten 11 und 19 Monate.
Schlussfolgerung: Patienten die unter Azacytidine und Venetoclax eine Remission mit tiefer MRD erreichen, können von längerer Remissionsdauer und Ueberleben profitieren.
Diese Studie bestätigt, dass tieferes Ansprechen für die Patienten einen Vorteil erbringt, im Vergleich zu weniger tiefem Ansprechen. Diese Erkenntnis ist nicht neu. Dass mit der Kombination Azacytidine und Venetoclax die tiefe MRD erreicht werden kann ist aber neu, insbesondere der erhebliche Prozentsatz der Patienten, die ein so tiefes Ansprechen auch ohne intensive Chemotherapie erreichen können.
Demethylation and Up-Regulation of an Oncogene after Hypomethylating Therapy
Quelle: Liu YC, et al. N Engl J Med. 2022 May 26;386(21):1998-2010
Die oben aufgeführten Artikel zeigen die Wertigkeit der hypomethylierenden Substanzen bei der AML, vor allem in Kombination hier mit dem BCL2 Inhibitor Venetoclax oder dem IDH1 Inhibitor Ivosidenib. Die Methylierung von Genen führt zu einer epigenetischen Modifikation welche zur Stilllegung der Gentranskription führen kann. Die Wirkung dieser Substanzen wird der De-Methylierung von Tumorsuppressorgenen zugeschrieben. Ob dies die hauptsächliche Wirkung dieser HMA ist, ist aber nicht letztlich klar, hingegen ist die Wirksamkeit dieser Substanzen bei myeloischen Neoplasien, insbesondere der akuten myeloischen Leukämie (AML) und dem Myelodysplastischen Syndrom (MDS) gut beschrieben. Theoretisch können aber durch diese Substanzen sowohl Tumorsuppressorgene demethyliert und somit aktiviert werden wie auch Onkogene.
Die Autoren untersuchen die Wirkung der HMA auf SALL4 einem bekannten Onkogen, das eine Rolle beim MDS und anderen Tumoren spielt. Knochenmarksproben wurden vor und nach HMA Behandlung bei MDS Patienten untersucht und die Assoziation zwischen SALL4 Expression und Behandlungserfolg beschrieben.
Auch wurden Leukämiezelllinien mit tiefer oder unmessbarer SALL4 Expression auf die Beziehung von SALL4 Methylierung und SALL4 Expression hin untersucht.
Die Autoren beschreiben eine SALL4 Aufregulierung in 40% bzw 30% der Patienten in 2 Kohorten und diese Aufregulierung war mit schlechtem Behandlungsresultat verbunden. Mittels einer Situsspezifischen Sonde wurde die Demethylierung in einer spezifischen Region beschrieben, welche für die SALL4 Expression wichtig war. Mittels dieser Technologie konnten die Autoren die Demethylierung und somit Aufregulierung einer Onkogenexpression nachweisen.
Klinik für Hämatologie
Hämatologische Diagnostik Labormedizin
Universitätsspital Basel und Blutspendezentrum beider Basel SRK
Petersgraben 4
4031 Basel
jakob.passweg@usb.ch