- Auswirkungen des Geschlechts auf die Pharmakokinetik und Pharmakodynamik
Geschlechtsspezifische Unterschiede in der Pharmakokinetik und Pharmakodynamik können die Arzneimittelwirkung erheblich beeinflussen. Frauen sind tendenziell höheren Arzneimittelkonzentrationen ausgesetzt als Männer, was zu einem höheren Risiko für unerwünschte Reaktionen führt. Der Artikel hebt diese Unterschiede hervor und unterstreicht die Bedeutung der Berücksichtigung von Geschlechtsunterschieden während der gesamten Arzneimittelentwicklung, der Marktüberwachung und in der klinischen Praxis, um die Sicherheit und Wirksamkeit von Arzneimitteln für alle Patienten zu verbessern.
Sex-related differences in pharmacokinetics and pharmacodynamics can significantly affect drug response. Women tend to be exposed to higher drug concentrations than men, leading to a higher risk of adverse reactions. The article highlights these differences and underscores the importance of considering sex and gender differences throughout drug development, post-market surveillance, and clinical practice to improve drug safety and efficacy for all patients.
Key words: Sex-specific pharmacokinetics, Gender differences in drug response, Adverse drug reactions, Clinical trial representation
Einleitung
Der Einfluss von Geschlecht und Gender im Bereich der Medizin, insbesondere im Zusammenhang mit der Behandlung mit Arzneimitteln, ist ein sehr aktuelles Thema. Der vorliegende Artikel befasst sich vor allem mit geschlechtsspezifischen Unterschieden bei der Reaktion auf medikamentöse Behandlungen.
Der Ursprung des Geschlechtsdimorphismus geht zurück bis zur Befruchtung und zur nachfolgenden Entwicklung eines Embryos, der die Geschlechtschromosomen XX oder XY trägt. In der Medizin werden Unterschiede in der Häufigkeit und Schwere bestimmter Erkrankungen auf diesen Dimorphismus zurückgeführt: Beispielsweise sind Autoimmunerkrankungen bei Frauen häufiger, während Gicht bei Männern häufiger auftritt. Die mit COVID-19 verbundene Morbidität und Mortalität ist bei Männern signifikant höher, was teilweise durch biologische Unterschiede zwischen den Geschlechtern erklärt wird (Modulation des Immunsystems und der Expression der ACE2-Rezeptoren, an die SARS-CoV-2 bindet, durch Sexualhormone) (1). Im Zusammenhang mit medikamentösen Behandlungen kann sich das Geschlecht auch auf die Pharmakokinetik (PK) und die Pharmakodynamik (PD) auswirken.
Geschlechtsspezifische Unterschiede bei der Pharmakokinetik
Es gibt zahlreiche anatomische, physiologische und biologische Unterschiede zwischen Männern und Frauen, die sich auf die PK auswirken können (Tab. 1).
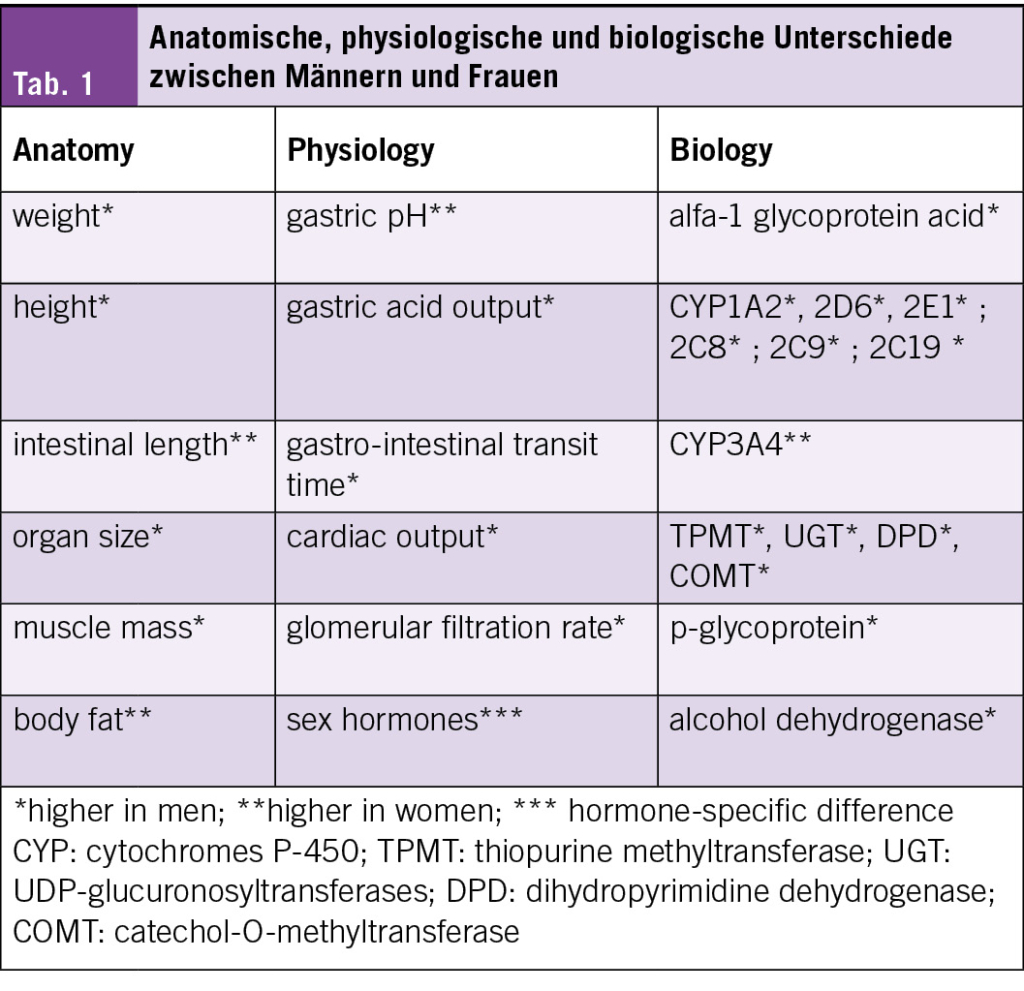
Der Einfluss des Geschlechts auf die verschiedenen PK-Parameter ist von den physikalisch-chemischen Eigenschaften und den Eliminationswegen des angewendeten Arzneimittels abhängig. Die schlussendliche Wirkung ist das Ergebnis der Einflüsse des Geschlechts auf die Phasen der Absorption, Verteilung, Verstoffwechselung und Ausscheidung des Wirkstoffs.
Die Magen-Darm-Passage ist bei Frauen langsamer, deshalb kann die Aufnahme bestimmter Wirkstoffe verzögert sein, wie z. B. beim NSAR Ketoprofen (2). Auch die aufgenommene Menge kann je nach Geschlecht variieren: Bei vorpubertären Mädchen und Jungen, bei denen es keine Unterschiede in den Eisenspeichern oder im Hämoglobinspiegel gab, war die Aufnahme von oral eingenommenem Eisen bei den Mädchen signifikant höher (3).
Im Vergleich zu Männern ist die Körperzusammensetzung von Frauen durch einen höheren Fettanteil und einen geringeren Wassergehalt gekennzeichnet. Bei lipophilen Substanzen wirkt Körperfett als Reservoir, und Wirkstoffe können bei Frauen eine verlängerte Eliminationshalbwertszeit aufweisen. Folglich ist auch die Zeit bis zum Erreichen des Steady State länger. Die maximale Plasmakonzentration von hydrophilen Wirkstoffen wiederum kann bei Frauen höher sein, da sich diese Arzneimittel in einem kleineren Volumen verteilen als bei Männern. Der Einfluss des Geschlechts auf die Verteilung ist jedoch begrenzt; er ist geringer als der Einfluss von Fettleibigkeit auf die Verteilung von lipophilen Wirkstoffen oder von fettfreier Körpermasse auf die Verteilung von hydrophilen Wirkstoffen.
Die Clearance (Metabolismus und Ausscheidung) ist der PK-Parameter, der am ausgeprägtesten durch das Geschlecht beeinflusst wird. Männer haben im Allgemeinen eine schnellere Clearance als Frauen, was auf die grösseren Ausscheidungsorgane (Leber, Nieren) und die unabhängig von der Grösse der Organe insgesamt höhere Enzymaktivität zurückzuführen ist. Da die Dosierungsempfehlungen für beide Geschlechter gleich sind und bis vor Kurzem auf PK-Studien basierten, die an Männern durchgeführt wurden, sind Frauen tendenziell systematisch überexponiert (4). Diese Überexposition ist in der Regel moderat, mit Konzentrationen von durchschnittlich +20 % im Vergleich zu Männern, was unter den interindividuellen Unterschieden bei einer moderaten Variabilität von rund 30 % liegt (5). Eine Ausnahme ist Zolpidem: Es wurde eine Exposition von +40–50 % bei Frauen festgestellt, was die FDA und Health Canada dazu veranlasste, die Dosierung bei Frauen ab 2013 zu halbieren (6, 7). Diese Empfehlung wurde von anderen Regulierungsbehörden, einschliesslich Swissmedic, nicht übernommen. Abgesehen davon wurde später in Frage gestellt, ob diese ungewöhnliche Entscheidung der FDA und von Health Canada sinnvoll war (8).
Geschlechtsspezifische Unterschiede bei der Pharmakodynamik
Es gibt auch bezüglich der PD Unterschiede zwischen den Geschlechtern, auch wenn diese weniger gut dokumentiert sind als PK-Unterschiede, da sie wahrscheinlich schwieriger zu untersuchen sind. In einer Studie wurde die maximale Wirksamkeit von Vasopressin (antidiuretisches Hormon) bei niedrigeren Konzentrationen bei Frauen als bei Männern beobachtet, und Hyponatriämie trat bei Frauen häufiger auf (9). Die Unterdrückung der Cortisolsekretion trat bei Frauen bei niedrigeren Konzentrationen von Methylprednisolon auf als bei Männern (10). Bei gesunden Freiwilligen führte Chinidin bei gleichen Konzentrationen zu einer stärkeren QT-Verlängerung bei Frauen als bei Männern (11).
Zusammenfassung
Das Geschlecht hat einen Einfluss auf das Ansprechen auf Arzneimittel, ist aber nur einer von mehreren Faktoren, und die PK-Variabilität innerhalb einer Population gleichen Geschlechts ist grösser als die PK-Variabilität zwischen den Geschlechtern. Viele Faktoren sind für die interindividuelle PK-Variabilität verantwortlich. Die wichtigsten sind die Nierenfunktion und die Leberfunktion, die bei der Verschreibung konsequent berücksichtigt werden müssen.
Dennoch sind Frauen im Vergleich zu Männern tendenziell höheren Wirkstoffkonzentrationen ausgesetzt. Obwohl diese Überexposition insgesamt moderat ist, ist sie wegen der systematischen Ausprägung problematisch und zumindest teilweise für die beobachtete signifikante Übervertretung von Frauen bei unerwünschten Arzneimittelwirkungen verantwortlich, da alle unerwünschten Wirkungen – in unterschiedlichem Ausmass – konzentrationsabhängig sind. Eine Studie über die Sicherheit neuer Arzneimittel ergab, dass bei Frauen im Vergleich zu Männern 60 % mehr unerwünschte Wirkungen auftraten (12). In einer Studie zu verschiedenen Klassen von onkologischen Behandlungen waren Frauen von schweren unerwünschten Wirkungen um 34 % häufiger betroffen, wobei die überproportionale Vertretung bei Immuntherapien sogar 49 % erreichte (13). Schliesslich entzog die FDA zwischen 1997 und 2000 zehn Arzneimitteln aus Sicherheitsgründen die Zulassung, wobei acht dieser zehn Arzneimittel mit signifikant höheren Risiken für Frauen in Verbindung gebracht worden waren (14). Neben der Überexposition können auch andere, eher genderspezifische Faktoren zu den häufigeren unerwünschten Wirkungen bei Frauen beitragen. Dazu gehören Unterschiede in der Empfindlichkeit gegenüber unerwünschten Wirkungen (PD-Unterschiede), die Exposition gegenüber einer grösseren Anzahl von Arzneimitteln und eine grössere Bereitschaft zur Meldung von unerwünschten Wirkungen bei Frauen als bei Männern (15, 16, 17).
Lange Zeit beruhte die Entwicklung von Arzneimitteln, insbesondere in den frühen Phasen, auf männlichen Versuchspersonen, hauptsächlich wegen allfälligen teratogenen Wirkungen. Auch wenn die Beteiligung von Frauen an klinischen Studien in den letzten zwei Jahrzehnten allmählich zugenommen hat, sind Frauen in den Phasen I und II immer noch in der Minderheit. Dasselbe gilt für präklinische Studien, die immer noch überwiegend mit männlichen Tieren durchgeführt werden (5). Eine bessere Repräsentation während der gesamten Arzneimittelentwicklung sowie die Analyse von Daten in geschlechtsspezifischen Untergruppen sollten zu einer besseren Beschreibung der PK/PD von Arzneimitteln bei Frauen führen, namentlich zu einer Verringerung der Verzerrung bei der Dosisfindung, und somit zur Markteinführung neuer Arzneimittel, die für die Patientengruppe der Frauen insgesamt besser geeignet und sicherer sind.
Nach der Marktzulassung ist es weiterhin wichtig, geschlechts- und genderspezifische Überlegungen zu berücksichtigen, insbesondere bei Phase-IV-Studien und in der Pharmakovigilanz, aber auch in der täglchen klinischen Praxis.
Erstpublikation
Der Originalartikel «Auswirkungen des Geschlechts auf die Pharmakokinetik und Pharmakodynamik», von Françoise Livio und Frédérique Rodieux, wurde in den «Swissmedic Vigilance-News», Edition 33 vom 25.11.2024, veröffentlicht.
Abteilung Klinische Pharmakologie, Departement für Medizin,
Centre Hospitalier Universitaire Vaudois (CHUV),
Rue du Bugnon 46
1005 Lausanne
Abteilung Arzneimittelsicherheit, Swissmedic,
Hallerstrasse 7
3012 Bern
Die Autorinnen haben keine Interessenkonflikte im Zusammenhang zu diesem Artikel deklariert.
1. Ya’qoub L, Elgendy IY, Pepine CJ. Sex and gender differences in COVID-19: More to be learned! Am Heart J Plus 2021;3:100011. doi: 10.1016/j.ahjo.2021.100011.
2. Magallanes L, Lorier M, Ibarra M, et al. Sex and food influence on intestinal absorption of ketoprofen gastroresistant formulation. Clin Pharmacol Drug Dev 2016;5(3):196-200. doi: 10.1002/cpdd.208.
3. Woodhead JC, Drulis JM, Nelson SE, et al. Gender-related differences in iron absorption by preadolescent children. Pediatr Res 1991;29(5):435-9. doi: 10.1203/00006450-199105010-00005.
4. Stader F, Marzolini C. Sex-related pharmacokinetic differences with aging. Eur Geriatr Med 2022;13(3):559-565. doi: 10.1007/s41999-021-00587-0.
5. Dekker MJHJ, de Vries ST, Versantvoort CHM, et al. Sex proportionality in pre-clinical and clinical trials: an evaluation of 22 marketing authorization application dossiers submitted to the European Medicines Agency. Front Med (Lausanne). 2021 Mar 11;8:643028. doi: 10.3389/fmed.2021.643028.
6. Greenblatt DJ, Harmatz JS, Singh NN, et al. Gender differences in pharmacokinetics and pharmacodynamics of zolpidem following sublingual administration. J Clin Pharmacol 2014;54(3):282-90. doi: 10.1002/jcph.220.
7. https://www.fda.gov/files/drugs/published/Drug-Safety-Communication–Risk-of-next-morning-impairment-after-use-of-insomnia-drugs–FDA-requires-lower-recommended-doses-for-certain-drugs-containing-zolpidem-%28Ambien–Ambien-CR–Edluar–and-Zolpimist%29.pdf (zuletzt aufgerufen am 04.09.2024).
8. Greenblatt DJ, Harmatz JS, Roth T. Zolpidem and gender: are women really at risk? J Clin Psychopharmacol 2019;39(3):189-199. doi: 10.1097/JCP.0000000000001026.
9. Juul KV, Klein BM, Sandström R, et al. Gender difference in antidiuretic response to desmopressin. Am J Physiol Renal Physiol 2011;300(5):F1116-22. doi: 10.1152/ajprenal.00741.2010.
10. Lew KH, Ludwig EA, Milad MA, et al. Gender-based effects on methylprednisolone pharmacokinetics and pharmacodynamics. Clin Pharmacol Ther 1993;54(4):402-14. doi: 10.1038/clpt.1993.167.
11. El-Eraky H, Thomas SH. Effects of sex on the pharmacokinetic and pharmacodynamic properties of quinidine. Br J Clin Pharmacol 2003;56(2):198-204. doi: 10.1046/j.1365-2125.2003.01865.x.
12. Martin RM, Biswas PN, Freemantle SN, et al. Age and sex distribution of suspected adverse drug reactions to newly marketed drugs in general practice in England: analysis of 48 cohort studies. Br J Clin Pharmacol 1998;46(5):505-11. doi: 10.1046/j.1365-2125.1998.00817.x.
13. Unger JM, Vaidya R, Albain KS, et al. Sex differences in risk of severe adverse events in patients receiving immunotherapy, targeted therapy, or chemotherapy in cancer clinical trials. J Clin Oncol 2022 May 1;40(13):1474-1486. doi: 10.1200/JCO.21.02377.
14. Heinrich J. Drug safety : most drugs withdrawn in recent years had greater health risks for women. United States general accounting office 2001. https://digital.library.unt.edu/ark:/67531/metadc297960/m1/3/ (zuletzt aufgerufen am 04.09.2024).
15. Sportiello L, Capuano A. Sex and gender differences and pharmacovigilance: a knot still to be untied. Front Pharmacol 2024;15:1397291. doi: 10.3389/fphar.2024.1397291.
16. Holm L, Ekman E, Jorsäter Blomgren K. Influence of age, sex and seriousness on reporting of adverse drug reactions in Sweden. Pharmacoepidemiol Drug Saf 2017;26(3):335-343. doi: 10.1002/pds.4155. Epub 2017 Jan 10. PMID: 28071845.
17. Watson S, Caster O, Rochon PA, et al. Reported adverse drug reactions in women and men: Aggregated evidence from globally collected individual case reports during half a century. EClinicalMedicine 2019;17:100188. doi: 10.1016/j.eclinm.2019.10.001.
info@onco-suisse
- Vol. 15
- Ausgabe 1
- März 2025






