- Ein Überblick über einige solide Tumore
Die WHO meldet erstmals eine Abnahme der Tabak-Raucher weltweit!
Eine erfreuliche Mitteilung kam auf Weihnachten von der WHO und lautet: «For the first time, the number of men using tobacco is on the decline, indicating a powerful shift in the global tobacco epidemic. By 2020, WHO projects there will be 10 million fewer tobacco users worldwide, than in 2018. The findings demonstrate how government-led action can protect communities from tobacco and save lives».
Es scheint, dass nach weit mehr als einem halben Jahrhundert auch politisch breit akzeptierter Evidenz der extrem hohen globalen Mortalität durch Tabakrauchen (> fast 8 Mio. Todesfälle/Jahr) erstmals ein positiver globaler Trend der Abnahme der Anzahl Raucher weltweit zu vermelden ist, dessen effektiv Mortalitätsreduzierende Wirkung erst noch abgewartet werden muss. Dabei sei festzuhalten, dass die Schweiz leider keine gute Figur abgibt, insbesondere auch bei der hohen Prävalenz der Raucherinnen. Insgesamt ist die Anzahl aller Raucher bei uns doppelt so hoch wie in Australien, Kalifornien oder Hawaii! Die an sich sehr einfache Präventionspolitik wird vom Parlament weiterhin hart geblockt zum grossen Nachteil der Bevölkerung – die Zigaretten kosten in den erfolgreichen Ländern z.T. ein Mehrfaches im Vergleich zu Schweiz. So ist es nicht erstaunlich, dass die Medienmitteilung festhält: «Europe is the region making the slowest progress in reducing tobacco use among females».
Pembrolizumab beim lokal fortgeschrittenen NSCLC: 5 Jahres OS Daten
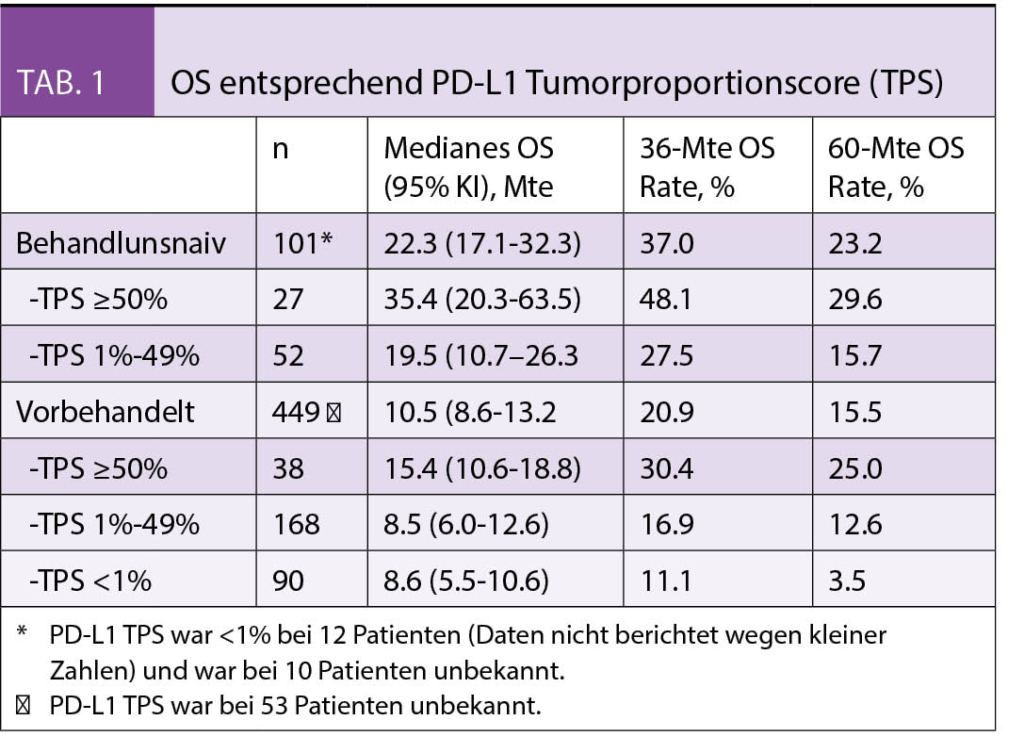
Beim Lungenkrebs konnte im Follow-up der KEYNOTE-001 Studie mit 550 Patienten (449 vorbehandelt, 101 als Firstline-Therapie) gezeigt werden, dass die 5-Jahres-Mortalität von Patienten mit lokal fortgeschrittenem nicht-kleinzelligem Lungenkrebs (NSCLC) (1) nach im Median 60,6 Monaten, also nach etwas über 5 Jahren, 100 (18%) der insgesamt 550 aufgenommenen Patienten noch am Leben waren. Unter denjenigen, die vor Studieneinschluss bereits eine oder mehrere erfolglose Chemotherapien erhalten hatten, waren es 15,5%; unter denjenigen, die Pembrolizumab als Firstline-Therapie erhielten, 23%. Im Vergleich zu historischen Kontrollen beim fortgeschrittenen Lungenkrebs ohne Immuntherapie erwarten wir eine 5-Jahres-Überlebensrate um die 5%.
Von den nicht-vorbehandelten Patienten mit einer PD-L1-Expression von mindestens 50% war fast ein Drittel (29,6%) nach 5 Jahren noch am Leben, unter denjenigen mit einer niedrigeren PD-L1-Expression (zwischen 1 und 49%) waren es immerhin noch 15,7%.
Unter den vorbehandelten Patienten betrugen die entsprechenden 5-Jahres-Überlebensraten 25% (PD-L1-Expression 50% oder höher) bzw. 12,6% (PD-L1-Expression unter 50%). Von denjenigen, bei denen die PD-L1-Expression unter 1% lag, überlebten nur noch 3,5% mindestens 5 Jahre. Von den Respondern hatten insgesamt 60 Patienten Pembrolizumab für mindestens 2 Jahre erhalten. Von diesen waren zum Zeitpunkt der aktuellen Auswertung noch 46 am Leben. Das heisst: 3 von 4 dieser Patienten überlebten auch die 5-Jahresmarke.
Immuntoxische Effekte durch die Therapie erlebten 17% der Behandelten. Am häufigsten war dabei eine Hypothyreose mit einer Inzidenz von 8 bis 9%, die aber fast immer als Grad 1/2 bewertet wurde. Die gefährlichste war die Pneumonitis, mit einer Inzidenz von rund 4%, wobei die Hälfte dieser Ereignisse als schwer (Grad 3 bis 5) eingestuft wurde.
Es wird also zentral sein, zukünftig die Patientenselektion weiter zu optimieren und die Wirksamkeit weiter zu verbessern z.B. durch Kombinationen mit weiteren Immuntherapeutika oder Chemotherapeutika und klugen Therapiesequenzen bzw. Erhaltungstherapien (Tab. 1).
Lurbinectin (Zepsyre®): ein neues Medikament für SCLC in Sicht
Lurbinectdin ist ein semi-synthetisches Analog von Trabectidine (Yondelis), also einem Abkömmling aus einer Seescheide aus der Tiefe des Meeres, eine Spezialität von Pharmamar. Lurbinectdin hemmt die RNA-Polymerase II und führt damit zu DNA Doppel Strang Brüchen mit anschliessender Apoptose. Ein Synergismus mit Anthrazyklinen wird postuliert.
In einer multizentrischen einarmigen Basket Studie wurden 105 vorbehandelte Patienten mit SCLC eingeschlossen (2). Die Patienten erhielten 3.2 mg/m2 Lurbinectdin als 1-h iv Infusion alle 3 Wochen. Grad 3-4 Toxizität wurde in 35% der Patienten registriert und bestand hauptsächlich aus Neutropenie (22.9%), Anämie (6.7%), Fatigue (6.7%), Thrombozytopenie (4.8%), febriler Neutropenie (4.8%), und Pneumonie (1.9%). Die Ansprechrate betrug 35.2% (37/105) und ebenso bemerkenswert war, dass weitere 35 Patienten eine SD (stable disease) aufwiesen, so dass die Krankheits-Kontrollrate erstaunlich hohe 68.6.% betrug. Eine Tumorregression wurde bei 65% der Patienten dokumentiert und 5 von 8 Patienten, welche auf eine Immuntherapie refraktär waren, haben angesprochen. Die mediane Dauer des Ansprechens betrug 5.8 Monate. Patienten, welche auf die vorgängige Therapie gut angesprochen hatten, zeigten eine Ansprechrate von 44% versus 22% für refraktäre Patienten. Nach einer medianen Beobachtungsdauer von 17.1 Monaten betrug das mediane OS 9.3 Monate und das 1. Jahres OS betrug 34.2%. Für die auf eine vorgängige Therapie ansprechende Patienten betrug das OS 11.9 Monate versus 5.0 Monate für primär resistente Patienten.
Eine grosse Phase 3 Zulassungs-Studie (3) («Atlantis» N:600) von Lurbinectdin mit Doxorubicin versus Standardtherapie sollte Mitte 2019 die nötige Fallzahl erreicht haben und nun in die finale Auswertung für 2020 gehen. Auf Grund der positiven Daten der Basket Studie aber wurde Lurbinectine (Zepsyre®, PM1183) im beschleunigten Zulassungverfahren bei der FDA im Dezember 2019 in das Zulassungsverfahren aufgenommen mit der Indikation als Zweitlinientherapie. Nun endlich nach > 20 Jahren ist wieder ein klar aktives vielversprechendes Medikament beim Kleinzeller am Horizont.
Ovarialkarzinom und die PARP-Inhibitoren in der Erhaltungstherapie
PARP-Inhibitoren wurden ursprünglich für die Behandlung von Patientinnen mit BRCA1/2-Mutationen entwickelt. Sie hemmen das Enzym Poly-ADP-Ribose-Polymerase (PARP), das Zellen bei der Reparatur von Mutationen in der DNA benötigen. Bei einem Defekt dieser DNA-Reparatur bei Patienten mit einer BRCA1/2-Mutationen können nur noch die intakten Zellen die Defekte einer homologen Rekombination (HRD) korrigieren.
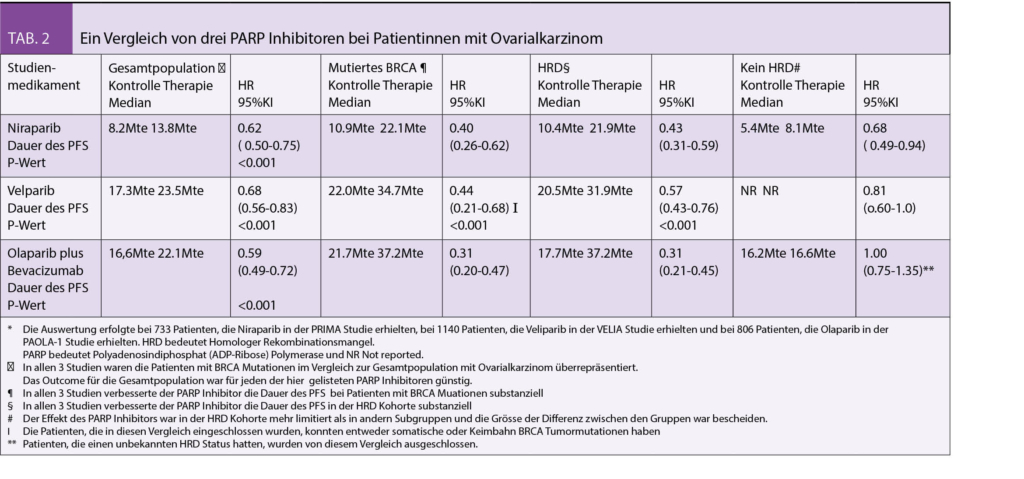
Im Dezember 2019 sind nun gleichzeitig 3 Originalpublikationen im NEJM zur Therapie der PARP-Inhibitoren bei Ovarialkarzinom erschienen (4-6). Es handelt sich um drei grosse randomisierte internationale Phase 3 Studien mit drei verschiedenen PARP-Inhibitoren: Niraprib (PRIMA-Studie), Velaparib (VELIA-Studie) und Olaparib (PAOLA-1-Studie), alle untersucht in der Indikation als Erhaltungstherapie nach erfolgreicher postoperativer 1. Linien Induktion durch ein Platin-Taxan Doublet z.T. auch mit Bevacizumab. Generell dazu ist zu bemerken, dass in der PAOLA-1 Studie Olaparib mit Bevacizumab versus Placebo mit Bevacizumab verglichen wurde und auch die Inklusionskriterien in den drei Studien differieren. Dies erklärt im Wesentlichen auch die moderaten Unterschiede in den Resultaten. Dabei fällt auf, dass diese Resultate für vergleichbare Populationen hinuntergebrochen für alle drei Substanzen dann doch wieder sehr ähnlich ausfallen. Die Zeit bis zu einem Rückfall wird durch die neuen Erhaltungstherapien mit den untersuchten drei PARP-Inhibitoren bei HDR mutierten Patientinnen ca. verdoppelt. Allerdings wurde eine lebensverlängernde Wirkung bisher für keinen der 3 untersuchten PARP-Inhibitoren nachgewiesen, bei allerdings noch zu kurzer gesamter Beobachtungszeit. Die besten Resultate ergaben sich erwartungsgemäss für BRCA1/2 mutierte Patientinnen und für die Patientinnen mit serösen und endometrialen Ovarialkarzinomen jedoch nicht bei Patientinnen mit muzinösen Ovarialkarzinomen. Neben den BRCA1/2-Mutationen gibt es ja noch weitere Störungen der homologen DNA-Rekombination (HRD), auf die heute im Tumorgewebe getestet werden kann wie hier in diesen Studien. Dabei konnte gezeigt werden, dass auch diese Patientinnen profitieren im Gegensatz zu den Patientinnen ohne nachweisebaren HRD-Defekt, die kaum oder gar nicht profitierten. Die Tabelle 2 aus dem begleitenden ausführlichen Editorial im NEJM (7) fasst die Resultate übersichtlich zusammen.
Entrectinib für Kinder mit ZNS-Malignomen und der Pediatric Match Trial
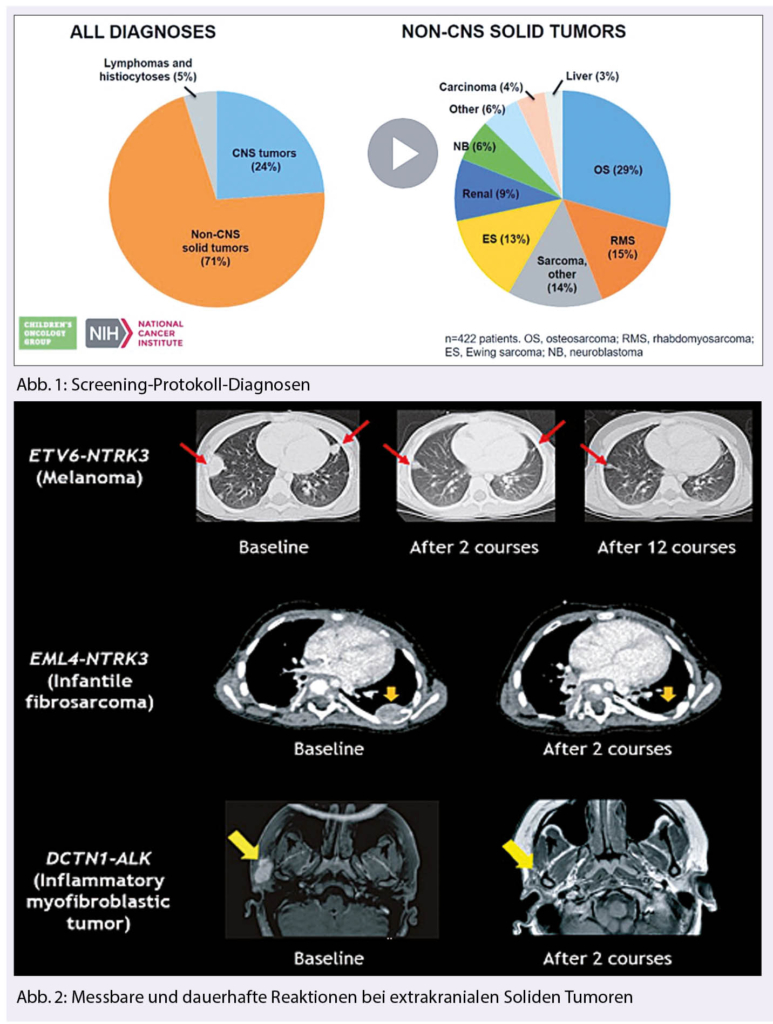
Entrectinib ist ein ZNS-gängiger oraler TrkA/B/C, ROS1 und ALK Tyrosinekinase Inhibitor. Die Wichtigkeit der Identifikation von medikamentös beeinflussbaren molekularen Zielstrukturen im pädiatrischen Setting wird durch diesen NCI-COG-Match Trial mit Entrectinib demonstriert. In dieser Studie (8) mit 29 Patienten (5 Monate bis 20 Jahre alt) mit refraktären Soliden Tumoren oder CNS-Malignomen wurde Entrectinib untersucht. Entrectinib wurde dabei generell gut toleriert: Dosis-limitierend waren erhöhtes Kreatinin, Dysgeusie, Fatigue und Lungenödem. Die empfohlene tägliche Dosisbetrug 550 mg/m2. Alle Responders hatten eine Tagesdosis ≥ 400 mg/m2. Alle 11 Kinder und Adoleszenten mit einer NTRK1/2/3, ROS1 oder ALK Fusion sowie ein Fall von Neuroblastom mit einer ALK-Mutation zeigten ein Ansprechen! Patienten ohne Nachweis des Targets von Entrectinib zeigten kein Ansprechen.
Von den 6 Patienten mit dem Entrectinib-Target und Solidem Tumor wurden eine CR und 5 PRs dokumentiert. Bei den 6 Patienten mit ZNS-Malignomen zeigte ebenfalls einer eine CR, 3 zeigten eine PR, ein Patient eine 2PR unconfirmed und bei einem Patienten ist es noch zu früh für die Response-Evaluation. Die Zeit bis zum Ansprechen betrug median 57 Tage. Entrectinib ist bei dieser Zielpopulation ein sehr wirksamer neuer Tyrosinkinase-Inhibitor, der nun prioritär weiter untersucht werden muss.
Diese Studie zeigt auch, dass das Finden von therapeutisch beeinflussbaren molekularen Zielstrukturen ein Königsweg ist, um bei seltenen Malignomen wie in der Pädiatrie Fortschritte zu erzielen- Genau dies beabsichtigt die NCI-COG-Pediatric Match Trial der Childrens Oncology Group des NCI. Hier wurden in einem kurzen Zeitraum von 17 Monaten 422 Kinder mit Soliden Tumoren (71%) und ZNS-Tumoren in 24% sowie 6% mit Lymphomen und Histiozytären Malignomen untersucht (9). Es standen 10 zielspezifische Behandlungsarme zur Verfügung. Von den Kindern unter 12 Jahren konnten 35% einem Behandlungsarm zugewiesen werden, von den Kindern > 12 Jahre 25%. Dabei fanden sich HRAS/KRAS/NRAS Mutationen (n = 16), BRAF Mutationen oder Fusionen (n = 14), oder NF1 Mutationen (n = 11). Andere Gene betrafen SMARCB1 (n = 14), ALK (n = 8), CDK4 (n = 8), PIK3CA (n = 7), PTEN (n = 7), FGFR1 (n = 5), und BRCA1/BRCA2 (n = 5).
Insgesamt konnte somit in gut einem Viertel der Kinder eine behandelbare molekulare Zielstruktur gefunden werden und es wird sich im weiteren Verlauf zeigen inwieweit diese Strategie der Personalisierten Onkologie in der Pädiatrie das klinische Ansprechen insgesamt beeinflussen wird.
Ausblick
Die CAR-T-Welt wendet sich zunehmend auch klassischen Targets für Solide Tumore zu wie z.B. EGFR und HER2. Auch wenn der Weg zum klinischen Erfolg hier holpriger sein mag als für die hämatologischen Malignome dürfen wir hoffnungsvoll gespannt sein auf diese weitere Entwicklung.
Mit der CRISPER-CAS9 Technologie wird in hunderten von Tumormodellen von vielen verschiedenen Tumorarten erfolgreich nach neuen Wachstum-steuernden Genen und neuen tumorassoziierten Fusionsgenen gesucht mit erstaunlichem Erfolg. Diese neu entdeckten Zielstrukturen bilden einen sehr wertvollen erweiterten Thesaurus für die Pipelines der innovativen therapeutischen Substanzen und diagnostischen Biomarker der nahen Zukunft. An vielen Fronten laufen Studien mit «liquid biopsies» zur Frühdiagnostik, zur Therapiestratifikation und zur Evaluation von Therapieverläufen.
Im Bereich der präventiven Onkologie wird auch in Europa das low dose CT-Screening von entsprechend definierten Rauchergruppen ebenso wie das HPV inkludierende moderne Cervix-Karzinom Screening vermehrt die politische mediale Ebene erreichen.
Auch im Bereich der Zugangsgerechtigkeit und der Preismodelle für innovative Medikamente und Therapieverfahren werden wir auf nationaler und internationaler Ebene harte politische Diskussionen erwarten dürfen. Es scheint eine kritische Schwelle der Akzeptanz auch in den reichsten Ländern überschritten zu sein. Das jetzt eine Ärztin die EU führt sollte mehr als ein Hoffnungsschimmer für eine patientenorientierte Diskussion sein.
Rosengartenstrasse 1d
9000 St. Gallen
thomas.cerny@kssg.ch
1. Garon EB et al. Five year long-term overall survival for patients with advanced NSCLC treated with pembrolizumab: results from KEYNOTE-001. J Clin Oncol 2019;37: (suppl abstract LBA9015)
2. Trigo JM et al. Efficacy and safety of lubrinectedin (PM1183, ZEPSYRE®) in small cell lung cancer (SCLC): results from a phase 2 study
3. Paz-Ares LG et al. Efficacy and safety profile of lurbinectedin in second-line SCLC patients: Results from a phase II single-agent trial. J Clin Oncol 2019;37 (suppl abstract 8505)
4. Gonzalez-Martin A et al Niraparib in patient with newly diagnosed advanced ovarian cancer. New Engl J Med. 2019; 381: 2391-2402
5. Coleman RL et al Veliparib with first-line chemotherapy and as maintenance therapy in ovarian cancer. New Engl J Med 2019;381:2403-2415
6. Ray-Coquard I et al. Olaparib plus Bevacizumab as first-line maintenance in ovarian cancer. N Engl J Med 2019; 381:2416-2428
7. Longo DL. Personalized medicine for primary treatment of serous ovarian cancer. NEJM 2019; 2471-74)
8. Robinson GW et al. Phase 1/1B trial to assess the activity of entrectinib un children and adolsecents with recurrent of refractory solid tumors including central nervous system J Clin. Oncol. 2019, 37; (Suppl. Abstracts 10009)
9. Parsons DW et al Identification of targetable molecular alterations in the NCI-COG pediatric MATCH trial .J Clin. Oncol. 2019, 37; (Suppl. Abstracts 10011)
info@onco-suisse
- Vol. 10
- Ausgabe 1
- Februar 2020