- Fünfzehn Jahre NPlate® (Romiplostim)
In seiner Einführung erinnerte er an das Launch-Symposium an der Charité vor 15 Jahren, anlässlich welcher Professor Matzdorff Rudolf Virchow zitierte, der sagte «es wird ja fleissig gearbeitet und viel mikroskopiert, aber es müsste wieder mal einer einen gescheiten Gedanken haben». Die Leute bei Amgen hatten den gescheiten Gedanken, wie der Referent feststellte. Nachdem die Stimulation der Thrombozyten mit dem endogenen Thrombopoetin (TPO) versagt hatte, hatten sie ein «Peptibody» biotechnisch hergestellt, mit zwei Domänen, einer Peptid-Thrombopoetin-Rezeptor-Bindungsdomäne, die die biologische Aktivität vermittelt, aber keine Sequenzhomologie zum endogenen TPO aufweist und somit keine Antikörper dagegen stimuliert und einer Antikörper-Fc-Domäne, die die Halbwertszeit im Blut verlängert. Die Wirkung dieses Peptibodys, der Romiplostim genannt wurde, entspricht dem endogenen Thrombopoetin; es stimuliert die Thrombopoese und bewirkt einen dosisabhängigen Anstieg der peripheren Thrombozyten.
Der Referent erinnerte an die Therapielandschaft 2009/2010. Die damalige Standardtherapie bestand aus Steroiden und bei starker Blutung i.v. Immunglobulinen, ev. Thrombozytenkonzentraten in der ersten Linie, in der zweiten Linie Azathiopirin, Vinca- Alkaloiden oder Splenektomie, dann TRA (Thrombopoetin-Rezeptor -Agonist), Rituximab, oder wie bisher und in der dritten Linie gleich wie in der 2. Linie ohne Splenektomie. In der post 3. Linie Anti D, Cyclophosphamid, Cyclosporin, Mycophenolat-Mofetil, Danazol, Dapson, Alemtuzumab, Kombinationschemotherapie und Stammzelltransplantation.
Immunthrombozytopenie
Romiplostim – Von der Markteinführung bis zum heutigen Behandlungsalltag
Die ITP ist definiert als Blutplättchenverminderung unter 100 Gpt/l. Die Inzidenz ist in Europa 1.6 bis 3.9 pro 100’000, die Prävalenz 16-20 pro 100’000. In Deutschland gibt es ca. 16’000 bis 20’000 ITP-Patienten, davon ist etwa die Hälfte unter regelmässiger Therapie, so Dr. med. Thomas Stauch, Jena. Es gibt zwei Altersspitzen: in jüngerem Alter sind die Frauen etwas häufiger, und in höherem Alter (ca. ab 65J) sind es eher die Männer, die an einer ITP leiden.
Pathophysiologie
Die Thrombozyten (Blutplättchen) stammen aus den Megakaryozyten, die im Knochenmark gebildet werden. An diese binden sich fälschlicherweise Antikörper (meistens als Folge einer Infektion). Man nennt dies molekulare Mimikry. Die Ähnlichkeit von Peptidsequenzen von Pathogenen und eigenem Gewebe führt zu einer Aktivierung autoreaktiver B- und T-Zellen, die dann Antikörper gegen körpereigene Strukturen, wie die Thrombozyten, bilden. Dabei zeigen bereits die Megakaryozyten eine gestörte Reifung und eine reduzierte Thrombozytenbildung. Die Antikörper-beladenen Thrombozyten werden als fehlerhaft erkannt und von den Makrophagen verspeist und abgebaut.
Die ITP ist primär eine Erkrankung mit Blutungszeichen. Aus Registerdaten von 302 Patienten geht hervor, dass 58 % Blutungszeichen hatten, 30 % mukosale Blutungen und 7 % schwere Blutungen. Der beste Thrombozyten-Schwellenwert ist 20 Gpt/l für jegliche Blutungen. Schwere Blutungen treten unabhängig vom Schwellenwert auf, was die Therapieentscheidung schwierig macht. Die Lebensqualität dieser Patienten ist eingeschränkt, was oft unterschätzt wird, und es gibt eine erhöhte Mortalität durch kardiovaskuläre Erkrankungen (HR 1.5), Infektionen (HR 2.4), Blutungen (HR 6.2) und hämatologische Malignome (HR 5.7).
Steroide sind immer noch das Mittel der Wahl bei der Erstlinientherapie. Bei schweren Blutungen Steroide in Kombination mit Immunglobulinen. Die langanhaltenden Remissionen liegen unter dieser Therapie bei 30 bis 40 %, d.h. zwei Drittel der Patienten haben eine Erkrankung, die wir weiter behandeln müssen. Damals hat man ziemlich heroisch Immunsuppressiva gegeben. Die Steroide haben verschiedene Nebenwirkungen wie etwa Osteoporose, Gewichtszunahme, Infektionen, so dass heute der internationale Konsens ist, dass die Erstlinientherapie mit Glukokortikoiden nur während 6-8 Wochen gegeben werden darf. Dann soll rasch zur Zweitlinientherapie übergeleitet werden. Hier hat sich in den letzten Jahren viel getan. Da sind die sogenannten Thrombopoetin-Agonisten, die an den Thrombozyten produzierenden Zellen eine vermehrte Produktion bewirken, aber auch Fostamatinib. ein Tyrosinkinasehemmer aus der Gruppe der SYK-Inhibitoren, der zur Behandlung der chronischen Immunthrombozytopenie (ITP) zugelassen ist. Fostamatinib inhibiert die sogenannte Milztyrosinkinase (Syk) insbesondere in Makrophagen. Dadurch wird die Signaltransduktion von B-Zellrezeptoren und Fc-aktivierenden Rezeptoren blockiert. Daraus resultiert eine verringerte Antikörper-vermittelte Zerstörung von Thrombozyten.
ITP-Timeline
Die Geschichte der ITP reicht von der Erstentdeckung im Jahre 1735 über die Selbstversuche von Harrington bis zur heutigen Therapie mit Romiplostin. Harrington führte sich das Blut eines ITP-Patienten zu und stellte dabei fest, dass seine Thrombozyten einen Abfall verzeichneten. Ein heroischer Versuch, der aber auch zeigte, dass die Thrombozytopenie aus dem Plasma entstehen muss. Kurz danach wurden die ersten Behandlungen mit Kortison durchgeführt. Nach Versuchen mit Immunsuppression, Behandlung mit i.v. Immunglobulinen, erfolgte 2009 die Zulassung von Romiplostim (NPlate®). Damit konnten die klassischen Wege der ITP-Therapie verlassen werden und es zeigte sich eine deutliche Zunahme der Thrombozyten unter der Therapie mit diesem Medikament. Die Entwicklung blieb aber nicht stehen. Mittlerweile sind weitere Medikamente zugelassen worden, wie Etrombopag, Avatrombopag und das bereits erwähnte Fostamatinib. 2022 wurden Rilzabrutinib in Phase 2- und Efgartigimob in Phase 3-Studien untersucht und im letzten Jahr Ianamulab mit 2 Arten der Unterdrückung von B-Zellen in einer Phase 3-Studie.
Thrombopoetin-Rezeptor-Agonisten
Thrombopoetin-Rezeptor-Agonisten steigern die Megakaryopoese durch Bindung an den Thrombopoetin-Rezeptor. Romiplostim bindet an die externe Membrankomponente, dies ist ein Unterschied zu Avatrombopag und Eltromopag, die an der internen Membrankomponente ansetzen. Bei Romiplostim gibt es daher keine Kreuzresistenz.
In Deutschland sind Avatrombopag (nur chronische ITP) seit 2019, Eltrombopag seit 2010, Romiplostim seit 2009 zugelassen. Eine therapiefreie Remission wurde in 25 % der Fälle gesehen.
Thrombopoetin-Rezeptor-Agonisten haben eine hohe Wirksamkeit auch im längerfristigen Verlauf, was auch bei splenektomierten Patienten (grössere Anzahl an Vortherapien daher geringere Wirkung) als auch bei nicht splenektomierten Patienten gezeigt werden konnte.
Zum Schluss erwähnte der Referent zwei wichtige Effekt der Therapie mit Romiplostim, einmal die wesentliche Verbesserung der Lebensqualität der Patienten mit ITP und zum Zweiten das deutlich verbesserte Überleben in der letzten Dekade. Er wies daraufhin, dass die Daten hauptsächlich aus Studien stammen und damit noch eher spärlich sind. Dies wird mit dem deutschen ITP-Register, welches seit 2022 existiert und Gegensand des nächsten Vortrags ist, nun korrigiert.
Therapiequalität im Fokus
Das deutsche ITP-Register – Hintergründe, Ziele und Ausblick
Ein Register ist besonders wertvoll für die Erforschung seltener Erkrankungen. Die ITP ist eine seltene Erkrankung und Studien sind entsprechend eher weniger häufig. Das Register dient der Evidenzgenerierung für die Leitlinienerstellung, Beantwortung relevanter klinischer Fragestellungen und Evaluation von Interventionsstudien. Es führt zu einer verbesserten Transparenz der Versorgung und es liefert die Datengrundlage für klinische Studien, so Frau Dr. med. Karolin Trautmann-Grill, Dresden.
ITP ist eine seltene Erkrankung. In Deutschland sind genaue Inzidenzen, Prävalenzen und Outcome nicht bekannt. Es gibt eine dezentrale Versorgung und keine ITP- Zentren. Die Leitlinienadhärenz bei der Therapiewahl ist eher schlecht. 30% der ITP-Patienten erhalten nach einem Jahr immer noch Steroid. Man rechnet in Deutschland mit einer Inzidenz von 2-4 pro 100’000 pro Jahr. Vermutlich gibt es ca. 2600 Neuerkrankungen pro Jahr. Die Prävalenz bei Erwachsenen beträgt 9-26 pro 100’000. Seltene Erkrankungen bedeuten eine besondere Herausforderung für Patienten und Ärzte. So kam die Idee zur Schaffung eines ITP- Registers zustande. Damit sollte eine bessere Vernetzung ermöglicht werden (Selbsthilfegruppen, Kliniken, ambulante Zentren, Studienplattform). Ein weiteres Ziel war die Förderung der Versorgungsforschung (Epidemiologie, Therapiesequenzen, Krankheitszeitverlauf). Eine Besonderheit des Deutschen ITP-Registers ist, dass auch Daten zur Lebensqualität der Patienten erfasst werden (von Patienten berichtete Outcomes, ITP-Patienten leiden in besonderem Masse an Fatigue). Zur Begleitforschung dient die Biobank Dresden.
Das Studienkonzept
Einschlusskriterien sind: Patienten ≥18 Jahre, Erstdiagnose ITP≤12 Monate, Wohnsitz Deutschland, unterzeichnete Einwilligungserklärung. Das ursprüngliche Ziel war 1100 Patienten, 50 Zentren, ca. 4 Patienten pro Zentrum pro Jahr. Es wurde eine jährliche Verlaufsdokumentation geplant. Erstdiagnose: Initialbogen + Basisdokumentation. Verlaufsbogen nach einem Jahr Beobachtungszeit, Verlaufsbogen nach 2 Jahren Beobachtungszeit etc.
Der Beginn des Registers war im November 2021 mit dem Ethikvotum in Jena, ab Dezember 2021 war die RedCap Datenbank produktiv. Der erste Patient wurde im Dezember 2021 eingeschlossen. Im Februar 2022 wurde die Website www.d-itp.de eröffnet, im Juni 2022 erfolgte die Initiierung des 2. Zentrums in Dresden und ab Juli 2022 erfolgte der weitere Rollout in Deutschland. Der Stand am 28.1.2024 waren 287 Patienten im Register eingeschlossen, das Biobanking betrug 181. Derzeit gibt es 58 Zentren in Deutschland, die gut über das ganze Land verteilt sind. Es wird jährlich eine Fortbildung und ein Patiententag durchgeführt. Es gibt nun auch eine europäische Initiative zur Vernetzung der Zentren.
Daten-Cut im November 2023: Demographie
Das Register umfasst 251 Patienten im Alter zwischen18-97 Jahren (median 64 Jahre). 48 % sind männlich, 52 % weiblich. 86% hatten eine primäre ITP, 13 % eine sekundäre ITP, bei 1% fehlt die Angabe.
Symptome bei Erstdiagnose
Über 75 % hatten keine Blutungssymptomatik, d.h. eine inzidentielle Blutung. Grad 1 Blutungen hatten ca. 15%, Grad 2 Blutungen etwa 4 % Grad 3 ca. 2 % und eine Person hatte eine Grad 4 Blutung.
Diese Population hat auch Komorbiditäten: Über 40 % haben eine arterielle Hypertonie, gegen 20 % einen Diabetes, etwa 6 % hatten Thromboembolien, was bei ITP wichtig ist, denn die ITP stellt per se ein Thromboembolie-Risiko dar. Mehr als 10 % hatten eine KHK und etwa 6 % einen Schlaganfall. Eine Antikoagulation wurde immerhin bei 16 % festgestellt (ein deutlicher Prozentsatz). Diese Patienten sind besonders gefährdet, an einem Blutungsereignis zu erkranken.
Therapiespektrum, 146 waren behandlungspflichtig
Prednisolon erhielten 69 Patienten, Dexamethason 61, Eltrombopag 21, Romiplostin 19, Avathromopag 3, Fostamatinib 3, Splenektomie 1, Rituximab 3.
Ausblick
Daten aus dem ersten Daten-Cut sollen am Europäischen Hämatologenkongress präsentiert werden.
Langfristig soll das Register als gemeinsame Studienplattform genutzt werden. Weitere Forschungsprojekte zur Pathogenese und Behandlung der ITP sind am Laufen. Das Register soll verstetigt werden und insgesamt soll es helfen, die Situation der ITP-Patient/-innen zu verbessern.
Abschliessend dankte die Referentin der Leitungsgruppe mit Prof. A. Matsdorff, PD Dr. med Oliver Meyer, Dr. med. A Georgi, Frau Arnold SHG-ITP Giessen, dem Zentrum Klinische Studien Jena, der Biobank Dresden und insbesondere der Firma Amgen für das unabdingbare Sponsoring eines derartigen Projekts.
Immunmodulation mit Romiplostim – das zeigt die IROM-Studie
Fast alle Behandlungsstrategien bei der ITP zielen darauf ab, die Blutung zu kontrollieren. Man versucht den vorzeitigen Thrombozytenabbau zu bremsen oder die Thrombozytenproduktion zu stimulieren, so Frau Dr. med. Alexandra Schifferli, Leitende Ärztin Hämatologie/Onkologie UKBB, Basel.
Nur wenige Medikamente wurden untersucht, die das Potenzial haben, die Immundysregulation – also die Ursache der ITP – zu behandeln und die verlorene Immuntoleranz zu induzieren. Die Ursache aller Autoimmunerkrankungen ist eine gestörte Immuntoleranz. Medikamente wie Rituximab, und Dexamethason haben das Potenzial die Immuntoleranz wieder zu induzieren, aber nur mit mässigen Langzeitergebnissen. Zwischen 2010 und 2015 wurde zunehmend von Patienten berichtet, dass sie ihre TPO-Mimetika sicher stoppen konnten, ohne ein Rezidiv zu erleiden. Dies wurde zunächst in retrospektiven Kohorten aber auch in prospektiven Studien gezeigt. Diese Gruppe von Patienten wird in den meisten Publikationen mit dem Akronym SROT (sustained remission of treatment) bezeichnet. Im Jahre 2010 wurde in einer kleinen Studie mit nur 10 Patienten eine verbesserte Aktivität der regulatorischen T-Zellen bei Patienten mit chronischer ITP gezeigt, die TPO-Mimetika erhielten. Die Daten dieser Studie deuteten auf eine Wiederherstellung der Immuntoleranz durch diese Medikamente hin (1). TPO-Mimetika sind eigentlich nur rein symptomatische Medikamente. Sie boosten die Produktion von Thrombozyten um die Hämostase zu verbessern und somit auch das Risiko von Blutungen zu vermindern. Um die Hintergründe für die Verbesserung der Grundkrankheit zu verstehen, wurde die IROM-Studie (2) geplant. Die Hypothese war, dass durch die Erhöhung der Thrombozyten, also der Masse des Antigens, eine Immuntoleranz erzeugt werden kann, analog zur Immuntoleranztherapie in der Allergologie. Bei der Antigen-Desensibilisierung in der Allergologie gibt man sehr hohe Dosen von Antigen über längere Zeit. Dies führt paradoxerweise dazu, dass der Körper denkt, wenn so viel Antigen im Umlauf ist, muss es doch normal oder ungefährlich sein und reagiert nicht mehr auf den Antigenstimulus. Nicht nur in der Allergologie kennt man diese Therapieform, sondern entsprechende Forschungsberichte gibt es auch beim Diabetes Typ 1, bei Multipler Sklerose und Colitis ulcerosa. Häufig versagen diese Therapien an der Tatsache, dass die vermeintlich wichtigsten Antigene nur die Spitze des Eisbergs sind. Die ideale Immuntoleranztherapie wäre eigentlich Organ-bezogen und nicht Antigen-bezogen. Diese Möglichkeit hätten wir bei der ITP mit den TPO-Mimetika, so die Referentin. Zusätzlich war den Forschern klar, dass die Thrombozyten auch Immunzellen sind, die sowohl mit dem angeborenen als auch dem erworbenen Immunsystem interagieren. Thrombozyten sind also nicht nur Zielscheibe des Geschehens bei der ITP, sondern vermutlich auch Akteure (3). Sie produzieren verschiedene Zytokine und sind das grösste Reservoir von TGFβ, einem starken inflammatorischen Zytokin.
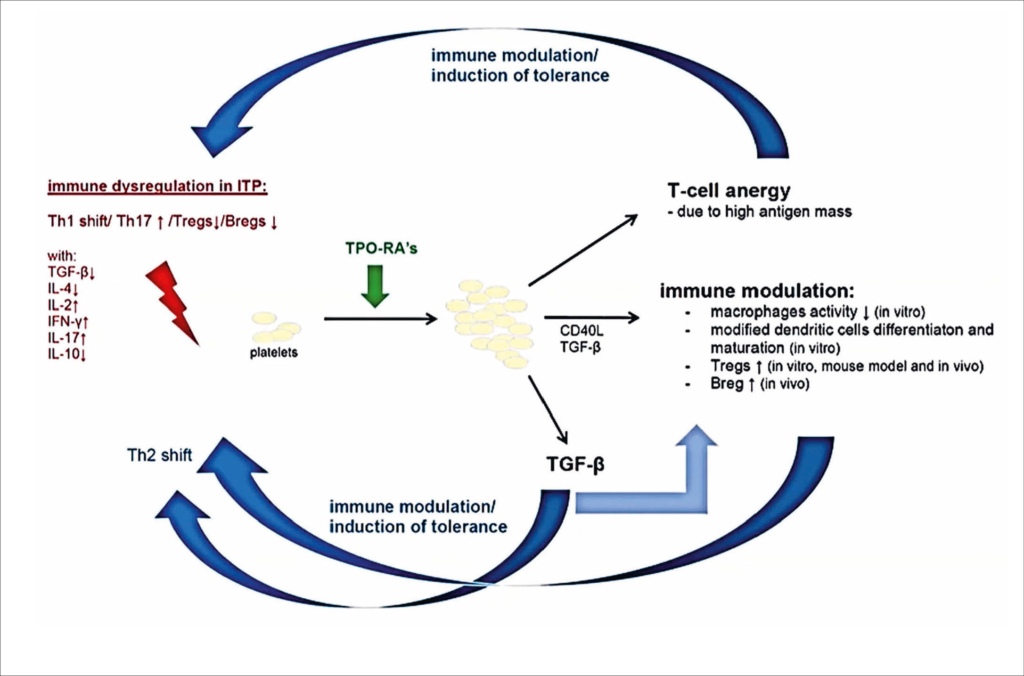
Hypothese zur Immunmodulation mit TPO- RA als Grundlage der IROM-Studie
Die Hypothese zur Immunmodulation mit TPO-RA, wie sie für die IROM-Studie (1) formuliert wurde, ist in der Abb. 1 wiedergegeben. Sie umfasst die folgenden Punkte: Thrombopoietin-Rezeptor-Agonisten (TPO-RAs) haben offensichtlich das Potenzial, den Krankheitsverlauf mit einer behandlungsfreien Remission von bis zu 30 % zu beeinflussen. Mögliche Mechanismen könnten die Exposition gegenüber hochdosiertem Antigen und/oder die angeborene Immunaktivität von Thrombozyten sein, insbesondere die Freisetzung von TGF-ß, die regulatorische T-Zellen (Tregs) stimulieren oder wiederherstellen kann. Tregs spielen eine grundlegende Rolle bei der Aufrechterhaltung der Immuntoleranz. Frühere Studien haben gezeigt, dass die Funktion der Tregs im peripheren Blut von ITP-Patienten verringert und beeinträchtigt ist.
Die IROM-Studie (4, 5)
2016 wurde die IROM-Studie nach 2 Jahren Vorbereitungszeit an 5 Orten eröffnet. Romiplostim war damals noch nicht als Second-Line Therapie zugelassen, sondern indiziert für die chronisch refraktäre ITP. Die Studie war konzipiert als nationale multi-center, open label, single arm, proof of concept Studie. Das Ziel war die Untersuchung möglicher immunmodulierender Wirkungen von Romiplostim bei Patienten mit ITP. Einschlusskriterien waren junge Erwachsene mit primärer ITP (initial 18j.- 45j., bei denen die Erstlinientherapie versagt hatte, nicht vertragen wurde oder die einen Rückfall erlitten hatten (unabhängig von der Krankheitsdauer). Der primäre Endpunkt war das Verhältnis TH1(TH17) / TH2(TREG). Zu den sekundären Endpunkten gehörten neben den immunologischen Daten auch die Rate der anhaltenden Remission ohne Behandlung (SROT) nach einem Jahr, sowie die Romiplostim-Dosis, die Thrombozytenzahl und Blutungen.
Studienplan
Romiplostim s.c. während 22 Wochen gegeben, wöchentliche Dosisanpassung je nach Thromboztenansprechen, Ziel 50-200 x 109/l (gemäss Produkteinformation). Follow-up bis Woche 52 (clinical visit und Blutbild), immunologisches Panel an Woche 1, 6, 12, 22, 52.
Resultate
Ansprechen der Thrombozyten und Romiplostim-Dosis: Bei SROT-Patienten war die Titration der Romiplostim-Dosis geringer und die Thrombozytenzahl reagierte schneller, höher und stabiler.
Die Thrombozytenzahl bei Patienten mit einem Rückfall zeigte eine sehr zackige Kurve über 22 Wochen Behandlungsdauer. Es zeigte ich eine starke Korrelation zwischen Thrombozytenzahl und TGF-β.
Die Beobachtung eines höheren Anstiegs der Thrombozyten und eines stärkeren Anstiegs des TGF-β bei Patienten mit SROT im Vergleich zu Patienten mit einem Rückfall bekräftigt die Hypothese, dass der tolerogene Stimulus von der Thrombozytenmasse kommt.
Die meisten Zytokinwerte sanken unmittelbar nach Behandlungsbeginn (bei allen Patienten).
Das Immunsystem kann durch Romiplostim beeinflusst werden (Tregs, proinflammatorische Zytokine, TGF-β).
Klinische Resultate: Bei 6 von 9 Patienten mit neu diagnostizierter ITP war das Absetzen von Romiplostim erfolgreich und führte zu einer anhaltenden behandlungsfreien Komplettremission nach einem Jahr, während alle Patienten mit chronischer ITP einen Rückfall erlitten und erneut mit verschiedenen Behandlungen beginnen mussten.
Diese Ergebnisse unterstützen die Annahme, dass eine frühzeitige Behandlung der ITP mit TPO-RAs, zB. Romiplostim, den natürlichen Verlauf der ITP positiv beeinflussen könnte. Eine Einschränkung der Studie in Bezug auf klinische Endpunkte ist die geringe Stichprobengrösse.
Fazit 15 Jahre Romiplostim
Die Therapie der ITP hat sich in den letzten 15 Jahren durch Romiplostim (NPlate®) und andere TPO-RAs grundlegend verändert, u.a. durch den Wegfall der Splenektomie und die Verkürzung der Erstlinientherapie mit Steroiden.
ITP-Registerdaten sind besonders wertvoll zur Erforschung und Qualitätssicherung und können künftig bei der Beantwortung relevanter klinischer Fragestellungen in Bezug auf die ITP beitragen.
Die Ergebnisse der IROM-Studie zeigen, dass eine frühzeitige Behandlung mit Romiplostim durch Immunmodulation den natürlichen Verlauf der ITP positiv beeinflussen kann.
riesen@medinfo-verlag.ch
1. Bao W et al. Improved regulatory T-cell activity in patients with chronic immune thrombocytopenia treated with thrombopoietic agents. Blood 2010 ; 116 :4639-4645.
2. Schifferli A and Kühne T. Thrombopoietin receptor agonists: a new immune modulatory strategy in immune thrombocytopenia. Sem. Hematol 2016;53:S31-S34
3. Yeaman M. Platelets at the nexus of antimicrobial defence. Nat Rev Microbiol 2014; 12: 426-437
4. Schifferli A et al Immunomodulation with Romiplostim in Young adult primary immune thrombocatopenia (ITP) as second line strategy (iROM study). Blood 2021 ; 138 : Suppl 1 : 3149. Doi.org/101182/blood-2021_146648.
5. Schifferli A et al. Immunomodulation with Romiplostim as a second-line strategy in primary immue thrombocytopenia : the iROM study Br J Haematol. 2023 ;203 :119-130
info@onco-suisse
- Vol. 14
- Ausgabe 2
- April 2024