- PARP-Inhibitoren – Durchbruch in der Erhaltungstherapie
Am diesjährigen Swiss Onocology & Hematology Congress diskutierten Prof. Cristiana Sessa, Bellinzona, PD Dr. Christian Kurzeder, Basel, und Prof. Jalid Sehouli, Berlin, im Rahmen des Tesaro Lunch Symposiums die zunehmende Bedeutung von PARP-Inhibitoren als Erhaltungstherapie beim rezidivierten Ovarialkarzinom. Das Ziel der Erhaltungstherapie ist es dabei, den Patientinnen ein möglichst langes Überleben bei guter Lebensqualität zu ermöglichen.
Die Rezidivrate beim Ovarialkarzinom liegt im Stadium FIGO II-IV bei rund 80%. Mit einer Erhaltungstherapie im Anschluss an die platinbasierte Chemotherapie kann die Progression hinausgezögert werden. Die Verfügbarkeit der PARP-Inhibitoren ermöglicht dabei im Vergleich zur traditionellen «Watch & Wait» Strategie deutlich längere progressionsfreie Phasen, ohne dass die Lebensqualität der Patientinnen wesentlich beeinträchtigt wird. Ein personalisiertes Therapiemanagement ist jedoch essenziell, um den bestmöglichen Outcome zu erreichen.
Erhaltungstherapie unabhängig vom BRCA-Status
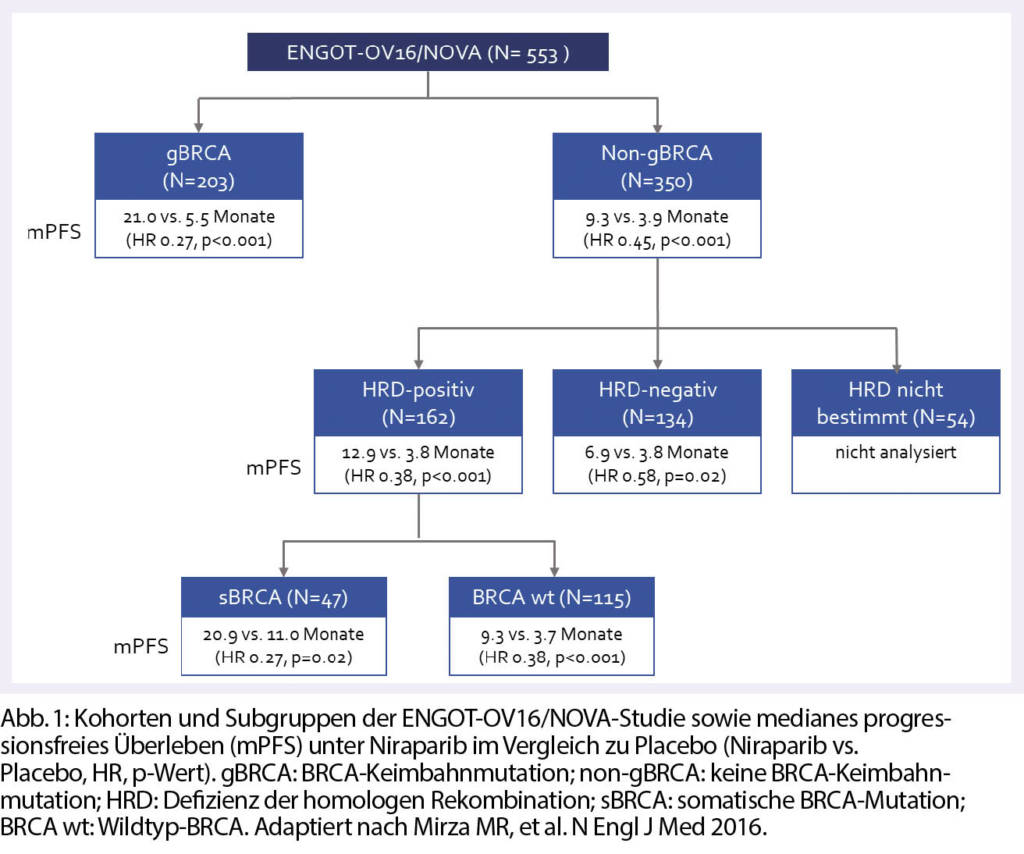
Durch eine Erhaltungstherapie mit einem PARP-Inhibitor kann das progressionsfreie Überleben (PFS) beim platinsensitiven, rezidivierten Ovarialkarzinom signifikant verlängert werden. Die Wahrscheinlichkeit, von einer Olaparib-Behandlung zu profitieren ist dabei gemäss einer retrospektiven Analyse der randomisierten, doppelblinden, placebo-kontrollierten Phase-II-Studie «Study 19» bei Patientinnen mit BRCA-Mutation am grössten. Dr. Kurzeder bezeichnete daher die doppelblinde, Phase-III ENGOT-OV16/NOVA-Studie in seinem Referat als «mutig», da mehr als die Hälfte der eingeschlossenen Patientinnen keine BRCA-Keimbahnmutation (non-gBRCA) aufwiesen. Die Resultate zeigten, dass im Vergleich zu Placebo unter Niraparib unabhängig vom BRCA-Mutationsstatus ein signifikanter PFS-Benefit erreicht wurde (Abb. 1). Zudem profitierte auch die Subgruppe ohne Defizienz der homologen Rekombination (HRD-negativ), was allgemein mit dem schlechtesten Therapieansprechen verbunden ist, von der Behandlung mit Niraparib (Abb. 1). Mit Blick auf die Daten der ENGOT-OV16/NOVA-Studie hielt Dr. Kurzeder daher fest, dass die genetische Testung als Basis der klinischen Entscheidungsfindung in den Hintergrund rückt.
Auch als Erstlinien-Erhaltungstherapie nach einer platinbasierten Chemotherapie konnte unter Niraparib unabhängig vom Biomarker-Status (PRIMA-Studie) und unter Olaparib beim BRCA-mutierten fortgeschrittenen Ovarialkarzinom (SOLO-1-Studie) eine Verbesserung des medianen PFS gezeigt werden.
Individuelles Therapiemanagement
Beim Übergang in die Erhaltungstherapie haben die meisten Patientinnen schon einige Behandlungen hinter sich. Die Erhaltung der Lebensqualität ist daher zentral und kann durch ein gutes Nebenwirkungsmanagement unterstützt werden, betonte Prof. Sehouli in seinem Referat. Als besonders belastend werden dabei nicht-hämatologische Nebenwirkungen, wie beispielsweise Nausea, empfunden. Obwohl diese trotz gutem Management teilweise bestehen bleiben, kann eine ausführliche Aufklärung zu Beginn der Therapie die Akzeptanz erhöhen. Prof. Sehouli erklärte, dass eine Thrombozytopenie 3./4. Grades meist nur zu Beginn der Therapie auftritt und wie in der ENGOT-OV16/NOVA-Studie gezeigt wurde, durch individuelle Dosisanpassungen ohne Einfluss auf die Wirksamkeit der Behandlung gut handhabbar ist. Als Prädiktoren für die Entwicklung einer Thrombozytopenie 3./4. Grades wurden ein Körpergewicht < 77 kg und eine Thrombozytenzahl < 150 000/μl identifiziert. Daher wurde Niraparib in der Schweiz in einer individuell angepassten Startdosierung von täglich 200 mg zugelassen (bei ≥ 77 kg und einer Thrombozytenzahl ≥ 150 000/μl: täglich 300 mg).
Blick in die Zukunft
Zum Schluss des Symposiums diskutierte Prof. Sessa mögliche Weiterentwicklungen im Bereich der Erhaltungstherapie. Insbesondere die Sequenz der Therapien und verschiedene Kombinationen könnten dabei einen entscheidenden Einfluss auf den Outcome haben. In verschiedenen Studien wird daher die Wirksamkeit und Sicherheit der PARP-Inhibitoren in Kombination mit Angiogenesehemmern und Immuntherapie untersucht. Erste Ergebnisse deuten laut Prof. Sessa auf weitere vielversprechende Entwicklungen hin.
Quelle: Tesaro Satellitensymposium «PARP inhibitors in gBRCAmut and Non-gBRCAmut ovarian cancer focus on Niraparib», 2. Swiss Oncology & Hematology Kongress (SOHC), 26. Juni 2019, Zürich.