- PSMA-Liganden PET/CT und -Therapie des Prostatakarzinoms
Die PSMA-PET/CT gilt als die sensitivste und spezifischste Methode zur Rezidiv-Suche des Prostatakarzinoms (PCa).
Die Kosten der PSMA-PET/CT werden aktuell von den Versicherungen routinemässig ausschliesslich für biochemische Rezidive des PCa übernommen. Die PSMA-Therapie zeigt bei austherapierten Patienten im kastrationsrefraktären, metastasierten Stadium grosses Potential. Sie hat in der Schweiz vor kurzem eine temporäre Zulassung erhalten.
La PSMA-PET/CT est considérée comme la méthode la plus sensible et la plus spécifique pour la recherche de récidive du cancer de la prostate (CPa). Les coûts de la PSMA-PET/CT sont actuellement couverts par les compagnies d’assurance exclusivement pour les récidives biochimiques de la PCa. La thérapie PSMA montre un grand potentiel chez les patients réfractaires à la castration, au stade métastique et ayant épuisé tous les traitements. En Suisse elle a récemment reçu une autorisation temporaire.
PSMA-PET/CT
Das Prostatakarzinom (PCa) ist weltweit der häufigste maligne Tumor bei Männern. Nach initialer Therapie entwickelt sich häufig ein biochemisches Rezidiv (1,2). Dabei stellt die Tumorsuche mit konventioneller Bildgebung wie z.B. der CT oder der MRI eine grosse Herausforderung dar. Noch bis vor wenigen Jahren galt die Positronen-Emissions-Tomographie in Kombination mit der Computertomographie (PET/CT) unter Verwendung von Cholin als eine der besten Methoden zur Detektion eines PCa-Rezidivs. Jedoch zeigt sie vor allem bei niedrigen PSA-Werten und hohem Gleason Score (GSC) signifikante Einschränkungen. Die 18F-FDG-PET/CT spielt nur bei entdifferenzierten PCa eine Rolle und ist daher nur selten indiziert.
Insgesamt bestand somit die Notwendigkeit zur Suche nach besseren diagnostischen Verfahren. Dabei lag der Fokus in den letzten Jahren vor allem auf dem Prostata-spezifischen Mem-
bran-Antigen (PSMA). PSMA ist ein transmembranes Protein, welches in PCa-Zellen signifikant stärker exprimiert wird als in normalen Prostatazellen (3). Es eignet sich als Zielstruktur in einer herausragenden Weise für eine molekulare Diagnostik und Therapie (4). Nach Jahren präklinischer Vorarbeiten gelang der Durchbruch mit der Herstellung des 68Gallium-markierten PSMA-Liganden «PSMA-11» am Deutschen Krebsforschungszentrum Heidelberg (DKFZ) (5, 6) und die klinische Einführung dieses Liganden in der PET/CT im Mai 2011 in der Nuklearmedizin der Uniklinik Heidelberg (7, 8). Seitdem hat sich diese neue diagnostische Methode, allgemein als «PSMA-PET/CT» bekannt, mit erstaunlicher Geschwindigkeit weltweit ausgebreitet und gilt als entscheidender Schritt vorwärts in der Diagnostik des rezidivierenden PCa und des Primär-Stagings bei Hochrisiko-PCa. Der Wirkmechanismus ist für eine molekulare Bildgebung optimal: 68Ga-PSMA-11 bindet an den zellexternen Bereich des PSMA-Rezeptors und wird anschliessend rasch und über die Zeit akkumulierend internalisiert. Eine gesonderte Vorbereitung der Patienten (z.B. Diät oder Pausieren von Medikamenten) ist nach aktuellem Kenntnisstand nicht erforderlich.
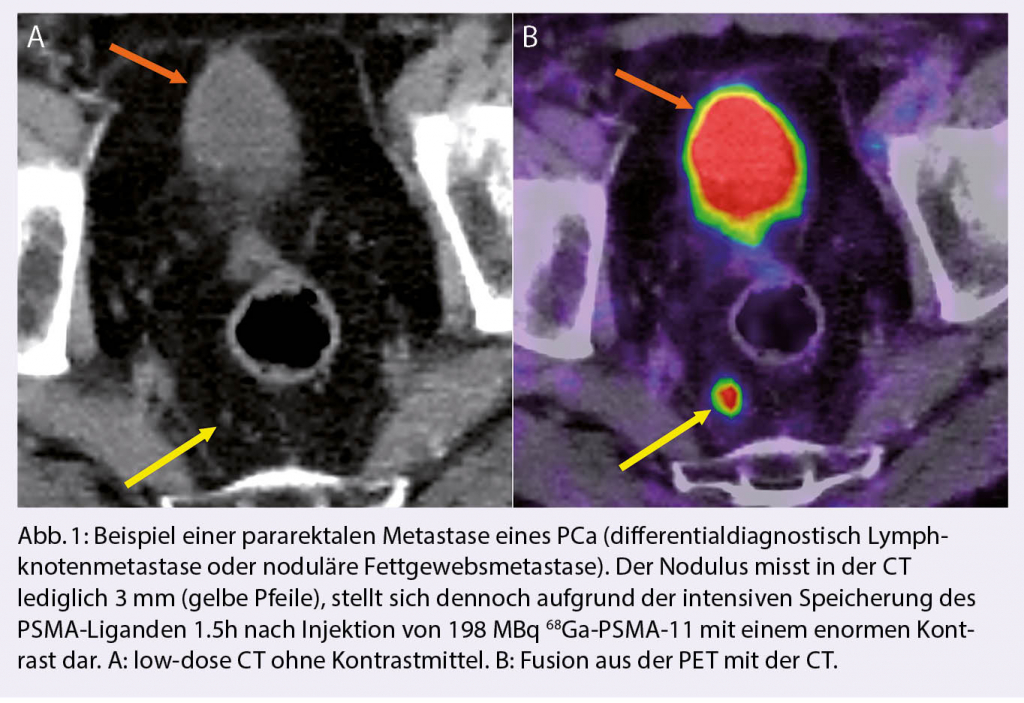
Bereits die ersten Publikationen zeigten das grosse Potential dieser neuen diagnostischen Modalität (7, 8). 68Ga-PSMA-11 PET/CT zeigte sich häufig imstande, auch kleine PCa-Herde mit einem hohen Kontrast darzustellen (Abb. 1). Vor allem bei niedrigen PSA-Werten und höherem GSC zeigt sie sich der etablierten Cholin-PET/CT als signifikant überlegen (9). Diese Ergebnisse wurden später auch von anderen Arbeitsgruppen bestätigt (10, 11), so dass mittlerweile in den meisten Zentren die PSMA-PET/CT die Cholin-PET/CT ersetzt hat. Bei PSMA-negativem PCa (schätzungsweise 5-10% aller PCa) kann die Cholin-PET/CT jedoch weiterhin hilfreich sein.
Bislang haben sich nur wenige Studien mit >200 Patienten mit der Wertigkeit der 68Ga-PSMA-11 PET/CT in Rezidiv-Situationen befasst. Die erste dieser Publikationen schloss 319 Patienten ein und zeigte, dass bei über 80% von ihnen die PET/CT zumindest einen pathologischen Herd zeigte (12). Im Durchschnitt aller 900 repräsentativen Tumorherde, die bei dieser Arbeit analysiert wurden, wurde eine vergleichsweise sehr hohe Tracer-Aufnahme nachgewiesen. Diese Analyse bestätigte somit die vorhergehenden Erfahrungen, dass PSMA-11 imstande ist, PCa-Metastasen mit sehr hohem Kontrast darzustellen.
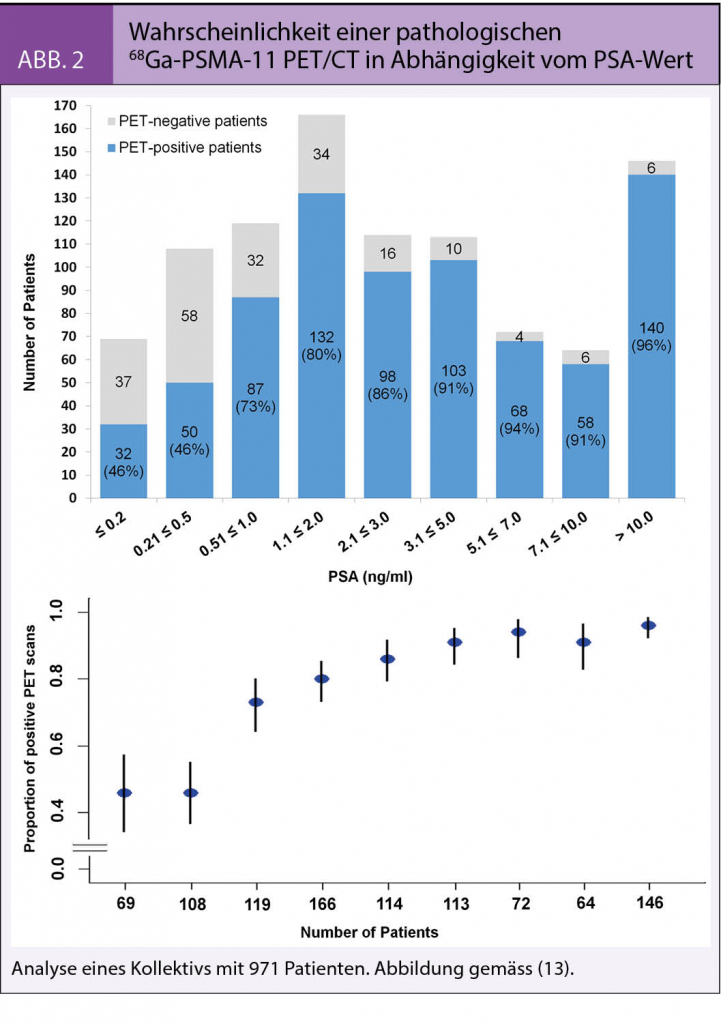
Erwartungsgemäss steigt die Wahrscheinlichkeit der Detektion von PCa-Herden auch in der PSMA-PET/CT mit der Höhe des Tumormarkers PSA. Die grösste Herausforderung stellen naturgemäss die sehr niedrigen PSA-Werte dar. Unter einem PSA-Wert von 0.5 ng/ml liegt die Wahrscheinlichkeit, zumindest einen Tumorherd in der 68Ga-PSMA-PET/CT zu entdecken, neueren Analysen an einem Patientenkollektiv von > 1000 zufolge, bei ca. 50% und steigt kontinuierlich bis zu einem PSA von 3 ng/ml auf deutlich mehr als 90% an (13). Sie erreicht jedoch, wie in der Abb. 2 ersichtlich, nie 100%, da schätzungsweise 5-10% aller PCa entweder überhaupt kein oder nicht ausreichend PSMA exprimieren.
Aus präklinischen Publikationen ist bekannt, dass PCa mit höherem GSC auch mehr PSMA exprimieren (14, 15). Bei der o.g. grossen Analyse bezüglich der Wahrscheinlichkeit für pathologische PSMA-PET/CT konnte zwar eine Tendenz zugunsten höherer GSC, jedoch kein signifikanter Unterschied zwischen höheren und niedrigeren GSC festgestellt werden (13).
Die Spezifität der 68Ga-PSMA-11 PET/CT ist als sehr hoch (> 95%) einzustufen, was in mehreren Studien bestätigt werden konnte (12,16–18). Es kann davon ausgegangen werden, dass jede umschriebene Mehrspeicherung in einem CT-morphologisch sichtbaren Korrelat bei Patienten mit einem biochemischen PCa-Rezidiv praktisch bis zum Beweis des Gegenteils als ein PCa-Herd gewertet werden muss. Zwar sind in den letzten Jahren multiple Fallbeschreibungen von PSMA-positiven Entitäten nicht-prostatischen Ursprungs veröffentlicht worden. Jedoch muss man beachten, dass deren Zahl nur einen minimalen Bruchteil der PCa-Herde darstellt, die täglich in der PSMA-PET/CT weltweit entdeckt werden.
Aus präklinischen Publikationen ist ferner bekannt, dass eine Androgen-Entzugs-Therapie (ADT) die PSMA-Expression in Tumormodellen steigern kann (19–21). In den beiden grössten Studien wurde tatsächlich festgestellt, dass Patienten unter laufender ADT signifikant häufiger einen pathologischen Befund in der PSMA-PET/CT aufwiesen, obwohl die ADT zu einer Volumenreduktion des Tumors und zu sinkenden PSA-Werten führt, welche wiederum die Tumordetektion beeinträchtigen (12, 13). Von den Autoren wurde jedoch als eine mögliche Ursache dieser Ergebnisse auch die Möglichkeit erwähnt, dass die ADT tendenziell bei Patienten mit fortgeschrittenem Tumorstadium, somit höherer Tumorlast, begonnen wird. Dennoch hielten die Ergebnisse viele Kollegen nicht davon ab, in Richtung einer höheren, ADT-verursachten PSMA-Expression zu spekulieren. Bei der genaueren Analyse der o.g. präklinischen Studien wird jedoch deutlich, dass die höhere PSMA-Expression der PCa-Zellen lediglich nach einer kurzzeitigen ADT (maximal 4 Wochen) zu beobachten war. Eine dieses Jahr erschienene Analyse hat eindrücklich demonstriert, dass eine Langzeit-ADT hingegen einen signifikant negativen Einfluss auf die Sichtbarkeit und Detektion von PCa-Herden in der PSMA-PET/CT zur Folge hat (22). Nur noch ein Bruchteil der vor der ADT sichtbaren Tumorherde war unter der Langzeit-ADT auch weiterhin sichtbar. Die Empfehlung der Autoren war konsequenterweise, dass bei der Rezidivsuche die PSMA-PET/CT entweder noch vor Beginn oder aber spätestens vier Wochen nach Beginn einer ADT durchgeführt werden sollte.
Es ist aktuell unbekannt, wie lange eine bereits laufende ADT pausiert werden sollte, um die maximale Sichtbarkeit des Tumors in der PSMA-PET/CT zu garantieren.
Regulatorische Situation der PSMA-PET/CT in der Schweiz
In der Schweiz ist aktuell eine temporäre Zulassung nur für 68Ga-PSMA-11 vorhanden, jedoch ist in der Zukunft zusätzlich mit alternativen PSMA-Liganden zu rechnen. Die Kosten für eine 68Ga-PSMA-11-PET/CT wurden zwischen Januar 2017 und Dezember 2018 von den Krankenversicherungen nach zyklischen Verhandlungen zwischen der Schweizerischen Gesellschaft für Nuklearmedizin und den Versicherungen ausschliesslich für die Tumorsuche nach biochemischem Rezidiv des PCa übernommen. Begleitet wurde dies von einer Registerstudie im Rahmen einer Swiss Extended PET Registry («SEPR»). Seit Januar 2019 ist diese Erfassung beendet und die PSMA-PET/CT wird für die Rezidivsituation unverändert ohne vorherige Kostengutsprachen oder Koppelungen an Studien von den Krankenversicherungen vergütet. Zudem ist die PSMA-PET/CT nicht mehr ausschliesslich an 68Ga-PSMA-11 gebunden; alternative PSMA-Tracer können nach Erfüllung behördlicher Voraussetzungen ebenfalls verwendet werden.
An der Kostenübernahme für die 68Ga-PSMA-11 PET/CT zum Primär-Staging bei Hochrisiko-PCa wird derzeit gearbeitet. Bis dahin ist eine Kostenrücksprache mit den Versicherungen oder die Selbstzahlung durch die Patienten erforderlich.
PSMA-basierte Therapie des metastasierten Prostatakarzinoms
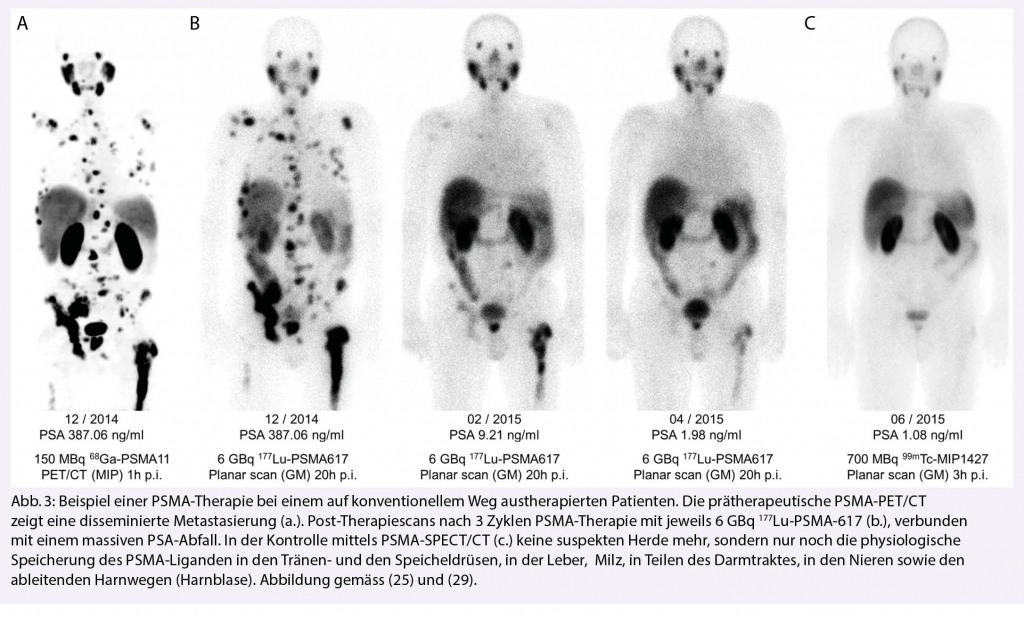
Die Zielstruktur PSMA eignet sich nicht nur zur Diagnostik, sondern in besonderem Masse auch für eine zielgerichtete, endogene Radiotherapie (Radioligandentherapie). Voraussetzung einer solchen Therapie ist eine ausreichend hohe PSMA-Expression der Tumorherde, die mittels PSMA-PET/CT evaluiert wird. Die ersten «PSMA-Therapien» mit radioaktiv markierten Liganden, ebenso wie die PSMA-PET/CT im Jahre 2011 klinisch erstmals eingeführt, wurden zunächst mit 131Iod-markierten Liganden durchgeführt (23, 24). Die PSMA-Therapie muss nach Tumorboardbeschluss durchgeführt werden. Sie ist bei Tumorprogress indiziert, wenn die zugelassenen Therapieoptionen zumindest der Erst- und Zweitlinie ausgeschöpft oder nicht zielführend sind oder einzelne zugelassene Therapieoptionen vom Patienten abgelehnt werden. Sofern sinnvoll, kann die PSMA-Therapie nach Tumorboardbeschluss auch in einem früheren Stadium eingesetzt werden. Seit 2013 werden nunmehr 177Lu-markierte Liganden, z.B. PSMA-617, eingesetzt. Die allgemeinen Erfahrungen mit PSMA-Therapien zeigen bereits nach einem einzigen Zyklus vielversprechende Ergebnisse (Abb. 3), auch wenn grundsätzlich eine Heilung nicht zu erwarten ist: bei > 60% der Patienten sinkt der PSA-Wert um mindestens 50%. In dosimetrischen Analysen konnten Herddosen von bis zu 162 Gy für eine verabreichte Aktivität von 7. 4 GBq 177Lu-PSMA-617 nachgewiesen werden (25). Aktuell werden 4-6 Zyklen zu je 6 – 7.4 GBq in Abständen von 6-8 Wochen empfohlen. Rund 1/3 der Patienten weisen eine sehr gute Response auf die PSMA-Therapie auf, bei 1/3 bleibt die Erkrankung zunächst stabil und 1/3 reagieren nicht auf die Therapie (26, 27). Die kurz- bis mittelfristigen Nebenwirkungen sind nach den ersten Zyklen insgesamt als gering einzustufen und betreffen vor allem die Tränen- und Speicheldrüsen, die physiologisch ebenfalls stark PSMA exprimieren. Die Nebenwirkungen auf das blutbildende Knochenmark zeigen sich moderat. Der aktuellen Datenlage zufolge können PSA-progressionsfreie Überlebensintervalle von durchschnittlich 4.5 Monaten erwartet werden (28), wobei darauf hinzuweisen ist, dass es sich bisher um end-stage Patienten handelt.
Regulatorische Situation der PSMA-Therapie in der Schweiz
Die PSMA-Therapie ist seit kurzem in der Schweiz temporär zugelassen, dem weltweit einzigen Land mit einer vergleichbaren Heilmittelbehörde. Anfang 2019 ist mit der Durchführung der ersten Therapien zu rechnen.
Klinik für Nuklearmedizin
Inselspital Bern
Freiburgstrasse 18
3010 Bern
ali.afshar@insel.ch
Klinik für Nuklearmedizin
Inselspital Bern
Freiburgstrasse 18
3010 Bern
Die Autoren deklarieren keine Interessenskonflikte in Verbindung mit dem vorgelegten Manuskript
- Die PSMA-PET/CT gilt als die sensitivste und spezifischste Methode sowohl zur Rezidiv-Suche des Prostatakarzinoms (PCa) als auch zum Primär-Staging des Hochrisiko-PCa.
- Eine gesonderte Vorbereitung der Patienten (z.B. Diät oder Pausieren von Medikamenten) ist nach aktuellem Kenntnisstand nicht erforderlich.
- Die PSMA-PET/CT sollte dem aktuellen Wissensstand nach entweder noch vor Beginn oder aber spätestens vier Wochen nach Beginn einer ADT durchgeführt werden, da die Langzeit-ADT einen signifikant negativen Einfluss auf die Visualität der PCa-Herde haben kann.
- Die Kosten für eine PSMA-PET/CT werden aktuell von den Krankenversicherungen ausschliesslich für biochemische Rezidive über-
nommen. - Die PSMA-Therapie zeigt bei auf konventionellem Wege austherapierten Patienten im kastrationsrefraktären, metastasierten Stadium grosses Potential. Im Jahr 2019 ist mit der Durchführung der ersten Therapien auch in der Schweiz zu rechnen.
Messages à retenir
- La méthode PSMA-PET/CT est considérée comme la méthode la plus sensible et la plus spécifique pour le dépistage de la récidive du cancer de la prostate (CPa) et la stadification primaire des CPa à haut risque.
- Selon l’état actuel des connaissances, il n’est pas nécessaire de préparer les patients séparément (par ex. régime alimentaire ou interruption de la médication).
- Selon les connaissances actuelles, la PSMA-PET/CT doit être effectuée soit avant l’apparition de l‘ADT, soit au plus tard quatre semaines après l’apparition de la FDP, car l‘ADT à long terme peut avoir un effet négatif important sur l’apparence visuelle des lésions de PCa.
- Les coûts d’une PSMA-PET/CT sont actuellement pris en charge par les caisses d’assurance maladie exclusivement pour les récidives biochimiques.
- Le traitement par la PSMA présente un grand potentiel chez les patients ayant épuisé tous les traitements conventionnels, étant réfractaires à la castration, au stade métastatique. Les premières thérapies devraient également être mises en œuvre en Suisse en 2019.
1. Freedland SJ, Presti JC, Amling CL, et al. Time trends in biochemical recurrence after radical prostatectomy: results of the SEARCH database. Urology. 2003;61:736-741.
2. Khuntia D, Reddy CA, Mahadevan A, Klein EA, Kupelian PA. Recurrence-free survival rates after external-beam radiotherapy for patients with clinical T1-T3 prostate carcinoma in the prostate-specific antigen era: what should we expect? Cancer. 2004;100:1283-92.
3. Bander NH. Technology insight: monoclonal antibody imaging of prostate cancer. Nat Clin Pract Urol. 2006;3:216-225.
4. Eder M, Eisenhut M, Babich J, Haberkorn U. PSMA as a target for radiolabelled small molecules. Eur J Nucl Med Mol Imaging. 2013;40:819-823.
5. Schäfer M, Bauder-Wüst U, Leotta K, et al. A dimerized urea-based inhibitor of the prostate-specific membrane antigen for 68Ga-PET imaging of prostate cancer. EJNMMI Res. 2012;2:23.
6. Eder M, Schäfer M, Bauder-Wüst U, et al. 68Ga-complex lipophilicity and the targeting property of a urea-based PSMA inhibitor for PET imaging. Bioconjug Chem. 2012;23:688-697.
7. Afshar-Oromieh A, Haberkorn U, Eder M, Eisenhut M, Zechmann CM. [68Ga]Gallium-labelled PSMA ligand as superior PET tracer for the diagnosis of prostate cancer: comparison with 18F-FECH. Eur J Nucl Med Mol Imaging. 2012;39:1085-1086.
8. Afshar-Oromieh A, Malcher A, Eder M, et al. PET imaging with a [68Ga]gallium-labelled PSMA ligand for the diagnosis of prostate cancer: biodistribution in humans and first evaluation of tumour lesions. Eur J Nucl Med Mol Imaging. 2013;40:486-495.
9. Afshar-Oromieh A, Zechmann CM, Malcher A, et al. Comparison of PET imaging with a (68)Ga-labelled PSMA ligand and (18)F-choline-based PET/CT for the diagnosis of recurrent prostate cancer. Eur J Nucl Med Mol Imaging. 2014;41:11-20.
10. Morigi JJ, Stricker PD, van Leeuwen PJ, et al. Prospective Comparison of 18F-Fluoromethylcholine Versus 68Ga-PSMA PET/CT in Prostate Cancer Patients Who Have Rising PSA After Curative Treatment and Are Being Considered for Targeted Therapy. J Nucl Med Off Publ Soc Nucl Med. 2015;56:1185-1190.
11. Schwenck J, Rempp H, Reischl G, et al. Comparison of (68)Ga-labelled PSMA-11 and (11)C-choline in the detection of prostate cancer metastases by PET/CT. Eur J Nucl Med Mol Imaging. 2017;44:92-101.
12. Afshar-Oromieh A, Avtzi E, Giesel FL, et al. The diagnostic value of PET/CT imaging with the (68)Ga-labelled PSMA ligand HBED-CC in the diagnosis of recurrent prostate cancer. Eur J Nucl Med Mol Imaging. 2015;42:197-209.
13. Afshar-Oromieh A, Holland-Letz T, Giesel FL, et al. Diagnostic performance of (68)Ga-PSMA-11 (HBED-CC) PET/CT in patients with recurrent prostate cancer: evaluation in 1007 patients. Eur J Nucl Med Mol Imaging. May 2017.
14. Marchal C, Redondo M, Padilla M, et al. Expression of prostate specific membrane antigen (PSMA) in prostatic adenocarcinoma and prostatic intraepithelial neoplasia. Histol Histopathol. 2004;19:715-718.
15. Kasperzyk JL, Finn SP, Flavin R, et al. Prostate-specific membrane antigen protein expression in tumor tissue and risk of lethal prostate cancer. Cancer Epidemiol Biomark Prev Publ Am Assoc Cancer Res Cosponsored Am Soc Prev Oncol. 2013;22:2354-2363.
16. Eiber M, Maurer T, Souvatzoglou M, et al. Evaluation of Hybrid 68Ga-PSMA Ligand PET/CT in 248 Patients with Biochemical Recurrence After Radical Prostatectomy. J Nucl Med Off Publ Soc Nucl Med. 2015;56:668-674.
17. Sahlmann C-O, Meller B, Bouter C, et al. Biphasic 68Ga-PSMA-HBED-CC-PET/CT in patients with recurrent and high-risk prostate carcinoma. Eur J Nucl Med Mol Imaging. 2016;43:898-905.
18. Herlemann A, Wenter V, Kretschmer A, et al. 68Ga-PSMA Positron Emission Tomography/Computed Tomography Provides Accurate Staging of Lymph Node Regions Prior to Lymph Node Dissection in Patients with Prostate Cancer. Eur Urol. 2016;70:553-557.
19. Wright GL Jr, Grob BM, Haley C, et al. Upregulation of prostate-specific membrane antigen after androgen-deprivation therapy. Urology. 1996;48:326-34.
20. Hope TA, Truillet CC, Ehman EC, et al. Imaging Response to Androgen Receptor Inhibition Using 68Ga-PSMA-11 PET: First Human Experience. J Nucl Med Off Publ Soc Nucl Med. September 2016.
21. Evans MJ, Smith-Jones PM, Wongvipat J, et al. Noninvasive measurement of androgen receptor signaling with a positron-emitting radiopharmaceutical that targets prostate-specific membrane antigen. Proc Natl Acad Sci U S A. 2011;108:9578-9582.
22. Afshar-Oromieh A, Debus N, Uhrig M, et al. Impact of long-term androgen deprivation therapy on PSMA ligand PET/CT in patients with castration-sensitive prostate cancer. Eur J Nucl Med Mol Imaging. July 2018.
23. Zechmann CM, Afshar-Oromieh A, Armor T, et al. Radiation dosimetry and first therapy results with a (124)I/ (131)I-labeled small molecule (MIP-1095) targeting PSMA for prostate cancer therapy. Eur J Nucl Med Mol Imaging. 2014;41:1280-1292.
24. Afshar-Oromieh A, Haberkorn U, Zechmann C, et al. Repeated PSMA-targeting radioligand therapy of metastatic prostate cancer with (131)I-MIP-1095. Eur J Nucl Med Mol Imaging. 2017;44:950-959.
25. Kratochwil C, Giesel FL, Stefanova M, et al. PSMA-Targeted Radionuclide Therapy of Metastatic Castration-Resistant Prostate Cancer with 177Lu-Labeled PSMA-617. J Nucl Med Off Publ Soc Nucl Med. 2016;57:1170-1176.
26. Rahbar K, Ahmadzadehfar H, Kratochwil C, et al. German Multicenter Study Investigating 177Lu-PSMA-617 Radioligand Therapy in Advanced Prostate Cancer Patients. J Nucl Med Off Publ Soc Nucl Med. 2017;58:85-90.
27. Hofman MS, Violet J, Hicks RJ, et al. [177Lu]-PSMA-617 radionuclide treatment in patients with metastatic castration-resistant prostate cancer (LuPSMA trial): a single-centre, single-arm, phase 2 study. Lancet Oncol. 2018;19:825-833.
28. Bräuer A, Grubert LS, Roll W, et al. 177Lu-PSMA-617 radioligand therapy and outcome in patients with metastasized castration-resistant prostate cancer. Eur J Nucl Med Mol Imaging. 2017;44:1663-1670.
29. Afshar-Oromieh A, Babich JW, Kratochwil C, et al. The Rise of PSMA Ligands for Diagnosis and Therapy of Prostate Cancer. J Nucl Med Off Publ Soc Nucl Med. 2016;57:79S-89S.
info@onco-suisse
- Vol. 9
- Ausgabe 2
- April 2019