- Toxizitäten bei Therapie mit Antikörper-Wirkstoff-Konjugaten
Antikörper-Wirkstoff-Konjugate (Antibody Drug Conjugates, ADC) gewinnen bei der Therapie zahlreicher Krebserkrankungen zunehmend an Bedeutung. Die ADC verbinden die Spezifität von Antikörpern mit der Wirkung von Toxinen. Doch obschon ADC sehr gezielt in den Tumorzellen wirken, weist jedes einzelne ADC-Arzneimittel spezifische Toxizitäten auf, die in der Onkologie nicht häufig beschrieben sind. Dieser Artikel bietet einen Überblick über die Nebenwirkungen, insbesondere auch das dermatologische Nebenwirkungsprofil, und zeigt präventive und therapeutische Interventionsstrategien auf.
Antikörper-Wirkstoff-Konjugate (ADC) haben aufgrund ihrer effektiven Wirkungsweise zu erheblichen Fortschritten in der Onkologie geführt. Zahlreiche ADC sind zugelassen und mehr als 100 befinden sich in der klinischen Entwicklung (1, 2). ADC bestehen aus drei Bestandteilen:
• Monoklonaler Antikörper, der gegen ein bestimmtes Tumorantigen gerichtet ist
• Zytostatikum (als Payload oder Warhead bezeichnet)
• Linker, der das Zytostatikum mit dem Antikörper verbindet
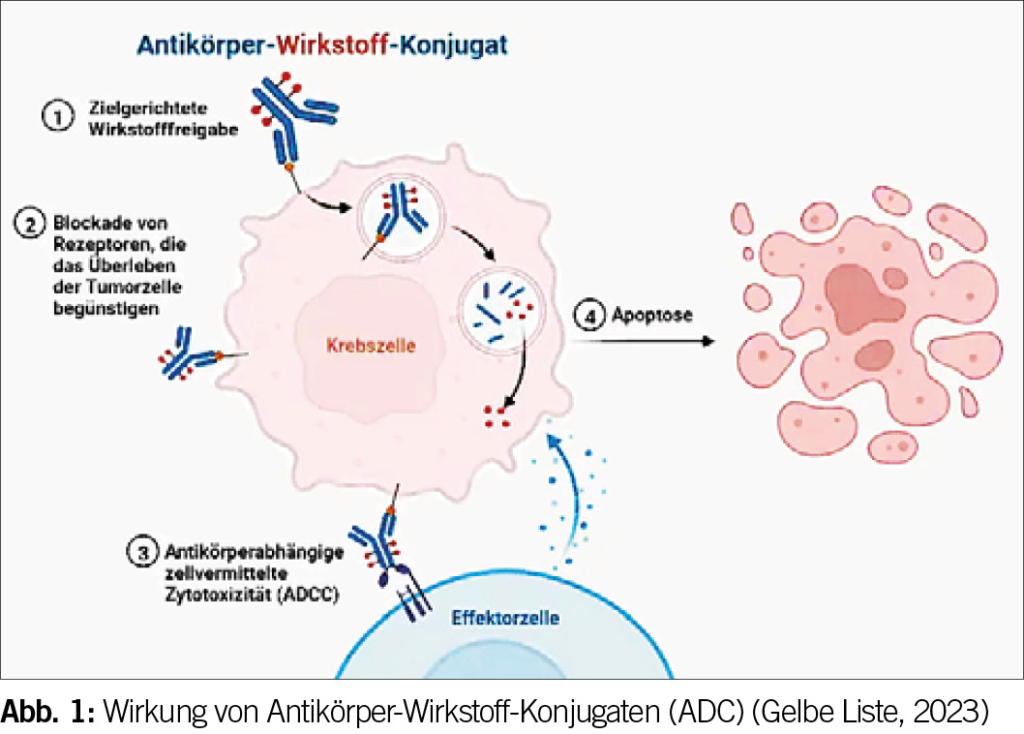
Die Antikörper der ADC sind als natürliche Bestandteile des Immunsystems in der Lage, Antigene zu erkennen und an diese zu binden. Antigene sind Strukturen, die sich auf der Oberfläche oder im Inneren einer Zelle befinden. An die Antikörper im ADC wird ein Zytostatikum gekoppelt. Ein ADC funktioniert wie ein trojanisches Pferd: Sobald der Antikörper an die Zielzelle angedockt hat, wird der ADC als Ganzes in die Zelle aufgenommen. Das Zytostatikum wird im Zellinneren vom Linker gelöst, und erst dann beginnt seine Wirkung. In manchen ADC werden Zellgifte verwendet, welche die Mikrotubuli-Polymerisation blockieren und dadurch den programmierten Zelltod einleiten. Die malignen Zellen lösen die zelltoxischen Prozesse über zelleigene, ADC-spaltende oder ADC-abbauende Enzyme selbst aus (Abb. 1).
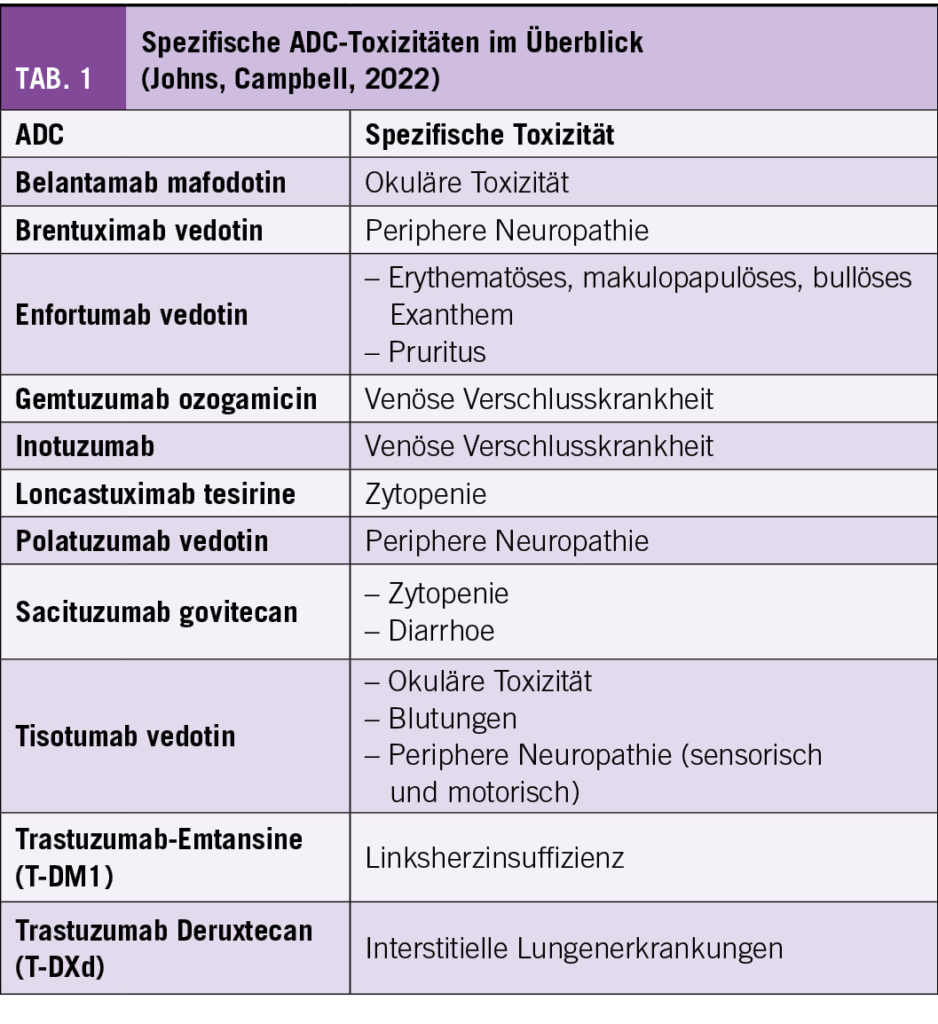
ADC wirken sehr präzise, weil die Antikörper spezifisch gegen Antigene gerichtet sind, die auf den Krebszellen vorkommen. Zytostatika können so in definierte Tumorzellen eingeschleust werden. Gesunde Zellen ohne das spezifische Oberflächenantigen werden weitgehend geschont. So lassen sich systemische Auswirkungen des eingesetzten Zellgifts und damit verbundene Nebenwirkungsrisiken minimieren. Und dennoch, ganz nebenwirkungsfrei sind auch ADC nicht (Tab. 1).
Spezifische ADC-Toxizitäten
Die Nebenwirkungen von ADC können je nach spezifischem Konjugat und individueller Reaktion der Patientinnen und Patienten stark variieren. Augen, Lungen, Haut und Nervensystem sind besonders häufig betroffen. Die Inzidenz von Infusionsreaktionen variiert je nach Konjugat und kann zwischen 10% und 50% liegen; die Symptome umfassen Fieber, Schüttelfrost, Übelkeit, Erbrechen, Kopfschmerzen, Hautausschlag und Atembeschwerden. Im Allgemeinen berichten etwa 50% der Patientinnen und Patienten über Fatigue und Asthenie. Auch die Inzidenz hämatologischer und gastrointestinaler Toxizitäten variiert je nach Konjugat und Dosierung (10-40%).
Dermatologisches Nebenwirkungsprofil
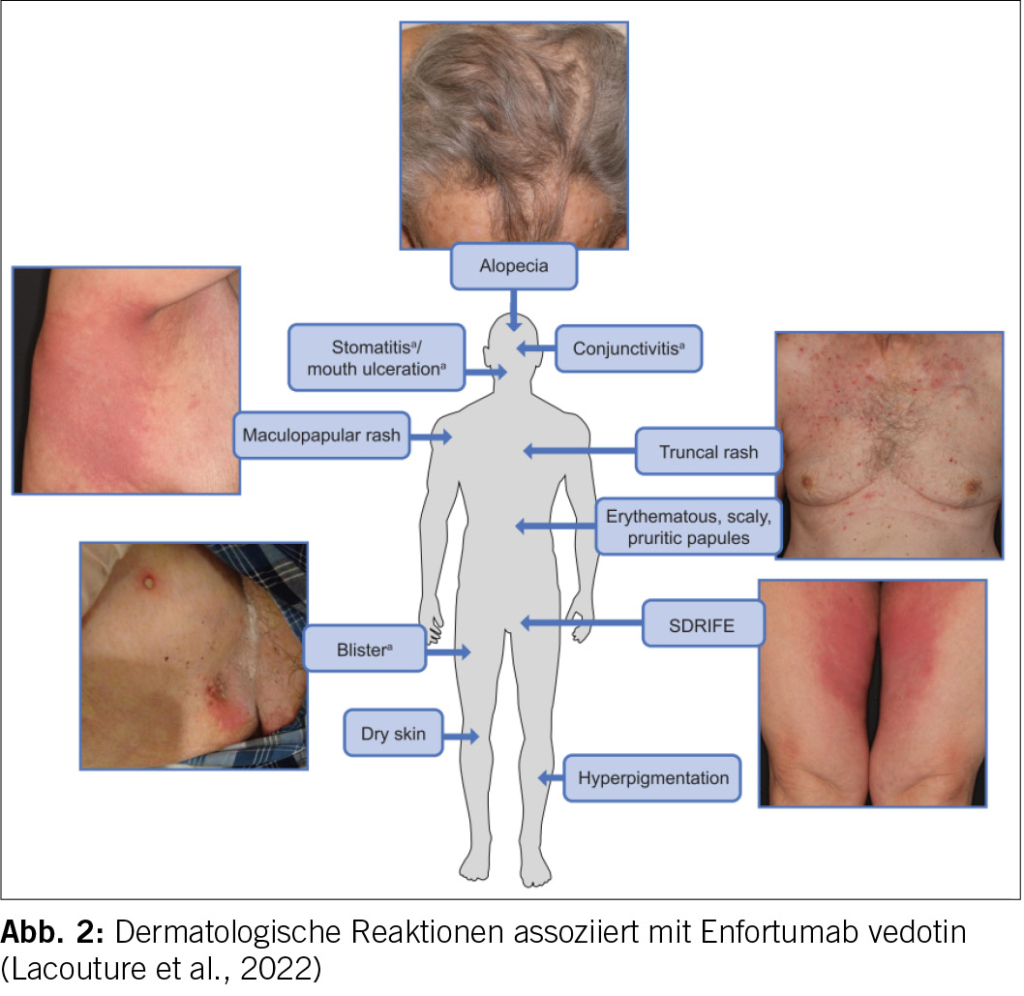
Häufigkeit und Schwergrad der Reaktionen an Haut, Schleimhaut, Haaren und Nägeln können je nach spezifischem ADC und individueller Reaktion variieren. Toxizität an Haarfollikeln (Alopezie an Kopfhaut oder Follikulitis an anderen Lokalisationen), Nägeln (Brüchigkeit, Struktur- oder Pigmentveränderungen bis zur Onycholyse) und Mukosa (generalisierte Mukositis, insbesondere oral, genital und okulär) zeigen sich bei vielen ADC. So führt die Behandlung mit Belantamab mafodotin und Tisotumab vedotin sehr häufig zu Konjunktivitis, Keratitis sicca sowie verringertem und verschwommenem Sehen. Bei der Anwendung von Enfortumab vedotin als Monotherapie leiden etwa 55 % der Patientinnen und Patienten innerhalb des ersten Behandlungszyklus an dermatologischen Reaktionen (Abb. 2). Die häufigsten Manifestationen sind makulopapulöses Exanthem (44%) und Pruritus (33%). Von einem Schweregrad ≥3 sind etwa 14,5% der Patientinnen und Patienten betroffen; die Symptome sind makulopapulöses oder erythematöses Exanthem, symmetrisches intertriginöses und flexurales Exanthem, bullöse oder exfoliative Dermatitis und palmar-plantares Erythrodysästhesie-Syndrom (4). Alopezie zeigt sich bei >45% der Behandelten (5/6). Unter Belantamab mafodotin und Tisotumab vedotin zeigt sich insbesondere die okuläre und mukosale Toxizität (5).
Präventive Strategien und Empfehlungen zur Basispflege
Es ist wichtig, dermatologische Reaktionen möglichst früh zu erkennen. Daher sollen Patientinnen und Patienten ab Behandlungsbeginn und während dem gesamten Therapieverlauf engmaschig und regelmässig auf dermatologische Nebenwirkungen überwacht werden (5). Eine frühzeitige Erfassung von Veränderungen kann den Bedarf an Notfallinterventionen deutlich verringern, das Risiko für Dosisreduktionen oder Therapieabbrüche reduzieren und die Lebensqualität verbessern. Die Patientinnen und Patienten müssen informiert werden über mögliche Symptome, Basispflege-Interventionen und «Red Flags» für die Kontaktaufnahme mit dem Behandlungsteam (Tab. 2).
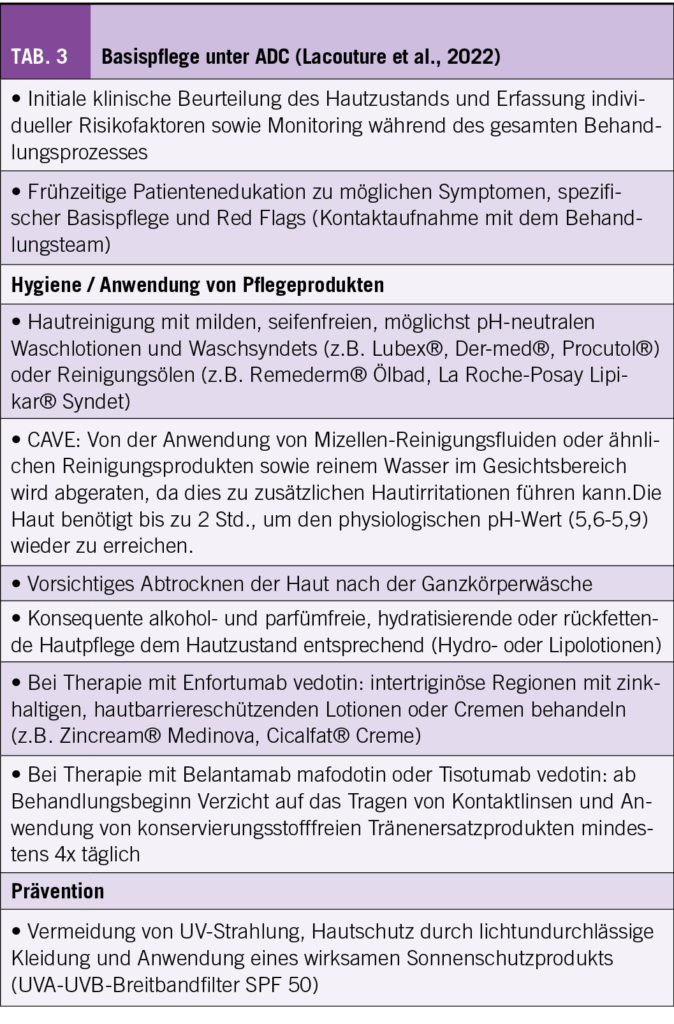
Allen Patientinnen und Patienten wird ab Behandlungsbeginn eine konsequente, alkohol- und parfümfreie, hydratisierende oder rückfettende Hautpflege dem Hautzustand entsprechend (Hydro- oder Lipolotionen) empfohlen. Unter Therapien mit Enfortumab vedotin wird zudem empfohlen, die intertriginösen Hautbereiche wie Achselhöhlen oder Leistengegend mit einer zinkhaltigen Feuchtigkeitscreme zu schützen. Die Belastung der Haut mit UV-Strahlung sollte während der ganzen Behandlung vermieden werden mittels Hautschutz durch lichtundurchlässige Kleidung und die Anwendung eines wirksamen Sonnenschutzproduktes (UVA-UVB-Breitbandfilter SPF 50). Ansonsten gelten die gleichen präventiven Interventionen wie bei anderen Onkologika-Therapien. Es werden milde, seifenfreie, möglichst pH-neutrale Waschlotionen oder Reinigungsöle empfohlen. Nach dem Baden oder Duschen sollte die Haut vorsichtig abgetrocknet werden, um Reizungen zu vermeiden (Tab. 3).
Da bei den ADC Belantamab mafodotin und Tisotumab vedotin eine okuläre Toxizität erwartet wird, empfiehlt man den Patientinnen und Patienten, ab Behandlungsbeginn mindestens 4x täglich konservierungsstofffreie Tränenersatzprodukte anzuwenden und auf das Tragen von Kontaktlinsen zu verzichten.
Die Broschüre der Onkologiepflege Schweiz zur Prävention von Veränderungen an Haut, Schleimhaut, Haaren und Nägeln bietet dazu eine gute Unterstützung (auf Deutsch, Französisch und Italienisch kostenlos zum Download verfügbar unter www.onkologiepflege.ch).
Therapeutische Interventionsstrategien
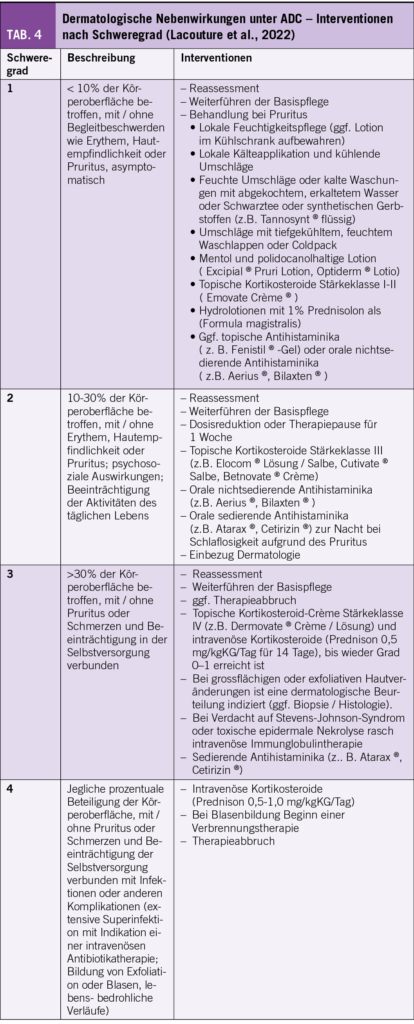
Die Behandlung ADC-assoziierter dermatologischer Reaktionen erfordert eine individuelle Herangehensweise, abhängig vom Schweregrad. Situativ kann eine Dosisreduktion oder Therapiepause erforderlich sein. Bei milden Hautreaktionen ist die Behandlung mit topischen Kortikosteroiden oder juckreizlindernden Dermatika in der Regel ausreichend, wobei die Empfehlungen zur Basispflege bis zu einem Schweregrad 2 fortgesetzt werden sollen. Bei schwerwiegenderen Reaktionen kann eine systemische Behandlung mit oralen oder intravenösen Steroiden indiziert sein, um die Entzündung zu kontrollieren. Antihistaminika und kühlende Dermatika können zur Symptomlinderung beitragen. Dabei ist die frühzeitige multiprofessionelle und multidisziplinäre Herangehensweise entscheidend, wie der Einbezug von Fachpersonen der Dermatologie ab einem Schweregrad 2 (Tab. 4).
Mukosale Toxizitäten und Veränderungen an den Haaren und Nägeln werden symptomatisch angegangen, wobei die gleichen Interventionen gelten wie bei anderen Onkologika-Therapien. Die Empfehlungen der Onkologiepflege Schweiz «Dermatologische Reaktionen unter medikamentöser Tumortherapie. Prävention und Interventionen» bietet dazu einen umfassenden Überblick.
Fazit
Werden Dermatotoxizitäten assoziiert mit ADC nicht frühzeitig und adäquat behandelt, können sie weitreichende Auswirkungen haben. Sie gefährden die Therapieadhärenz, die Durchführung der wirksamen Antitumortherapie, die Lebensqualität der Patientinnen und Patienten und erhöhen die Behandlungskosten. Eine systematische, gemeinsame Herangehensweise innerhalb des interprofessionellen und interdisziplinären Behandlungsteams hat einen positiven Einfluss auf Betreuungsqualität, Patientenzufriedenheit und Kosteneffizienz und sollte daher zwingend angestrebt werden. Die Herausforderungen an das gesamte onkologische Behandlungsteam sind umfassend und bedingen eine sorgfältige Absprache untereinander und ein proaktives Vorgehen.
Erstpublikation in der Zeitschrift Onkologiepflege 2023/4
Cornelia Kern Fürer
Dipl. Pflegefachperson HF/BScN, MAS
HöFa I Onkologische Pflege
Pflegeexpertin Onkologie, Spital Grabs
Co-Leitung Weiterbildungen, Onkologiepflege Schweiz
Fachdozentin an diversen Bildungsinstitutionen
7000 Chur
1. Zhu Y, Liu K, Wang K, Zhu H. Treatment-related adverse events of antibody-drug conjugates in clinical trials: A systematic review and meta-analysis. Cancer. 2023 Jan 15;129(2):283-295. doi: 10.1002/cncr.34507. Epub 2022 Nov 21. PMID: 36408673; PMCID: PMC10099922.
2. Johns AC, Campbell MT. Toxicities From Antibody-Drug Conjugates. Cancer J. 2022 Nov-Dec 01;28(6):469-478. doi: 10.1097/PPO.0000000000000626. PMID: 36383910.
3. Donaghy H. Effects of antibody, drug and linker on the preclinical and clinical toxicities of antibody-drug conjugates. MAbs. 2016 May-Jun;8(4):659-71. doi: 10.1080/19420862.2016.1156829. Epub 2016 Apr 5. PMID: 27045800; PMCID: PMC4966843.
4. Seagen and Astellas Pharma US Inc. Padcev (enfortumab vedotinejfv) for injection [prescribing information]. 2021. Available at https://astellas.us/docs/PADCEV_label.pdf. Accessed July 13, 2021.
5. Lacouture ME, Patel AB, Rosenberg JE, et al. Management of dermatologic events associated with the nectin-4–directed antibody-drug conjugate enfortumab vedotin. Oncologist. 2022;27:e223–e232.
6. Powles T, Rosenberg JE, Sonpavde GP, et al. Enfortumab vedotin in previously treated advanced urothelial carcinoma. N Engl J Med. 2021;384:1125–1135
7. Gelbe Liste (2023) Antikörper Wirkstoff Konjugate. https://www.gelbe-liste.de/wirkstoffgruppen/antikoerper-wirkstoff-konjugate