- Übersicht und Expertenkommentar zu 6 klinischen Fragestellungen
Die amerikanische Gesellschaft für klinische Onkologie (ASCO) hat kürzlich im Journal of Clinical Oncology (JCO) ihre aktualisierten Empfehlungen zur Verhinderung und Behandlung von venösen Thromboembolien bei Patienten mit Krebs publiziert. Es handelt sich hierbei um eine Aktualisierung der Empfehlungen von 2015, die damals gegenüber den Empfehlungen von 2013 im Wesentlichen unverändert waren. Die jetzige Aktualisierung der Empfehlungen gegenüber der publizierten Version von 2015 unterscheidet sich vor allem durch den Einschluss der direkten oralen Antikoagulantien (DOACs), von denen in der Schweiz als Thrombin-Inhibitor das Dabigatran (Pradaxa) und als F Xa-Inhibitoren das Rivaroxaban (Xarelto), Apixaban (Eliquis) und Edoxaban (Lixiana) kommerziell verfügbar sind. Daher wird sich diese Übersicht vor allen Dingen mit der Anwendung von DOACs in Situationen beschäftigen, die durch sechs klinische Fragen beschrieben werden, auf denen die Empfehlungen der ASCO beruhen.
L’ American Society for Clinical Oncology (ASCO) a récemment publié dans le Journal of Clinical Oncology (JCO) ses recommandations actualisées pour la prévention et le traitement de la thromboembolie veineuse chez les patients atteints de cancer. Il s’ agit d’ une mise à jour des recommandations de 2015 qui étaient essentiellement inchangées par rapport aux recommandations de 2013. La mise à jour actuelle des recommandations diffère de la version publiée de 2015 principalement par l’ inclusion des anticoagulants oraux directs (DOAC), dont le dabigatran (Pradaxa) est disponible sur le marché suisse en tant qu’ inhibiteur de la thrombine et le rivaroxaban (Xarelto), l’ apixaban (Eliquis) et l’ edoxaban (Lixiana) sont disponibles comme inhibiteurs F Xa. Par conséquent, cet aperçu portera principalement sur l’ utilisation des DOAC dans des situations fondées sur six questions cliniques sur lesquelles se fondent les recommandations de l’ ASCO.
1. Sollten hospitalisierte Patienten mit aktivem Malignom eine Thromboembolie Prophylaxe erhalten?
Hospitalisierte Patienten mit aktivem Malignom sollten immer eine Thromboembolie-Prophylaxe erhalten, wenn keine Blutungsneigung oder unmittelbare Kontraindikationen bestehen. Dieser Grundsatz wird auch von der ASCO-Expertengruppe aufrechterhalten. Allerdings lassen die Experten offen, ob hospitalisierte Patienten ohne zusätzliche Risikofaktoren bei aktivem Malignom zwingend eine Thromboembolie-Prophylaxe erhalten sollten. Nach den ASCO-Guidelines brauchen Patienten mit aktivem Malignom keine Thromboembolie-Prophylaxe, wenn sie lediglich zu kleineren Prozeduren oder zur Chemotherapie hospitalisiert werden bzw. eine Stammzelltransplantation durchführen lassen.
Quintessenz und Kommentar: Bei hospitalisierten Patienten mit aktivem Malignom sollte bei Abwesenheit von Komplikationen oder Kontraindikationen die Thromboembolie-Prophylaxe die Regel sein. Ausnahmen davon sollten aktiv begründet werden müssen. Eine Datenerhebung in der Schweiz (Kucher et al., Ann Oncol, 2010) zeigte, dass Patienten, die nach einer Hospitalisation eine Thromboembolie entwickelt haben, zu einem relevanten Teil während der Hospitalisation keine adäquate Thromboembolie-Prophylaxe erhalten haben. Dies spricht dafür, dass hospitalisierte Patienten mit aktivem Malignom auch ohne zusätzliche Risikofaktoren eine Thromboembolie-Prophylaxe erhalten sollten, solange keine Kontraindikationen oder Blutungsneigung bestehen. Bei Patienten mit kleinen Prozeduren scheint das vorgeschlagene Vorgehen dann sinnvoll, wenn vorher keinerlei Thromboembolie nachgewiesen worden ist. War hingegen eine Thromboembolie in der Vergangenheit bekannt, dann sollte auch bei kleinerem Risiko eine Thromboembolie-Prophylaxe durchgeführt werden, wenn keine Komplikationen oder Kontraindikationen bestehen.
2. Sollten ambulante Patienten mit aktivem Malignom, die sich einer systemischen Chemotherapie unterziehen, während dieser Zeit eine Thromboseprophylaxe erhalten?
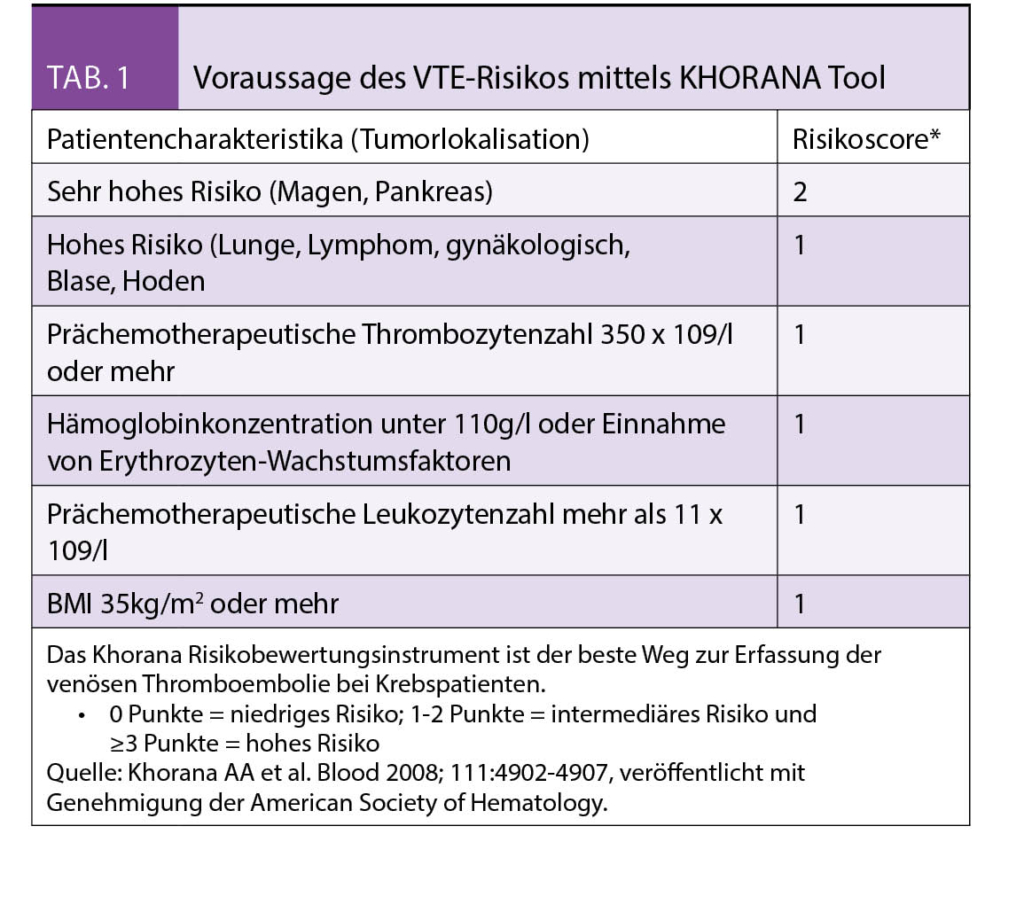
Ambulante Patienten mit aktivem Malignom benötigen keine pharmakologische Thromboembolie-Prophylaxe. Hier sind allerdings die wichtigen, später in den ASCO-Empfehlungen formulierten Ausnahmen zu berücksichtigen. Dazu gehören Patienten mit hohem Risiko (Khorana Score ≥ 2, Tabelle 1). Diese können in Abwesenheit von Komplikationen und Kontraindikationen mit niedrigmolekularem Heparin (NMH) oder DOACs therapiert werden. Eine weitere, möglicherweise noch wichtigere Ausnahme stellt die Behandlung mit Thalidomid- oder Lenalidomid-haltiger Therapie beim multiplen Myelom dar. Hier sollte auf jeden Fall eine antithrombotische Prophylaxe durchgeführt werden, wobei diese aus meiner Sicht primär mit NMH durchgeführt werden sollte. Erste Beobachtungen zeigen, dass eine solche Prophylaxe auch mit DOACs möglich ist. Die entsprechenden prospektiven kontrollierten Studien dazu fehlen jedoch noch.
Quintessenz und Kommentar: Ambulante Patienten mit aktivem Malignom benötigen generell keine medikamentöse Thromboembolie-Prophylaxe, mit zwei Ausnahmen: bei hohem Risiko (Khorana score ≥ 2) oder Myelombehandlung mit einem Thalidomid- oder Lenalidomid-haltigen Präparat.
3. Sollten Patienten mit aktivem Malignom, die sich einem chirurgischen Eingriff unterziehen müssen, eine perioperative Thromboseprophylaxe erhalten?
Alle Patienten mit aktivem Malignom, die sich einem chirurgischen Eingriff mittleren bis grösseren Ausmasses unterziehen müssen, sollten eine perioperative pharmakologische Thromboembolie-Prophylaxe erhalten. Diese sollte mittels NMH durchgeführt werden, wenn keine Komplikationen im Sinne eines erhöhten Blutungsrisikos oder Kontraindikationen bestehen. Dabei sollte die perioperative Prophylaxe präoperativ begonnen werden. Die pharmakologische Thromboembolie-Prophylaxe ist die Behandlung der Wahl, kann aber durch mechanische Kompressionsmethoden ergänzt werden (und zeigt dann möglicherweise sogar eine erhöhte Effizienz). Mechanische Kompressionsmethoden sollten aber niemals als alleinige Behandlungsmodalität verwendet werden, es sei denn, die pharmakologische Thromboembolie-Prophylaxe wäre kontraindiziert. Die pharmakologische Thrombose-Prophylaxe bei Patienten mit aktivem Malignom und mittlerem bis grösserem chirurgischen Eingriff sollte postoperativ mindestens für 7-10 Tage fortgeführt werden, Patienten mit grösserer abdominaler oder pelviner Chirurgie sollten bis zu vier Wochen postoperativ behandelt werden.
Quintessenz und Kommentar: Die perioperative Thromboembolie-Prophylaxe bei Malignom-Patient mit chirurgischen Eingriffen sollte präoperativ beginnen und postoperativ eine Woche bzw. vier Wochen nach abdominaler oder pelviner Chirurgie fortgesetzt werden. Dabei sollte die Behandlungsindikation bei fehlenden Komplikationen und Kontraindikationen eher liberal gestellt werden.
4. Welche ist die beste Methode, bei Patienten mit aktivem Malignom und nachgewiesener Thromboembolie ein Thromboembolie-Rezidiv zu verhindern?
Die initiale Behandlung einer nachgewiesenen Thromboembolie bei einem Patienten mit aktivem Malignom kann mit einer der entsprechend zugelassenen Medikationen (inkl. DOACs) durchgeführt werden. Bei Verwenden von Heparin sollte niedrigmolekulares Heparin bevorzugt eingesetzt werden. Zu längerfristiger Antikoagulation im Sinne der Rezidivprophylaxe empfiehlt die ASCO-Expertengruppe die Gabe von NMH, Edoxaban oder Rivaroxaban vor der Gabe von Vitamin-K-Antagonisten. Eine langfristige Antikoagulation sollte bei Patienten mit weiter bestehendem, aktivem Malignom bzw. über längere Zeit verabreichte Chemotherapie in Betracht gezogen werden. Die Verwendung von Vena Cava Filtern sollte laut ASCO-Guidelines nur bei Vorliegen einer absoluten Kontraindikation zur Antikoagulation bei akuten Thromboembolien innerhalb der letzten vier Wochen in Betracht gezogen werden. (In einer kürzlich veröffentlichten, randomisierten Studie bei Trauma-Patienten (Kwok et al, NEJM, 2019) zur Fragestellung der Vena Cava Filter führte deren früher Einsatz nicht zu einer Reduktion der symptomatischen Lungenembolien oder von Todesfällen bis 90 Tage nach Filtereinsatz. Ein möglicher Benefit zeigte sich nur bei Patienten, die nicht innerhalb von sieben Tagen nach Filtereinsatz antikoaguliert werden konnten.)
Patienten mit primären oder sekundären ZNS-Malignomen und bestehender Thromboembolie wie auch Patienten mit inzidentell festgestellter Thromboembolie sollten auch so wie andere Malignom-Patienten behandelt werden.
Bei Patienten mit isolierten subsegmentalenLungenembolien oder viszeralen venösen Thrombosen sollte nach spezifischer Beurteilung eine antithrombotische Therapie in Betracht gezogen werden; bei solchen Krankheitsbildern ist insbesondere auch an die Möglichkeit myeloproliferativer Erkrankungen zu denken.
Quintessenz und Kommentar: Die Behandlung einer akuten Thromboembolie mit einem der zugelassenen Antithrombotika stellt, unabhängig von der Genese der Thromboembolie, immer eine On-label-Behandlung dar (dies gilt ebenso für die Rezidivprophylaxe). Thromboembolien bei Tumorpatienten (auch bei ZNS-Befunden, wobei hier potentielle Blutungskomplikationen immer in die differenzialtherapeutischen Überlegungen einzubeziehen sind) können heute auch mit DOACs behandelt werden, wobei die aktuelle Datenlage vor allem Edoxaban oder Rivaroxaban präferiert, allerdings ist dabei von einem Klasseneffekt auszugehen. Bei ausgeprägten und/oder grossvolumigen Befunden sollte weiterhin, mindestens initial, die Behandlung mit NMH in Betracht gezogen werden, da hier (im Gegensatz zu den DOACs) sowohl ein anti-Xa wie auch ein anti-IIa Effekt zum Tragen kommt. Nach allen verfügbaren Daten ist der Einsatz von Vena Cava Filtern bei Tumorpatienten nicht mit einem besseren Outcome, jedoch mit einer (potentiell) höheren Komplikationsrate vergesellschaftet.
5. Sollten Patienten mit aktivem Malignom, aber ohne nach-gewiesene Thromboembolie, eine antithrombotische Therapie erhalten um zu versuchen, das Überleben zu verlängern?
Antikoagulantien sollten bei Patienten mit Malignomen ohne Thromboembolien nicht eingesetzt werden, um zu versuchen, das Ansprechen auf eine Chemotherapie zu verbessern oder eine Lebensverlängerung zu erreichen.
Quintessenz und Kommentar: Es liegen bisher keine überzeugenden Daten vor, die den Einsatz von Antikoagulantien als Zusatz zu einer Chemotherapie oder als Primärprophylaxe unterstützen. Hingegen sollte nicht vergessen werden, dass der Einsatz von Antikoagulantien in der Rezidivprophylaxe tatsächlich zu einer Verbesserung des klinischen Verlaufes beiträgt.
6. Was ist bekannt über den Sinn einer Risikostratifizierung bei Patienten mit aktivem Malignom und was ist bekannt über das Bewusstsein der Patienten zu dieser Problematik?
Bei Tumorpatienten variiert das Thromboembolie-Risiko innerhalb der Population substantiell. Daher sollte eine periodische Beurteilung des Thromboembolie-Risikos erfolgen, insbesondere bei «Meilensteinen» der Behandlung wie Beginn einer Chemotherapie oder einer Hospitalisation. Individuelle Risikofaktoren (zum Beispiel Biomarker, Tumortyp) können ein individuell erhöhtes Risiko nur ungenügend identifizieren. Im ambulanten Bereich können validierte Scores wie zum Beispiel der Khorana Score (Tabelle 1) verwendet werden, um einen Entscheid über eine prophylaktische Behandlung zu unterstützen.
Dabei sollten Patienten durch das Behandlungsteam im Hinblick auf das Thromboembolie-Risiko, insbesondere zusätzliche Risikofaktoren wie grössere chirurgische Eingriffe und Immobilisation, aufgeklärt werden.
Quintessenz und Kommentar: Im stationären Bereich ist insbesondere die stringente, konsequente Vorgehensweise des vorgegebenen Procedere für die Prophylaxe relevant. Solange keine Prophylaxe durchgeführt wird, sollte bei allen Tumorpatienten konsequent eine repetitive Risikobeurteilung erfolgen; im Zweifelsfalle sollte die Indikation zur Prophylaxe bei Tumorpatienten liberal gestellt werden.
Zentrum für Labormedizin
Frohbergstrasse 3
9001 St. Gallen
wolfgang.korte@zlmsg.ch
Beyer, BMS, Daiichi Sankyo, Boehringer Ingelheim, Pfize