- Diabète de type 2 et néphropathie 2022
Depuis le dernier article paru dans la Gazette Médicale en 2017 (01 _ 2017 _ la gazette médicale _ info@geriatrie), il y a eu un changement historique de la prise en charge de patients diabétiques de type 2 présentant une néphropathie diabétique albuminurique. En effet des études randomisées contrôlées de haute qualité ont été publiées entre 2019 et 2022 et ont changé l’ algorithme de prise en charge (1,2). Cet article a pour but de refaire le point par rapport à la néphropathie diabétique
Epidémiologie et dépistage
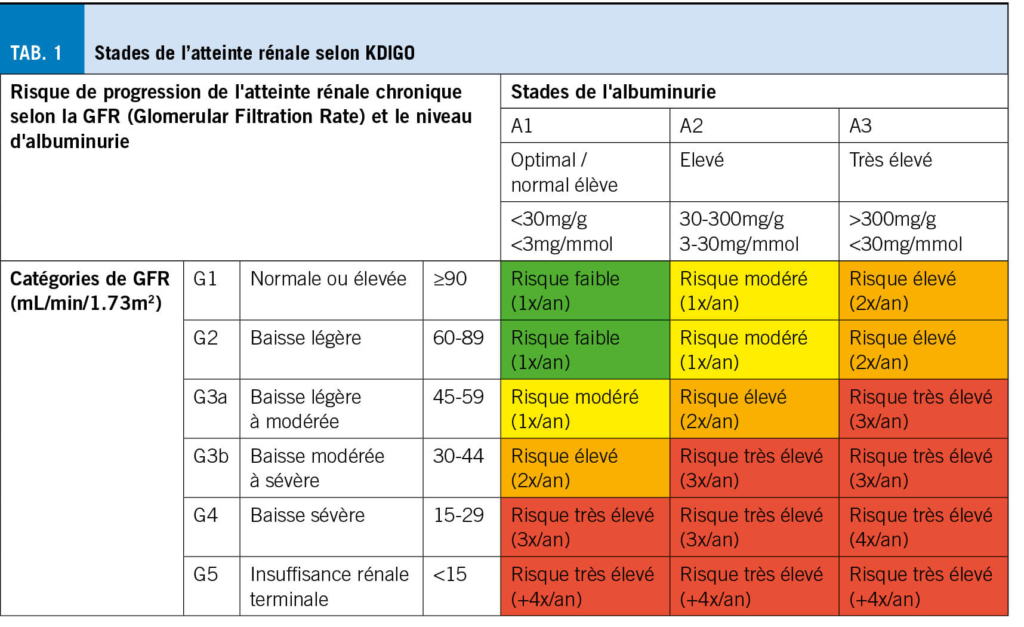
La prévalence de la néphropathie diabétique est en augmentation en raison du vieillissement de la population et de l’ augmentation de la prévalence du diabète de type 2. Le médecin de premier recours et le diabétologue restent en première ligne pour le dépistage de la néphropathie diabétique. Une évaluation annuelle avec une estimation de la filtration glomérulaire (eGFR selon CKD-EPI basé sur la créatinine) et un rapport albumine/créatinine urinaire sur un spot est recommandée chez tout adulte diabétique. Un stix ou sédiment urinaire sera fait pour compléter ce bilan et d’ autres causes d’ atteinte rénale seront recherchées en cas de sédiment pathologique. La fréquence des contrôles sera augmentée chez les personnes présentant déjà une néphropathie (Tab.1). On parle de maladie rénale chronique en cas d’ eGFR < 60ml/min/année et/ou lors d’ un stade A2-A3 de l’ albuminurie. Mais adapté à l’ âge, cette classification peut être affinée (si âge<40 ans <75ml/min/1.73 m2, si âge >65 ans <45ml/min/1.73 m2). Finalement tout patient avec un stade A3 de l’ albuminurie présente un déclin accéléré de la fonction rénale et nécessite une prise en charge multifactorialle intensive (contrôle glycémique, tensionnelle, lipidique, poids, tabac, adhésion au traitement…).
Algorithme de prise en charge
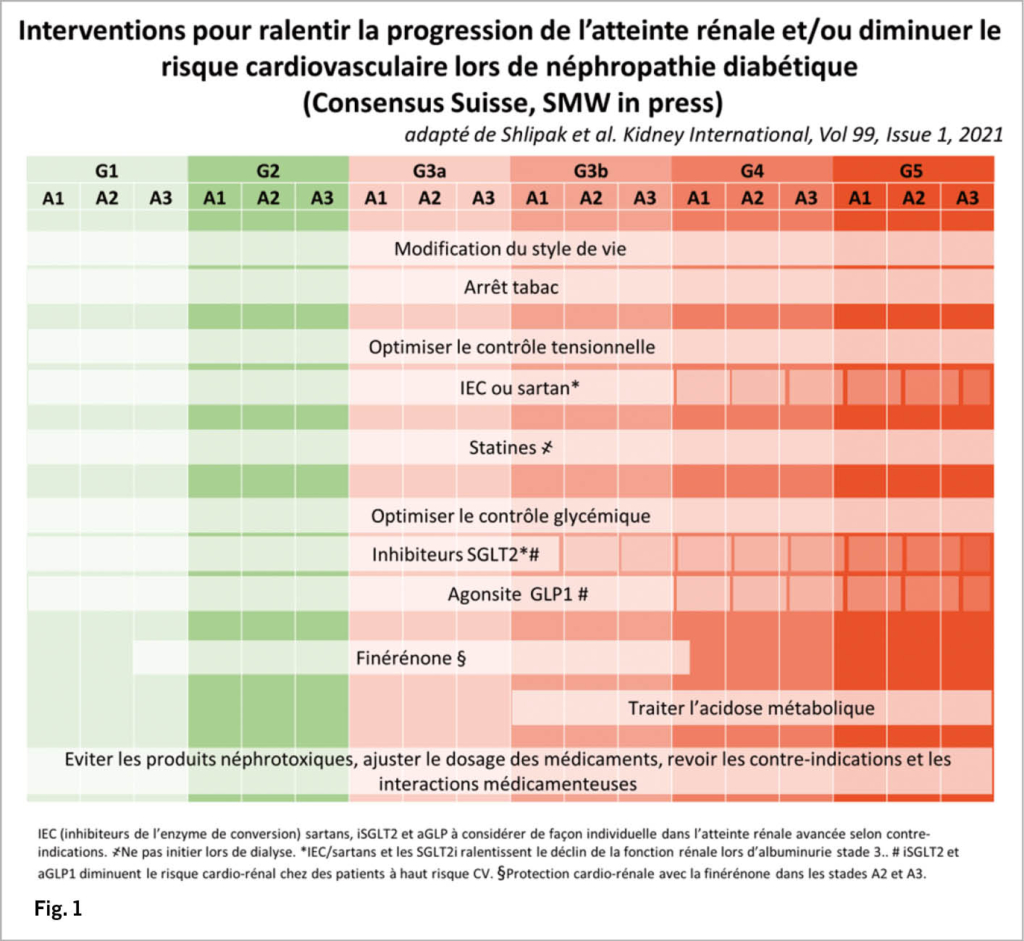
La prise en charge du patient avec une néphropathie diabétique est multiple et complexe. Un consensus suisse sur la néphropathie diabétique résume en détail les connaissances actuelles et la prise en charge thérapeutique (Fig.1) (2). Il y aura des objectifs chiffrés (glycémique, tensionnelle, lipidique) mais aussi des objectifs de protection rénale (IEC ou Sartan, SGLT2i, finérénone). Il sera important d’ exclure d’ autres causes d’ atteinte rénale (dans 20% des cas) et d’ adresser le patient au néphrologue en cas de doute. L’ objectif thérapeutique est d’ améliorer la qualité de vie tout en ralentissant le déclin de la fonction rénale et en diminuant le risque cardiovasculaire. La très grande majorité de patients diabétiques avec une néphropathie vont mourir de maladie cardiovasculaire avant d’ atteindre l’ insuffisance rénale terminale. La prise en charge multidisciplinaire s’ impose parfois avec un suivi médical, infirmier, diététique, pharmacien et podologique. L’ amélioration de l’ auto-soin et l’ adhésion au traitement sont aussi des facteurs qui peuvent avoir un impact positif sur le pronostic.
Médicaments néphroprotecteurs
IEC/Sartans: Le blocage du système rénine-angiotensine par les inhibiteurs de l’ enzyme de conversion ou les sartans sont en première ligne lors de néphropathie albuminurique. Les études qui remontent il y a plus de 20 ans montrent une diminution des événements rénaux. Par contre leur association (IEC, sartan, inhibiteur de la rénine) n’ est pas proposée car les études ont montré une augmentation des effets indésirables. Un dosage de la créatinine et de la kaliémie est proposé 1-2 semaines après le début du traitement qui sera mis en suspens en cas d’ élévation de la créatinine de plus de 30%. Une kaliémie élevée fera rechercher d’ autres causes favorisants comme les AINS, l’ acidose métabolique et l’ alimentation riche en potassium.
SGLT2 inhibiteurs (SGLT2i) (3,4,5,6) : Les SGLTi induisent une glucosurie en inhibant la réabsorption rénale de glucose/sodium. Ces médicaments améliorent le contrôle glycémique lors de eGFR>45ml/min/1.72 m2, diminuent le risque d’ hospitalisation pour insuffisance cardiaque (lors de eGFR > 20ml/min/1.73m2) et ralentissent le déclin de la fonction rénale et l’ albuminurie (lors de eGFR > 25ml/min/1.73m2). L’ introduction d’ un SGLT2i dès un stade KDIGO G2A3 de l’ albuminurie peut retarder la survenue de l’ insuffisance rénale terminale de plus de 10 ans. Ces médicaments de prix moyen sont pris en une prise orale par jour. La tolérance est le plus souvent bonne. Il est néanmoins important d’ informer le patient des effets secondaires, en particulier le risque de mycose génitale (5-10% de risque) et l’ importance d’ une bonne hydratation. Leur utilisation est contre-indiquée pour l’ instant chez les diabétiques de type 1 en raison du risque d’ acido-cétose. Ce risque est bas chez le diabétique de type 2 mais doit être recherché en cas de douleurs abdominales /nausées. Finalement, comme pour les bloqueurs du système rénine-angiotensine, un contrôle de la créatinine/kaliémie est recommandée 1-2 semaines après l’ introduction d’ un SGLT2i chez les personnes avec une atteinte rénale ou des antécédents d’ insuffisance rénale aigue. Il faut relever que les analyses récentes montrent une diminution du risque d’ insuffisance rénale aigue et d’ hyperkaliémie sous SGLT2i.
Finérénone (7-9) : La finérénone est un antagoniste non stéroïdien des récepteurs minéralocorticoïdes (MRA). Il se distingue des MRA stéroidiens (aldactone, eplérénone) par l’ absence d’ effets secondaires sexuels collatéraux. C’ est le premier MRA avec preuve de néphro- et cardio-protection des patients diabétiques de type 2 avec une néphropathie albuminurique. Le risque d’ hyperkaliémie est par contre un facteur limitant, ce traitement ne peut être introduit lors de kaliémie ≤4.8mmol/l et nécessite un monitoring fréquent avec retrait lors de kaliémie au dessus de 5.5mmol/l. Son utilisation chez des patients diabétiques avec une atteinte rénale (jusqu’ à 25ml/min/1.73m2) est reconnue par Swissmedic mais son prix est encore en négociation. En raison de l’ abondance d’ étude positives avec les SGLT2i, le recours à la finérénone se fera en 2ème intention, après l’ introduction des SGLT2i. Même si les études manquent, leur association pourrait être intéressante avec des effets synergiques et une diminution du risque d’ hyperkaliémie.
Cibles thérapeutiques
Contrôle glycémique : en prévention primaire de la néphropathie diabétique, une cible d’ HbA1C <6.5-7% est recommandée. Dès un eGFR<60ml/min, les cibles peuvent être assouplies, comme le risque d’ hypoglycémie augmente lors d’ atteinte rénale et de traitement d’ insuline, de sulfonyurées ou de glinides. Une personne âgée en dialyse avec une espérance de vie limitée aura une cible de <8.5%. Si les SGLT2i seront choisis en priorité chez les personnes avec une néphropathie albuminurique, ce traitement ne suffira pas toujours à obtenir un bon contrôle glycémique. En cas de BMI au-dessus de 28kg/m2, un GLP1a sera proposé comme il apporte une protection cardiovasculaire et ralentit la progression de l’ albuminurie. L’ association GLP1a et SGLT2i nécessite cependant un accord préalable de l’ assurance maladie.
Contrôle tensionnelle : chez la personne diabétique de 18-64 ans la cible est une pression artérielle systolique de 130mmHg au cabinet ou plus bas si cela est toléré. Pour les personnes de 65ans ou plus, la cible est une pression artérielle systolique de 130-139mmHg. En cas d’ atteinte rénale, la cible est de 130-139mmHg si toléré avec une cible pour la pression artérielle diastolique de 70-79mmHg.
Contrôle lipidique : lors de diabète et d’ atteinte rénale (non dialysé, selon KDIGO >G3b ou G3aA2 ou A3) le risque cardiovasculaire est considéré comme très élevé. Dans ce cas, la cible initiale est un Ldl cholesterol <1.8mmol/l avec 50% de réduction. Dans un deuxième temps, une cible <1.4mmol/l est proposée surtout en cas de maladie cardiovasculaire avérée. Les statines restent en première ligne thérapeutique lors de néphropathie diabétique.
Bilan des complications
Dès une atteinte rénale significative, un bilan plus étendu des complications est proposé, incluant le bilan de l’ anémie, l’ acidose métabolique, le bilan phosphocalcique. Une collaboration étroite avec le néphrologue est indiquée en cas d’ altérations.
Conclusions
De nouvelles thérapies efficaces dans la néphropathie diabétique albuminuriques sont à présent disponibles, comme les SGLT2i et la finérénone. Ces nouvelles thérapies diminuent le risque rénal et cardiaque chez ces patients à haut risque. La prise charge de ces patients est complexe, doit être multifactorielle et multidisciplinaire, avec un accompagnement thérapeutique pour améliorer l’ adhésion au traitement.
Médecin adjoint, PD
Service d’endocrinologie, diabétologie et métabolisme
et Service de néphrologie
Centre hospitalier universitaire vaudois (CHUV)
Rue du Bugnon 17
CH-1011 Lausanne
L’ auteur n’ a pas déclaré de conflits d’ intérêts en rapport avec cet article.
1. ElSayed NA, Aleppo G, Aroda VR, Bannuru RR, Brown FM, Bruemmer D,
Collins BS, Hilliard ME, Isaacs D, Johnson EL, et al. 11. Chronic Kidney Disease and Risk Management: Standards of Care in Diabetes-2023. Diabetes Care. 2023;46:S191-S202.
2. Zanchi A, Jehle AW, Lamine F, Vogt B, Czerlau C, Bilz S, Seeger H and de Seigneux S. Diabetic kidney disease in type 2 diabetes: a consensus statement from the Swiss Societies of Diabetes and Nephrology. Swiss Med Wkly. 2023;153:40004.
3. Perkovic V, Jardine MJ, Neal B, Bompoint S, Heerspink HJL, Charytan DM, Edwards R, Agarwal R, Bakris G, Bull S, et al. Canagliflozin and Renal Outcomes in Type 2 Diabetes and Nephropathy. N Engl J Med. 2019.
4. Heerspink HJL, Stefansson BV, Correa-Rotter R, Chertow GM, Greene T, Hou FF, Mann JFE, McMurray JJV, Lindberg M, Rossing P, et al. Dapagliflozin in Patients with Chronic Kidney Disease. N Engl J Med. 2020;383:1436-1446.
5. The E-KCG, Herrington WG, Staplin N, Wanner C, Green JB, Hauske SJ, Emberson JR, Preiss D, Judge P, Mayne KJ, et al. Empagliflozin in Patients with Chronic Kidney Disease. N Engl J Med. 2023;388:117-127.
6. Nuffield Department of Population Health Renal Studies G and Consortium SiM-AC-RT. Impact of diabetes on the effects of sodium glucose co-transporter-2 inhibitors on kidney outcomes: collaborative meta-analysis of large placebo-controlled trials. Lancet. 2022;400:1788-1801.
7. Bakris GL, Agarwal R, Anker SD, Pitt B, Ruilope LM, Rossing P, Kolkhof P, Nowack C, Schloemer P, Joseph A, et al. Effect of Finerenone on Chronic Kidney Disease Outcomes in Type 2 Diabetes. N Engl J Med. 2020;383:2219-2229.
8. Rossing P, Filippatos G, Agarwal R, Anker SD, Pitt B, Ruilope LM, Chan JCN, Kooy A, McCafferty K, Schernthaner G, et al. Finerenone in Predominantly Advanced CKD and Type 2 Diabetes With or Without Sodium-Glucose Cotransporter-2 Inhibitor Therapy. Kidney Int Rep. 2022;7:36-45.
9. Pitt B, Filippatos G, Agarwal R, Anker SD, Bakris GL, Rossing P, Joseph A, Kolkhof P, Nowack C, Schloemer P, et al. Cardiovascular Events with Finerenone in Kidney Disease and Type 2 Diabetes. N Engl J Med. 2021;385:2252-2263.
la gazette médicale
- Vol. 12
- Ausgabe 2
- März 2023