- Hyperactivité vésicale de la personne âgée : du diagnostic au traitement
L’hyperactivité vésicale est la combinaison d’une urgenturie et d’une pollakiurie qui résulte d’une perturbations du contrôle végétatif et/ou d’une atteinte myogène (1). La génération d’une contraction involontaire et précoce du détrusor limite alors la capacité fonctionnelle de la vessie (normalement 300-600 cm3). Associée ou non à un autre trouble fonctionnel et/ou une incontinence urinaire (IU), l’hyperactivité vésicale altère la qualité de vie et est un facteur de risque de chute, de fracture, de déclin fonctionnel et d’entrée en institution (1).
L’hyperactivité vésicale (HV) de la personne âgée est cependant souvent occultée par les patients (gêne, banalisation, résignation, honte, crainte) et/ou les professionnels (gêne, banalisation). Sa prise en charge est souvent médiocre (1). Le dépistage des troubles fonctionnels urinaires devrait cependant être systématique dans cette population.
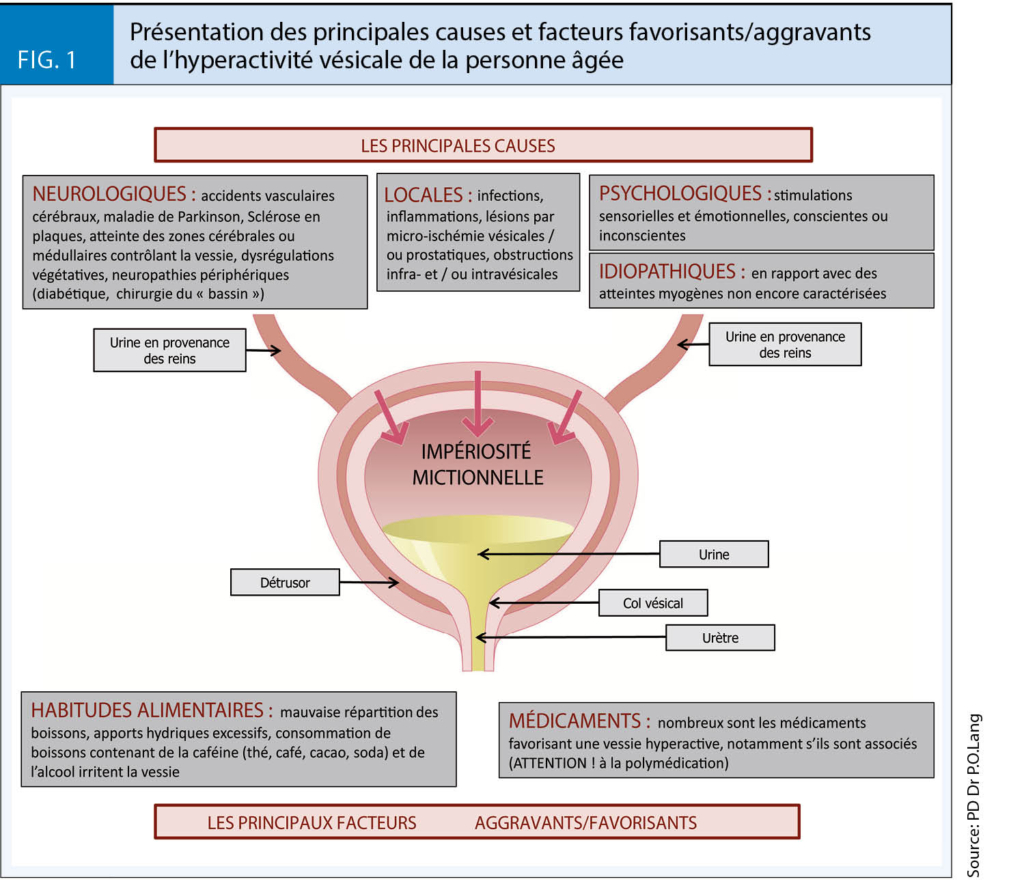
Spécifiquement, pour l’HV, il s’agit de l’identifier, d’en caractériser la ou les causes (fig. 1), d’évaluer son intensité et son retentissement et enfin d’élaborer une prise en charge adaptée aux souhaits du patient, à son état fonctionnel, ses capacités cognitives, ses comorbidités et leurs traitements.
Démarche diagnostique
Elle doit permettre de distinguer les HV induites par une pathologie potentiellement curable, de celles associées aux maladies neurologiques qui néces-sitent des investigations spécialisées, et des HV a priori idiopathiques (fig. 1) (1).
Anamnèse
Elle précisera les deux symptômes cardinaux (urgenturie + pollakiurie, ± IU), leur durée d’évolution et le mode évolutif. Il est important d’identifier le niveau de gêne au quotidien par rapport à la pollakiurie. Les symptômes de troubles de la vidage: attente initiale, poussée à la miction, sensation de résidu, etc. ainsi qu’une dysurie ou des douleurs associées sont à demander. Une nycturie doit être systématiquement recherchée (2). Les antécédents et le contexte seront précisés. L’infection et les pathologies intra-vésicales (tumeurs, calculs, corps étrangers) ainsi que les obstructions infra-vésicales constituent des causes réversibles. Les atteintes neurologiques médullaires et/ou centrales sont souvent irréversibles et parfois progressives. En l’absence de cause identifiable, on parle d’HV idiopathique. Il faut systématiquement rechercher les facteurs favorisants/aggravants et notamment les médicaments (fig. 1) (1).
Révision des médicaments
En présence d’une HV la prise d’un inhibiteur de l’acétylcholin-estérase, de diurétiques de l’anse ou thiazidiques doit être systématiquement recherchée. Ces molécules peuvent accentuer l’urgenturie, la pollakiurie et/ou la nycturie (1). L’ensemble des médicaments ayant un effet antimuscarinique doit aussi être listé (3). L’attention devra se porter aussi sur les molé-cules majorant le risque de rétention (4), notamment en présence d’un résidu post-mictionnel (RPM) > 100 mL.
Examen clinique et évaluation gériatrique
Il recherche des signes neurologiques évocateurs d’une cause sous-jacente, des complications cutanées en cas d’IU ainsi que l’absence de causes locorégionales – gynécologiques, tumeur, malformations – demandant un toucher rectal est chez l’homme. L’analyse fonctionnelle évalue la marche et le risque de chute. Une évaluation cognitive est un préalable essentiel en vue de l’instauration d’un traitement symptomatique (1).
Examens complémentaires
Devant toute HV nouvelle, majorée, ou résistante au traitement un examen cytobactériologique des urines est systématique (5). Les infections seront traitées et en présence d’une hématurie isolée, une cystoscopie devra être envisagée. Le calendrier mictionnel est très utile pour écarter une pollakiurie secondaire à une polyurie (> 3 L de diurèse/24 heures) et apprécier les volumes et les horaires des mictions et des apports hydriques (1). Si le bilan urodynamique est systématique en cas de maladie neurologique ou avant une chirurgie, les indications doivent se limiter aux diagnostics non clairs après une démarche clinique bien conduite ou à l’inefficacité d’un traitement d’épreuve (2). En cas d’origine obstructive, une débimétrie et une mesure du RPM sont à faire (1).
Démarche thérapeutique
Les objectifs de prise en charge doivent être centrés sur la préservation de l’autonomie fonctionnelle et des capacités cognitives. Ils seront formulés selon l’intensité et le retentissement de l’HV et les objectifs du patient avec une application raisonnée et raisonnable des données de la littérature (2). S’il n’existe pas de consensus validé chez les patients âgés, l’approche sera progressive et ajustée à l’état fonctionnel, les fonctions cognitives, les comorbidités et les traitements pris.
En première intention (dans tous les cas):
l’identification des facteurs favorisants / aggravants comportementaux, médicamenteux et de mode de vie (fig. 1) dont la correction améliore souvent les symptômes. Cette étape est particulièrement importante chez les patients les plus fragiles chez qui la prise en charge pharmacologique est souvent plus délicate (6).
Les mesures les plus efficaces sont (1) :
- suspendre les médicaments potentiellement aggravant
- assurer une bonne hydratation en limitant les apports le soir et les boissons irritantes (alcool, café, sodas, thés)
- favoriser le transit en limitant la constipation (alimentation riche en fibres et respect des besoins)
- privilégier une vie active et une alimentation équilibrée
- proposer un calendrier de vidange vésicale (passage aux WC à heures fixes et avant les sorties
- mesures d’ergothérapie concernant l’habillement (velcro à la place de boutons), et l’aménagement de l’environnement (accès facilité et sécurisé aux WC, chaise percée, urinal anti-renversement, étui pénien, …
- adapter le type et le format des protections
Le sondage vésical n’a pas d’indication dans l’HV même en présence d’une plaie chronique ou d’une escarre (4).
En seconde intention :
La démarche thérapeutique repose sur la neurostimulation du nerf tibial postérieur (TENS) (7) ou les techniques de renforcement du plancher pelvien. Le TENS est efficace et bien toléré (1) et consiste en la stimulation par une électrode collante percutanée en regard du nerf tibial postérieur lors de séances quotidiennes de 20 minutes. Le renforcement musculaire a un effet significatif sur les symptômes et la qualité de vie (8, 9). S’il s’agit d’alternatives efficaces aux médicaments, une bonne coopération des patients est nécessaire. Ces techniques doivent même être proposées avant ou à la place des médicaments
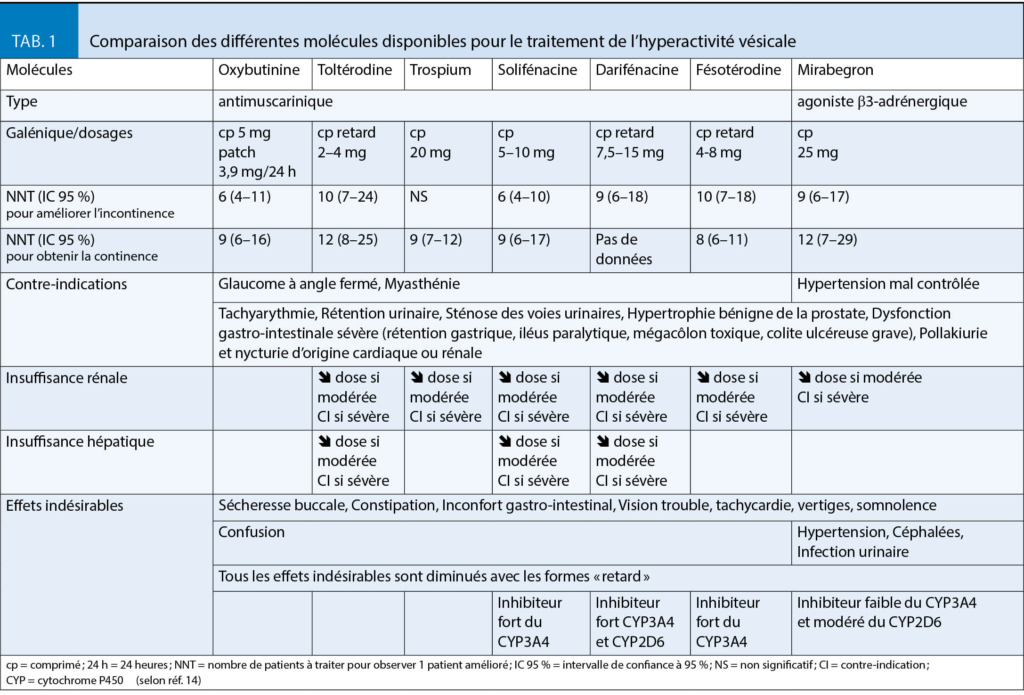
Le traitement médicamenteux repose sur les antimuscariniques et/ou un agoniste des récepteurs β3-adrénergiques. L’efficacité est similaire mais les profils de tolérance sont différents (tab. 1) (1).
- Les antimuscariniques : Le chlorure de trospium nécessite des prises à distance des repas ; la solifénacine, darifénacine, et fésotérodine sont les molécules les plus récentes. Il faut privilégier celles traversant faiblement (solifénacine, toltérodine) ou pas (trospium, fésotérodine, darifénacine) la barrière hémato-encéphalique (3). Elles sont déconseillés si RPM > 100 mL. En présence d’un traitement par donépézil, rivastigmine, ou galantamine, l’association d’un antimuscarinique est incohérente (3). Les formulations à libération immédiate sont plus efficaces et les formes retard mieux tolérées. Le bénéfice sur le risque de chutes n’a pas été démontré (10).
- L’agoniste des récepteurs β3-adrénergiques n’a pas d’effets antimuscariniques mais il induit aussi sécheresse buccale, constipation, somnolence et vertiges en plus des effets adrénergiques sur la tension et la fréquence cardiaque (1). Globalement, sa tolérance et son efficacité semblent supérieures à celles des antimuscariniques (11).
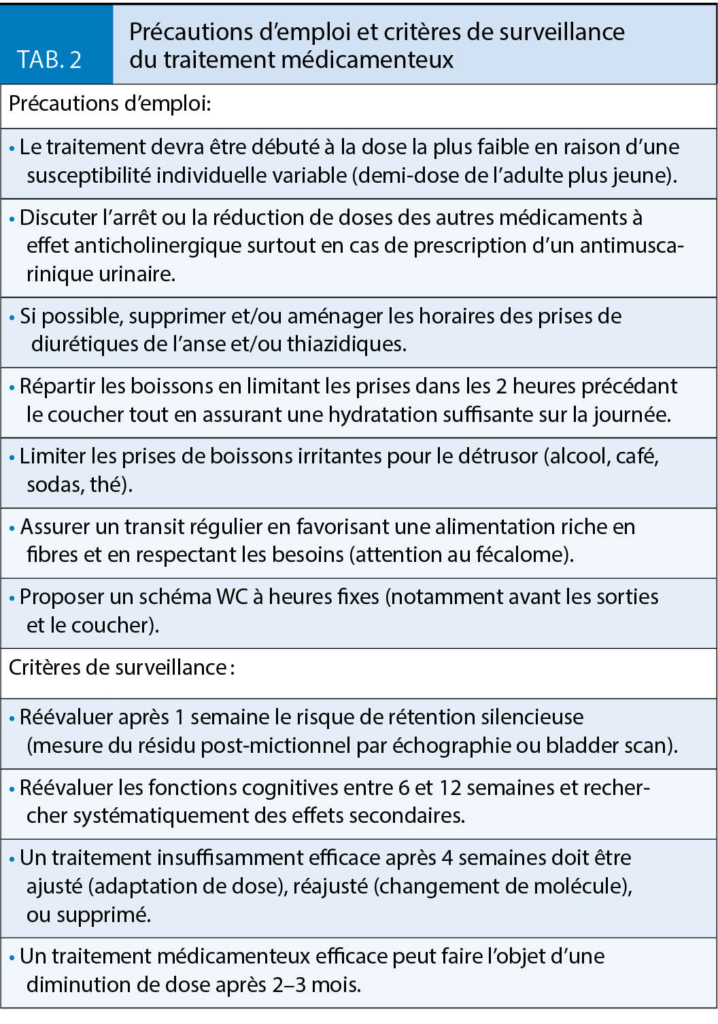
Dans tous les cas, les effets secondaires limitent l’observance (tab. 1) et nécessitent une utilisation raisonnée chez les patients fragiles, polymorbides, et/ou polymédiqués. Certaines précautions doivent être systématiquement respectées (tab. 2) (1).
En troisième intention :
L’injection endoscopique dans le détrusor de toxine botulique (12) ou la neurostimulation des racines sacrées (NMS) (13) peuvent être proposer en 3ème intention. Les injections se font sous anesthésie locale et sont efficaces pour 6 mois environ. Elles peuvent cependant perturber la miction normale et favoriser les rétentions (ce qui peut nécessiter transitoirement un auto-sondage). La technique est utile pour les vessies neurologiques mais aussi pour certaines formes idiopathiques (12). Elle ne peut se faire sous anticoagulant ou clopidogrel ; l’aspirine n’est par contre pas une contre-indication (1).
La chirurgie est réservée aux vessies neurologiques ou aux HV secondaire à une obstruction infra-vésicale et aux échappements / résistances à la NMS et à la toxine botulique (1). Il s’agit par contre d’une chirurgie lourde (entérocystoplastie d’agrandissement ou conduit iléal selon Bricker) qui est souvent la solution ultime lorsque toutes les alternatives ont échouées et/ou en cas d’HV très invalidante.
Genolier Klinik und Montchoisi Klinik
Route du Muids 3
1272 Genolier
plang@genolier.net
plang@genolier.net
L’auteur n’a aucun conflit d’intérêt en rélation avec cet article.
- Le diagnostic est clinique et repose avant tout sur l’analyse des
symptômes - Le bilan étiologique et la recherche des facteurs aggravants sont
indispensables et guident la prise en charge (fig. 1) - Le traitement de première intention repose sur les mesures hygiéno-diététiques et comportementales
- Le traitement pharmacologique n’est qu’un traitement de seconde ligne dont l’efficacité et la tolérance peuvent être limitées
- L’approche thérapeutique doit être individualisée selon les souhaits
du patient, son état fonctionnel, ses capacités cognitives, ses comorbidités et ses traitements
1. Ishida M et al. Comment je prends en charge une hyperactivité vésicale chez un patient âgé hospitalisé. Médecine Thérapeutique 2018;in press
2. Akrour R, Ishida M, Lang PO. Dépistage et évaluation de l’incontinence urinaire chez les patients âgés complexes : étude exploratoire en gériatrie aiguë. Neurol Psychiatr Geriatr 2017;17:270-8
3. Csajka C, Bremond C, Lang PO. Détecter et évaluer l’impact des médicaments anticholinergiques Rev Med Suisse 2017;13:1931-7
4. Akrour R et al. Comment optimiser l’utilisation des cathéters urinaires chez les patients âgés hospitalisés. Médecine Thérapeutique 2018;in press
5. Reuben DB et al. Geriatrics at your fingertips. 18th Edition ed: American Geriatrics Society, New York; 2016
6. Boudon A, Riat F, Rassam-Hasso Y, Lang PO. Polymorbidité et Polypharmacie : Comment optimiser la prise en charge des patients âgés complexes ? Swiss Med Forum 2017;17:306-12
7. Sharma N et al. Efficacy of Transcutaneous Electrical Nerve Stimulation in the Treatment of Overactive Bladder. J Clin Diagn Res 2016;10:QC17-QC20
8. Parker WP, Griebling TL. Nonsurgical Treatment of Urinary Incontinence in Elderly Women. Clin Geriatr Med 2015;31:471-85
9. Stenzelius K et al. The effect of conservative treatment of urinary incontinence among older and frail older people: a systematic review. Age Ageing 2015;44:736-44
10. Hunter KF et al. Falls risk reduction and treatment of overactive bladder symptoms with antimuscarinic agents: a scoping review. Neurourol Urodyn 2011;30:490-4
11. Liao CH, Kuo HC. High satisfaction with direct switching from antimuscarinics to mirabegron in patients receiving stable antimuscarinic treatment. Medicine (Baltimore) 2016;95:e4962
12. Eldred-Evans D, Sahai A. Medium- to long-term outcomes of botulinum toxin A for idiopathic overactive bladder. Ther Adv Urol 2017;9:3-10
13. Sukhu T et al. Sacral neuromodulation in overactive bladder: a review and current perspectives. Res Rep Urol 2016;8:193-9
14. Lang PO et al. Hyperactivité vésical e chez le patient âgé hospitalisé : une approche structurée. Neurol Psychiatr Geriatr 2018;in press
la gazette médicale
- Vol. 7
- Ausgabe 5
- Mai 2018