- Hyperkaliémie en cas d’ insuffisance cardiaque chronique
L’ hyperkaliémie (HK) est un trouble électrolytique potentiellement mortel. Elle est principalement due à un déplacement du potassium hors des cellules ou à une diminution de l’ excrétion rénale de potassium. Ce trouble électrolytique se produit souvent chez les patients souffrant d’ une maladie cardiovasculaire. Malgré l’ hyperkaliémie, le maintien du blocage du SRAA en cas d’ insuffisance cardiaque (IC) avec fraction d’ éjection réduite (FE-VG) est essentiel, car l’ arrêt ou la réduction de la dose s’ accompagne d’ une augmentation de la mortalité. Même en cas de fraction d’ éjection gauche (FE VG) ≥ 40 %, l’ administration d’ un inhibiteur du SGLT2 en plus d’ un ARM peut être envisagée. La prévention, la détection et le traitement de l’ hyperkaliémie revêtent donc une importance capitale, en particulier chez les patients cardio-rénaux métaboliques.
Hyperkalemia (HK) is a potentially life-threatening electrolyte disorder. The main causes are a shift of potassium from the cells or reduced renal excretion of potassium. It is common in patients with cardiovascular disease. Maintenance of RAAS blockade in heart failure (HF) with reduced LV EF despite hyperkalemia is essential, as discontinuation or dose reduction is associated with increased mortality. The addition of an MRA to an SGLT2 inhibitor may also be considered when LVEF is ≥ 40 %. Therefore, the prevention, detection and treatment of hyperkalemia, especially in patients with cardiorenal metabolic disorders, is of great importance.
Key words: Hyperkalemia, Heart failure, RAASi, MRA, Finerenon, CKD, Diabetes Type 2, Potassium binder
Introduction
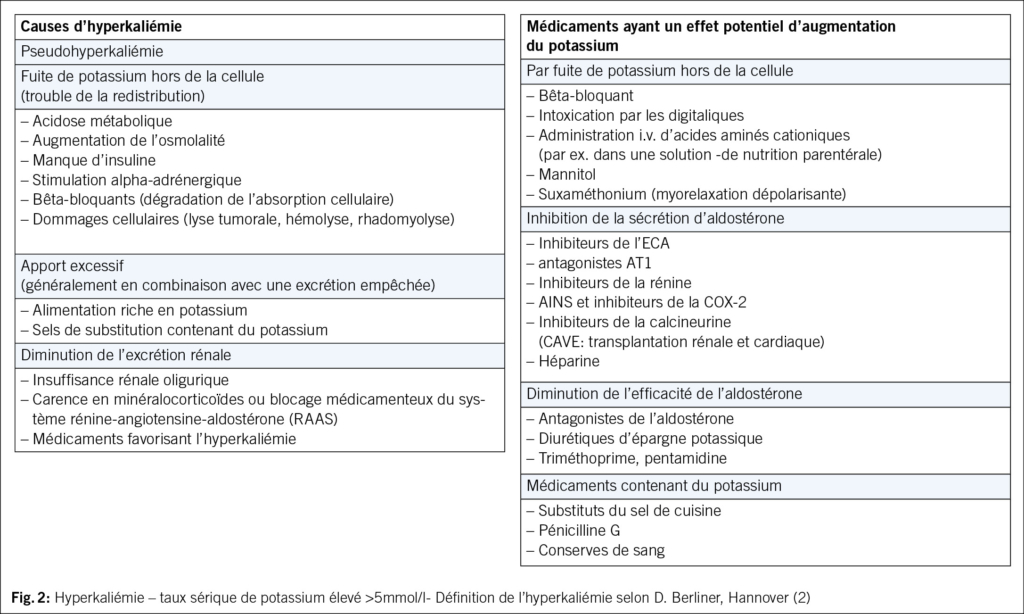
Une hyperkaliémie (HK) > 5.0–5.5 mmol/l est principalement due à un déplacement du potassium hors des cellules (redistribution) ou à une excrétion rénale anormale de potassium. Une hyperglycémie en cas de diabète sucré, une acidose ou une désintégration cellulaire étendue entraînent un déplacement des cellules (hyperglycémie en cas de diabète sucré, acidose, désintégration cellulaire étendue) qui provoque une augmentation temporaire de la concentration plasmatique de potassium, tandis qu’ une diminution de l’ excrétion rénale de potassium provoque une HK persistante. L’ altération de l’ excrétion rénale de potassium peut résulter d’ une diminution de la libération de sodium dans le néphron distal, d’ une diminution du taux ou de l’ activité des minéralocorticoïdes ou d’ anomalies dans le canal collecteur cortical. Dans certains cas, ces trois troubles sont présents simultanément. Une absorption excessive de potassium (provenant de certains aliments ou de sels de substitution) peut également provoquer une hyperkaliémie, mais généralement en cas de fonction rénale réduite. Si le débit de filtration glomérulaire (DFG) est > 60 ml/min/1.73m2, une hyperkaliémie est inhabituelle. Une nécrose tissulaire ou certains médicaments peuvent également en être responsables (1, 2).
Le potassium est absorbé dans la partie supérieure de l’ intestin grêle et se trouve à 98 % dans la cellule. Son antagoniste physiologique est le sodium, qui est principalement extracellulaire. Ensemble, ils sont essentiels à la physiologie cellulaire. L’ homéostasie du potassium est décisive pour la physiologie des cellules. Elle est également essentielle pour le maintien du potentiel de repos des membranes cellulaires, en particulier dans les cellules cardiaques. Tout déséquilibre peut entraîner des troubles électrophysiologiques, y compris des arythmies cardiaques malignes.
90 % du potassium est éliminé par voie rénale avec une variabilité circadienne, 10 % par voie gastro-intestinale. Le contrôle hormonal est assuré par l’ insuline, les catécholamines et l’ aldostérone (1).
Épidémiologie, physiopathologie
Chez la population générale, l’ hyperkaliémie est rare (2–3 %). Son incidence est cependant sous-estimée, car aucun dépistage du potassium n’ est effectué, même chez les patients à haut risque. On trouve également différents seuils de potassium pour l’ hyperkaliémie. Souvent, celle-ci n’ est que temporaire. Il n’ existe toutefois pas d’ études prospectives à ce sujet.
Un blocage du SRAA avec un IEC/ARB/ARNI et un ARM est très efficace dans le cas de diverses maladies cardio-rénales: il est antihypertenseur, cardio- et néphroprotecteur. Chez les patients souffrant d’ une insuffisance cardiaque (IC) avec fraction d’ éjection réduite (HFrEF), les inhibiteurs du Système Rénine-Angiotensine-Aldostérone (SRAAi), y compris les antagonistes des récepteurs aux minéralocorticoïdes (ARM), améliorent les symptômes, réduisent le risque d’ hospitalisation et de décès par IC. Ils sont par ailleurs recommandés par les directives américaines et européennes sur l’ insuffisance cardiaque (recommandation IA). Les inhibiteurs du SGLT2 ont également ces propriétés protectrices, indépendamment de la FEVG.
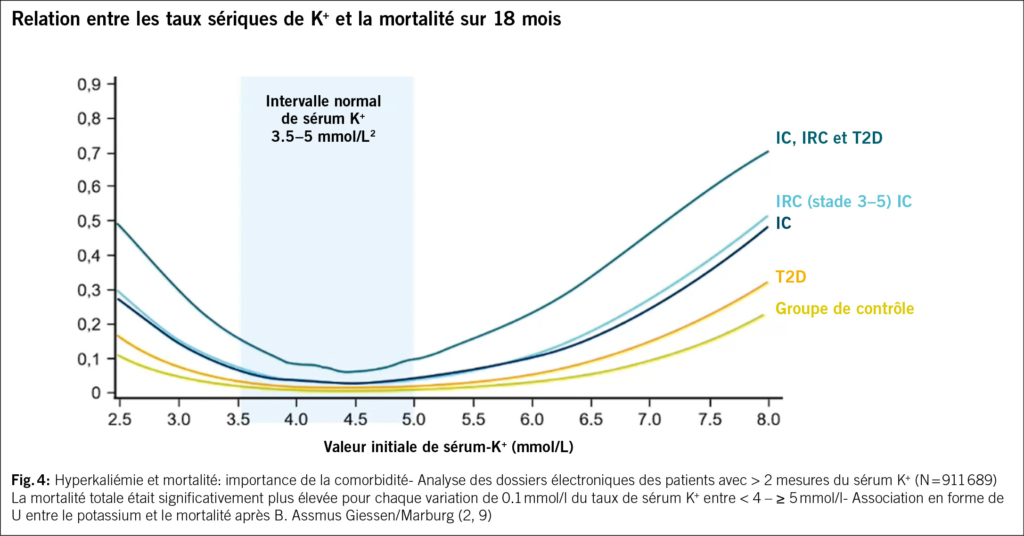
L’ hyperkaliémie potentielle résultant du SRAAi est souvent un problème chez les patients âgés multimorbides souffrant d’ insuffisance cardiaque (IC). Elle survient en particulier en présence d’ une insuffisance rénale chronique (IRC) et/ou d’ un diabète sucré de type 2 (DT2). L’ hyperkaliémie est associée à une mortalité accrue et à un risque d’ hospitalisation plus élevé (1–4). Le risque d’ hyperkaliémie le plus élevé est observé chez les personnes qui bénéficient le plus d’ une inhibition du SRAA:
• jusqu’ à 40–50 % en cas d’ IRC de plus d’ un an avec un DFGe < 30 ml/min/1.73 m2, en particulier chez les personnes atteintes de DT2 et sous SRAAi, avec toutefois un risque d’ acidose métabolique;
• jusqu’ à 40 % en cas d’ insuffisance cardiaque sévère à partir d’ une dose de spironolactone de 50 mg/jour.
• en cas de statut après une hyperkaliémie.
Les patients atteints d’ IRC et d’ IC doivent généralement s’ attendre à des épisodes d’ hyperkaliémie récurrents et croissants, ces épisodes survenant alors à des intervalles plus courts. Dans le registre suédois de l’ insuffisance cardiaque, sur 43 000 patients, 51 % avaient une IRC, 24 % un DT2, 13 % une IRC+DT2 et 21 % une fibrillation atriale. L’ hyperkaliémie est un marqueur de risque de mauvais résultats, notamment en raison d’ une utilisation non optimale du traitement par SAARi. En raison d’ une hyperkaliémie, d’ une augmentation de la créatinine, d’ une hypotension, de l’ âge et de la fragilité, les médicaments contre l’ IC ne sont pas utilisés conformément aux directives (5, www.ukidney.com). Un travail récent publié dans le JACC a également mis en évidence une hyperkaliémie récurrente en cas d’ IRC (G3/G4) chez 6 337 patients âgés, dont 2129 patients avec IC. Cela a entraîné une mortalité globale accrue, plus d’ événements cardiovasculaires et plus d’ arythmies (6).
Une hyperkaliémie est classée en différents degrés de gravité – cf. Fig. 1.
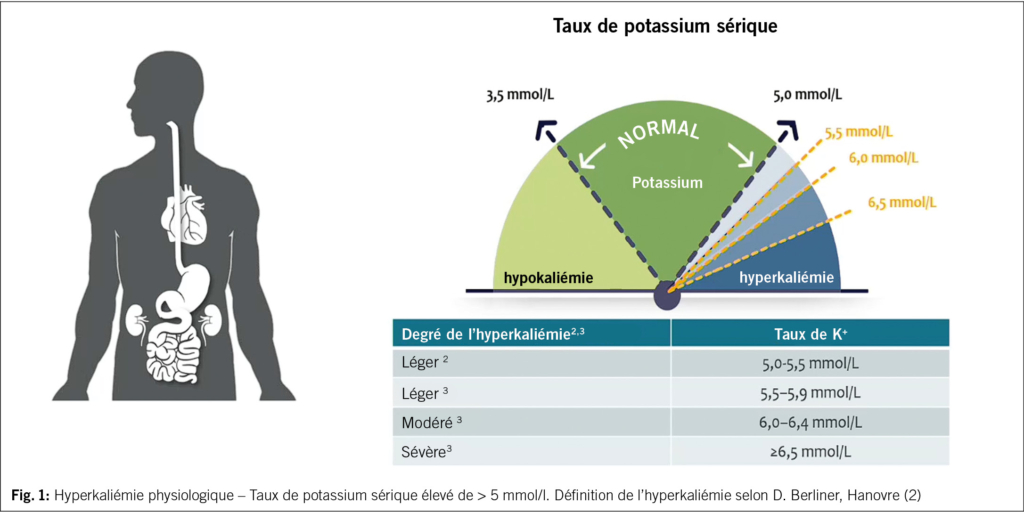
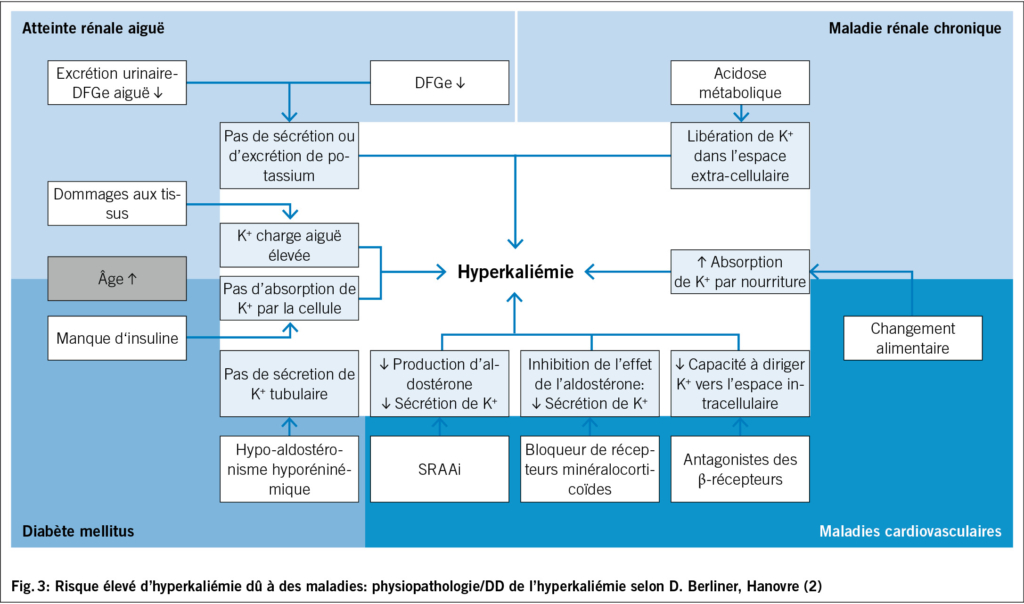
La valeur est élevée à partir d’ un potassium sérique de > 5 mmol/l. Une valeur ≥ 6.0 mmol/l est dangereuse. En cas de potassium sérique confirmé à hauteur de ≥ 6.5 mmol/l, une hospitalisation d’ urgence avec monitorage par ECG et mise en place de mesures thérapeutiques spécifiques est nécessaire en raison d’ une menace vitale. Pour ce qui est du diagnostic différentiel et de la physiopathologie d’ une IC, voir les Fig. 2 et Fig. 3 (1–4). C’ est la raison pour laquelle une hyperkaliémie doit être détectée à un stade précoce.
Clinique
L’ hyperkaliémie est généralement asymptomatique ou symptomatique, avec des symptômes non spécifiques tels que nausées, vomissements, diarrhée, paresthésies péronières, fourmillements et engourdissements. Ainsi, elle n’ est pas reconnue pendant longtemps. Des manifestations neuromusculaires telles que des paresthésies et des fasciculations des extrémités peuvent également apparaître. En cas d’ hyperkaliémie sévère (supérieure à 6,5 mmol/l), des paralysies ascendantes avec, en fin de compte, une tétraplégie flasque des extrémités ou un iléus sont possibles. Un effet dépolarisant avec des modifications typiques de l’ ECG se produit jusqu’ à 67 % en cas d’ hyperkaliémie aiguë (> 6,0-6,4 mmol/l). Cela comprend une onde T pointue (à ≥ 5,5-6 mmol/l dans 31,8 %), une faible amplitude de l’ onde P (> 6-6,5 mmol/l), un allongement de l’ intervalle P-R et un QRS large (26,2 %). Des troubles de la conduction, des bradycardies, une perte de P avec onde sinusoidale, FV, une asystole peuvent se produire avec un (K+) > 8–9 mmol/l. Cependant, les symptômes et l’ ECG ne sont pas de bons prédicteurs de la mortalité. La sensibilité et la spécificité sont faibles, en particulier pour les maladies cardiaques. Arythmies létales sans ECG préalable. L’ ECG ne peut pas être utilisé pour exclure une hyperkaliémie. C’ est pourquoi des contrôles réguliers du potassium et de la créatinine sont essentiels, en particulier lors de changements de médicaments et de doses, toutes les 1 à 2 semaines (1,2,7,8).
L’ importance de l’ ARM dans le traitement de l’ IC chronique
L’ IC est, indépendamment de la FEVG, une maladie chronique évolutive, avec une mortalité élevée et un risque important de récidive, en particulier d’ hospitalisation. Il est donc essentiel d’ optimiser le traitement par SAARi tant que le potassium sérique est inférieur à 5,0 mmol/l, car ce traitement a un effet cardioprotecteur et néphroprotecteur. En cas d’ HFrEF, l’ association des «fantastic four» (IECi/ARNI, bêtabloquant, SGLT2i, ARM) améliore la mortalité globale de 61 % (9). Le facteur décisif est ici la titration rapide pour atteindre le dosage correct, conformément aux directives de l’ ESC (10, 11).
La spironolactone est associée à une incidence plus faible d’ hypokaliémie et à une amélioration de la survie, même en cas d’ hyperkaliémie modérée (2, 12). Dans l’ insuffisance cardiaque (IC), les hypokaliémies dangereuses sont nettement plus rares sous ARM en association avec des diurétiques.
Selon l’ étude STRONG-HF, une stratégie d’ optimisation intensive après une hospitalisation aiguë – avec une augmentation rapide de la médication conforme aux directives et un suivi étroit réduit les symptômes, améliore la qualité de vie et diminue le risque de réadmission après 6 mois (13). Des effets similaires ont été observés dans les études ATLAS et BIOSTAT-HF avec IECi/ARB, ou un bêtabloquant à la dose correcte. L’ une des causes de la non-prescription ou du report de l’ augmentation de la dose du SAARi ou du MRA était une détérioration de la fonction rénale et/ou une hyperkaliémie. Dans jusqu’ à 76 % des cas, ces médicaments ne sont pas utilisés par la suite (2, 11, 12, 14). La réduction de la dose ou l’ arrêt du RAASi entraîne un risque de mortalité plus que doublé. C’ est pourquoi il est essentiel de déterminer la dose maximale tolérée (13, 15, 16).
Sous ARNI, le risque d’ hyperkaliémie modérée à sévère et d’ augmentation de la créatinine est légèrement plus faible que sous énalapril dans le cas d’ une IC (PARADIGM-HF). Il en va de même sous traitement par un SGLT2i (10, 15, 17).
Les ARMs sont considérés comme essentiels en cas d’ IC, à condition que la pression artérielle systolique soit supérieure à 100 mmHg, que le DFGe soit supérieur à 30 ml/min/1.73 m² et que le taux de potassium sérique soit inférieur à 5 mmol/l. Comme les inhibiteurs du SGLT2 (recommandation IA), ils peuvent être utilisés indépendamment de la FEVG, mais n’ ont actuellement qu’ une indication IIb/C en cas de FEVG ≥ 40 % (15). En cas de DFGe < 30 ml/min, l’ ARM et l’ ARNI doivent être évités, tandis qu’ en cas d’ IRC au stade G4-5, les preuves sont limitées, à l’ exception des inhibiteurs du SGLT2, ce qui rend nécessaire une concertation interdisciplinaire entre cardiologie et néphrologie. En cas de FEVG < 40 % (HFrEF), des ARMs stéroïdiens tels que la spironolactone ou l’ éplérénone (recommandation IA) sont prescrits. L’ étude RALES a montré une réduction de 30 % de la mortalité et de 35 % des hospitalisations pour insuffisance cardiaque avec 25 mg de spironolactone/jour (19); dans EMPHASIS-HF, l’ éplérénone a réduit la mortalité cardiovasculaire et les hospitalisations pour insuffisance cardiaque de 37 %, avec 11.8 % des patients ayant développé une hyperkaliémie (20). L’ eplérénone provoque un peu moins d’ hypotension et évite la gynécomastie par rapport à la spironolactone.
En cas d’ IC avec FEVG ≥ 40 % (HFmrEF: 41–49 % ou HFpEF: FEVG ≥ 50 %), la place thérapeutique des ARMs restait incertaine jusqu’ à l’ ESC 2024, tandis que les inhibiteurs du SGLT2 continuent d’ être recommandés. L’ étude TOPCAT 2014, qui présentait des lacunes méthodologiques, était neutre.
Le finérénone
Ce nouvel ARM non stéroïdien (NS) semble présenter un avantage certain avec un bénéfice plus important (sélectivité et puissance élevées, t/2 plus court, répartition tissulaire équilibrée entre le cœur et les reins), mais aussi avec moins d’ effets indésirables (pas de métabolites, pas d’ effets indésirables liés au sexe, moins d’ hyperkaliémie, encore moins d’ effet sur la pression sanguine). Éliminé via le CYP3A4, le DFGe doit être initialement > 25 ml/min/1.73 m2.
Dans l’ étude FINEARTS-HF randomisée, en double aveugle et contrôlée par placebo, le finérénone (F) a montré chez 6001 patients âgés, symptomatiques et à risque d’ insuffisance cardiaque une FEVG d’ au moins 40 % (NYHA II-IV, NT-pro-BNP élevé, cardiopathie structurelle, diurétiques), avec un DFGe d’ au moins 25 ml/min/1.73 m2 (48 % < 60 ml/min/1. Le critère d’ évaluation composite primaire a également montré une réduction significative de 18 % de l’ aggravation de l’ insuffisance cardiaque. Le critère d’ évaluation composite primaire a également montré une réduction significative de 18 % de l’ aggravation de l’ insuffisance cardiaque. En revanche, il n’ y avait pas de différence entre la finénérone et le placebo en ce qui concerne la mortalité cardiovasculaire. La qualité de vie a été nettement améliorée. Les patients âgés et tous les autres sous-groupes en ont également profité (21).
Ces résultats soutiennent l’ utilisation des MRA non stéroïdiens chez les patients avec insuffisance cardiaque ayant une fraction d’ éjection légèrement réduite ou préservée – avec ou sans insuffisance rénale chronique.
Avant le début du traitement, le taux de potassium sérique doit être compris entre 4.8 et 5.0 mmol/l, car le finénarone est associé à un risque accru d’ hyperkaliémie (K+ > 5.5: 14.3 % vs. 6.9 %, > 6.0: 3.0 % vs. 1.4 %). Cependant, sous réserve d’ une surveillance étroite et d’ une adaptation de la dose, le bénéfice clinique de finérénone par rapport au placébo a été maintenu même chez les patients dont le taux de potassium est passé à plus de 5.5mmol/l. L risque d hyperkaliémie était de 2.46. La différence médiane de potassium entre le finérénone et le placébo était de 0.2mmol/l (22). Le finérénone a réduit le risque du critère d’ évaluation primaire de manière similaire chez les femmes et les hommes atteints de cette forme d’ IC, avec une tolérance similaire (23).
L’ une des principales différences entre l’ étude FINEARTS HF et de nombreuses autres études sur l’ IC est que près de 20 % des patients ont été inclus dans l’ étude soit à l’ hôpital. Un aspect particulier de l’ étude FINEARTS-HF est que près de 20 % des patients ont été recrutés lors d’ un séjour hospitalier ou peu après la sortie. Les bénéfices du traitement par finérénone en particulier, et peut-être aussi des ARM en général, étaient au moins aussi importants chez les patients qui venaient d’ être hospitalisés que chez ceux qui étaient plus éloignés d’ une aggravation de l’ IC (24).
Chez les patients de FINEARTS-HF, une population présentant un faible risque d’ effets secondaires indésirables, le finérénone n’ a pas modifié de manière significative les résultats du critère d’ évaluation combiné de la fonction rénale. Le finérénone a entraîné une réduction plus importante de la filtration glomérulaire au départ, mais n’ a pas entraîné de différence significative de la filtration glomérulaire au cours de l’ évolution. Cependant le finérénone a entraîné une réduction précoce et durable de l’ albuminurie et a réduit le risque d’ apparition d’ une nouvelle micro-et macroalbuminurie (25). Une diminution de DFGe (> 15 %) au début d’ un traitement (23 %) ne devrait pas automatiquement conduire à l’ arrêt de l’ ARM. Une baisse initiale du DFGe était associé à une incidence plus élevée de l’ insuffisance rénale chronique. Contrairement à ce qui se passe sous placébo, la perte d’ activité rénale n’ est pas associée à une aggravation du pronostic. Selon les auteurs, si le taux de potassium sérique est inférieur à 5.5 mmol/l, il est possible de continuer à augmenter la dose avec prudence (26). Il est important de continuer à contrôler régulièrement le taux de potassium et de créatinine /DFGe) au début du traitement à raison d’ une fois par semaine.
Même dans un sous-groupe encore très petit de 14 % des participants à l’ étude traités par SGLT2i, le traitement par ARM avec finérénone a montré des effets similaires à ceux observés chez les patients non prétraités. Les données les plus récentes indiquent que l’ utilisation combinée d’ un SGLT2i et d’ un ARMM peut offrir une protection supplémentaire contre les événements cardiovasculaires et jouer un rôle additif chez les personnes atteintes de CI avec ou sans IRC avec une FEVG légèrement réduite ou préservée (21, 27).
D’ après une méta-analyse des quatre études menées jusqu’ à présent sur l’ IC avec ARM, les ARMs stéroïdiennes réduisaient le risque de décès cardiovasculaire ou d’ hospitalisation pour IC chez les patients atteints d’ une HFrEF et les ARMs non stéroïdiennes réduisent significativement le risque d’ hospitalisation pour IC chez les patients atteints d’ une HFmrEF ou d’ une HFrEF. Le risque absolu d’ une hyperkaliémie sévère (K+) > 6 mmol/l était faible – environ 3 % dans le groupe de traitement par ARM (28). Les hyperkaliémies étaient cliniquement contrôlables dans tous les sous-groupes d’ un traitement combiné avec le finérénone, avec une réduction d’ hyperkaliémies d’ urgence liées au traitement en association avec les SGLT2i.
Les données d’ études futures pourraient conduire à une recommandation plus forte des MRA dans l’ insuffisance cardiaque chronique (FEVG ≥ 40 %). Actuellement, contrairement à la néphropathie diabétique, l’ autorisation de mise sur le marché de finérénone (Kerendia®) pour l’ insuffisance cardiaque n’ est pas encore disponible dans l’ UE et en Suisse (une extension de l’ autorisation est attendue pour 2026).
Dans la néphropathie diabétique (stades G3/G4) avec albuminurie, le finérénone a démontré, dans l’ analyse FIDELITY (n = 13 026, 3 ans), des effets rénoprotecteurs, une réduction du risque d’ événements cardiovasculaires (HR 0.86) et du progrès de la maladie rénale (HR 0.77) sur un large éventail de patients (IRC et DT2). Le dépistage de l’ albuminurie pour identifier les patients à risque de DT2 facilite la réduction de la charge cardiovasculaire et rénale. Une hyperkaliémie a été détectée chez 1.7 % des patients (29).
Les premières données suggèrent que la combinaison du finérénone avec des inhibiteurs du SGLT2 et des agonistes des récepteurs GLP-1 offre un bénéfice rénal supplémentaire tout en réduisant le risque d’ hyperkaliémie (30, 31). Actuellement, le finérénone est recommandé en complément des IEC ou des ARA chez les patients diabétiques de type 2, afin de réduire les événements cardiovasculaires et la progression de l’ insuffisance rénale (pour une DFGe > 60 ml/min/1.73 m² et un UACR ≥ 300 mg/g ou une DFGe de 25–60 ml/min/1.73 m² et un UACR ≥ 30 mg/g). (32).
Mesures en cas d’ hyperkaliémie
Exclusion d’ une pseudo-hyperkaliémie:
En présence d’ une élévation du potassium sérique, il faut d’ abord écarter toute erreur préanalytique, par exemple par:
• Hémolyse (stase prolongée, vide excessif)
• Déplacement intracellulaire (effet du glucose à 25–30 °C)
• Centrifugation retardée (> 2 h) ou temps de repos insuffisant du sang total (< 20 min)
En cas de suspicion de pseudo-hyperkaliémie, il convient de répéter la prise de sang et de doser en parallèle la créatinine, la LDH ainsi que de réaliser, cliniquement, une gazométrie sanguine.
Recherche des causes en cas d’ hyperkaliémie confirmée
Examiner s’ il s’ agit d’ une ingestion excessive (aliments riches en potassium, sels de substitution), d’ une destruction cellulaire (rhabdomyolyse, lyse tumorale, hémolyse), d’ un trouble de la répartition (acidose, déficit en insuline), d’ une altération de l’ élimination rénale ou d’ un hypoaldostéronisme. Il faut également vérifier la médication concomitante (par exemple, AINS, bêta-bloquants, diurétiques épargneurs de potassium) et le statut volémique.
En cas d’ hyperkaliémie sévère, les médicaments de blocage du SRAA doivent être interrompus (2, 15, 18).
Une autre mesure visant à réduire le taux de potassium consiste, si cela est indiqué, à utiliser un inhibiteur de SGLT2, qui entraîne une diminution significative du taux de potassium sérique. Cela a pu être démontré dans un grande méta-analyse de 6 études RCT portant sur 49 875 patients atteints de DT2 et présentant un risque cardiovasculaire élevé ou IRC avec une hyperkaliémie sévère ≥ 6.5 mmol/l sans risque d’ hypokalièmie (33).
Liants modernes du potassium selon KDIGO 2024
Cyclosilicate de sodium (CCS) (Lokelma®)
• Mécanisme d’ action: se lie au potassium dans le tractus gastro-intestinal en échange de Na+ et de H+
• Début d’ action: 1–12 h; effets secondaires: troubles gastro-intestinaux légers, hypokaliémie (3–4 %), œdèmes
• Dosage: Initialement 3 × 10 g (chacun dans 45 ml d’ eau), puis 5 g tous les 2 jours jusqu’ à un maximum de 10 g/jour
Patiromer (Veltassa®) (35)
• Mécanisme d’ action: se lie au potassium dans le côlon en échange de Ca²+
• Début d’ action: 4–24 h; effets secondaires: troubles gastro-intestinaux légers, hypokaliémie, hypomagnésémie, intolérance au fructose
• Dosage: Initialement 1 × 8,4 g dans 80 ml d’ eau; augmentation progressive jusqu’ à un maximum de 25,2 g/jour
• Remarque: laisser un intervalle de 3 heures par rapport rapport aux médicaments dont la biodisponibilité pH-dépendante peut être affectée (par exemple, ciprofloxacine, lévothyroxine, metformine).
Autre prise en charge
• Si le taux de K est < 5 mEq/l, la thérapie par inhibiteurs du SRAA doit être intensifiée – un contrôle régulier du potassium est essentiel.
• Pour la prévention, en particulier en cas d’ hyperkaliémie aiguë ou chronique, des diurétiques et – si indiqué – des inhibiteurs du SGLT2 sont utilisés, ceux-ci réduisant significativement le potassium sérique (HR: 0,84) sans risque d’ hypokaliémie.
Traitement d’ urgence en cas d’ hyperkaliémie sévère (≥ 6,5 mmol/l)
Déplacement intracellulaire du potassium
• Administration IV d’ insuline + glucose et/ou inhalation de salbutamol
– En cas d’ acidose (< 18 mmol/l de bicarbonate), administration de NaHCO₃
– Pour un K ≥ 6,5 mmol/l, ajout d’ une administration IV de calcium
– Remarque: Ces mesures sont transitoires et peuvent entraîner un phénomène de rebond.
Élimination du potassium
Selon le statut volémique: administration IV de Lasix ou apport volumique
• En cas de MRC sévère/insuffisance rénale terminale, recours à l’ hémodialyse
• Utilisation d’ un liant moderne du potassium
Recommandation des lignes directrices
Selon les recommandations internationales (ERC, AHA/ACC/HFSA, KDIGO, ESC), en cas de taux de K ≥ 6.0 mmol/l, un liant moderne du potassium, patiromer ou CCS (35, 36), devrait être instauré, sauf si une étiologie traitable est identifiée. Ces médicaments réduisent le taux de potassium sérique d’ environ 1 mmol/l et permettent chez de nombreux patients l’ initiation ou l’ augmentation de la thérapie par inhibiteurs du SRAA ou par antagonistes des récepteurs minéralocorticoïdes (MRA) (dans 74–89 % des cas). Un contrôle quotidien du potassium n’ est pas nécessaire, mais une surveillance régulière des électrolytes est recommandée.
Cet article est une traduction (version courte) de «der informierte arzt – die informierte ärztin» 02_2025
Copyright
Aerzteverlag medinfo AG
Zelglistrasse 17
8127 Forch
L’ auteur n’ a pas déclaré de conflit d’ intérêts en rapport avec cet article.
1. Palmer BF, Clegg DJ. Diagnose und Behandlung der Hyperkali- ämie. Cleve Clin J Med. 2017; 84 (12):934-942. DOI: 10.3949/ CCJM.84A.17056. PMID: 29244647.
2. Cardiomed Live Vortrag «Hyperkaliämie im Spektrum der Kardiologie» vom 02.12.2024: Prof. Dres: M.Boehm, Homburg/ D. Berliner, Hanno- ver/ B. Assmus, Giessen u. Marburg/ I. Emrich Saarland
3. Gilbertson D. et al., Nephrol Dial Transplant 2018;33 (suppl 1) Abs SP 324
4. Humphrey T. et al., How common is hyperkalaemia? A systema- tic review and meta-analysis of the prevalence and incidence of hyperkalaemia reported in observational studies, Clinical Kidney J 2021,15(4):727-737
5. Thomsen RW et al. Elevated potassium levels in patients with chronic kidney disease: occurrence, risk factors and clinical outcomes-a Danish population-based cohort study. Nephrol Dial Transplant. 2018 Sep 1;33(9):1610-1620. doi: 10.1093/ndt/gfx312.
6. Bakris G. et al., Effects of recurrent hyperkalaemia on cardiovascular outcomes and mortality JACC Adv. 2024 Nov, 3 (11) 101331
7. Clase CM et al., Potassium homeostasis and management of dyskale- mia in kidney diseases: conclusions from a Kidney Disease: Impro- ving Global Outcomes (KDIGO) Controversies Conference, Kidney Int.2020;97:42-61
8. Montague BT. et al., Retrospective review frequency of ECG changes in hyperkalemia, Clin J Am Soc Nephrol. 2008;3(2):324-330
9. Tromp et al., A Systematic Review and Network Meta-Analysis of Pharmacological Treatment of Heart Failure With Reduced Ejection Fraction, JACC Heart Fail.
2022;10(2):73-84
10. Heidenreich PA. et al., 2022 AHA/ACC/HFSA Guideline for the Management of Heart Failure: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines Circulation 2022;145(18):e895-e1032
11. Fonarow GC et al., Rapid and Intensive Guideline-Directed Medical Therapy for Heart Failure, JACC 2023,81 (22):2145-2148
12. Vardeny O et al., Incidence, predictors, and outcomes related to hypo- and hyperkalemia in patients with severe heart failure treated with a mineralocorticoid receptor antagonist. Circ Heart Fail. 2014 Jul;7(4):573-579
13. Mebazaa A. et al., Safety, tolerability and efficacy of up-titration of guideline-directed medical therapies for acute heart failure (STRONG-HF): a multinational, open-label, randomised, trial, Lancet 2022 Dec 3;400 (10367):1938-1952
14. Komajda M. et al., Physicians’ adherence to guideline-recommended medications in heart failure with reduced ejection fraction: data from the QUALIFY global survey, eur j heart fail 2016, 18:514-522
15. McDonagh TA et al
16. Epstein M. et al., Evaluation of the treatment gap between clinical guidelines and the utilization of renin-angiotensin-aldosterone system inhibitors, Am J Manag Care, 2015 Sep.;21(11 Suppl): S212-20.
17. Mc Murray J.J.V. et al., Angiotensin–Neprilysin Inhibition versus Enalapril in Heart Failure, PARADIGM-HF, N Engl J Med 2014;371:993-1004
18. Mullens W. et al., Renal effects of guideline-directed medical therapies in heart failure: a consensus document from the Heart Failure Association of the European Society of Cardiology Eur J Heart Fail 2022 Apr;24(4):603-619. doi: 10.1002/ejhf.2471. Epub 2022 Mar 27
19. B. Pitt et al., The Effect of Spironolactone on Morbidity and Mortality in Patients with Severe Heart Failure, N Engl J Med 1999;341:709-717
20. Zannad F. et al., Eplerenone in patients with systolic heart failure and mild symptoms, EMPHASIS-HF, N Engl J Med 2011 Jan 6;364(1):11-21
21. Salomo S.D. et al., Finerenone in Heart Failure with Mildly Reduced or Preserved Ejection Fraction, FINEARTS-HF, N Engl J Med 2024 September 1, 2024, 391:1475-1485, DOI: 10.1056/NEJMoa2407107
22. Vardeny O. et al., Finerenone, Serum Potassium, and Clinical Outcomes in Heart Failure With Mildly Reduced or Preserved Ejection Fraction, JAMA Cardiol 2025 Jan 1;10(1):42-48. doi: 10.1001/jamacardio.2024.4539
23. M. Chimura et al., Finerenone in Women and Men With Heart Failure With Mildly Reduced or Preserved Ejection Fraction: A Secondary Analysis of the FINEARTS-HF Randomized Clinical Trial, JAMA Cardiol 2025 Jan 1;10(1):59-70. doi: 10.1001/jamacardio.2024.4613
24. Desai A.S. et al., Finerenone in Patients With a Recent Worsening Heart Failure Event The FINEARTS-HF Trial, JACC 2025, 85(2): 106-116
25. Causland Mc F.R. et al., Finerenone and renal outcomes in patients with heart failure: the FINEARTS-HF study, JACC. 2025 Januar, 85 (2) 159–168 DOI: 10.1016/J.JACC.2024.10.091. Epub 25. Oktober 2024
26. Matsumoto S et al. Initial Decline in Glomerular Filtration Rate With Finerenone in HFmrEF/HFpEF. J Am Coll Cardiol 2025;85:173–185; https://doi.org/10.1016/j.jacc.2024.11.020
27. Vaduganathan M. et al., Effects of the Nonsteroidal MRA Finerenone With and Without Concomitant SGLT2 Inhibitor Use in Heart Failure, Circulation 2025;151:149–158. DOI: 10.1161/CIRCULATIONAHA.124.072055
28. Jhund P.S. et al., Mineralocorticoid receptor antagonists in heart failure: an individual patient level, meta-analysis, Lancet 2024; 404( 10458):1119-1131
29. Agarwal R et al., Cardiovascular and kidney outcomes with finerenone in patients with type 2 diabetes and chronic kidney disease: the FIDELITY pooled analysis, Eur Heart J 2022 Feb. 10;43(6):474-484
30. Singh A. et al., ASN Kidney Week 2024, Abstract TH-OR46
31. Fu E.L. et al., SGLT-2 inhibitors, GLP-1 receptor agonists and DPP-4 inhibitors and risk of hyperkalaemia among people with type 2 diabetes in clinical practice: population based cohort study, BMJ 2024; 385:e078483
32. Marx-Schütt K. et al., Konsensuspapier zum Management kardiovasulärer Erkrankungen bei chronischer Nierenkrankheit, Konsensuspapier DGK u. DGfN, Die Kardiologie 2025,https:// doi.org/10.1007/s12181-024-00716-6
33. Neuen BL. et al., Sodium-Glucose Cotransporter 2 Inhibitors and Risk of Hyperkalemia in People With Type 2 Diabetes: A Meta-Analysis of Individual Participant Data From Randomized, Controlled Trials, Circulation 2022,145, (19): 1460-1470
34. KDIGO 2024, CLINICAL PRACTICE GUIDELINE FOR THE EVALUATION AND MANAGEMENT OF CHRONIC KIDNEY DISEASE, Kidney International (2024) 105 (Suppl 4S), S117–S314
35. Butler J. et al., Patiromer for the management of hyperkalemia in heart failure with reduced ejection fraction: the DIAMOND trial, Eur Heart J, 43, 41, 1 November 2022: 4362–4373
36. Kosiborod MN. et al., Sodium Zirconium Cyclosilicate for Management of Hyperkalemia During Spironolactone Optimization in Patients with Heart Failure, J Am Coll Cardiol. 2024 Nov 15: S0735-1097(24)10430
37. Rastogi A, et al. ZORA: Maintained RAASi Therapy with Sodium Zirconium Cyclosilicate Following a Hyperkalaemia Episode: A Multi-Country Cohort Study, presented at American Society of Nephrology Kidney Week, 1-5th November 2023, Philadelphia, PA, USA