- Insuffisance rénale chronique
L’ insuffisance rénale chronique est une maladie longtemps silencieuse, dont le diagnostic précoce est primordial afin d’ établir une prise en charge et des traitements permettant d’ en ralentir la progression et de diminuer la morbi-mortalité associée. Une approche multidisciplinaire est indispensable.
L’ insuffisance rénale chronique (IRC) est une maladie très prévalente et grevée d’ un haut taux de morbi-mortalité, particulièrement cardiovasculaire(1). La détection des patients qui en souffrent n’ est toutefois pas aisée, puisque la maladie rénale chronique reste silencieuse jusque dans les stades avancés. Il existe néanmoins plusieurs mesures permettant de ralentir sa progression, raison pour laquelle il est important de la rechercher activement, surtout chez les patients à risque. Par ailleurs, même si cette prise en charge précoce ne permet pas d’ éviter l’ évolution vers l’ insuffisance rénale dite terminale, c’ est-à-dire nécessitant le recours à la dialyse ou/et à la transplantation rénale, elle diminue la morbi-mortalité associée à l’ IRC.
Classification de l’ Insuffisance Rénale Chronique
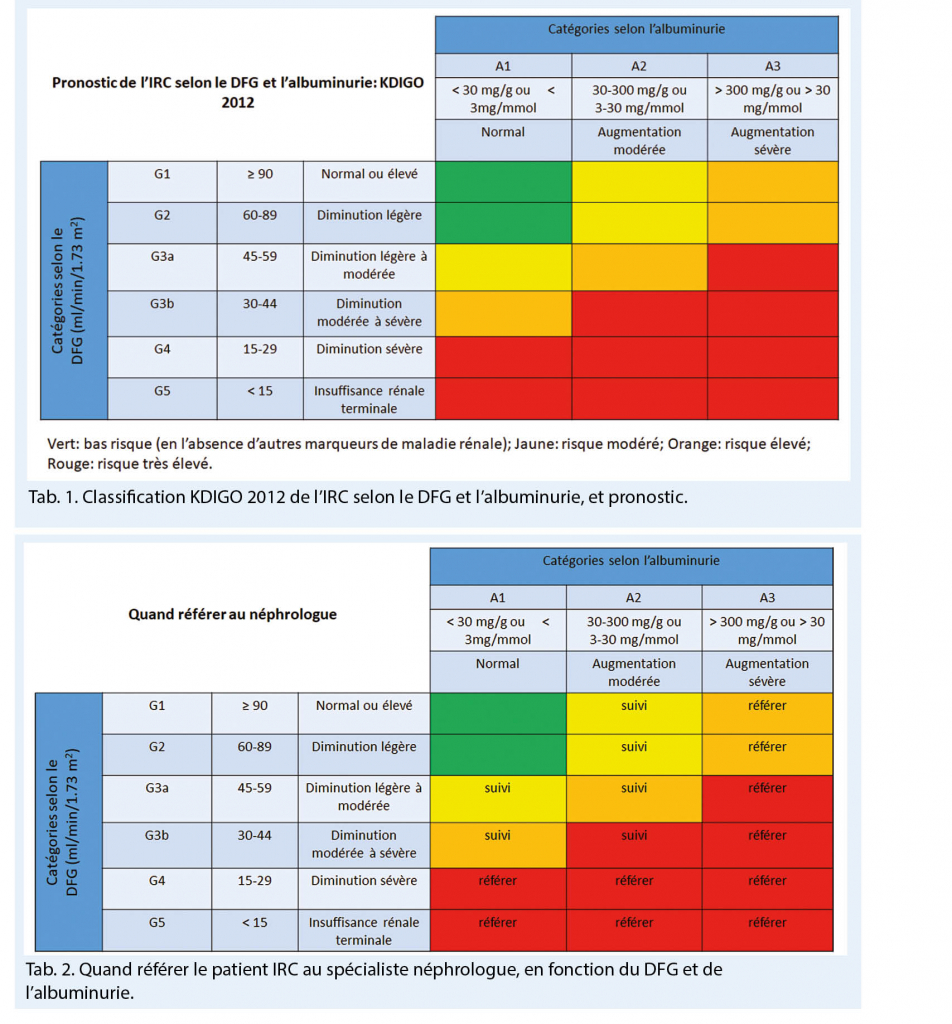
Afin d’ aider le médecin dans sa prise en charge des patients insuffisants rénaux chroniques, une classification tenant compte à la fois de la valeur du débit de filtration glomérulaire (DFG) mais également de l’ albuminurie, a été développée. Cette classification caractérise la maladie rénale en 5 stades de sévérité croissante, indépendamment de la néphropathie sous-jacente (Table 1)(2).
L’ IRC est définit par la société internationale de néphrologie- KDIGO (Kidney Disease Improving Global Outcomes) comme une altération de la fonction rénale avec un DFG < 60 ml / min/1.73 m2 et/ou de la structure rénale depuis au moins 3 mois, une albuminurie > 30 mg / j, des anomalies du sédiment urinaire, une dysfonction tubulaire, des anomalies structurelles à l’ imagerie rénale, ou la transplantation rénale.
Le DFG est le meilleur index de la fonction rénale. Plusieurs équations pour le calcul du DFG ont été développées au cours des années (Cockcroft-Gault, MDRD, etc). L’ équation CKD-EPI est la plus fiable et est largement utilisée depuis 2009(3). Le DFG est exprimé en ml / min / 1.73 m2. La valeur est donc ajustée à une surface corporelle standardisée ce qui permet de l’ estimer sans connaitre le poids et la taille du patient. Chez les patients avec des surfaces corporelles très différentes, il est important de désajuster la valeur du DFG à la surface corporelle afin d’ obtenir une valeur représentative de la filtration glomérulaire notamment pour l’ adaptation des doses de médicaments. Par ailleurs, la formule CKD-EPI utilisée prend en compte la créatininémie. La valeur de créatinine dépendant de la masse musculaire, cette équation n’ est pas suffisamment précise si elle est utilisée chez un patient cachectique, obèse ou dénutri. Dans ces différents cas, on utilisera alors une variante l’ équation CKD-EPI basée sur la cystatine C (4). Plusieurs calculateurs sont disponibles en application (Qxmd calculate, etc).
Etiologie de l’ Insuffisance Rénale Chronique
L’ anamnèse détaillée permettra de rechercher des antécédents médicaux tels qu’ une hypertension ou un diabète, une histoire de maladie lithiasique, une anamnèse familiale positive de maladie rénale, des antécédents d’ infections urinaires à répétition, d’ hématurie, d’ œdèmes, ainsi que des symptômes systémiques compatibles avec une maladie immunologique ou inflammatoire. Il ne faut pas oublier la prématurité, la pré éclampsie, la prise chronique médicamenteuse et les épisodes d’ insuffisance rénale aigüe, à rechercher dans les antécédents. L’ examen clinique est assez peu spécifique hormis la palpation des reins polykystiques, mais doit comporter une mesure soignée de la tension artérielle, ainsi que la recherche de souffles cardiaques et vasculaires ainsi que d’ éventuelles lésions cutanées. Les causes les plus fréquentes d’ insuffisance rénale chronique dans la population sont le diabète et l’ hypertension. A elles deux, ces pathologies comprennent environ 60% des causes d’ IRC. Néanmoins, ce chiffre est surestimé en raison de la difficulté à différencier une hypertension primaire d’ une hypertension secondaire à une maladie rénale. En revanche, les glomérulonéphrites et les néphrites interstitielles sont sous-diagnostiquées.
Le bilan biologique a pour but de préciser le diagnostic suspecté par l’ anamnèse et l’ examen clinique ainsi que d’ évaluer les conséquences de l’ IRC. Le bilan de départ doit comprendre la recherche d’ une anémie, de troubles électrolytiques, acido-basiques et du métabolisme phosphocalcique, de même qu’ un sédiment urinaire complet. Le sédiment urinaire permettra de rechercher une hématurie voire de l’ identifier comme glomérulaire ou non-glomérulaire (selon les laboratoires). Par ailleurs, le rapport protéinurie/créatininurie sera quantifié par un spot urinaire. Un bilan immunologique, une immunoélectrophorèse des protéines à la recherche d’ une gammapathie monoclonale ainsi qu’ un dépistage des sérologies virales HIV, HBV et HCV doivent être considérés. L’ analyse structurelle des reins (taille, épaisseur corticale, différentiation corticomédullaire, kystes, rein unique) ainsi que leur vascularisation sera précisée par un ultrason de l’ appareil urinaire, qui permettra également d’ exclure une cause obstructive. Une biopsie rénale sera envisagée dans le syndrome néphrotique d’ origine non diabétique, dans les glomérulonéphrites rapidement progressives ou si l’ étiologie de l’ insuffisance rénale n’ est pas claire malgré les examens.
Prise en charge
Une fois le diagnostic établi, le traitement peut être spécifique comme par exemple un traitement immunosuppresseur dans la néphrite lupique ou métabolique comme le contrôle optimal du diabète dans la néphropathie diabétique. Dans toutes les situations, la prise en charge des patients souffrant d’ insuffisance rénale chronique comporte des mesures « néphroprotectrices » afin de ralentir la progression de la maladie. Parmi celles-ci, le traitement de l’ hypertension est essentiel, car son impact est le plus important sur la progression de l’ IRC. Les cibles de l’ hypertension ont été récemment révisées. Les guidelines européennes de 2018 préconisent de viser une tension artérielle systolique comprise entre 130 et 139 mmHg(5). Au-delà de cette cible, un traitement antihypertenseur sera introduit, en association avec des mesures hygiéno-diététiques telles que l’ activité physique et la restriction en apport sodé (< 5g de sel/24h). Les inhibiteurs de l’ enzyme de conversion (IEC) et du système rénine-angiotensine (SRA) seront à prescrire en priorité, en raison de leur effet néphroprotecteur démontré. Les deux autres interventions qui freinent la progression sont la restriction protéique et la correction de l’ acidose métabolique. La restriction protéique modérée (0.8 g de protéines / kg poids corporel / jour) comporte peu de risque de malnutrition, et est facile à implémenter(6). Une restriction plus importante, plus efficace, nécessite un suivi diététique et se discute de cas en cas.
Un point primordial de la prise en charge est l’ éviction des néphrotoxiques, qu’ il s’ agisse de médicaments (ex. AINS), de l’ exposition au produit de contraste (dans la mesure du possible), ou de situations pouvant engendrer une déshydratation aigue, elle-même responsable d’ une insuffisance rénale aigue. Le patient doit être éduqué afin qu’ il prenne l’ habitude de stopper transitoirement ses traitements anti hypertenseurs, ou ses diurétiques en cas de diarrhées, vomissements, ou lors de fortes chaleurs, ou qu’ il discute avec son médecin traitant l’ introduction de nouveau médicament par un tiers. En effet, il est indispensable d’ être attentif lors de la prescription des médicaments à leur mode d’ élimination et d’ adapter la dose en cas d’ élimination rénale. L’ éduction thérapeutique prend ici toute son importance pour amener le patient à comprendre sa maladie et son évolution, les enjeux du traitement et l’ amener à devenir actif dans sa prise en charge médicale. Par ailleurs, les recommandations KDIGO préconisent la prescription d’ une statine chez tous patients de plus de 50 ans connu pour une IRC, quelles que soient les valeurs du bilan lipidique en raison du risque cardiovasculaire très élevé associé à l’ IRC.
Traitement
L’ IRC se complique de plusieurs perturbations biologiques, qui peuvent être corrigées par des adaptations que ce soit au niveau diététique ou des traitements. Ces adaptations sont essentielles même si elles ne modifient pas toutes la progression vers l’ insuffisance rénale terminale. Elles modifient en revanche la morbi-mortalité cardiovasculaire et la qualité de vie.
L’ anémie rénale est un diagnostic d’ exclusion (7). Elle est rare au-dessus d’ un DFG de 30 ml / min / 1.73 m2 (8). Avant de retenir le diagnostic d’ anémie rénale, des carences en vitamine B12, folates et fer doivent être exclues. Par ailleurs, la recherche de spoliation doit être effectuée si l’ anamnèse ou les antécédents le font suspecter. Une cause hématologique doit également être évoquée. A noter que la carence martiale se définit chez le patient IRC par une ferritine < 300-500 µg / l associée à une saturation de la transferrine < 30%. Le cas échéant, la substitution martiale s’ administre de préférence par voie intraveineuse. Après correction des carences, si l’ anémie persiste, le traitement consiste en des injections d’ EPO, pour viser une valeur d’ hémoglobine comprise entre 100 et 115 g / l. Les injections se font par voie sous-cutanée.
Une autre complication fréquente en cas d’ IRC est la survenue d’ hyperkaliémie. En plus du défaut d’ excrétion rénale, plusieurs médicaments régulièrement prescrits dans l’ IRC peuvent augmenter le risque (ex : IEC, SRA, spironolactone…)(9). Une diminution des aliments riches en potassium (fruits et légumes essentiellement) doit être conseillée avec si nécessaire une consultation diététique. Il n’ est pas rare qu’ il faille stopper des médicaments hyperkaliémants voire de prescrire des résines qui captent le potassium digestif. Une surveillance régulière de la kaliémie est nécessaire.
L’ hyperphosphatémie favorise les calcifications vasculaires et est associée à une augmentation de la mortalité cardiovasculaire (10). Il est donc essentiel de la corriger même s’ il est difficile de démontrer l’ impact des interventions sur la mortalité. L’ apport de phosphates étant exogène, une consultation diététique sera très utile afin de conseiller le patient sur les aliments et boissons à éviter. Cette consultation devra se faire en tenant compte des autres ajustements diététiques mentionnés ci-dessus (apports protéiques, apports en potassium, etc). Si l’ approche diététique est insuffisante, deux types de chélateurs du phosphate sont à notre disposition. Tout d’ abord, les chélateurs calciques : ceux-ci comportent un risque augmenté de calcification vasculaire surtout si l’ apport de calcium élémentaire est supérieur à 1500 mg/j (alimentation comprise). Leur utilisation est conseillée aux patients présentant une hypocalcémie ou un bilan calcique négatif. Les chélateurs non calciques sont préférés en cas d’ hypercalcémie. Leur efficacité n’ est pas supérieure, mais les risques d’ hypercalcémie sont diminués. Leurs effets sur les calcifications vasculaires montrent une tendance favorable mais les évidences sont faibles. En revanche, les prix sont nettement plus élevés et leur prescription peut être restreinte (ou non remboursée) chez le patient non dialysé. N’ étant pas absorbés, ils sont généralement bien tolérés mais des effets secondaires digestifs tels des douleurs abdominales, une constipation ou des nausées peuvent survenir. L’ acidose métabolique est également une complication de l’ insuffisance rénale (11). Elle se définit par une valeur de bicarbonates inférieure à 22 mmol / l. L’ acidose métabolique peut aggraver une hyperkaliémie. Nous recommandons une correction par l’ administration de bicarbonates per os, en visant un taux sanguin normal (12). La correction de l’ acidose métabolique ralentit la progression de l’ IRC, réduit la déminéralisation osseuse, et améliore le bilan nutritionnel.
Quand l’ IRC s’ aggrave, l’ avis du spécialiste peut devenir nécessaire (Table 2)(13). Le néphrologue pourra également aborder au cours de sa consultation, les sujets de la substitution rénale par la dialyse ou la transplantation rénale au moment opportun.
L’ insuffisance rénale chronique nécessite donc une prise en charge globale afin d’ en ralentir la progression.
HUG, Service de Néphrologie
Département des Spécialités de Médecine
4, rue Gabrielle Perret Gentil
1211 Genève 14
cyrielle.alves@hcuge.ch
HUG, Service de Néphrologie
Département des Spécialités de Médecine
4, rue Gabrielle Perret Gentil
1211 Genève 14
Les auteurs n’ ont déclaré aucun conflit d’ intérêts en relation avec cet article.
- La détection précoce de l’ IRC est essentielle afin de ralentir sa progression.
- L’ éviction de tout néphrotoxique est indispensable.
- Un bon contrôle biologique permettra de diminuer la survenue de complications cardiovasculaires.
1. Webster et al. Chronic Kidney Disease. Lancet 2017;389(10075):1238-1252.
2. KDIGO 2012 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease
3. AS Levey et al. A new equation to estimate glomerular filtration rate. Ann Intern Med. 2009;150(9):604-12.
4. Dharnidharka et al. Serum cystatin C is superior to serum creatinine as a marker of kidney function: A meta-analysis. Am J Kidney Dis 2002;40:221-6.
5. 2018 ESC/ESH Guidelines for the management of arterial hypertension. Journal of Hypertension 2018
6. WE Mitch, G Remuzzi. Diets for patients with chronic kidney disease, still worth prescribing. J Am Soc Nephrol 2004;15:234-7.
7. JL Babitt , H Lin. Mechanisms of anemia in CKD. J Am Soc Nephrol 2012;23:1631-4.
8. Astor et al. Association of kidney function with anemia: the Third National Health and Nutrition Examination Survey (1988-1994). Arch Intern Med. 2002;162(12):1401.
9. Gennari, Segal. Hyperkalemia: An adaptive response in chronic renal insufficiency. Kidney Int. 2002;62(1):1.
10. Palmer, Gardner M Tonelli. Phosphate-Binding Agents in Adults With CKD: A Network Meta-analysis of Randomized Trials. Am J Kidney Dis 2016 (68)
11. Kraut N. Madias. Metabolic acidosis of CKD: an update. Am J Kidney Dis 2016 ;67(2):307-17.
12. A Rossier et al. Sodium bicarbonate to slow the progression of chronic kidney disease. Rev Med Suisse 2011;7(284):478-82.
13. NA Smart et al. Early referral to specialist nephrology services for preventing the progression to end-stage kidney disease. Cochrane Database of Systematic Reviews 2014
la gazette médicale
- Vol. 8
- Ausgabe 2
- März 2019