- Lorsque la COVID-19 atteint le quatrième âge
La maladie à coronavirus 2019 (COVID-19) touche de façon disproportionnée la population âgée et met à l’épreuve les Etablissements Médico-Sociaux (EMS). Les hôpitaux étant en crise, avec peu de traitements spécifiques disponibles pendant les premières vagues, il a été souvent décidé de garder les résidents infectés dans leur lieu de vie et de ne pas les transférer à l’hôpital. Les cliniciens responsables de ces patients doivent donc prendre des décisions thérapeutiques. Cette revue résume les traitements à considérer aujourd’hui chez les patients dans les EMS.
Abstract: The coronavirus disease 2019 (COVID-19) is disproportionately affecting the elderly population and is putting a strain on Medical and Social Establishments (EMS). With hospitals in crisis, and with few specific treatments available during the first waves, it was often decided to keep infected residents in their homes and not transfer them to hospital. Clinicians responsible for these patients must therefore make treatment decisions. This review summarises the treatments to be considered today for patients in EMS.
Key Words: Coronavirus disease 2019 (COVID-19), Medical and Social Establishments
Introduction
La pandémie de la maladie à coronavirus 2019 (COVID-19) a mis à mal le système de santé. Au niveau mondial, les premières mesures prises pour alléger la charge hospitalière comprenaient la suspension des chirurgies électives (1), la télémédecine (2) et le maintien des résidents infectés dans les Etablissements Médicosociaux (EMS) (3). La population gériatrique a été touchée de manière disproportionnée par la pandémie. Il y a eu transmission de la COVID-19 au sein même des EMS (4) et l’ âge avancé est un facteur important de mauvaise évolution, voire de mortalité (5, 6). De nombreux EMS ont traité leurs résidents sur place, sans les transférer dans des milieux peu adaptés comme les soins intensifs. Certains ont même instauré des équipes mobiles ou des infrastructures spéciales (3, 4). Face à la pandémie qui dure, la recherche a montré de nouvelles options thérapeutiques.
Cette revue se focalise sur les traitements adaptés aux personnes âgées qui pourraient être utilisés en dehors d’ un contexte hospitalier.
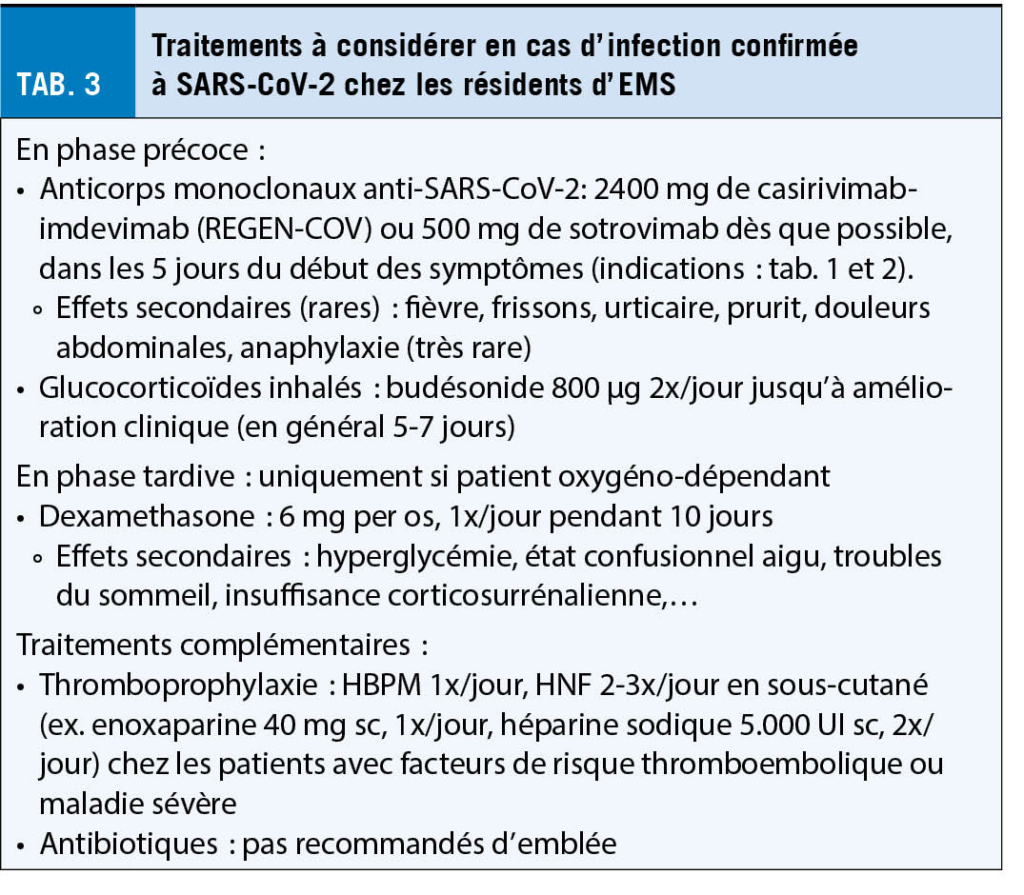
Traitements
En prévention :
Anticorps monoclonaux anti-SARS-CoV-2
Un essai clinique a montré une diminution de 81% du taux d’ infection symptomatique à SARS-CoV2 lors d’ administration de casirivimab et imdevimab (REGEN-COV) dans les 96 heures après un diagnostic de COVID-19 chez une personne vivant sous le même toit (1.5% versus 7.8%, p<0.001). Une dose de 1200 mg de REGEN-COV (600 mg casirivimab et 600 mg imdevimab) était administrée par voie sous-cutanée. Ce traitement était bien supporté, la plupart des participants n’ ayant aucun effet secondaire ou des effets secondaires mineurs (7). Notons que dans cette étude, la population âgée de >65 ans était peu représentée (10%).
Ce traitement n’ est actuellement pas approuvé par Swissmedic dans cette indication.
En phase précoce:
Glucocorticoïdes inhalés
Deux essais cliniques ont montré un effet positif des glucocorticoïdes inhalés en stade précoce sur l’ évolution de la COVID-19 sans réduction de la mortalité.
L’ étude STOIC a montré une diminution du nombre d’ hospitalisations ou de traitements d’ urgence de 14% chez les patients recevant le traitement habituel à 1% chez les patients sous budésonide inhalé (p=0.004). Le nombre de patients à traiter (NNT) pour prévenir une hospitalisation ou traitement d’ urgence était de 8 (8).
L’ étude PRINCIPLE a montré une diminution du temps de récupération de 15 jours dans le groupe contrôle à 12 jours chez les patients sous budésonide inhalé. Cette étude n’ a pas montré de réduction du risque d’ hospitalisation ou de décès à 28 jours par rapport aux soins habituels (9). Au vu d’ un certain bénéfice et d’ une bonne tolérance, le budésonide inhalé 800 µg 2x/jour est recommandé par la Société suisse d’ infectiologie (SSI) comme option de traitement ambulatoire chez les patients présentant une toux sèche, en début d’ évolution et ce, jusqu’ au soulagement des symptômes (5-7 jours) (10). Notons toutefois que les populations âgées étaient peu représentées dans ces études.
Anticorps monoclonaux anti-SARS-CoV-2
Une étude de phase 3 a montré une diminution du taux d’ hospitalisation/décès chez les patients traités par 2 dosages différents de REGEN-COV comparés au placebo. Le dosage de 1200 mg a montré une réduction de 70% du taux d’ hospitalisation/décès (1% versus 3,2%) et la dose de 2400 de 71% (1,3% versus 4,6%). Le NNT était de 28. Le temps médian jusqu’ à résolution des symptômes était de 4 jours plus court avec REGEN-COV (10 jours versus 14 jours ; p<0.001). Le traitement est bien toléré avec de rares effets indésirables de gravité modérée (<0.1% – 0.2%), notamment fièvre, frissons, urticaire, prurit, douleurs abdominales. Un seul épisode d’anaphylaxie a été rapporté durant l’ étude (11). Ces résultats sont similaires à ceux d’ une étude évaluant le sotrovimab, un nouvel anticorps monoclonal anti-SARS-CoV-2, montrant une réduction de 85% du risque d’ hospitalisation/décès. Le sotrovimab aurait l’ avantage théorique d’ être actif contre le variant omicron (12).
Le traitement de REGEN-COV ou de sotrovimab est administré en une seule dose intraveineuse [IV] sur 30 minutes (10). Il pourrait aussi être administré par voie sous-cutanée, mais ce n’ est pas recommandé car étudié uniquement pour la prévention/prophylaxie post-expositionelle (7, 12).
Les anticorps monoclonaux dirigés contre le SARS-CoV-2 sont recommandés par la SSI en phase précoce pour tout patient infecté par le SARS-CoV-2 et présentant des facteurs de risque de mauvaise évolution (tab. 1) (10, 13). Pour l’ instant, la perfusion se fait à l’ hôpital de jour, mais une administration à l’ EMS pourrait être envisageable après accord du médecin traitant en charge et des spécialistes en infectiologie.
Plasma convalescent
Une méta-analyse des études chez des patients hospitalisés a montré un bénéfice avec diminution de la mortalité chez les patients recevant du plasma convalescent. Le NNT pour prévenir un décès était calculé a 11. Un autre élément important pour la diminution de la mortalité était la transfusion précoce dans les 3 jours de l’ admission à l’ hôpital (14). Cependant, en ambulatoire, son utilisation est controversée avec une étude importante ne montrant pas d’ impact sur la mortalité (15) et une autre démontrant une diminution de la mortalité lors d’ une administration chez des patients âgés (≥ 75 ans) dans les 3 jours de l’ apparition des premiers symptômes (16).
A l’ heure actuelle, au vu de la disponibilité d’ anticorps monoclonaux pour la même indication, l’ utilisation de plasma convalescent en Suisse est réservée à des situations particulières (patients sévèrement immunosupprimés) et est effectuée en milieu hospitalier et dans le cadre d’ études cliniques.
La fluvoxamine est un anti-dépresseur, inhibiteur sélectif de la recapture de la sérotonine. Un essai clinique a montré que son utilisation (100 mg 2x/j per os pendant 10 jours) dans les 7 premiers jours de symptômes chez des patients à risque de mauvaise évolution permet de diminuer de 68% le taux d’ hospitalisation/consultations prolongées aux urgences (16% versus 11%) (17). L’ utilisation de fluvoxamine n’ a pas eu d’ effet sur la mortalité. Le taux d’ effets indésirables était similaire entre les deux groupes. Cependant, l’ âge moyen des participants à l’ étude était de 50 ans (17). La sécurité de l’ emploi de fluvoxamine dans une population plus âgée et polymorbide est à vérifier au vu du risque important d’ interactions médicamenteuses avec la fluvoxamine qui est un puissant inhibiteur du cytochrome P450. La fluvoxamine n’ est aujourd’ hui pas recommandée par la SSI.
Le molnupiravir est un antiviral oral, analogue du ribonucléoside. L’ étude de phase 3 MOVe-OUT, a montré que l’ utilisation de molnupiravir chez des patients ambulatoires à risque de mauvaise évolution dans les 5 jours d’ une COVID légère ou modérée, a réduit le risque d’ hospitalisation/décès de 30 % par rapport au placebo (6.8% versus 9.7%, p=0.02) (18). Le traitement était bien toléré.
Le traitement a été approuvé par l’ Agence Européenne des médicaments (EMA : European Medicines Agency) et l’ Agence Américaine des produits alimentaires et médicamenteux (FDA : Food and Drug Administration), mais en exprimant une retenue quant à son efficacité. A noter qu’ au Royaume-Uni, l’ utilisation de ce médicament, n’ est approuvé que dans le cadre d’ un essai clinique
(https://www.panoramictrial.org/). La Task Force Suisse COVID-19 ne s’ est pas encore prononcée sur l’ utilisation du molnupiravir.
En phase tardive :
Dexamethasone
L’ étude RECOVERY a démontré que le traitement par dexaméthasone orale à raison de 6 mg une fois par jour pendant 10 jours réduit de façon significative la mortalité à 28 jours mais uniquement chez les patients hospitalisés nécessitant une supplémentation en oxygène (19). Par contre, chez les patients non-hypoxiques, une méta-analyse montre que leur utilisation peut être néfaste (19, 20).
La dexamethasone fait partie du traitement standard des patients hypoxémiques hospitalisés avec une COVID-19. Il serait envisageable de l’ utiliser chez des résidents d’ EMS devenant oxygéno-dépendants et non-éligibles pour un transfert à l’ hôpital. L’ équipe en charge du patient devra peser le pour et le contre d’ un tel traitement au vu des effets secondaires de la dexamethasone, tels que les états confusionnels ou les décompensations diabétiques (21).
Autres traitements à considérer :
Thromboprophylaxie
La survenue d’ évènements thromboemboliques chez les patients atteints de COVID-19 a bien été démontrée. En milieu hospitalier, divers schémas de thromboprophylaxie à dosage standard et renforcé ont été adoptés. Sauf contre-indication absolue, les recommandations proposent une thromboprophylaxie par héparine sous-cutanée non fractionnée (HNF) deux ou trois fois par jour, héparine de bas poids moléculaire (HBPM) sous-cutanée une fois par jour ou fondaparinux, prophylaxie à adapter au poids des patients (22). En ambulatoire, la thromboprophylaxie reste un sujet débattu et certains experts proposent des algorithmes pour stratification du risque thromboembolique et évaluation de l’ introduction d’ un traitement (23). Une thromboprophylaxie par HBPM ou HNF en sous-cutané chez des cas sélectionnés pourrait être envisagée chez les résidents des EMS avec maladie sévère et/ou facteurs de risque thromboembolique.
Antibiothérapie
La surinfection ou co-infection bactérienne d’ une COVID-19 est rare (<10%) chez les patients hospitalisés (24). Cependant, l’ utilisation d’ antibiotiques est plus importante que les taux réels de co- et surinfection bactérienne sans diminuer la mortalité (25). De ce fait, l’ introduction d’ une antibiothérapie n’ est pas recommandée d’ emblée et reste à corréler à l’ évolution clinique.
Vitamine D
L’ effet immunomodulateur de la vitamine D et son rôle comme booster de l’ immunité innée contre le SARS-CoV-2 est sujet de controverse (26). Une méta-analyse de 3 études montre un certain bénéfice avec une diminution des admissions aux soins intensifs chez les patients recevant une supplémentation en vitamine D sans impact sur la mortalité. Cependant, l’ analyse est limitée par une hétérogénéité importante entre les études (27).
Chez les patients gériatriques, à risque de déclin fonctionnel, atteints de COVID-19, une supplémentation quotidienne en vitamine D est envisageable, compte tenu du potentiel effet bénéfique, bien que controversé, pour la santé musculo-squelettique chez ces patients souvent carencés.
Conclusions
La pandémie a conduit à une utilisation exagérée de traitements contre le SARS-CoV-2 en l’ absence d’ évidence. En tant que médecins, notre rôle est de traiter nos patients mais il est aussi de notre devoir de « primum non nocere ». Les thérapies expérimentales, non-approuvées ou insuffisamment étudiées ne doivent être utilisées que dans le cadre d’ études. Lors de l’ introduction de nouveaux traitements, il est important d’ être conscients de leurs indications, contre-indications et effets indésirables, et ceci encore d’ avantage chez des patients fragiles et polymorbides en EMS.
Abréviations :
ARDS Acute Respiratory Distress Syndrome
COVID-19 nouvelle maladie à coronavirus 2019
EMS Etablissements Médico-sociaux
NNT number needed to treat = nombre de patients à traiter pour prévenir
SSI Société Suisse d’Infectiologie
EMA European Medicines Agency
FDA Food and Drug Administration
HBPM Héparine de bas poids moléculaire
HNF Héparine non fractionnée
Elisavet Stavropoulou1, Dre Eve Rubli Truchard2,
Pr Oriol Manuel1, Dre Noémie Boillat-Blanco1
1 Centre Hospitalier Universitaire Vaudois, Service des maladies
infectieuses, Département de Médecine, Lausanne
2 Centre Hospitalier Universitaire Vaudois ; Service de gériatrie et
réadaptation gériatrique, Département de Médecine, Lausanne
noemi.boillat@chuv.ch
Copyright Aerzteverlag medinfo AG
Centre Hospitalier Universitaire Vaudois, Service des maladies
infectieuses, Département de Médecine
Lausanne
noemi.boillat@chuv.ch
Centre Hospitalier Universitaire Vaudois, Service des maladies
infectieuses, Département de Médecine
Lausanne
Les auteurs n’ ont aucun conflit d’ intérêts à déclarer.
◆ Chez les patients atteints de COVID-19 précoce avec des facteurs de risque de progression vers une maladie grave, un traitement par
anticorps monoclonaux anti-SARS-CoV-2 est recommandé dans les
5 jours du diagnostic.
◆ La dexamethasone est indiquée uniquement en cas de COVID-19 hypoxique, sinon risque d’être néfaste. Les effets secondaires sont à prendre en compte dans la balance risques-bénéfices
◆ La co-infection/surinfection bactérienne est rare en cas de COVID-19 et l’administration d’antibiotiques n’est pas recommandée.
◆ Chez des patients atteints d’une maladie sévère ou avec des facteurs de risques thromboemboliques, une thromboprophylaxie par héparine de bas poids moléculaire doit être envisagée.
1. Collaborative CO. Elective surgery cancellations due to the COVID-19 pandemic: global predictive modelling to inform surgical recovery plans. Br J Surg. 2020;107(11):1440-9.
2. Patel SY, Mehrotra A, Huskamp HA, Uscher-Pines L, Ganguli I, Barnett ML. Trends in Outpatient Care Delivery and Telemedicine During the COVID-19 Pandemic in the US. JAMA Intern Med. 2021;181(3):388-91.
3. Poupin P, N’Diaye D, Chaumier F, Lemaignen A, Bernard L, Fougere B. Management of COVID-19 in a French Nursing Home: Experiences from a Multidisciplinary Mobile Team. J Frailty Aging. 2021;10(4):363-6.
4. Stall NM, Farquharson C, Fan-Lun C, Wiesenfeld L, Loftus CA, Kain D, et al. A Hospital Partnership with a Nursing Home Experiencing a COVID-19 Outbreak: Description of a Multiphase Emergency Response in Toronto, Canada. J Am Geriatr Soc. 2020;68(7):1376-81.
5. Wolff D, Nee S, Hickey NS, Marschollek M. Risk factors for Covid-19 severity and fatality: a structured literature review. Infection. 2021;49(1):15-28.
6. Cangiano B, Fatti LM, Danesi L, Gazzano G, Croci M, Vitale G, et al. Mortality in an Italian nursing home during COVID-19 pandemic: correlation with gender, age, ADL, vitamin D supplementation, and limitations of the diagnostic tests. Aging (Albany NY). 2020;12(24):24522-34.
7. O’Brien MP, Forleo-Neto E, Musser BJ, Isa F, Chan KC, Sarkar N, et al. Subcutaneous REGEN-COV Antibody Combination to Prevent Covid-19. N Engl J Med. 2021;385(13):1184-95.
8. Ramakrishnan S, Nicolau DV, Jr., Langford B, Mahdi M, Jeffers H, Mwasuku C, et al. Inhaled budesonide in the treatment of early COVID-19 (STOIC): a phase 2, open-label, randomised controlled trial. Lancet Respir Med. 2021;9(7):763-72.
9. Yu LM, Bafadhel M, Dorward J, Hayward G, Saville BR, Gbinigie O, et al. Inhaled budesonide for COVID-19 in people at high risk of complications in the community in the UK (PRINCIPLE): a randomised, controlled, open-label, adaptive platform trial. Lancet. 2021;398(10303):843-55.
10. SSI. Guidelines, COVID-19 : Options thérapeutiques chez les patients suivis en ambulatoire. 2021 [updated 08.09.2021. Available from: https://ssi.guidelines.ch/guideline/3930/33111.
11. Weinreich DM, Sivapalasingam S, Norton T, Ali S, Gao H, Bhore R, et al. REGEN-COV Antibody Combination and Outcomes in Outpatients with Covid-19. N Engl J Med. 2021.
12. Gupta A, Gonzalez-Rojas Y, Juarez E, Crespo Casal M, Moya J, Falci DR, et al. Early Treatment for Covid-19 with SARS-CoV-2 Neutralizing Antibody Sotrovimab. N Engl J Med. 2021;385(21):1941-50.
13. Recommandations de la Société suisse d’ infectiologie (SSI) et du Clinical Care Group (CCG) de la Swiss National COVID-19 Science Task Force concernant l’ utilisation de thérapies par anticorps monoclonaux. [updated 28 avril 2021. Available from: https://ssi.guidelines.ch/api/filestore/XySWVs5IiWPS7P5ppdCrogpxSxJZ8YsSUXARkg/data/Empfehlungen-der-schweizerischen-gesellschaft-fuer-infektiologie-ssi-und-clinical-care-group-ccg-der-swiss-national-covid-19-science-task-force-zum-einsatz-monoklonaler-antikoerpertherapien.pdf.
14. Klassen SA, Senefeld JW, Johnson PW, Carter RE, Wiggins CC, Shoham S, et al. The Effect of Convalescent Plasma Therapy on Mortality Among Patients With COVID-19: Systematic Review and Meta-analysis. Mayo Clin Proc. 2021;96(5):1262-75.
15. Korley FK, Durkalski-Mauldin V, Yeatts SD, Schulman K, Davenport RD, Dumont LJ, et al. Early Convalescent Plasma for High-Risk Outpatients with Covid-19. N Engl J Med. 2021.
16. Libster R, Perez Marc G, Wappner D, Coviello S, Bianchi A, Braem V, et al. Early High-Titer Plasma Therapy to Prevent Severe Covid-19 in Older Adults. N Engl J Med. 2021;384(7):610-8.
17. Reis G, Dos Santos Moreira-Silva EA, Silva DCM, Thabane L, Milagres AC, Ferreira TS, et al. Effect of early treatment with fluvoxamine on risk of emergency care and hospitalisation among patients with COVID-19: the TOGETHER randomised, platform clinical trial. Lancet Glob Health. 2022;10(1):e42-e51.
18. Jayk Bernal A, Gomes da Silva MM, Musungaie DB, Kovalchuk E, Gonzalez A, Delos Reyes V, et al. Molnupiravir for Oral Treatment of Covid-19 in Nonhospitalized Patients. N Engl J Med. 2021.
19. Group RC, Horby P, Lim WS, Emberson JR, Mafham M, Bell JL, et al. Dexamethasone in Hospitalized Patients with Covid-19. N Engl J Med. 2021;384(8):693-704.
20. Sahu AK, Mathew R, Bhat R, Malhotra C, Nayer J, Aggarwal P, et al. Steroids Use in Non-Oxygen requiring COVID-19 Patients: A Systematic Review and Meta-analysis. QJM. 2021.
21. Noreen S, Maqbool I, Madni A. Dexamethasone: Therapeutic potential, risks, and future projection during COVID-19 pandemic. Eur J Pharmacol. 2021;894:173854.
22. Spyropoulos AC, Levy JH, Ageno W, Connors JM, Hunt BJ, Iba T, et al. Scientific and Standardization Committee communication: Clinical guidance on the diagnosis, prevention, and treatment of venous thromboembolism in hospitalized patients with COVID-19. J Thromb Haemost. 2020;18(8):1859-65.
23. Skeik N, Smith JE, Patel L, Mirza AK, Manunga JM, Beddow D. Risk and Management of Venous Thromboembolism in Patients with COVID-19. Ann Vasc Surg. 2021;73:78-85.
24. Garcia-Vidal C, Sanjuan G, Moreno-Garcia E, Puerta-Alcalde P, Garcia-Pouton N, Chumbita M, et al. Incidence of co-infections and superinfections in hospitalized patients with COVID-19: a retrospective cohort study. Clin Microbiol Infect. 2021;27(1):83-8.
25. Schons MJ, Caliebe A, Spinner CD, Classen AY, Pilgram L, Ruethrich MM, et al. All-cause mortality and disease progression in SARS-CoV-2-infected patients with or without antibiotic therapy: an analysis of the LEOSS cohort. Infection. 2021.
26. Vimaleswaran KS, Forouhi NG, Khunti K. Vitamin D and covid-19. BMJ. 2021;372:n544.
27. Shah K, Saxena D, Mavalankar D. Vitamin D supplementation, COVID-19 and disease severity: a meta-analysis. QJM. 2021;114(3):175-81.
la gazette médicale
- Vol. 11
- Ausgabe 1
- Januar 2022