- Maculopathie
La maculopathie est un terme générique qui définit toutes pathologies de la zone centrale de la rétine appelée macula. Cette région anatomique est responsable de la vision fine et précise et en grande partie de la perception des couleurs (1). Les maculopathies sont le plus généralement évolutives et acquises bien qu’ il existe des formes congénitales et génétiques. Les formes les plus fréquentes sont la dégénérescence maculaire liée à l’ âge (DMLA) et les maculopathies d’ origine diabétique. On retrouve aussi des causes toxiques et médicamenteuses (exemple : Hydroxychloroquine). Nous nous proposons d’ aborder brièvement les deux maculopathies les plus courantes que sont la DMLA et la maculopathie diabétique.
Les patients atteints de maculopathie, même dans les cas les plus sévères, ne perdent pas complétement la vue et gardent un champ visuel périphérique et une bonne capacité visuelle d’ orientation dans leur environnement ; néanmoins, ils ne seront plus en mesure de lire, conduire, etc. et seront considérés comme légalement aveugles (cécité légale) en cas d’ acuité visuelle inférieure à 0.1.
Même si les moyens thérapeutiques actuels ont permis d’ améliorer la prise en charge de nombreuses sortes de maculopathie, il n’ existe actuellement pas de traitement curatif dans la plupart des cas. Il n’ y a de plus aucun moyen de récupérer une fonction maculaire perdue en raison d’ une atrophie de l’ épithélium pigmentaire ou du tissu rétinien.
La dégénérescence maculaire liée à l’ âge (DMLA)
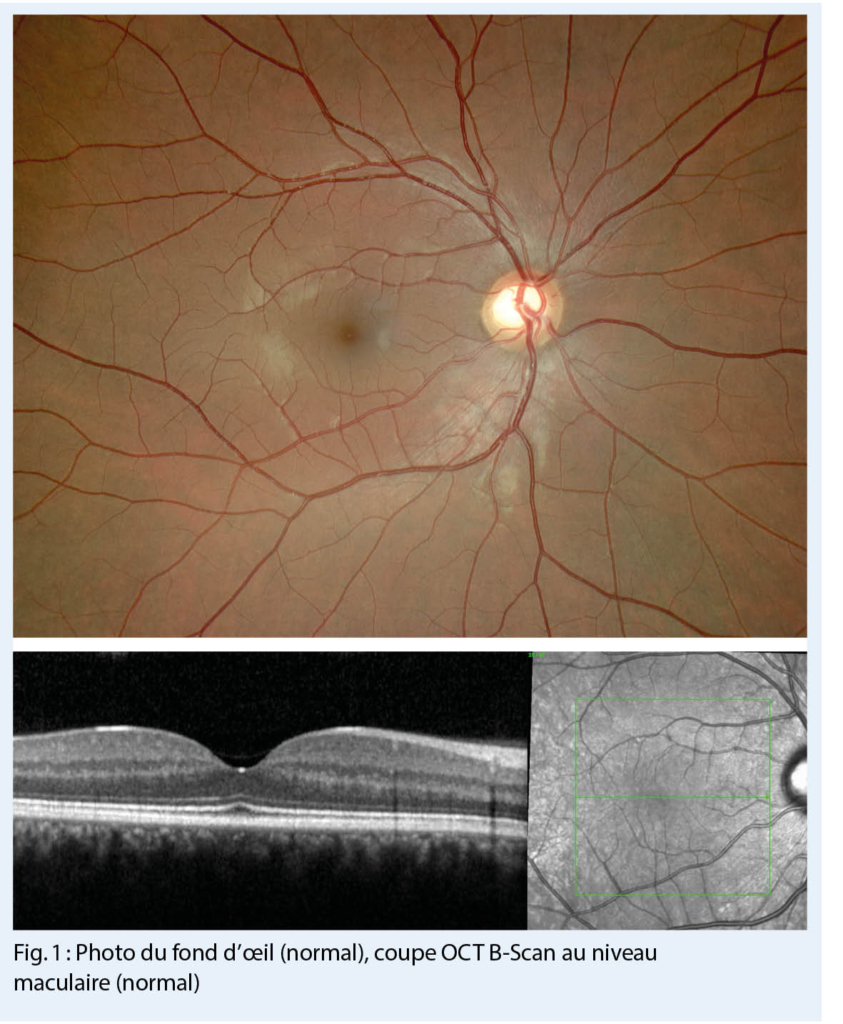
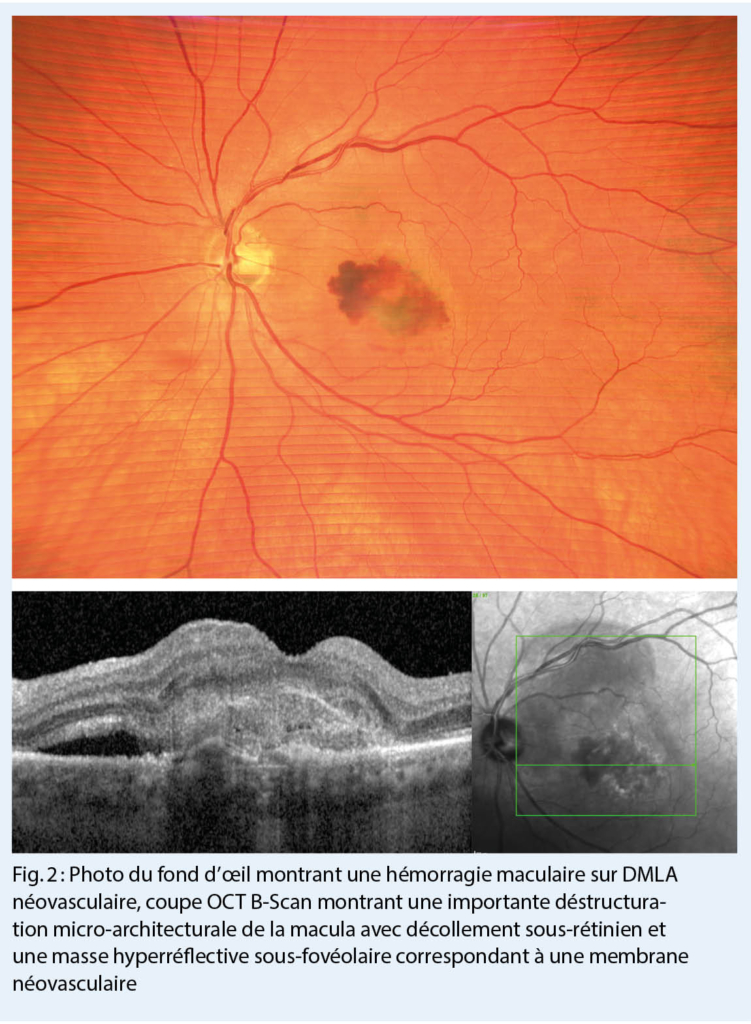
Il s’ agit de la maculopathie la plus fréquente (fig. 1, 2). Elle affecte les personnes âgées dans la plupart des cas de plus de 60 ans. C’ est une des causes majeures de malvoyance dans les pays développés. Elle affecte actuellement des millions de personnes. La cause initiale de la DMLA reste inconnue, bien que l’âge, les facteurs génétiques et le tabagisme actif aient été clairement identifiés comme des facteurs de risque de la DMLA (2, 3, 4).
La DMLA à un stade précoce est souvent peu, voire asymptomatique. Dans les formes plus avancées, les patients remarquent souvent la présence de métamorphopsies (déformation des lignes en raison d’ une irrégularité de la neuro-rétine), baisse de sensibilité au contraste et besoin accru de lumière, flou visuel central et perte d’ acuité visuelle, scotomes et dyschromatopsies. Il existe deux grands types de DMLA, la DMLA sèche et la DMLA humide (5).
DMLA sèche
La DMLA sèche est la plus courante et représente 80% des cas selon l’American Academy of Ophthalmology. On constate l’ accumulation de déchets métaboliques qui s’ accumulent à l’ interface de l’ épithélium pigmentaire (EP) et de la rétine externe sous forme de Drüsens. Il en résulte une perte progressive de ce couple EP/photorécepteurs interdépendant provoquant la dégradation progressive de la fonction visuelle centrale.
DMLA humide
La DMLA humide est plus rare mais elle est plus grave que la DMLA sèche car son évolution est plus brutale. Les deux formes ne sont pas exclusives et on constate souvent une forme sèche qui évolue brutalement vers une forme humide avec dégradation aiguë et sévère de la vision. Cette condition survient lorsque des vaisseaux sanguins anormaux (appelés néovaisseaux) se développent sous /dans la rétine avec comme conséquences une importante perturbation de l’ architecture microanatomique de la macula et l’ apparition d’ une accumulation de liquide intratissulaire (voire même la présence d’ une hémorragie).
Symptômes
Il est important de reconnaître les symptômes suspects de DMLA qui doivent alerter les cliniciens pour orienter le patient vers le spécialiste pour une évaluation complète et pour déterminer l’urgence du traitement. Chez une personne âgée de plus de 55 ans, les signes alarmants sont les suivants :
1) diminution progressive ou soudaine de la vision non améliorée avec la correction optique
2) scotome central
3) métamorphopsie, micropsies ou macropsies
4) difficultés dans les activités de la vie quotidienne (p. ex. regarder la télévision, lecture, etc.).
La métamorphopsie est un symptôme clé dans l’ évaluation d’ un patient atteint de DMLA. Les métamorphopsies sont un signe distinctif chez les patients atteints de maladies maculaires et peuvent être facilement reconnues à l’ aide de la grille d’ Amsler. Les patients sont souvent invités à utiliser en autosurveillance la grille d’Amsler à la recherche de déformations des lignes ou d’ amputation partielle du cadrillage. En l’ absence de toute manifestation suggérant une progression de la DMLA, les patients sont suivis sur une base annuelle.
Traitement
Chez les patients atteints de DMLA précoce, il est important d’identifier les facteurs de risque modifiables liés au mode de vie. Il est recommandé de suspendre la fumée, de privilégier une alimentation équilibrée et saine, riche en fruits, légumes (antioxydants naturels) et poisson (la principale source d’ oméga-3 acides gras polyinsaturés, tels que l’ acide docosahexaénoïque et l’ acide eicosapentaénoïque (7). L’ activité physique semble aussi jouer un rôle favorable (finalement les facteurs de risque et protecteurs sont similaires aux maladies cardio-vasculaires).
Les personnes atteintes de DMLA dans les formes précoces peuvent bénéficier de la prise de compléments alimentaires, vitamines et minéraux. Ces suppléments contiennent de la vitamine C, de la vitamine E, du bêta-carotène, du cuivre, de la lutéine, de la zéaxanthine et du zinc. Ces vitamines ne guérissent pas, n’inversent pas ou ne préviennent pas la DMLA, mais elles peuvent ralentir la progression de la maladie, selon les différentes études qui ont montré un avantage de ces préparations par rapport à un placebo (AREDS and AREDS2) (8, 9). A préciser que les préparations les plus récentes sont de plus en plus exemptées de bêta-carotène qui, couplé à un tabagisme actif, augmente le risque de néoplasie pulmonaire.
Il n’ existe actuellement aucun traitement curatif pour cette maladie. Il n’ y a pas de traitement spécifique pour la DMLA sèche. Concernant la forme humide de la maladie, il existe depuis une dizaine d’ année des injections intra-vitréennes de médicaments anti-vasoprolifératifs (anti VEGF) qui permettent de stabiliser, voire même fréquemment d’ améliorer l’ acuité visuelle et le profil maculaire en inhibant la croissance des membranes néovasculaires. Malheureusement, l’ efficacité du traitement diminue rapidement au cours des semaines suivantes et un suivi rapproché et de nombreuses injections au long cours sont nécessaires.
Dans des situations bien particulière, le recours à la photothérapie dynamique à la Visudyne (vertéporfine) reste indiqué en monothérapie ou le plus fréquemment en association avec les injections d’ anti VEGF. La thérapie photodynamique utilise un laser spécial pour permettre une thrombose et fibrose de la membrane néovasculaire. Un produit photosensibilisateur (vertéporfine) est injecté dans une veine périphérique du bras et va se distribuer notamment dans l’ œil avec un tropisme augmenté pour les néovaisseaux. La lumière du laser va réagir avec la vertéporfine et permettre la destruction des néovaisseaux.
Maculopathie diabétique
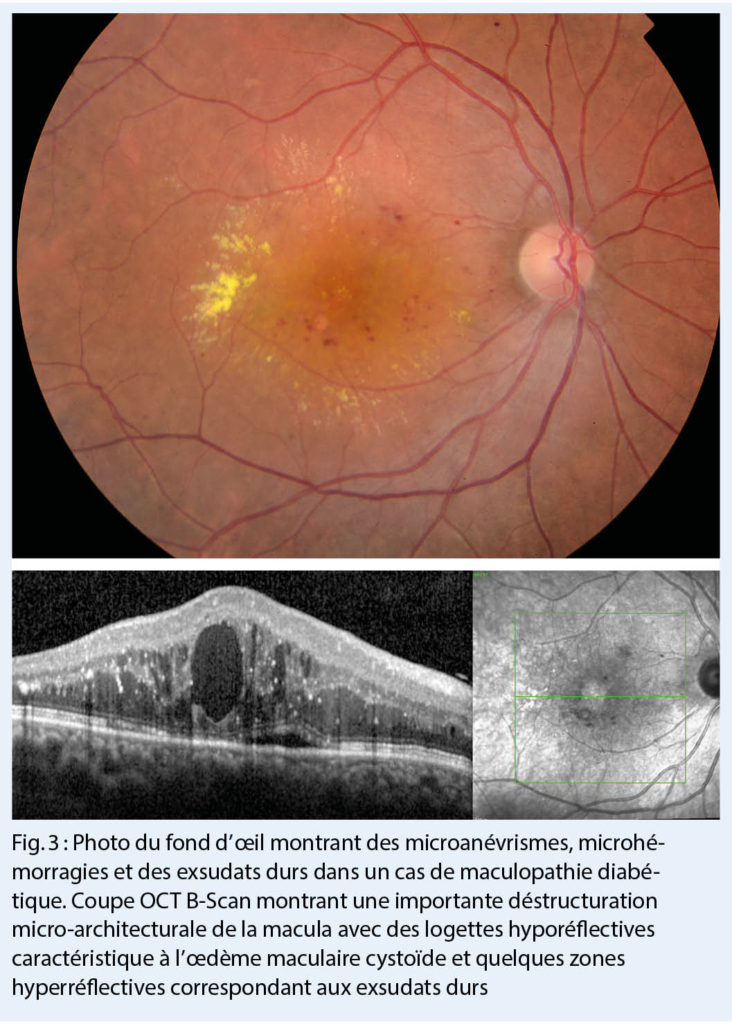
La maculopathie diabétique est la cause la plus fréquente de perte de vision chez les personnes diabétiques (fig. 3)(11).
On distingue deux formes de maculopathie diabétique :
La maculopathie ischémique : forme plus rare, qui est incurable et entraîne souvent une déficience visuelle majeure.
La maculopathie œdémateuse (aussi appelée « œdème maculaire diabétique (OMD) ») : forme la plus fréquente, sa prévalence chez les patients atteints de rétinopathie diabétique est de 2,7% -11% (12, 13) et cela dépend du type de diabète et de la durée de la maladie. Pour les deux types de diabète, 1 et 2, après une durée de 25 ans, il est d’ environ 30%. Le risque de développer un œdème maculaire diabétique dans le cadre d’ un diabète augmente avec le nombre d’ années de diabète, une pression artérielle systolique plus élevée et une glycémie mal contrôlée. Le seul facteur oculaire associé à l’ OMD est la sévérité de la rétinopathie diabétique (RD), plus la RD est avancée, plus le risque d’ OMD est grand (14).
Symptômes
Au début, l’ OMD ne génère aucune douleur ni signes particuliers. Les personnes diabétiques peuvent ainsi en être atteints sans ressentir le moindre trouble visuel et donc sans le savoir. Puis, avec le temps, certains symptômes apparaissent :
1) Baisse de l’ acuité visuelle et notamment gêne à la lecture avec flou visuel, difficulté à reconnaître les visages, etc.
2) Perte de sensibilité aux contrastes
3) Difficulté à percevoir correctement les couleurs.
Traitement
La reconnaissance des facteurs de risque de l’ OMD a conduit à des essais cliniques randomisés sur un meilleur contrôle de la pression artérielle et de la glycémie dans le but de réduire la prévalence de la maladie. « The diabetes control and complications trial » a montré qu’ un contrôle strict de la glycémie chez les patients atteints de diabète de type 1 réduisait de 29 % l’ incidence cumulée de l’ œdème maculaire à 9 ans de suivi et de moitié l’ application du traitement laser focal pour l’ OMD (15, 16). L’ étude prospective sur le diabète au Royaume-Uni (The United Kingdom Prospective Diabetes Study) était un essai clinique randomisé analogue portant sur des patients atteints de diabète de type 2. Il a montré qu’ un contrôle plus strict de la glycémie réduisait de 29 % la nécessité d’ un traitement au laser à 10 ans, par rapport à un contrôle moins strict ; 78 % des traitements au laser étaient pour l’ OMD (17). Il a également montré qu’ une réduction moyenne de la pression artérielle systolique de 10 mmHg et une réduction de la pression artérielle diastolique de 5 mmHg sur un suivi médian de 8,4 ans entraînaient une réduction de 35 % des traitements au laser rétiniens, dont 78% pour l’ OMD (18). Il existe donc un lien étroit entre ces changements et les effets rétiniens. Une intervention multifactorielle visant à réduire l’ hémoglobine glyquée, la pression artérielle élevée et les lipides sériques élevés peut produire des effets mesurables sur l’ épaisseur maculaire en seulement 6 semaines et forme une base rationnelle sur laquelle appliquer des interventions ophtalmiques spécifiques (19).
Traitements ophtalmiques spécifiques
Plusieurs modalités de traitements existent pour l’ OMD, on a souvent recours à une combinaison de traitements variables selon les situations :
1) Injections intravitréennes des anti-VEGF
2) Injections intravitréennes de corticostéroïdes (notamment implant à libération continue sur plusieurs mois (Ozurdex®, Iluvien, etc.)
3) Injections combinées des anti-VEGF et corticostéroïdes intra-
vitréens
4) Focal/grid laser photocoagulation
5) Subthreshold laser photocoagulation
6) Vitrectomie.
Copyright Aerzteverlag medinfo AG
Service d’ ophtalmologie de l’ Université de Lausanne
Hôpital ophtalmique Jules-Gonin
Fondation Asile des aveugles
Av. de France 15
CP 133
1000 Lausanne 7
mohamed.sherif@fa2.ch
Service d’ ophtalmologie de l’ Université de Lausanne
Hôpital ophtalmique Jules-Gonin
Fondation Asile des aveugles
Av. de France 15
CP 133
1000 Lausanne 7
Unité de chirurgie vitréo-rétinienne
Hôpital Ophtalmique Jules-Gonin
Fondation Asile des Aveugles
Département d’ Ophtalmologie
Université de Lausanne
Avenue de France 15
1004 Lausanne
retinechirurgicale@fa2.ch
Les auteurs n’ ont déclarée aucun conflit d’ intérêts en rapport avec cet article.
- La maculopathie est un terme générique qui définit toutes pathologies de la zone centrale de la rétine appelée macula
- Les formes les plus fréquentes sont la dégénérescence maculaire liée à l’ âge (DMLA) et la maculopathie d’ origine diabétique
- La cause initiale de la DMLA reste inconnue, bien que l’âge, les facteurs génétiques et le tabagisme actif aient été clairement identifiés comme des facteurs de risque. La DMLA sèche est la plus courante, par contre la DMLA humide est plus rare mais plus grave. Concernant cette dernière forme des injections intra-vitréennes de médicaments anti-vasoprolifératifs (anti VEGF) permettent de stabiliser l’ acuité visuelle.
- La maculopathie œdémateuse est la forme la plus courante de maculopathie diabétique. Un contrôle strict de la glycémie ainsi que la réduction moyenne de la pression artérielle entraînent une réduction de l’incidence cumulée de l’œdème maculaire.
1. Kanski JJ. Clinical Ophthalmology: A Systematic Approach. 6th édition 2007.
2. Chen Y, Zeng J, Zhao C, et al. Assessing susceptibility to age-related macular degeneration with genetic markers and environmental factors. Arch Ophthalmol. 2011;129(3):344–351.
3. Velilla S, García-Medina JJ, García-Layana A, et al. Smoking and age-related macular degeneration: review and update. J Ophthalmol. 2013;2013:895147.
4. Myers CE, Klein BE, Gangnon R, Sivakumaran TA, Iyengar SK, Klein R. Cigarette smoking and the natural history of age-related macular degeneration: the Beaver Dam Eye Study. Ophthalmology. 2014;121:1949–1955.
5. Ferris FL, III, Wilkinson CP, Bird A, et al. Clinical classification of age-related macular degeneration. Ophthalmology. 2013;120(4):844–851.
6. Simunovic MP. Metamorphopsia and its quantification. Retina. 2015;35(7):1285–1291.
7. Carneiro Â, Andrade JP. Nutritional and lifestyle interventions for age-related macular degeneration: a review. Oxid Med Cell Longev. 2017;2017:6469138.
8. Age-Related Eye Disease Study Research Group A randomized, placebo-controlled, clinical trial of high-dose supplementation with vitamins C and E, beta carotene, and zinc for age-related macular degeneration and vision loss: AREDS report no. 8. Arch Ophthalmol. 2001;119(10):1417–1436.
9. Age-Related Eye Disease Study 2 Research Group Lutein + zeaxanthin and omega-3 fatty acids for age-related macular degeneration: the Age-Related Eye Disease Study 2 (AREDS2) randomized clinical trial. JAMA. 2013;309(19):2005–2015.
10. Age-Related Eye Disease Study 2 Research Group Lutein + zeaxanthin and omega-3 fatty acids for age-related macular degeneration: the Age-Related Eye Disease Study 2 (AREDS2) randomized clinical trial. JAMA. 2013;309(19):2005–2015.
11. Klein R, Klein BE, Moss SE, Cruickshanks KJ. The Wisconsin epidemiologic study of diabetic retinopathy. XV. The long-term incidence of macular edema. Ophthalmology. 1995;102:7–16.
12. 4. Xie XW, Xu L, Wang YX, Jonas JB. Prevalence and associated factors of diabetic retinopathy. The Beijing eye study 2006. Graefes Arch Clin Exp Ophthalmol. 2008;246:1519–26.
13. Wong TY, Klein R, Islam FM, Cotch MF, Folsom AR, Klein BE, et al. Diabetic retinopathy in a multi-ethnic cohort in the United States. Am J Ophthalmol. 2006;141:446–55.
14. Klein R, Klein BE, Moss SE, Cruickshanks KJ. The Wisconsin epidemiologic study of diabetic retinopathy: XVII. The 14-year incidence and progression of diabetic retinopathy and associated risk factors in type 1 diabetes. Ophthalmology. 1998;105:1801–15.
15. Progression of retinopathy with intensive versus conventional treatment in the diabetes control and complications trial. Diabetes control and complications trial research group. Ophthalmology. 1995;102:647–61.
16. Early worsening of diabetic retinopathy in the diabetes control and complications trial. Arch Ophthalmol. 1998;116:874–86.
17. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). UK prospective diabetes study (UKPDS) group. Lancet. 1998;352:837–53.
18. Tight blood pressure control and risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 38. UK prospective diabetes study group. BMJ. 1998;317:703–13.
19. Singh R, Abhiramamurthy V, Gupta V, Gupta A, Bhansali A. Effect of multifactorial intervention on diabetic macular edema. Diabetes Care. 2006;29:463–4.
la gazette médicale
- Vol. 9
- Ausgabe 6
- November 2020