- Plaies chroniques
Les plaies chroniques concernent majoritairement des patients âgés, polymorbides, bien souvent polymédiqués et dénutris. Elles sont fréquemment d’ origine multifactorielle et les conséquences sur la qualité de vie sont dramatiques (douleurs chroniques, perte d’ autonomie, isolement social, dépression contextuelle etc.), faisant de la plaie chronique un facteur de morbidité important. Il s’ agit d’ un problème de santé publique. La prise en charge est donc complexe, avec plusieurs chevaux de bataille, et nécessite donc l’ installation d’ un réseau de soin multidisciplinaire au centre duquel se situe le patient dont l’ éducation thérapeutique est primordiale. Nous aborderons dans cet article la prise en charge globale des plaies chroniques, spécifiquement celle des ulcères des membres inférieurs, sous forme de guide pratique selon notre expertise.
Les plaies chroniques sont un problème de santé publique. Elles concernent environ 1 à 1.5 % de la population des pays industrialisés. La prévalence augmente avec le vieillissement de la population. La prise en charge est complexe, souvent longue (mois, voire années) comprenant visites médicales, examens complémentaires, soins de plaie spécialisés le plus souvent quotidiens, physiothérapie etc. Pour l’ Union Européenne, ces coûts s’ élèvent à 2-4 % des coûts de la santé globaux (1). Sur le plan individuel, les coûts peuvent être un frein à la prise en charge créant des situations sociales dramatiques, encore peu fréquentes heureusement en Suisse.
Le risque majeur d’ une plaie chronique est la complication infectieuse, i.e. la surinfection locale ou loco-régionale pouvant entraîner une hospitalisation de moyenne à longue durée.
Au quotidien, l’ impact sur la qualité de vie peut être dramatique en fonction de la sévérité de la plaie, si elle s’ accompagne d’ écoulement, de douleurs, d’ odeur nauséabonde etc. Une impotence fonctionnelle peut s’ installer de même qu’ un isolement social voire un état dépressif réactionnel.
La plaie chronique est donc une pathologie fréquente aux causes et conséquences multiples, mettant à rude épreuve le patient et les professionnels de la santé. Il convient d’ instaurer un partenariat solide entre les différents intervenants et avec le patient, clé principale au succès de la prise en charge, avec comme objectif commun la cicatrisation de la plaie et l’ amélioration de la qualité de vie du patient.
Etape 1 : recherche des facteurs favorisants
Une plaie chronique est par définition une plaie de plus de 6 semaines, qui ne cicatrise pas. Elle est donc témoin d’ un trouble ou retard de la cicatrisation.
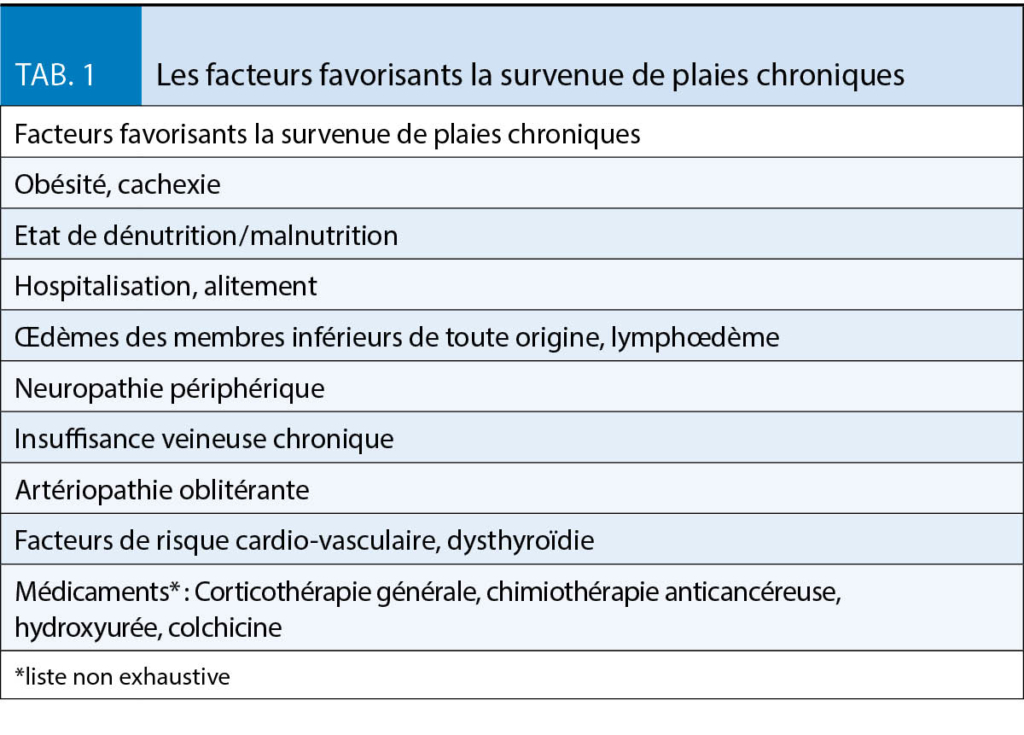
Ce retard de cicatrisation peut être secondaire à des problèmes vasculaires (artériel et/ou veineux), une stase chronique, des défauts d’ oxygénation (ischémie), un état de malnutrition ou dénutrition. Un ou plusieurs de ces facteurs peuvent se retrouver chez le même patient. Il nous faut donc considérer le patient dans sa globalité avec ses co-morbidités.
Le tableau 1 illustre les facteurs favorisants la survenue de plaies chroniques.
Les 3 types de plaies les plus fréquemment rencontrés sont : les escarres, les ulcères des membres inférieurs et les plaies liées au pied diabétique.
Dans cet article nous considérerons uniquement les ulcères des membres inférieurs. Les ulcères des membres inférieurs sont principalement d’ origine vasculaire, avec une prédominance veineuse (70 %) suivie des ulcères artériels et artério-veineux (20 %) (2).
Etape 2 : recherche des signes cliniques orientant vers une cause vasculaire
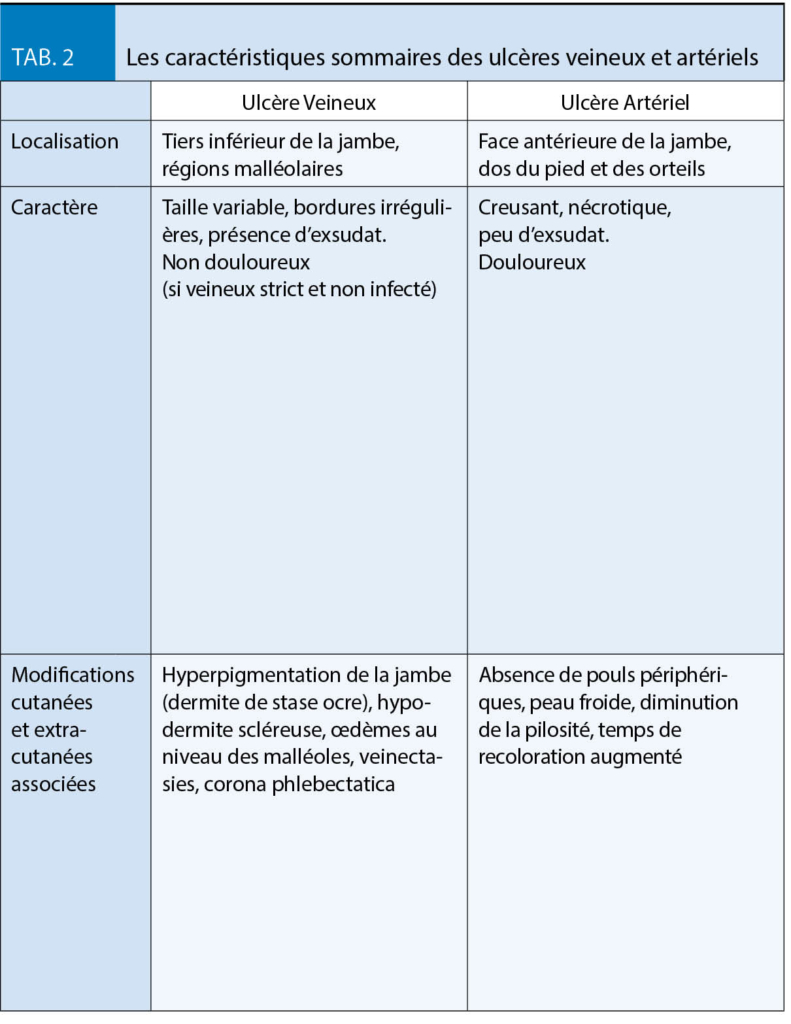
Le tableau 2 illustre les caractéristiques sommaires des ulcères veineux et artériels.
Bien souvent, une bonne anamnèse associée à un examen cutané, neurologique et vasculaire détaillé permet d’ identifier dans la majorité des cas l’ origine de l’ ulcère (2).
Etape 3 : Examens complémentaires
Dépistage d’ une malnutrition / dénutrition
La dénutrition est fréquente et touche 4-10 % des personnes âgées vivant à domicile (3). La prévalence est également importante chez les patients hospitalisés. La dénutrition est un facteur favorisant et/ ou la conséquence d’ un retard de la cicatrisation pouvant engendrer un cercle vicieux.
Pour rappel, la cicatrisation est un processus complexe dépendant de l’ interaction entre différents types cellulaires (kératinocytes, fibroblastes, cellules endothéliales et immunocompétentes) et comprenant grossièrement 4 phases ; détersion, phase hémorragique et inflammatoire, réparation (cicatrisation dermique, cicatrisation épidermique) et phase de remodelage.
Les facteurs métaboliques et nutritionnels ont une place importante car ils interviennent dans la réaction inflammatoire, la prolifération cellulaire et la synthèse protéique. Lors du processus de cicatrisation, les dépenses énergétiques augmentent
par conséquence et les réserves nutritionnelles sont mobilisées. L’ intensité de ce processus est proportionnelle à la sévérité de la lésion pouvant ainsi induire ou aggraver un état de malnutrition ou dénutrition.
Il est ainsi important de faire un dépistage nutritionnel à la première visite et à chaque changement de l’ état clinique. En pratique, nous réalisons un score à l’ aide du Nutrition Risk Screening (NRS) ou Mini Nutritional Assessment (MNA). A ce stade, nous ne réalisons pas nécessairement de bilan biologique. S’ il existe un état de malnutrition ou dénutrition, nous adressons les patients à la consultation diététique ou nutritionnelle pour suite de bilan et prise en charge.
Frottis bactériologique
Une plaie chronique est par définition colonisée par différents germes. Lorsqu’ une ou plusieurs colonies bactériennes prennent le dessus et engendre une réaction de l’ hôte, on parle alors d’ infection. Les signes cliniques sont alors : rougeur, douleur (nouvelle ou aggravée), écoulement + / - jaune, vert, mauvaise odeur, nécrose, augmentation de la taille de la plaie, œdème. Cette surinfection peut être locale ou loco-régionale : on parle alors de dermohypodermite infectieuse.
Il n’ est pas recommandé de réaliser d’ emblée un frottis bactériologique car l’ attitude thérapeutique ne sera pas modifiée devant l’ absence de signe clinique de surinfection.
A retenir donc que le frottis bactériologique n’ est réalisé que lors d’ une suspicion clinique de surinfection.
Bilan artériographique et/ ou veineux
Une alliance avec le/la médecin angiologue est nécessaire. Il convient en effet de réaliser un examen artériographique et / ou veineux des membres inférieurs selon la suspicion clinique afin de déceler une cause traitable ; stadifier l’ artériopathie et / ou rechercher des varices alimentant l’ ulcère. S’ il existe une cause traitable sous-jacente, il convient de la traiter afin de garantir une cicatrisation optimale et durable (diminution des risques de récidive).
Etape 4 : Traitement
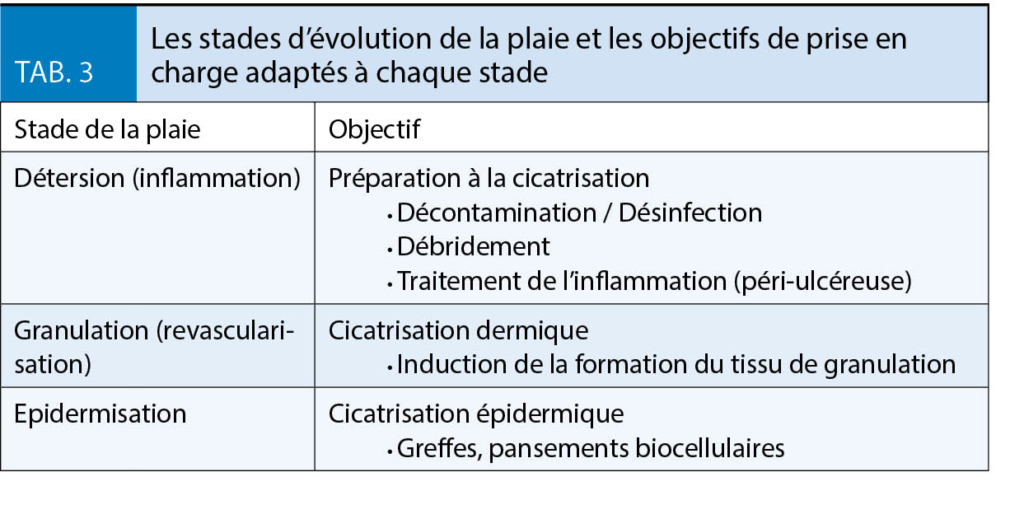
Dans un premier temps, il convient de traiter la cause comme discuté plus haut. En association, des soins locaux sont proposés dont le choix sera en fonction de l’ état de la plaie (infectée ou pas) et de son stade d’ évolution. Le but d’ un pansement est d’ assurer un milieu favorable pour la cicatrisation, ni trop humide ni trop sec. Les stades d’ évolution de la plaie suivent les phases de la cicatrisation ; détersion (phase inflammatoire), granulation (cicatrisation dermique, revascularisation) et épidermisation (cicatrisation épidermique) (4). A chaque stade d’ évolution, les pansements doivent répondre à un objectif précis, résumé dans le tableau 3.
L’ infirmier (-ère) agissant en première ligne est sentinelle et garant de l’ adéquation du traitement local. L’ alliance médico-infirmière est vitale.
Décontamination de la plaie
En l’ absence d’ infection aigue, les antiseptiques ne sont pas nécessaires. Ils peuvent être au contraire délétères et freiner la cicatrisation. Un nettoyage simple à l’ eau et savon sous la douche ou avec NaCl 0.9 % permet de réduire la colonisation bactérienne et d’ éliminer en partie le matériel fibrinonécrotique. Si la plaie est infectée, des soins locaux antiseptiques suffisent la plupart du temps sans nécessité de recourir aux antibiotiques locaux ou systémiques sauf en cas de dermohypodermite infectieuse bien évidemment.
Débridement
Le débridement permet d’ éliminer les tissus fibrinonécrotiques qui sont un obstacle à la cicatrisation. Deux techniques de détersion sont possibles : chimique ou mécanique. En pratique, nous utilisons conjointement les deux méthodes.
- Débridement chimique (autolytique)
Les hydrogels, les hydrofibres, les alginates et certains hydrocolloïdes ont cette propriété (7).
- Débridement mécanique
Il se pratique à l’ aide d’ un scalpel, pince ou Stieffel® (lame circulaire). L’ application d’ une antalgie topique permet de diminuer la douleur et d’augmenter la qualité de ce geste (cf. partie douleur).
En cas de zone nécrotique étendue ou douleur importante malgré les anesthésiants topiques et antalgiques, la détersion peut s’ effectuer au bloc opératoire.
- La larvothérapie (biochirurgie)
Lucilia sericata est l’ espèce de mouche utilisée pour la larvothérapie. Ces larves se nourrissent exclusivement de tissus morts et de cette manière défibrinent les ulcères. C’ est une méthode rapide mais temporaire. Les études in vitro ont montré que les sécrétions de ces larves agissaient comme des facteurs de croissance sur les fibroblastes, favorisant la cicatrisation (5).
Pansements
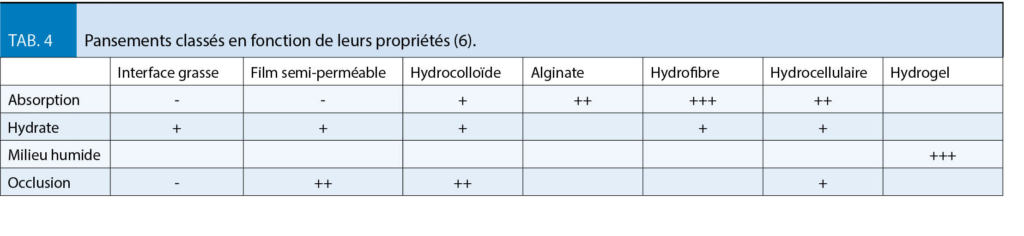
Les pansements assurent une protection mécanique et diminuent les douleurs pouvant être occasionnées par la mise à nu du derme. Le but est d’ obtenir un milieu propice à la cicatrisation ; apport d’ humidité, pouvoir absorbant plus ou moins important, propriétés fibrinolytiques, actions sur le biofilm etc.Le tableau 4 résume les pansements classés en fonction de leurs propriétés (6).
La greffe cutanée et les substituts cutanés
Il existe différents types de greffe cutanée ; peau mince, demi-épaisse, totale ou en pastille (7). Le but est de recouvrir la plaie à des fins de cicatrisation et d’ antalgie. La zone receveuse doit être propice, à savoir : fond propre (pas de fibrine, pas de nécrose), absence d’ infection ou de suintement trop important, bien vascularisée. Ce geste peut se pratiquer en ambulatoire, mais l’ hospitalisation est préférable pour assurer une bonne prise de greffe dépendante notamment d’ un maintien du membre au repos.
Le domaine des substituts cutanés, issus des biothérapies, est actuellement en plein essor. Ils sont une alternative moderne et rapide à la greffe cutanée.
Par exemple l’ Apligraf® qui est composé d’ une couche épidermique (kératinocytes humains néonataux) et d’ une couche dermique (collagène bovin et fibroblastes humains néonataux). Son efficacité a été démontrée supérieure aux pansements classiques si les indications sont respectées (8).
Dernièrement, il est possible de réaliser des greffes de membrane amniotique humaine (couche interne de placenta) ayant des propriétés cicatrisantes, anti-inflammatoires et anti-bactériennes (9).Cette pratique est courante en ophtalmologie et n’ est en pratique pas encore réalisée dans notre service. Les résultats sont prometteurs selon les études. Il existe également des pansements fait de placenta complet déshydraté (NuShield®). Les études ont montré la supériorité de ce pansement par rapports aux pansements classiques (10).
Autre nouveauté, la thérapie avec des cellules souches dérivées du tissu adipeux autologue. Le tissu adipeux est constitué d’ adipocytes et des cellules vasculaires stromales. Ces dernières contiennent des cellules progénitrices mésenchymateuses pluripotentes et des cellules souches. Cette thérapie favorise la cicatrisation des ulcères avec un retard de cicatrisation (11).
Thérapie hyperbare
La thérapie hyperbare est l’ administration d’ oxygène à une pression supérieure à la pression atmosphérique, augmentant ainsi la pression partielle d’ oxygène dans le sang et les tissus. Les ulcères sont ainsi mieux oxygénés. L’ oxygénation intermittente de l’ ulcère accroît la production des facteurs de croissance ; elle a un effet microcirculatoire avec réduction des oedèmes et des effets anti infectieux (12). L’ hyperbarie peut donc être envisagée comme association thérapeutique afin de potentialiser la prise en charge.
Les HUG sont les seuls hôpitaux universitaires en Suisse à disposer d’un centre de médecine hyperbare.
La scarification
Elle se fait à l’ aide d’ un bistouri après le nettoyage de la plaie et consiste à inciser les berges de l’ ulcère. Le but est de faire saigner la plaie afin de « relancer » /stimuler l’ inflammation et d’ apporter ainsi des facteurs de cicatrisation. Ce geste concerne les ulcères atones, i.e. sans signes d’ inflammation ni dynamisme (« ulcère sec qui stagne »), car pour rappel, il n’ y a pas de cicatrisation possible sans inflammation.
Etape 5 : Gestion de la douleur
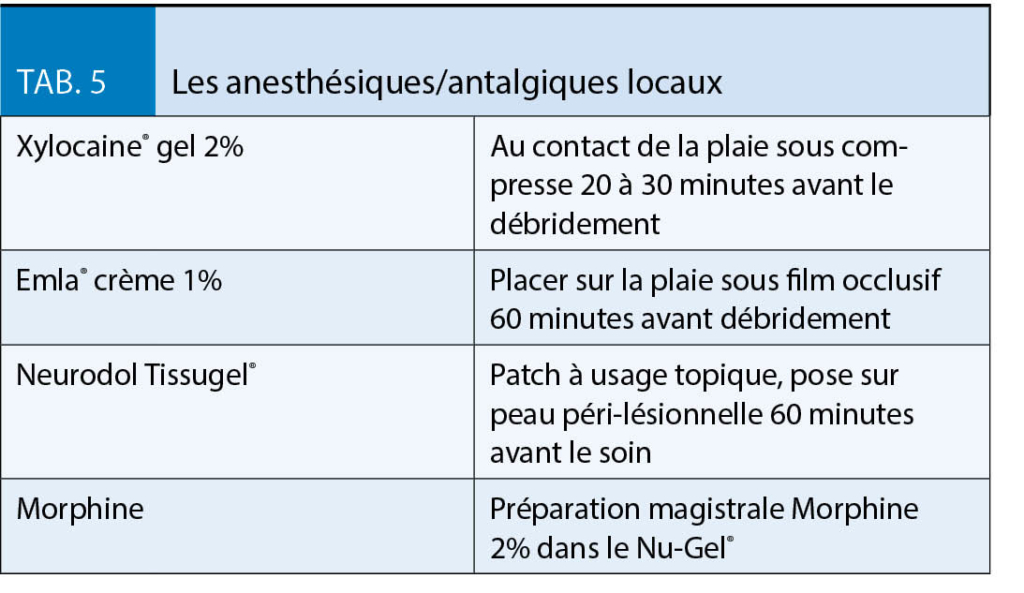
Elle est souvent négligée bien qu’ impérative. Nous avons la possibilité d’ utiliser des traitements anesthésiants et/ou antalgiques locaux associés à l’ antalgie classique per os et/ou MEOPA. Les traitements antalgiques topiques sont utiles pour les soins locaux, notamment la détersion mécanique. Le tableau 5 résume les anesthésiques/antalgiques locaux disponibles. Si la gestion de l’ antalgie reste difficile, nous faisons volontiers appel à l’ équipe mobile de la douleur.
Etape 6 : Gestion des facteurs favorisants et prévention
Contention élastique et drainages lymphatiques
Une alliance avec le/la physiothérapeute est primordiale. La contention élastique est essentielle dans la prise en charge des ulcères veineux. La pression de compression recommandée est entre 30 et 40 mmHg. Il est démontré que le port de bas de contention non seulement favorise la cicatrisation mais diminue également les risques de récidive (13). En cas d’ insuffisance artérielle avec un IPS < 0.5, la contention élastique est contre-indiquée. Chez les patients avec une artériopathie légère à modérée (IPS entre 0.5 et 0.8), une contention est possible avec des bandes de contention moins comprimantes et un suivi clinique (2). En pratique, si le pouls pédieux est palpé, la contention est prescrite. Les drainages lymphatiques ont une place également importante. Le but est de diminuer la stase chronique, l’ œdème et le lymphoedème, réduisant ainsi la pression aux membres inférieurs (frein à la cicatrisation) et le risque de surinfection loco-régionale.
Facteurs de risque cardio-vasculaires
Une alliance avec le/la médecin traitant est primordiale.
L’ état hyperglycémique et le tabac contribuent au retard de cicatrisation, les facteurs de risque cardio-vasculaires doivent être pris en charge.
Etape 7 : enseignement thérapeutique du patient
Une alliance avec le/la patient(e) est primordiale. Elle ne survient qu’ à l’ étape numéro 7 pour des soucis rédactionnels, mais détrône bien évidemment toutes les étapes et est à considérer en premier lieu.
L’ éducation thérapeutique permet au patient d’ acquérir des connaissances et compétences nécessaires pour qu’ il puisse vivre de façon optimale avec sa maladie chronique et son traitement. Il est ainsi acteur de sa prise en charge. Nos recommandations auprès du patient sont nombreuses et parfois fastidieuses, l’ éducation thérapeutique augmente les chances du suivi de celles-ci et est affaire de tous les soignants.
Prenons en exemple la contention, quiconque ne comprenant pas l’ intérêt du port de bas / bandes de contention ne peut se soumettre à les enfiler (mesure souvent pénible) en pleine canicule. Une étude américaine faite sur 203 patients a démontré l’ impact de 1 heure d’ éducation thérapeutique sur la prévention d’ ulcère et amputation chez les patients diabétiques. Dans le groupe bénéficiant de l’ éducation thérapeutique, il y a eu une diminution significative de l’ amputation et de la survenue des ulcères (14).
Service de dermatologie et vénéréologie
Hôpitaux Universitaires de Genève
Rue Gabrielle-Perret-Gentil 4
1205 Genève
Service de dermatologie et vénéréologie
Hôpitaux Universitaires de Genève
Rue Gabrielle-Perret-Gentil 4
1205 Genève
CC (Chargée de Cours)
Service de dermatologie et vénéréologie
Hôpitaux Universitaires de Genève
Rue Gabrielle-Perret-Gentil 4
1205 Genève
laurence.trellu@hcuge.ch
Les auteurs n’ont déclaré aucun conflit d’intérêts en rapport avec cet article.
- Une prise en charge optimale fait intervenir différentes spécialités devant s’organiser en réseau solide où le patient est l’acteur central.
- Nous n’avons abordé que les aspects médicaux, mais les aspects sociaux et économiques (pansements non remboursés à la hausse etc.) sont à considérer au même titre.
- La plaie chronique est un problème de santé publique, dont la prévalence est en augmentation, et consiste un vrai challenge thérapeutique.
1. www.safw-romande.ch
2. Singer AJ, Tassiopoulos A, and Kirsner R. Evaluation and Management of LowerExtremity Ulcers. N Engl J Med. 2017;377:1559
3. Yerly N, Nguyen S, Major K et al. Approche ambulatoire de la dénutrition chez la personne âgée. Rev Med Suisse 2015; volume 11. 2124-2128
4. Salomon D, Vischer U, Terumalai et al. Handout Soins de plaies complexes. 2003
5. Raposio E, Bortolini S, Maistrello L et al. Larval Therapy for Chronic Cutaneous Ulcers: Historical Review and Future Perspectives. Wounds. 2017;29:367-373.
6. Toutous Trellu L. Plaies chroniques les plus fréquentes, principes de la prise en charge. info@gériatrie. 2012 ;21-23.
7. Serra R, Rizzuto A, Rossi Aet al. Skin grafting for the treatment of chronic leg ulcers – a systematic review in evidence-based medicine. Int Wound J. 2017;14:149-157
8. Zaulyanov L, Kirsner RS. A review of a bi-layered living cell treatment (Apligraf) in the treatment of venous leg ulcers and diabetic foot ulcers. Clin Interv Aging. 2007;2:93-8.
9. Castellanos G, Bernabé-García Á, Moraleda JM et al. Amniotic membrane application for the healing of chronic wounds and ulcers. Placenta. 2017 Nov;59:146-153
10. Bianchi C, Cazzell S, Vayser D et al. A multicentre randomised controlled trial evaluating the efficacy of dehydrated humanamnion/chorion membrane (EpiFix® ) allograft for the treatment of venous leg ulcers. Int Wound J. 2018;15:114-122.
11. Konstantinow A, Arnold A, Djabali K,et al. Therapy of ulcus cruris of venous and mixed venous arterial origin with autologous, adult, native progenitor cells from subcutaneous adipose tissue: a prospective clinical pilot study. J Eur Acad Dermatol Venereol. 2017;31:2104-2118.
12. Thistlethwaite KR, Finlayson KJ, Cooper PD et al. The effectiveness of hyperbaric oxygen therapy for healing chronic venous leg ulcers: A randomized, double-blind, placebo-controlled trial. Wound Repair Regen. 2018 ;26:324-331
13. O’Meara S, Cullum N, Nelson EA et al. Compression for venous leg ulcers. Cochrane Database Syst Rev. 2012;14:11
14. Malone JM, Snyder M, Anderson G, et al. Prevention of amputation by diabetic education. Am J Surg. 1989;158:520-3.
la gazette médicale
- Vol. 8
- Ausgabe 7
- Dezember 2019