- Akutes oligurisches Nierenversagen – Bauchgefühl gegen Bildgebung
Anamnese und Befunde
Beschwerden
Die notfallmässige Zuweisung des 68-jährigen Patienten erfolgte aus der urologischen Sprechstunde bei Auftreten einer akuten Nierenkrankheit mit dialysepflichtiger Hyperkaliämie. Der Patient berichtete über eine abnehmende Urinmenge während der letzten zwei bis drei Tage, wobei er am Vorstellungstag gar keinen Urin mehr habe lösen können. Zudem bemerkte er eine zunehmende Müdigkeit seit ca. einer Woche. Seit ca. acht Wochen litt er an beidseitigen, intermittierenden Flankenschmerzen sowie einer Drangproblematik mit Pollakisurie, was zu einer externen urologischen Vorstellung und seither regelmässigen Einnahme nicht steroidaler Antirheumatika (NSAR) geführt hatte.
Zehn Tage vor Hospitalisation war extern mittels TUR-B die Diagnose eines muskelinvasiven und ungünstig differenzierten Urothelkarzinoms der Harnblase gestellt worden, wobei die Ureterostien als nicht darstellbar dokumentiert wurden.
An weiteren Diagnosen waren eine arterielle Hypertonie sowie eine nicht behandelte Schlafapnoe bekannt, zudem bestand ein Status nach Ablation einer AV-Knoten-Reentry-Tachykardie. Die Dauermedikation bestand aus Hydrochlorothiazid 25 mg/Tag sowie neu seit acht Wochen aus Diclofenac bis 3 x täglich 50 mg, Pantoprazol 20 mg, Solifenacin und Mirabegron 25 mg.
Status
Die klinische Untersuchung des euvolämen Patienten war, bis auf hypertensive Blutdruckwerte von 180/106 mmHg, unauffällig. Es bestand insbesondere keine abdominale Druckdolenz und keine Klopfdolenz über den Nierenlogen.
Labordiagnostik
Vier Wochen vor Hospitalisation war zuletzt ein Kreatinin von 95 µmol/l gemessen worden. Nun zeigte sich im Eintrittslabor eine akute Nierenkrankheit mit einem Kreatinin von 1376 µmol/l (94–97 µmol/l) mit folgenden Komplikationen: Hyperkaliämie von 7.0 mmol/l (3.6–4.8 mmol/l), Hyperphosphatämie von 2.96 mmol/l (0.8–1.50 mmol/l), metabolische Azidose mit pH venös 7.26 (7.38–7.43), Bikarbonat 15.2 mmol/l (21–28 mmol/l) und pCO₂ 4.47 kPa (4.90–6.70 kPa). Im grossen Blutbild zeigten sich keine relevanten Veränderungen. Das Urinsediment war pathologisch mit einer Leukozyturie sowie einer nicht glomerulären Mikrohämaturie (45 Erythrozyten/Gesichtsfeld, normal 0–5). Die geringe Proteinurie von ca. 140 mg/Tag (davon 80 mg/Tag Albuminurie) beurteilten wir als nicht relevant. Die Urinindizes sprachen für ein renales Nierenversagen (Fe-Natrium 3.4 % , Fe-Harnstoff 54 %).
Differenzialdiagnostische Überlegungen
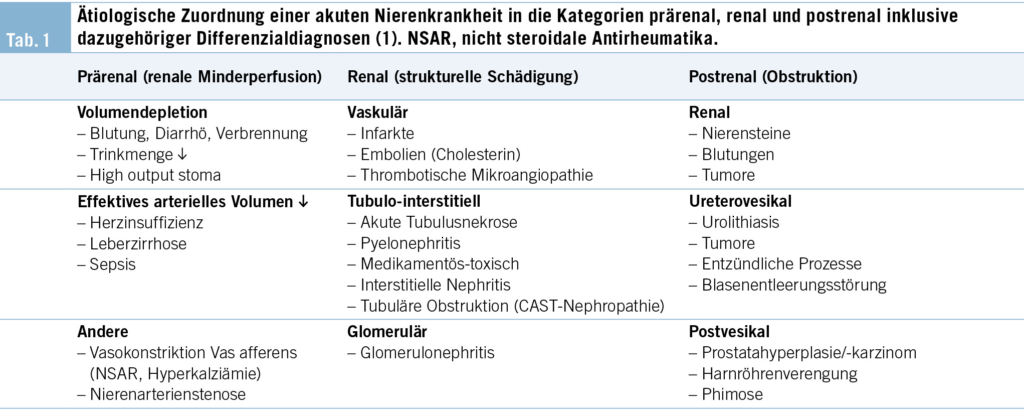
Aufgrund der Anamnese mit rezentem urologischem Eingriff (TUR-B, dabei nicht einsehbare Ureterostien) und postinterventionell einsetzender Oligurie stand eine postrenale Ätiologie differenzialdiagnostisch im Vordergrund. Ebenso möglich waren eine akute interstitielle Nephritis auf die seit mehreren Wochen eingenommenen NSAR und/oder das Pantoprazol. Eine prärenale Ätiologie sahen wir bei anamnestisch fehlendem Volumenverlust, klinischer Euvolämie sowie Hypertonie und Normokardie als unwahrscheinlich an, zudem sprachen die Urinindizes dagegen (Tab. 1). Allerdings hätte die achtwöchige NSAR-Einnahme, über den Effekt einer Vasokonstriktion am glomerulären Vas afferens, ein Nierenversagen anderweitiger Ätiologie zusätzlich verschärfen können.
Weiteres diagnostisches Vorgehen und Therapie
Zur Korrektur der schweren Hyperkaliämie mit spitzen T-Wellen im EKG erfolgte eine notfallmässige Hämodialyse über einen jugulären Dialysekatheter. Eine Bedside-Sonografie auf der Notfallstation zeigte normal grosse Nieren ohne Nierenbeckenkelchektasie und eine nahezu leere Blase. Trotz sonografisch fehlender Nierenstauung wurde, aufgrund der suggestiven Anamnese für ein postrenales Nierenversagen, für den Folgetag eine CT-gesteuerte, perkutane Nephrostomie-Einlage rechts mit gleichzeitiger Nierenbiopsie geplant. Für den Fall, dass danach eine relevante Diurese einsetzen sollte, war zusätzlich die Einlage auf der Gegenseite angedacht. Die Nephrostomie-Einlage erwies sich jedoch als technisch schwierig – bei fehlender Erweiterung des Nierenbeckens gelang die korrekte Platzierung der Nadel im ersten Versuch nicht. Bei deutlicher Blutung durch die Interventionsnadel während des zweiten Versuchs musste die Einlage abgebrochen werden. Die periinterventionell gewonnene Nierenbiopsie zeigte einen geringen und potenziell reversiblen Tubulusschaden, der ätiologisch nicht weiter zugeordnet werden konnte. Es bestanden wenig chronische Schäden und keine Hinweise für eine interstitielle Nephritis oder Glomerulonephritis, wobei die Aussagekraft bzgl. Letzterem bei nur drei getroffenen Glomeruli eingeschränkt war.
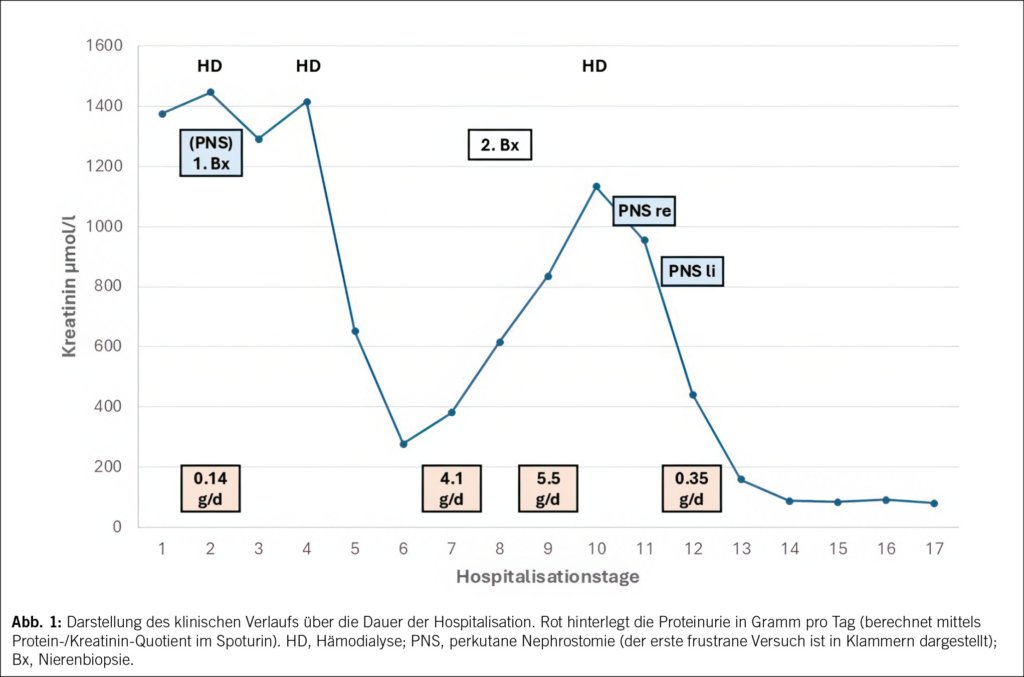
Wenige Tage nach der frustranen Nephrostomie-Einlage und nach einer weiteren Hämodialyse setzte die Diurese spontan wieder ein, sodass wir von einer Erholung des unklaren Tubulusschadens ausgingen. Parallel zeigten sich die Nierenretentionswerte deutlich rückläufig. Innert zweier Tage sank das Kreatinin bis auf 278 µmol/l, so- dass eine postrenale Ätiologie unwahrscheinlich schien (Abb. 1). Nur zwei Tage später kam es jedoch erneut zum Einbruch der Diurese (320 ml/Tag) mit täglichem Anstieg des Kreatinins bis auf maximal 1133 µmol/l – der Patient musste ein drittes Mal dialysiert werden. Wir wiederholten die Sonografie, die weiterhin keine Nierenstauung zeigte, und schlossen eine Makroperfusionsstörung duplexsonografisch aus. Im Urinsediment zeigte sich unverändert eine nicht glomeruläre Mikrohämaturie und in der Urin-Protein-Differenzierung neu eine ausgeprägte glomeruläre Proteinurie im nephrotischen Bereich mit total 4 g/Tag (Protein-/Kreatinin-Quotient im Spoturin 413 mg/mmol), wovon Albumin, IgG und Transferrin 90 % der Gesamtproteinurie ausmachten. Proteine tubulären oder postrenalen Ursprungs (α1-Mikroglobulin und retinolbindendes Protein bzw. α2-Makroglobulin) fanden sich nicht. Die Urinindizes sprachen, analog zur ersten Episode, für eine renale Problematik.
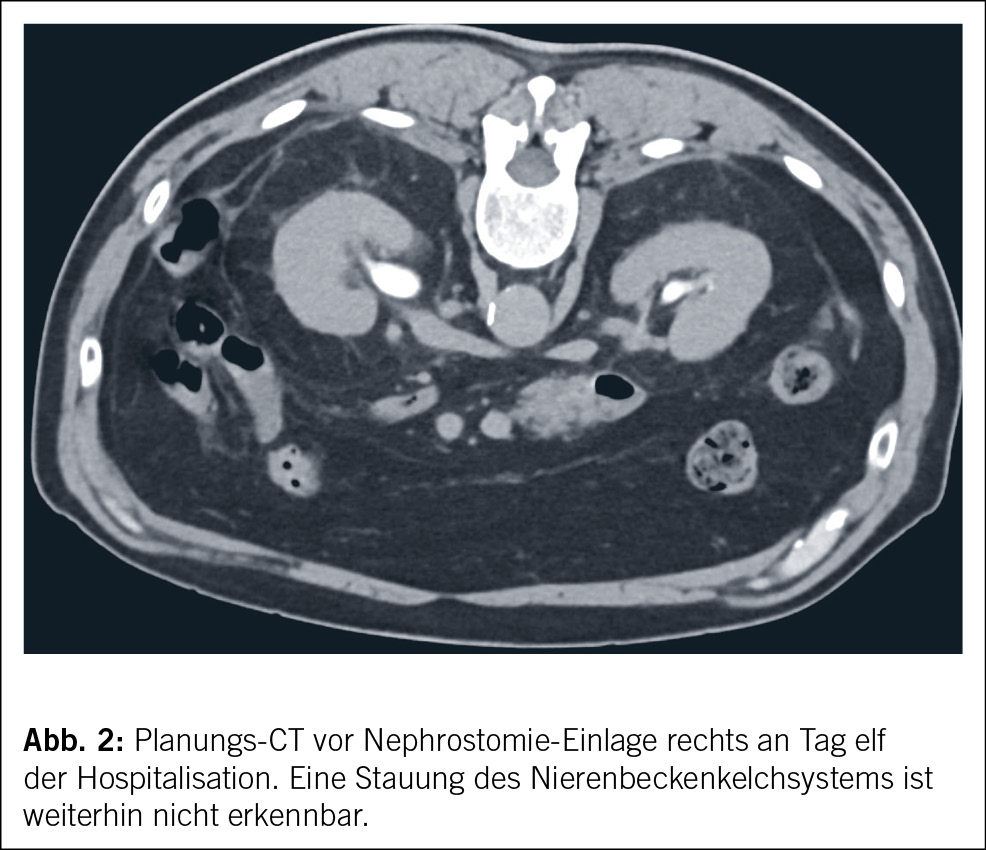
Bei unklarer Ätiologie des erneut dialysepflichtigen Nierenversagens und Entwicklung einer Proteinurie im nephrotischen Bereich erfolgte eine Rebiopsie der Nieren. Diese brachte jedoch keinen Erkenntnisgewinn. Wieder zeigte sich ein Tubulusschaden unbekannter Ätiologie bei glomerulärem Normalbefund und somit ohne Korrelat für die ausgeprägte Proteinurie. Eine prärenale und renale Ätiologie des Nierenversagens war nun klinisch, (duplex-)sonografisch und bioptisch nahezu ausgeschlossen worden, sodass wir die Diagnostik eines postrenalen Nierenversagens forcierten, auch aufgrund des raschen Wechsels oligurischer und polyurischer Phasen. Zehn Tage nach Hospitalisation gelang schliesslich die Nephrostomie-Einlage rechts und bei sofort einsetzender Diurese bzw. Polyurie (Diurese von 3.6 Liter innert zwölf Stunden) am Folgetag auch links. Dabei waren beide Nierenbecken während der CT-gesteuerten Punktion weiterhin nicht erweitert (Abb. 2).
Diagnose
Obstruktives Nierenversagen ohne Hydronephrose
Weiterer Verlauf
Nach beidseitiger perkutaner Nephrostomie-Anlage kam es zu einer raschen und andauernden Verbesserung der Nierenfunktion. Drei Tage postinterventionell hatten sich die Kreatininwerte bereits auf 87 µmol/l erholt und entsprachen damit den Ausgangswerten. Die Nephrostomien wurden belassen und das Harnblasenkarzinom mit neoadjuvanter Chemotherapie und im Verlauf Zystoprostatektomie behandelt.
Kommentar
Postrenale Nierenfunktionsverschlechterungen gehen in aller Regel mit einer bildgebend sichtbaren Erweiterung des Nierenbeckenkelchsystems und/oder Ureters einher. In ca. 5 % kommt es jedoch zum Auftreten einer «non-dilated obstructive nephropathy». Die Ursachen sind vielfältig, am häufigsten ist aber eine Assoziation mit Tumoren des kleinen Beckens. Weniger häufig sind retroperitoneale Raumforderungen (Lymphome, Retroperitonealfibrose), die die Ureteren ummauern und eine Ureterdilatation damit verhindern. Die fehlende Entwicklung einer Hydronephrose kann auch durch eine Abnahme der glomerulären Filtration anderweitiger Ursache (z. B. schwere Hypovolämie) mit bedingt sein (2, 3). Das Auftreten einer unselektiven, glomerulären Proteinurie ist bei postrenalem Nierenversagen sicherlich ungewöhnlich. Bei histologisch unauffälligen Glomeruli muss die Ursache in einer Veränderung der intraglomerulären Druckverhältnisse liegen. In Anbetracht der stark schwankenden Diurese mit oligo- und polyurischen Phasen halten wir eine undulierende ein- oder beidseitige Hyperfiltration für die wahrscheinlichste Ätiologie der glomerulären Proteinurie (4). Das Ausmass der Proteinurie muss bei Bestimmung mittels Protein-/Kreatinin-Quotient im Spoturin kritisch beurteilt werden. Bei zum Zeitpunkt des Auftretens schwankender Nierenfunktion und Diurese sowie einem eher tiefen Urinkreatinin um 3.5 mmol/l kann eine Überschätzung der Proteinurie nicht ausgeschlossen werden.
Abkürzungen
Bx Biopsie
CT Computertomografie
EKG Elektrokardiogramm
Fe-Natrium/Fe-Harnstoff Fraktionierte Natrium-/Harnstoffexkretion
NSAR Nicht steroidale Antirheumatika
PNS Perkutane Nephrostomie
TUR-B Transurethrale Blasenresektion
Historie
Manuskript eingereicht: 19.09.2024
Angenommen nach Revision: 18.12.2024
Klinik für Transplantationsimmunologie und Nephrologie
Universitätsspital Basel
Petersgraben 4
4031 Basel
susanneandrea.winkler@usb.ch
Die Autorenschaft hat keine Interessenkonflikte im Zusammenhang mit diesem Artikel deklariert.
Ein postrenales Nierenversagen lässt sich bildgebend nie gänzlich ausschliessen. Bei klinisch hochgradigem Verdacht sollte diese Verdachtsdiagnose, ungeachtet einer unauffälligen Bildgebung, interventionell mittels ante- oder retrograder Pyelografie weiter abgeklärt werden. Der typische Patient für eine «non-dilated obstructive nephropathy» ist 50–70 Jahre alt, männlich, hat eine akut einsetzende Oligo-/Anurie mit rapidem Kreatininanstieg und einen abdominopelvinen Tumor in der Vorgeschichte. Eine rasche Diagnosestellung und Intervention sind entscheidend, um eine vollständige Erholung der Nierenfunktion nach Dekompression zu ermöglichen.
1. Ambühl, Patrice M. Ursachen und Pathogenese des akuten Nierenversagens. SMF 2001. https://smf.swisshealthweb.ch/fileadmin/assets/SMF/2001/smf.2001.04062/smf-2001-04062.pdf; letzter Zugriff: 14.09.2024.
2. Rascoff JH, Golden RA, Spinowitz BS, Charytan C. Nondilated obstructive nephropathy. Arch Intern Med. 1983;143:696–8. doi:10.1001/archinte.1983.00350040086011.
3. Feliciangeli V, Noce A, Montalto G, Germani S, Miano R, Asimakopoulos AD. Non-dilated obstructive nephropathy. Clin Kidney J. 2024. sfae249. doi: https://doi.org/10.1093/ckj/sfae249
4. Everaert K, Hoebeke P, Delanghe J. A review on urinary proteins in outflow disease of the upper urinary tract. Clin Chim Acta. 2000;297:183-9. doi: 10.1016/s0009-8981(00)00245-x. PMID: 10841920.
PRAXIS
- Vol. 114
- Ausgabe 3
- März 2025