- Medikamentöse Osteoporosebehandlung – sinnvoll bei allen Hochbetagten?
Osteoanabol wirkende Osteoporosemedikamente wurden besser verfügbar. Das osteoanabole Therapieprinzip weisst eine stärkere, schneller einsetzende frakturreduzierende Wirkung auf als die antiresorptiven Präparate. Auch wurde neu erkannt, dass die Bedeutung einer ersten Fragilitätsfraktur als Risikofaktor zeitabhängig ist: Je weniger Zeit seit der ersten Fraktur vergangen ist, umso höher ist das dadurch bedingte Re-Frakturrisiko. Patient_innen, die älter als 65 Jahre alt sind und deren Index-Fragilitätsfraktur weniger als zwei Jahre her ist, werden deshalb in einer eigenen Kategorie «Imminent Fracture Risk» gruppiert. Diese Neuerungen wurden durch eine Aktualisierung der Osteoporosetherapieleitlinie umgesetzt. Demnach soll Patient_innen in der Risikokategorie «Imminent Fracture Risk» möglichst schnell eine osteoanabole Osteoporosetherapie angeboten werden, um möglichst viele Frakturen zu vermeiden. Einer allzu strikten Umsetzung dieses Algorithmus bei hochbetagten Frakturpatient_innen stehen wir kritisch gegenüber. Eigene Daten deuten nämlich darauf hin, dass über 30 % dieser Subpopulation den Effekt einer neu begonnenen Osteoporosetherapie gar nicht erleben. Wir propagieren eine klinisch basierte Indikationsstellung zur Osteoporosetherapie. Hierfür schlagen wir eine für osteologische Zwecke modifizierte «Question Surprise» vor. «Würde es mich überraschen, wenn ich die/den gleichen/n Patientin/Patienten in einem Jahr erneut wegen einer Fraktur behandeln müsste?» Wird die Frage mit «Nein» beantwortet, dann könnte diese/r Patient/in ein/e Kandidat/Kandidatin für eine spezifische Osteoporosebehandlung sein.
Osteoporose und deren korrekte Behandlung sind Gegenstand zahlreicher Publikationen: Was gibt es Neues?
Über eine Vitamin-D-Supplementierung, die richtige Dosierung und allfällige Spiegelbestimmungen ist in den letzten Jahren viel und kontrovers geschrieben worden. Deshalb beschreiben wir diesbezüglich in diesem Artikel am Ende bei den «Key Messages» lediglich unser eigenes Vorgehen. Hier soll vielmehr der Fokus auf einer korrekten Indikationsstellung für die spezifische Therapie einer Osteoporose bei hochbetagten Frakturpatientinnen und -patienten liegen.
Mit dem humanisierten Sklerostinantikörper Romosozumab (Evenity®) ist ein neuer Wirkstoff mit grossem Wirkpotenzial für die Osteoporosetherapie verfügbar geworden. Die Kontraindikation bei Vorliegen eines kardiovaskulären Ereignisses in der Anamnese sowie die Notwendigkeit zur einmal monatlichen s.c.-Injektion sind allerdings Schwachstellen im Hinblick auf eine Anwendung bei betagten Frakturpatientinnen und -patienten. Fast gleichzeitig wurden durch den Wegfall des Patentschutzes Generika des bislang einzigen osteoanabolen Medikaments Teriparatid (Forsteo®) mit deutlich geringeren Behandlungskosten pro Monat verfügbar. Mit Abaloparatid wurde im Dezember 2022 ein weiteres osteoanabol wirkendes Molekül für die Therapie in der EU zugelassen [1], und in der Schweiz wurde das Zulassungsverfahren im Dezember 2022 eröffnet. Den genannten Medikamenten haftet allerdings allesamt der Nachteil an, dass sie eine s.c.-Injektion erfordern. Damit ist der Kreis möglicher Anwender unter hochbetagten Frakturpatient-innen natürlicherweise begrenzt. In Summe kann trotzdem festgehalten werden, dass die osteoanabolen Osteoporose-Therapieoptionen erweitert worden sind.
Schon lange bekannt und deshalb auch im FRAX-Algorithmus berücksichtigt ist die Tatsache, dass eine Fraktur in der Anamnese als Hauptrisikofaktor für das Erleiden von weiteren Frakturen zu betrachten ist. Die aktuelle Datenlage zeigt, dass dieser Effekt in den ersten beiden Jahren nach Erleiden der «Index-Fragilitätsfraktur» am stärksten ausgeprägt ist [2]. Auch aufgrund dieser Erkenntnis wurde zuletzt das Konzept des «Imminent Fracture Risk» neu in die Behandlungsalgorithmen und Therapieleitlinien eingeführt und mit einer breiten Therapieindikation verknüpft: Möglichst jede_r betagte Frakturpatient_in soll zeitnah zur Index-Fragilitätsfraktur eine spezifische Osteoporosetherapie erhalten [3]. Im Fall einer vertebralen oder anderen typischen Osteoporosefraktur sogar primär eine osteoanabole. Mit diesem Vorgehen soll das Ziel erreicht werden, eine möglichst grosse Zahl von Frakturen zu vermeiden, weil eine im Sinne der Frakturvermeidung effektive Therapie in der Phase mit dem höchsten Refrakturrisiko durchgeführt wird. Diese Empfehlung wird auch von der Schweizer Vereinigung gegen Osteoporose (SVGO) als der nationalen Fachorganisation mitgetragen [3].
Für Personen, die aufgrund ihres Alters und des Allgemeinzustandes das Ende eines geplanten Therapieintervalls mit grosser Wahrscheinlichkeit erleben, ist diese Empfehlung sicher als evidenzbasiert zu betrachten. Dass spezifische Osteoporose-Medikamente bis ins hohe Alter wirken, wurde gezeigt [4]. Unter Wirkeintritt verstehen wir in diesem Zusammenhang den Zeitpunkt, ab welchem sich die Refrakturrate in der placebokontrollierten Studie beim Verumarm im Vergleich zum Placeboarm erkennbar vermindert. Und das findet – je nach Molekül und Anwendungsform unterschiedlich – jedoch nicht vor dem Ablauf von 12 Monaten seit Therapiebeginn statt [4].
In der Patientenpopulation «hochbetagte Frakturpatient_innen» fällt eine markante Übersterblichkeit im Vergleich zur naturgemäss ohnehin schon hohen Mortalität der altersentsprechenden Referenzpopulation auf [5]. In Kombination könnten diese Fakten – also Übersterblichkeit und Latenz bis zum Wirkeintritt – dazu führen, dass die erhoffte frakturvermeidende Wirkung einer neu begonnenen Osteoporosebehandlung von betagten Frakturpatient_innen gar nicht mehr erlebt wird. Ist dieses Szenario eher theoretischer Natur oder klinisch relevant? Und wie kann man diese komplexen Zusammenhänge in ein «Shared Decision Making» einfliessen lassen?
Indikationsstellung für eine medikamentöse Osteoporosetherapie aufgrund eines individuellen Gesprächs mit der/m Patientin/Patienten und/oder mit Angehörigen
Hierfür scheint uns eine neue Art der Darstellung erforderlich, mit der die Situation der individuellen Patientin/des individuellen Patienten reflektiert wird.
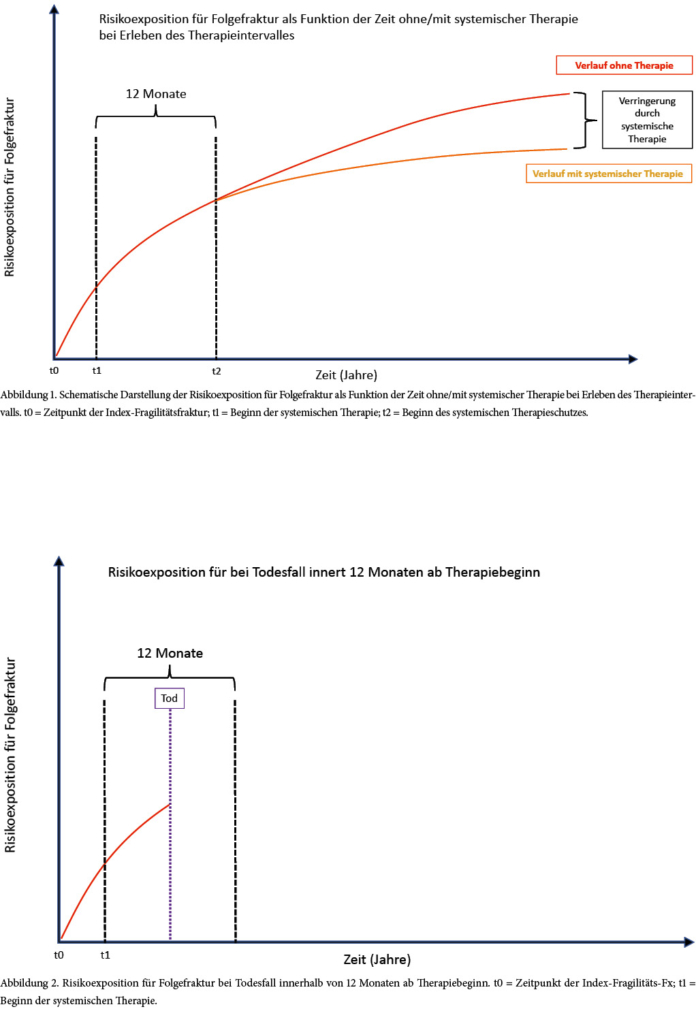
Auf der horizontalen Achse ist die Zeit (Jahre) abgetragen. Auf der vertikalen Achse ist die Gesamtrisikoexposition für das Erleiden einer weiteren Fragilitätsfraktur abgetragen. Unter Risikoexposition soll das im Verlauf aufgetretene Gesamtrisiko verstanden werden, dem der/die Patient_in beginnend vom Zeitpunkt t0 ausgesetzt war (Abb. 1).
Der/die Patient_in habe zum Zeitpunkt t0 eine erste Fragilitätsfraktur erlitten. Diese muss in Zukunft – neben möglichen anderen Risikofaktoren – bei der Berechnung des Gesamtrisikos für das Erleiden von weiteren Fragilitätsfrakturen in Betracht gezogen werden. Der Risikobeitrag durch die erste Fragilitätsfraktur ist gemäss jüngsten Untersuchungen in den ersten beiden Jahren höher – die Kurve der Gesamtrisikoexposition steigt deshalb auch in den ersten beiden Jahren nach der ersten Fraktur schneller an –, um danach etwas abzuflachen (rote Kurve).
Die Gesamtrisikoexposition kann vermindert werden, wenn nach der ersten Fragilitätsfraktur – leitliniengerecht – mit einer systemischen Osteoporosetherapie begonnen wird [6].
Dabei gilt es zu beachten:
- Die Risikoreduktion fällt umso deutlicher aus, je effektiver der frakturreduzierende Effekt des eingesetzten Medikaments ist.
- Es wird eine Latenzzeit von einem Jahr ab Therapiebeginn bis zum Einsetzen der Medikamentenwirkung im Sinn einer Reduktion des Refrakturrisikos angenommen.
Die Latenzzeit beginnt, nachdem die Medikamenteneinnahme begonnen und kontinuierlich fortgesetzt wurde. Diese Überlegungen sind grundsätzlich korrekt, wenn der/die Patient_in das gesamte geplante Therapieintervall erlebt, beziehungsweise wenn sie/er über diese ganze Zeit eine gute Compliance aufweist.
Gerade mit hochbetagten Patient_innen muss aber auch das in Abbildung 2 dargestellte Szenario diskutiert werden.
Je grösser die Gebrechlichkeit, umso grösser das Risiko, dass die betroffene Person möglicherweise stirbt, bevor das Therapieintervall beendet ist. Wegen der Latenz bis zum Wirkeintritt einer spezifischen Osteoporosetherapie könnte beim Tod der behandelten Person kurz nach Therapiebeginn die Situation entstehen, dass die erhoffte Wirkung nicht mehr erlebt wird. Ist dieses Ereignis eher theoretischer Natur oder klinisch relevant?
Um diese Frage zu beantworten, untersuchten wir anhand der bereits laufenden Qualitätssicherungsmassnahme über unseren «Fracture Liaison Service», wie häufig das oben beschriebene Szenario in einem Real World Setting auftritt [7, 8].
Von Januar 2021 bis Juni 2022 wurden alle Personen über 65 Jahre erfasst, die wegen einer Fraktur stationär behandelt wurden. Es waren 1381 Teilnehmende mit einem mittleren Alter von 83 Jahren. Ausgeschlossen wurden lediglich Patient_innen mit einem Hochenergietrauma als Unfallursache oder isolierte Finger, Zehen oder Schädelfrakturen ebenso wie Frakturen aufgrund von Knochenmetastasen.
Nachdem für 373 Teilnehmende die Resultate der 1-Jahres-Follow-up-Untersuchung vorliegen, zeigte sich der folgende Trend: Zwar erleiden tatsächlich 10 % der Patient_innen «at imminent fracture risk» schon im Folgejahr eine weitere Fraktur. Dagegen starben aber auch mehr als 30 % im gleichen Zeitraum!
Welche konkreten Handlungsanweisungen können daraus gezogen werden?
Weil diese Daten im Rahmen eines Qualitätssicherungsprogramms prospektiv gewonnen wurden, sind wir überzeugt, dass die genannten Prozentzahlen die Realität widerspiegeln.
Der FRAX-Algorithmus wird fortlaufend an neue Erkenntnisse angepasst [9, 10, 11]. In Zukunft werden mit lernenden Systemen sicher noch Softwaretools entwickelt [12], die uns Kliniker auch bei so komplexen Aufgaben wie einer individualisierten Indikationsstellung zur Osteoporosetherapie noch besser unterstützen. Bis es aber so weit ist, sind pragmatische Lösungen gefragt, um die neuen, intensiven Osteoporosemedikamente denjenigen Patient_innen zukommen zu lassen, die am meisten davon profitieren.
In der Palliativmedizin stehen Kolleginnen und Kollegen vor der noch viel schwierigeren Entscheidung: Soll eine kranke Person palliativ behandelt werden, ja oder nein? Dahinter verbirgt sich eine Frage, die nicht beantwortet werden kann: Wie lange hat dieser Mensch noch zu leben? Dieses Dilemma wird umgangen mit der «Question Surprise» [13] der Palliativmediziner_innen: «Würde es mich überraschen, wenn diese Person innerhalb der nächsten 12 Monate sterben würde?» Durch diesen Kunstgriff wird eine statistische, prozentuale Angabe in eine binäre «Ja oder Nein»-Entscheidung umgesetzt, ohne dass für diese «Konversion» ein fixer Schwellenwert angegeben werden muss.
Prinzipien der Palliativmedizin angewendet auf die Osteoporosetherapie
Die Problemstellung ist ähnlich gelagert wie die oben aufgeführte Situation in der Palliativmedizin: Das errechnete 10-Jahres-Frakturrisiko (FRAX) in Prozent muss in eine Therapieentscheidung «Ja oder Nein» umgesetzt werden. Für Patient_innen, die das Ende eines geplanten Therapiezyklus erleben, ist der Schwellenwert in Leitlinien festgelegt und bekannt. Für hochbetagte Frakturpatient_innen kann dieser wegen des relevanten, bei der Festlegung der Schwelle zur Therapieindikation nicht berücksichtigten Mortalitätsrisikos aber nicht einfach übernommen werden. Die Mortalität ist zwar z.B. im FRAX dahingehend berücksichtigt, dass die 10-Jahres-Frakturwahrscheinlichkeit im hohen Alter wieder sinkt – damit ist aber nicht abgebildet, dass die Wahrscheinlichkeit, den Therapieeffekt zu erleben, genauso absinkt.
Deshalb modifizieren wir die aus der Palliativmedizin bekannte «Surprise»-Frage für osteologische Zwecke wie folgt: «Würde es mich überraschen, wenn ich diese Person innerhalb des nächsten Jahres wegen einer weiteren Fraktur behandeln müsste?» Auf diese Art wird die gerade bei Hochbetagten relevante Frage nach der Restlebenserwartung zwanglos mit dem errechneten Frakturrisiko verknüpft. Dadurch wird eine Risikoangabe in Prozent wie sie vom FRAX-Algorithmus erhalten werden kann, in eine binäre, d.h. «Ja oder Nein»-Antwort auf die Frage zur Therapieindikation umgewandelt [14]. Die Antwort auf die oben gestellte Frage kann uns helfen zu bestimmen, in welche Richtung wir unsere Therapieempfehlung formulieren sollen.
Leitender Arzt
Orthopädie und Traumatologie
Universitätsspital Basel
4031 Basel
Schweiz
norbert.suhm@usb.ch
Es bestehen keine Interessenskonflikte.
Historie
Manuskript akzeptiert: 15.02.2023
Danksagung
Wir danken AgNovos Healthcare, USA, für die finanzielle Unterstützung bei der Durchführung der Qualitätssicherungsmassnahme. Wir bedanken uns bei Frau Irina Fischer für das Korrekturlesen und die Unterstützung beim Editieren. Wir bedanken uns bei Mr. James Pilachowski für die digitale Umsetzung der Abbildungen.
ORCID
Norbert Suhm
https://orcid.org/0000-0001-8258-9944
- Die Verfügbarkeit osteoanaboler Osteoporosetherapien wurde verbessert.
- Deren Anwendung wird u.a. für Personen empfohlen, die in die Fraktur-Risikogruppe «Imminent Fracture Risk» fallen, d.h. für Personen im Alter von > 65 Jahren, die eine vertebrale oder sonstige Major Fragilitätsfraktur vor weniger als zwei Jahren erlitten haben.
- Die Latenz bis zum Wirkeintritt einer neu begonnenen spezifischen Osteoporosetherapie beträgt je nach Medikament und Applikationsform bis zu 12 Monate. Bei der Indikationsstellung zur spezifischen Osteoporosetherapie bei hochbetagten Frakturpatient_innen könnte deshalb bei bis zu 30 % der Betroffenen der Fall eintreten, dass der erhoffte Therapieeffekt nicht mehr erlebt wird.
- Die Beantwortung der für osteologische Zwecke modifizierten «Question Surprise»: «Wäre ich überrascht, wenn ich diese/n Patientin/Patienten während des nächsten Jahres wegen einer weiteren Fraktur behandeln müsste?» könnte hilfreich sein, um diejenigen Hochbetagten zu identifizieren, die von einer Osteoporosebehandlung wirklich profitieren würden, d.h., bei einer Nein-Antwort könnte das Pendel eher in Richtung einer Therapieindikation ausschlagen.
- In diesem Fall sollte dann allerdings die Wahl tatsächlich eher auf eine intensive, osteoanabole Therapie fallen, denn eine jährliche Refrakturrate von über 10 % in dieser Subpopulation muss ernst genommen werden.
- Unabhängig von der Entscheidung betreffend eine spezifische Therapie der Osteoporose versuchen wir bei jeder/m, hochbetagten Frakturpatientin/-patienten die Osteoporose-Basisprophylaxe sicherstellen zu können. Dazu gehört eine Vitamin-D-Supplementierung mit 800IE bis 1000IE täglich oder ein entsprechendes wöchentliches bis monatliches Aequivalent. Bei der Applikationsfrequenz berücksichtigen wir unter anderem den Aufwand für das Tropfenzählen bei der täglichen Gabe, insbesondere bei institutionalisierten Personen. Bei Neubeginn der Vitamin-D-Supplementierung geben wir einmalig die Lade-Dosis von 20 000IE. Vitamin-D-Spiegelbestimmungen führen wir bei diesem Vorgehen keine durch.
- Calciumsupplemente setzen wir eher zurückhaltend ein. Stattdessen versuchen wir eine ausreichende tägliche Aufnahme über die Ernährung zu erreichen beziehungsweise über den Calciumgehalt des konsumierten Mineral-(Trink)-Wassers.
1. Siebebnand S. Neues Osteoporose-Mittel in der EU zugelassen. Pharmazeutische Z. 2013. https://www.pharmazeuti
sche-zeitung.de/neues-osteoporose-mittel-in-der-eu-zuge
lassen-137603/; letzter Zugriff: 22.02.2023.
2. Roux C, Briot K. Imminent fracture risk. Osteoporos Int. 2017;
28:1765–1769. DOI 10.1007/s00198-017-3976-5.
3. Ferrari S, Lippuner K, Lamy O, et al. 2020 recommendations for osteoporosis treatment according to fracture risk from the Swiss Association against Osteoporosis (SVGO). Swiss Med Wkly. 2020;150:w20352.
4. Rizzoli R, Branco J, Brandi M-L, et al. Management of osteoporosis of the oldest old Osteoporos Int. 2014;25:2507–2529. DOI 10.1007/s00198-014-2755-9.
5. Li N, Hiligsmann M, Boonen A, et al. The impact of fracture liaison services on subsequent fractures and mortality: a systematic literature review and meta-analysis. Osteoporos Int. 2021;32:1517–1530. https://doi.org/10.1007/s00198-021-05911-9.
6. Ayers C, Kansagara D, Lazur B, Fu R, Kwon A, Harrod C. Effectiveness and Safety of Treatments to Prevent Fractures in People With Low Bone Mass or Primary Osteoporosis: A Living Systematic Review and Network Meta-analysis for the American College of Physicians. Ann Intern Med. 2023;176(2):182–195. DOI: 10.7326/M22-0684.
7. Geiger I, Kammerlander C, Höfer C, et al. Implementation of an integrated care programme to avoid fragility fractures of the hip in older adults in 18 Bavarian hospitals – study protocol for the cluster-randomised controlled fracture liaison service FLS-CARE. BMC Geriatr. 2021;21(1):43. DOI: 10.1186/s12877-020-01966-1.
8. Javaid MK, Sami A, Lems W, et al. A patient-level key performance indicator set to measure the effectiveness of fracture liaison services and guide quality improvement: a position paper of the IOF Capture the Fracture Working Group, National Osteoporosis Foundation and Fragility Fracture Network. Osteoporos Int. 2020;31(7):1193–1204. DOI: 10.1007/s00198-020-05377-1.
9. Kanis JA, Johansson H, Harvey NC, et al. The use of 2-, 5-, and 10-year probabilities to characterize fracture risk after a recent sentinel fracture. Osteoporosis Int. 2021;32:47–54.
10. Järvinen TL, Jokihaara J, Guy P, Alonso-Coello P, Collins GS, Michaëlsson K, Sievänen H. Conflicts at the heart of the FRAX tool. CMAJ. 2014;186(3):165–167. DOI: 10.1503/cmaj.121874.
11. Vandenput L, Johansson H, McCloskey EV, et al. Update of the fracture risk prediction tool FRAX: a systematic review of potential cohorts and analysis plan. Osteoporos Int. 2022;33(10):2103–2136. DOI: 10.1007/s00198-022-06435-6.
12. Blaker K, Wijewardene A, White E, et al. Electronic search programs are effective in identifying patients with minimal trauma fractures. Osteoporos Int. 2022;33(2):435-441. DOI: 10.1007/s00198-021-06105-z.
13. Downar J, Goldman R, Pinto R, Englesakis M, Adhikari NK. The “surprise question” for predicting death in seriously ill patients: a systematic review and meta-analysis. CMAJ. 2017;189(13):E484-E493. DOI: 10.1503/cmaj.160775.
14. Morgott M, Heinmüller S, Hueber S, Schedlbauer A, Kühlein T. Do guidelines help us to deviate from their recommendations when appropriate for the individual patient? A systematic survey of clinical practice guidelines. J Eval Clin Pract. 2020;26(3):709–717. DOI: 10.1111/jep.13187.
PRAXIS
- Vol. 113
- Ausgabe 1
- Januar 2024