- Rheumatoide Arthritis in der Hausarztpraxis – Was ist vor und während der Therapie zu beachten?
Einleitung
Die rheumatoide Arthritis (RA) ist mit einer Prävalenz von ca. 200 Fällen/100 000 Personen eine der häufigsten rheumatologischen Erkrankungen. In der Schweiz ist bis zu 1 % der Bevölkerung betroffen, Frauen dreimal häufiger als Männer. Die Prävalenz der RA nimmt mit steigendem Lebensalter zu, mit einem Erkrankungsgipfel zwischen dem 30. und 50. Lebensjahrzehnt (1, 2).
Die RA ist ein heterogener Erkrankungskomplex unklarer Ätiologie. Ausgelöst wird die für die Symptomatik verantwortliche synoviale Entzündungsreaktion durch eine Kombination von genetischer Prädisposition und Umweltfaktoren (3, 4, 5).
Symptome der RA treten häufig schleichend auf, initial vor allem Gelenkschwellungen und Schmerzen in wenigen Gelenken mit im Verlauf zunehmend polyartikulär symmetrischem Muster. Häufig sind die Handgelenke, Finger- oder Zehengrundgelenke und proximalen Fingergelenke involviert, aber auch grössere Gelenke können betroffen sein. Morgensteifigkeit kann auftreten. Im Frühstadium werden Schmerzen und Schwellungen durch die Entzündungsreaktion ausgelöst, in späteren Stadien kommt es zur irreversiblen Destruktion des Knochen- und Knorpelgewebes (5). Deshalb ist eine frühzeitige Diagnose und entsprechend rascher Therapiebeginn mit disease-modifying antirheumatic drugs (DMARDs) notwendig (6).
Kurzübersicht über die Therapieoptionen und Therapiestrategie
Therapieziele sind
1. die Verbesserung der Lebensqualität,
2. die Verhinderung von Knochendestruktionen und
3. die Kontrolle der Entzündungsreaktion und damit Reduktion der kardiovaskulären Mortalität.
Aufgrund der irreversiblen Knochendestruktion bei aktiver RA ist ein früher Therapiebeginn innerhalb der ersten Wochen essenziell. Dadurch können Prognose und Langzeit-Outcome massgeblich verbessert werden (5, 7). Diagnosestellung, Wahl der Medikation und Überwachung der Therapie sollten durch einen Facharzt für Rheumatologie erfolgen. Ziel ist eine anhaltende Remission oder zumindest eine niedrige Krankheitsaktivität (8).
Grundpfeiler der Therapie sind sogenannte DMARDs. DMARDs bezeichnen eine heterogene Gruppe von Medikamenten, die, zusätzlich zur Symptomkontrolle, die Krankheitsaktivität der RA positiv beeinflussen können. Unterschieden werden conventional synthetic disease-modifiying antirheumatic drugs (csDMARDs), targeted synthetic disease-modifiying antirheumatic drugs (tsDMARDs) und biological disease-modifiying antirheumatic drugs (bDMARDs) (5).
Zu den csDMARDs gehören eine heterogene Gruppe von Wirkstoffen, dazu zählen Methotrexat (MTX), Leflunomid, Sulfasalazin und Hydroxychloroquin.
TsDMARDs umfassen die JAK-Inhibitoren, zu diesen gehören Tofacitinib, Baricitinib, Upadacitinib und Filgotinib (letzteres ist in der Schweiz nicht zugelassen).
Zu den bDMARDs zählen TNF-α-Inhibitoren wie Adalimumab, Etanercept, Golimumab, Certolizumab Pegol und Infliximab. Weitere Wirkstoffgruppen der bDMARDs sind CD20-Antikörper (Rituximab), aber auch Anti-T-Zell-Kostimulatoren (Abatacept) und IL-6-Inhibitoren (Tocilizumab, Sarilumab). Tab. 1 gibt einen Überblick über die verschiedenen DMARDs-Gruppen, die in der RA-Therapie relevant sind (5).
CsDMARDs, insbesondere MTX, sind die präferierte Erstlinientherapie der RA. Bei Kontraindikationen oder früher Intoleranz gegen MTX können Leflunomid und/oder Sulfasalazin als alternative Erstlinientherapien erwogen werden. Lässt sich die Krankheitsaktivität mit einem csDMARD nicht ausreichend kontrollieren, wird die Therapie um ein weiteres csDMARD erweitert. Bei weiterhin ungenügender Krankheitskontrolle ist eine zusätzliche Therapie mit einem bDMARD oder – abhängig vom Risikoprofil – mit einem tsDMARD (JAK-Inhibitor) zu evaluieren (6).
Glukokortikoide, seit den 1950er-Jahren eine tragende Säule in der RA-Therapie, sollten gemäss EULAR-Empfehlungen aufgrund des Risikoprofils nur initial beziehungsweise überbrückend bis zum Eintreten des Therapieerfolgs bei Behandlung mit einem DMARD zur Anwendung kommen (9). Die EULAR-Empfehlungen betonen explizit, die Therapiedauer mit Glukokortikoiden so kurz wie möglich und die Dosis so niedrig wie nötig zu halten. Ziel ist ein Sistieren der Glukokortikoidtherapie nach drei Monaten. Persistierender Bedarf von Glukokortikoiden über vier Monate nach Therapiebeginn mit einem csDMARD hinaus wird als Therapieversagen des csDMARD gewertet, und ein Wechsel soll evaluiert werden (6, 10).
Im Gegensatz zu den aktuellen Empfehlungen wird davon ausgegangen, dass bis zu 60 % der Patient/-innen eine Dauertherapie mit Glukokortikoiden erhalten (9).
Was ist vor Beginn einer Therapie mit einem DMARD oder einem hoch dosierten Glukokortikoid zu beachten?
Die Therapie mit DMARDs und/oder hoch dosierten Glukokortikoiden stellt ein erhöhtes Risiko für Infektionen dar. Gleichzeitig korreliert auch eine hohe Krankheitsaktivität ohne Therapie mit einer erhöhten Rate an Infektionen (11, 12, 13).
Prinzipiell sollten deshalb bei allen Patient/-innen Differenzialblutbild, C-reaktives Protein, Blutsenkungsgeschwindigkeit, Nieren- und Leberwerte bestimmt werden. Relevant sind zudem das Screening und die Prophylaxe bestimmter Infektionskrankheiten sowie die Kontrolle und Komplettierung des Impfstatus (9, 14).
EULAR- und SGR-Empfehlungen zu Screening und Prophylaxe von Infektionen
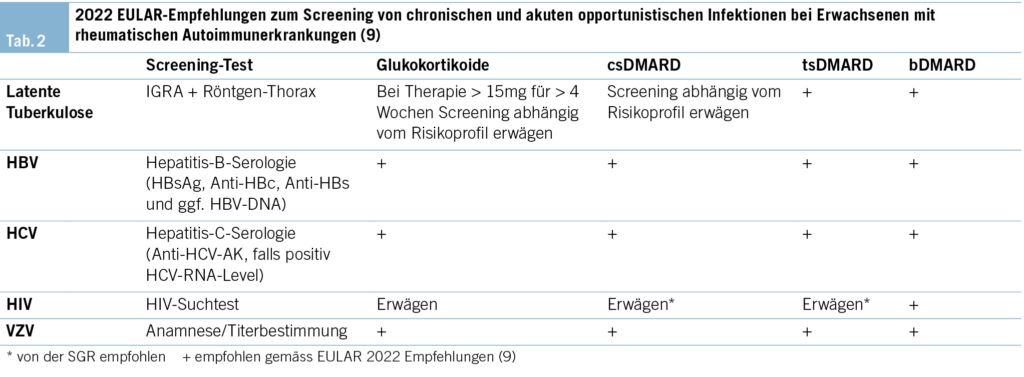
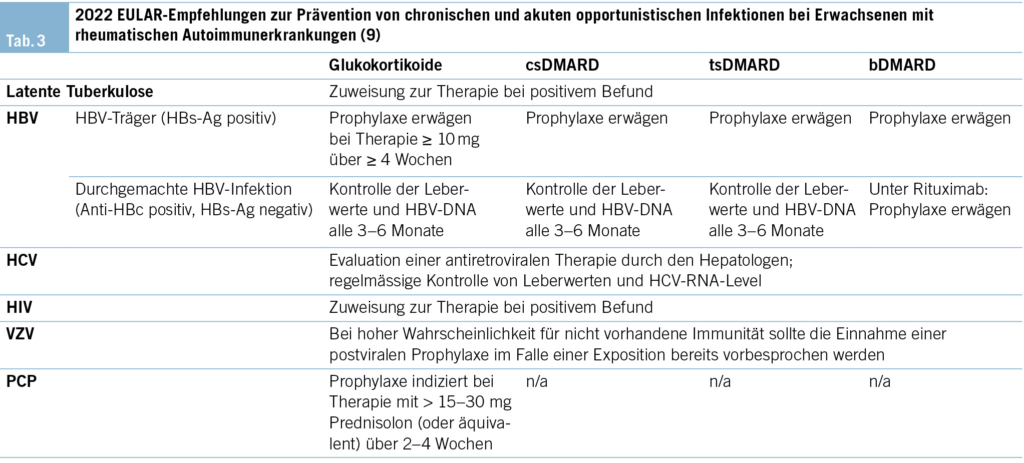
Um Screening und Prävention von Infektionskrankheiten europaweit bei entzündlichen rheumatischen Erkrankungen zu vereinheitlichen, wurden die 2022 veröffentlichten EULAR-Empfehlungen zu Screening und Prävention von chronischen und akuten opportunistischen Infektionen bei Erwachsenen mit rheumatischen Autoimmunerkrankungen erstellt (9). Tab. 2 und Tab. 3 geben einen Überblick über die relevanten EULAR-Empfehlungen betreffend Screening und Prophylaxe.
Die SGR empfiehlt vor Therapiebeginn mit einem DMARD ein Screening auf Hepatitis B, C sowie HIV (15, 14). Die farbige Kennzeichnung der relevanten DMARDs in Tab. 1 bezeichnet jeweils die empfohlenen Basisscreenings vor Therapiebeginn gemäss den Behandlungsempfehlungen der SGR (14).
Dauer und Dosis einer Glukokortikoidtherapie sind in der Fachliteratur nicht einheitlich definiert. Wo genaue Angaben bestehen, werden diese in Klammern () erwähnt.
Latente Tuberkulose
Patient/-innen unter Therapie mit einem bDMARD oder tsDMARD haben ein erhöhtes Risiko für die Reaktivierung einer latenten Tuberkulose, weshalb diese vor Therapiestart ausgeschlossen werden sollte. Unter csDMARDs und hoch dosierter Glukokortikoidtherapie (definiert als > 15mg/d über > 4 Wochen) ist ein Screening bei Vorhandensein zusätzlicher Risikofaktoren (z.B. Alkohol – oder Nikotinabusus, Herkunft aus bzw. Leben in Endemiegebieten) empfohlen. Das Screening auf latente Tuberkulose erfolgt mittels Interferon Gamma Release Assay (IGRA) und einem Röntgen-Thorax (9).
Hepatitis-B-Virus (HBV)
Das Risiko einer HBV-Reaktivierung ist abhängig von der geplanten Therapie sowie dem HBV-Status der Patient/-innen. HBV-Träger (HBs-Ag positiv) haben ein erhöhtes Risiko für eine Reaktivierung. Diese sollten betreffend einer antiviralen Prophylaxe hepatologisch mit beurteilt werden. Eine Therapie mit bDMARDs und eine Dauertherapie mit Glukokortikoiden (≥ 10mg/d über ≥ 4 Wochen gemäss ACR-Guideline) gelten als Hochrisikofaktoren für eine HBV-Reaktivierung. Die Datenlage für andere DMARDs ist weniger aussagekräftig. Patient/-innen mit durchgemachter HBV-Infektion (Anti-HBc positiv und HBs-Ag negativ) haben ein niedrigeres Risiko für eine Reaktivierung. Bei diesen Patient/-innen sollten alle drei bis sechs Monate Kontrollen von Leberwerten und HBV-DNA erfolgen. Eine Besonderheit besteht bei Patient/-innen unter Rituximab, diese haben ein sehr hohes Risiko für eine Reaktivierung, insbesondere wenn keine hohen Anti-HBs-AK-Titer vorhanden sind. Bei dieser Patient/-innen-Gruppe sollte daher eine antivirale Prophylaxe vor bzw. während der Behandlung der RA evaluiert werden. Bei Nachweis einer akuten HBV-Infektion und/oder Reaktivierung einer HBV-Infektion (Konversion von HBs-Ag negativ zu positiv oder Ansteigen/Auftreten der HBV-DNA) unter Therapie muss der Patient hepatologisch beurteilt werden (9).
Hepatitis-C-Virus (HCV)
Eine HCV-Serologie (Anti-HCV-AK) sollte bei allen Patient/-innen erwogen werden. Bei erhöhten Leberwerten oder bestehenden Risikofaktoren für eine HCV-Infektion ist ein Screening vor Beginn einer antirheumatischen Therapie zwingend. Bei Nachweis von HCV-Antikörpern sollte die HCV-RNA-Last bestimmt und eine antiretrovirale Therapie durch den Hepatologen evaluiert werden (9).
Human Immunodeficiency Virus (HIV)
Obwohl die Datenlage betreffend Screening auf HIV bisher ungenügend ist, wird ein Screening auf HIV vor Beginn einer Therapie mit bDMARDs empfohlen (9). In der Schweiz empfiehlt die SGR ein Screening auf HIV vor Beginn von DMARDs (14).
Varizella-Zoster-Virus (VZV)
Aufgrund der hohen Variabilität betreffend VZV-Immunität werden von der EULAR keine spezifischen Empfehlungen bezüglich Titerbestimmung vor Therapiebeginn abgegeben. Mindestens sollte die VZV-Immunität mittels detaillierter Anamnese ermittelt werden. Falls Unsicherheit über den Status besteht oder keine Immunität vorhanden ist, sollte mit den Patient/-innen bereits vor Beginn einer DMARD- oder hoch dosierten Glukokortikoidtherapie eine postvirale Prophylaxe im Falle einer Exposition besprochen werden (9).
Pneumocystis jirovecii Pneumonie (PCP)
Eine PCP-Prophylaxe sollte bei Patient/-innen mit hoch dosierter Glukokortikoidtherapie oder bei Kombination mit Immunsuppressiva erwogen werden. Bei einer Therapie mit 15–30 mg Prednisolon/d oder Äquivalenzdosis über mehr als zwei bis vier Wochen erscheint eine PCP-Prophylaxe vorteilhaft (9).
Impfempfehlungen
Dieser Absatz gibt eine Übersicht über das 2019 Update der EULAR Impfempfehlungen und der 2024 SGR-Impfempfehlungen für Patient/-innen mit entzündlichen rheumatischen Erkrankungen. Diese Empfehlungen beziehen sich auf Patient/-innen mit entzündlichen rheumatischen Erkrankungen und nicht spezifisch auf Patient/-innen mit RA.
Grundsätzlich sollte der Impfstatus gemäss BAG-Impfplan vor Therapiebeginn und dann einmal jährlich kontrolliert und aufgefrischt werden. Impfungen sind bevorzugt in Phasen mit ruhender bzw. niedriger Krankheitsaktivität durchzuführen. Die Mehrheit der vorhandenen Studien wurde bei Patient/-innen mit ruhender Krankheitsaktivität durchgeführt, folglich ist die Studienlage betreffend Effektivität und Sicherheit von Impfungen während aktiver Erkrankung bisher ungenügend. Impfungen sind vor der Initiierung einer immunsuppressiven Therapie, insbesondere vor einer Anti-B-Zelltherapie (z.B. Rituximab), durchzuführen. Geplante Auslandsaufenthalte sollten erfragt werden, um auch die Reiseimpfungen vor Beginn einer Therapie zu komplettieren. Der Therapiestart sollte jedoch keinesfalls aufgrund noch ausstehender Impfungen verzögert werden (16, 17).
Totimpfstoffe
Totimpfstoffe können auch unter einer Glukokortikoid-oder einer DMARD-Therapie geimpft werden. Impfungen sind unter diesen Therapien sicher und ausreichend effektiv, eine Ausnahme stellen Anti-B-Zell-Therapien (z.B. Rituximab) dar. Die EULAR empfiehlt hier, benötigte Impfungen frühestens sechs Monate nach der letzten Gabe und vier Wochen vor der nächsten Gabe durchzuführen. Falls ein solches Zeitfenster nicht eingehalten werden kann, ist es auch möglich, unter Therapie zu impfen. Allerdings besteht dann wahrscheinlich eine suboptimale Immunantwort (16). Studien zu Impfungen unter Therapie mit anderen bDMARDs zeigten generell eine ausreichende immunologische Antwort.
Lebendimpfstoffe
Lebendimpfstoffe sind unter immunsuppressiver Therapie aufgrund des Risikos einer Infektion generell kontraindiziert. Lebendimpfungen sollten daher mindestens vier Wochen vor Beginn einer immunsuppressiven Therapie verabreicht werden. Die Gelbfieber-Impfung ist aufgrund des Infektionsrisikos zu vermeiden oder nur unter Pausierung der immunsuppressiven Therapie durchzuführen (16).
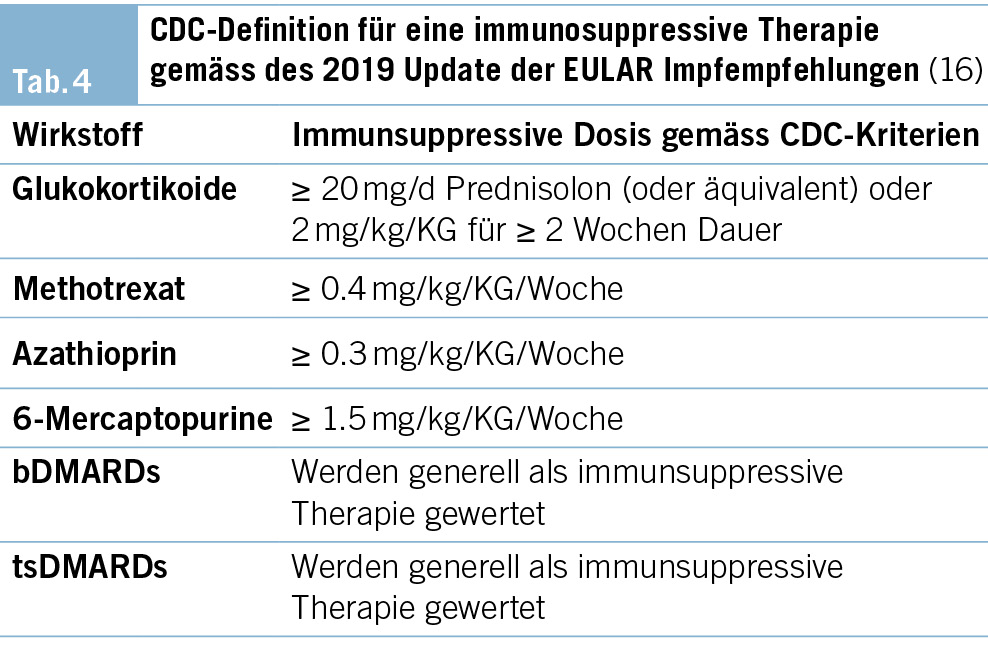
Das Vorliegen einer immunsuppressiven Therapie wird in den EULAR-Empfehlungen analog zur CDC-Definition festgelegt, siehe hierzu Tab. 4. Unklarheit besteht, inwieweit ein Patient unter niedrig dosierter Langzeit-Glukokortikoidtherapie als immunsupprimiert zu betrachten ist (16).
Die SGR empfiehlt:
– Falls Lebendimpfstoffe notwendig sind, sollte die Basistherapie frühestens einen Monat nach der letzten Lebendimpfung begonnen werden.
– Eine bestehende DMARD-Therapie sollte mindestens 3 Monate vor einer Lebendimpfung abgesetzt werden, bei Glukokortikoiden (≥ 20mg/d) reicht ein Zeitraum von einem Monat vor der geplanten Impfung.
– Nach Leflunomid-Therapie sollte erst nach zwei Jahren eine Lebendimpfung erfolgen.
– Unter Rituximab ist der Impferfolg während B-Zell-Depletion reduziert. Daher sollten Impfungen wenn möglich vier Wochen vor Therapiebeginn erfolgen (17).
Tetanus-Impfung
Vor Therapiebeginn sollte eine Auffrischimpfung für Diphtherie und Tetanus erfolgen (16, 17). Eine adäquate Effektivität kann auch unter immunsuppressiver Therapie angenommen werden. Eine Ausnahme stellt die Therapie mit Rituximab dar, hier sollte wegen der geringeren Immunantwort in Hochrisikosituationen die zusätzliche Gabe von Tetanus-Immunglobulinen erwogen werden (16).
Influenza-Impfung
Die saisonale Influenza-Impfung ist prinzipiell empfohlen. Unter Therapie (ausser Rituximab) ist eine ausreichende Effektivität gegeben (16).
SARS-CoV-2-Impfung
Betreffend SARS-CoV-2 sollten alle Patient/-innen eine Grundimmunisierung mit zwei Impfdosen (drei Impfdosen bei immunsupprimierten Patient/-innen) desselben RNA-Impfstoffes im Abstand von einem Monat erhalten. Auffrischimpfungen sollten vier oder mehr Monate nach der letzten COVID-19-Erkrankung oder Impfung erfolgen (17).
Pneumokokken-Impfung
RA Patient/-innen haben grundsätzlich ein erhöhtes Risiko für pulmonale Infekte und insbesondere auch für eine Pneumokokken-Infektion (18). Eine Pneumokokken-Impfung ist in dieser Patient/-innen-Gruppe daher empfohlen (16). Die SGR empfiehlt gemäss BAG-Empfehlungen eine einmalige Impfung mit Prevenar 13®. Patient/-innen, die vorgängig mit Pneumovax® geimpft wurden, wird frühestens 12 Monate nach der letzten Pneumovax®-Impfung eine einmalige Prevenar-13®-Impfung empfohlen. Prinzipiell sollte zur Influenza-Impfung ein Monat Abstand gehalten werden (17).
Hepatitis-A-Impfung
Gemäss 2019 EULAR-Empfehlungen sollten Patient/-innen mit einem Risiko für eine Hepatitis A (z.B. seronegative Patient/-innen bei Reisen in Endemiegebiete) eine Hepatitis-A- Impfung erhalten. Aufgrund der eingeschränkten Immunität nach einmaliger Impfung ist eine zweite HAV-Impfung nach sechs Monaten mit Titerbestimmung empfohlen (16).
Hepatitis-B-Impfung
Patient/-innen mit Risikofaktoren sollten eine Hepatitis- B-Impfung erhalten. Hierzu zählen immunsupprimierte Patienten, aber auch HBV-seronegative Patient/-innen, die in Endemiegebiete reisen, medizinisches Personal, Haushaltsmitglieder mit chronischer HBV-Infektion und Men who have sex with men (16). Die Impfung besteht aus drei Dosen, wobei der monovalente Impfstoff oder der bivalente Impfstoff mit Hepatitis A verwendet werden kann. Eine Titerbestimmung vier Wochen nach der letzten Impfung sollte erwogen werden (17).
Herpes Zoster-Impfung
Die SGR empfiehlt generell allen Patient/-innen ≥ 65 Jahre eine Herpes-Zoster-Impfung mit dem Totimpfstoff Shingrix®. Die vollständige Impfung beinhaltet zwei Dosen im Abstand von zwei bis sechs Monaten. Zostavax®, der attenuierte Lebendimpfstoff, ist bei immunsupprimierten Patient/-innen kontraindiziert (17).
Die Herpes-Zoster-Impfung ist für alle Patient/-innen mit Monotherapie eines csDMARD, bDMARD oder unter niedrig dosierter Glukokortikoidtherapie (< 20mg/d) ≥ 50 Jahre empfohlen.
Patient/-innen unter Therapie mit JAK-Inhibitoren oder einer Kombinationstherapie aus DMARDs und/oder hoch dosierten Glukokortikoiden (≥ 20mg/d) wird die Herpes-Zoster-Impfung bereits ab ≥ 18 Jahren empfohlen (17).
Varizella-Zoster-Virus (VZV)-Impfung
Für bisher nicht an Windpocken erkrankte und nicht geimpfte Personen (13 Monate bis 39 Jahre) besteht die BAG-Empfehlung für eine Impfung. Dieser Lebendimpfstoff darf nicht unter Immunsuppression verabreicht werden (17).
Weitere Punkte
Haushaltsmitglieder von immunsupprimierten Patient/-innen sollten dazu angehalten werden, alle Impfungen gemäss offiziellem Impfplan durchzuführen. Eine Ausnahme ist die orale Polio-Impfung, diese sollten Haushaltskontakte aufgrund des Risikos einer Übertragung nicht durchführen. Zusätzlich sollten stark immunsupprimierte Patient/-innen das Windelwechseln bei Säuglingen vermeiden, die innerhalb der letzten vier Wochen die Rotaviren-Impfung erhalten haben. Weiter sollte der Kontakt zu Personen, die nach Varizellen- oder Herpes-Zoster-Impfung Hautläsionen entwickeln, vermieden werden (16). Gemäss SRG besteht bei jeder Lebendimpfung von Kontaktpersonen das Risiko einer Übertragung, ausser bei MMR- und Varizellen-Impfung (17).
Randomisierte Studien haben eine höhere Effektivität unter Pausierung von MTX um den Impfzeitpunkt für die Sars-CoV-2-Impfung und die saisonale Influenza-Impfung gezeigt. Jedoch war das Risiko für einen Krankheitsschub erhöht. Die EULAR empfiehlt daher aktuell keine Pausierung von MTX (16, 17, 19, 20).
Relevante Internetadressen
www.rheuma-net.ch
www.eular.org
www.rheumatology.org
www.rheumaliga.ch
Abkürzungen
ACPA Anti-cyclic citrullinated peptide antibodies
bDMARDs Biological disease-modifiying antirheumatic drugs
BSR Blutsenkungsreaktion
CCP-AK Antikörper gegen cyclisch-citrullinierte Peptide
CRP C-reaktives Protein
csDMARDs Conventionel synthetic disease-modifiying antirheumatic drugs
EULAR European Alliance of Associations for Rheumatology
IL-6 Interleukin 6
MTX Methotrexat
PCP Pneumocystis jirovecii Pneumonie
RA Rheumatoide Arthritis
RF Rheumafaktor
TNF-a Tumornekrosefaktor-a
tsDMARDs Targeted synthetic disease-modifiying antirheumatic drugs
Historie
Manuskript eingegangen: 29.10.2024
Angenommen nach Revision: 06.01.2025
Tellerweg 30
4102 Binningen
melanie.kraus@hin.ch
Die Autorenschaft hat keine Interessenkonflikte im Zusammenhang mit diesem Artikel deklariert.
1. Black RJ, Cross M, Haile LM, Culbreth GT, Steinmetz JD, Hagins H, et al. Global, regional, and national burden of rheumatoid arthritis, 1990–2020, and projections to 2050: a systematic analysis of the Global Burden of Disease Study 2021. Lancet Rheumatol. 2023 Oct 1;5(10):e594–610.
2. Arthritis – Rheumaliga Schweiz [Internet]. [cited 2024 Oct 5]. Available from: https://www.rheumaliga.ch/rheuma-von-a-z/arthritis
3. Scherer HU, Häupl T, Burmester GR. The etiology of rheumatoid arthritis. Vol. 110, Journal of Autoimmunity. Academic Press; 2020.
4. Gravallese EM, Firestein GS. Rheumatoid Arthritis — Common Origins, Divergent Mechanisms. New England Journal of Medicine. 2023 Feb 9;388(6):529–42.
5. Di Matteo A, Bathon JM, Emery P. Rheumatoid arthritis. Vol. 402, The Lancet. Elsevier B.V.; 2023. p. 2019–33.
6. Smolen JS, Landewé RBM, Bergstra SA, Kerschbaumer A, Sepriano A, Aletaha D, et al. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2022 update. Ann Rheum Dis. 2022 Nov 10;82(1):3–18.
7. Smolen JS, Aletaha D, Bijlsma JWJ, Breedveld FC, Boumpas D, Burmester G, et al. Treating rheumatoid arthritis to target: Recommendations of an international task force. Ann Rheum Dis. 2010;69(4):631–7.
8. Schneider M, Baseler · G, Funken O, Heberger · S, Kiltz U, Klose · P, et al. Management der frühen rheuma toiden Arthritis [Internet]. Available from: www.springermedizin.de
9. Fragoulis GE, Nikiphorou E, Dey M, Zhao SS, Courvoisier DS, Arnaud L, et al. 2022 EULAR recommendations for screening and prophylaxis of chronic and opportunistic infections in adults with autoimmune inflammatory rheumatic diseases. Ann Rheum Dis. 2023 Jun 1;82(6):742–53.
10. Hua C, Buttgereit F, Combe B. Glucocorticoids in rheumatoid arthritis: Current status and future studies. Vol. 6, RMD Open. BMJ Publishing Group; 2020.
11. Au K, Reed G, Curtis JR, Kremer JM, Greenberg JD, Strand V, et al. High disease activity is associated with an increased risk of infection in patients with rheumatoid arthritis. Ann Rheum Dis [Internet]. 2011 May 1 [cited 2024 Oct 7];70(5):785–91. Available from: https://ard.bmj.com/content/70/5/785
12. Listing J, Gerhold K, Zink A. The risk of infections associated with rheumatoid arthritis, with its comorbidity and treatment. Rheumatology (Oxford) [Internet]. 2013 Jan [cited 2024 Oct 10];52(1):53–61. Available from: https://pubmed.ncbi.nlm.nih.gov/23192911/
13. Weaver A, Troum O, Hooper M, Koenig AS, Chaudhari S, Feng JY, et al. Rheumatoid arthritis disease activity and disability affect the risk of serious infection events in RADIUS 1. J Rheumatol [Internet]. 2013 Aug [cited 2024 Oct 10];40(8):1275–81. Available from: https://pubmed.ncbi.nlm.nih.gov/23772079/
14. Behandlungsempfehlungen [Internet]. [cited 2024 Oct 3]. Available from: https://www.rheuma-net.ch/de/fachinformationen/behandlungsempfehlungen
15. Conley B, Bunzli S, Bullen J, O’Brien P, Persaud J, Gunatillake T, et al. What are the core recommendations for rheumatoid arthritis care? Systematic review of clinical practice guidelines. Vol. 42, Clinical Rheumatology. Springer Science and Business Media Deutschland GmbH; 2023. p. 2267–78.
16. Furer V, Rondaan C, Heijstek MW, Agmon-Levin N, Van Assen S, Bijl M, et al. 2019 update of EULAR recommendations for vaccination in adult patients with autoimmune inflammatory rheumatic diseases. Ann Rheum Dis. 2020 Jan 1;79(1):39–52.
17. Schweizerische Gesellschaft für Rheumatologie Impfempfehlungen für Patienten mit entzündlich-rheumatischen Erkrankungen [Internet]. [cited 2024 Oct 24]. Available from: https://www.rheuma-net.ch/de/doc/impfempfehlungen-fuer-patienten-mit-entzuendlich-rheumatischen-erkrankungen/viewdocument/68
18. Shea KM, Edelsberg J, Weycker D, Farkouh RA, Strutton DR, Pelton SI. Rates of Pneumococcal Disease in Adults With Chronic Medical Conditions. 2014;
19. Park JK, Lee MA, Lee EY, Song YW, Choi Y, Winthrop KL, et al. Effect of methotrexate discontinuation on efficacy of seasonal influenza vaccination in patients with rheumatoid arthritis: A randomised clinical trial. Ann Rheum Dis. 2017 Sep 1;76(9):1559–65.
20. Park JK, Lee YJ, Shin K, Ha YJ, Lee EY, Song YW, et al. Impact of temporary methotrexate discontinuation for 2 weeks on immunogenicity of seasonal influenza vaccination in patients with rheumatoid arthritis: a randomised clinical trial. Ann Rheum Dis [Internet]. 2018 Jun 1 [cited 2024 Oct 10];77(6):898–904. Available from: https://pubmed.ncbi.nlm.nih.gov/29572291/
21. Schweizerischer Impfplan [Internet]. [cited 2024 Oct 5]. Available from: https://www.bag.admin.ch/bag/de/home/gesund-leben/gesundheitsfoerderung-und-praevention/impfungen-prophylaxe/schweizerischer-impfplan.html
PRAXIS
- Vol. 114
- Ausgabe 3
- März 2025