- Selten, jedoch schwerwiegend: Metabolische Azidose durch gleichzeitige Anwendung von Paracetamol und Flucloxacillin
Ein 60-jähriger polymorbider Patient entwickelte während einer wochenlangen Behandlung mit Flucloxacillin und Paracetamol eine schwere metabolische Azidose. Die Azidose hatte eine gemischte Ätiologie und wurde durch eine 5-Oxoprolinakkumulation bei vorbestehen-den Risikofaktoren für einen Glutathionmangel sowie eine Ketoazidose bei Malnutrition ausgelöst. Nach supportiver Behandlung mit N-Acetylcystein sowie Hämofiltration war die Azidose vollständig rückläufig.
Schlüsselwörter: Oxoprolin, Hungerazidose, metabolische Azidose mit grosser Anionenlücke, Flucloxacillin, Paracetamol
Anamnese und Befunde
Ein sechzigjähriger Patient mit einer langjährigen Anamnese einer rheumatoiden Arthritis unter Immunsuppression mit Prednison, Adalimumab, Azathioprin und Hydroxychloroquin wurde aufgrund von Fieber und Rückenschmerzen in die Notaufnahme eingewiesen, nachdem vor zehn Tagen starke lumbale Schmerzen mit Ausstrahlung in die Beine erstmals aufgetreten waren. Bei Verdacht auf einen Schub der rheumatoiden Arthritis erhöhte der Hausarzt die Prednison-Dosis auf 60 mg täglich. Bei diesem septischen und hypotonen Patienten zeigte die Computertomographie Impressionsfrakturen der lumbalen Wirbelkörper 3 und 4, bilaterale Psoasabszesse sowie eine Spondylodiszitis als Infektfokus.
Der Patient wurde auf die Intermediate-Care-Station aufgenommen und eine empirische antiinfektive Therapie mit Piperacillin/Tazobactam und Vancomycin eingeleitet. Die Immunsuppression reduzierten wir auf Prednison 20 mg als Monotherapie. Nach dem Nachweis von Staphylococcus aureus in den Blutkulturen wechselten wir zu Flucloxacillin (kon-tinuierliche Infusion mit 12 g/24h). Nach Quantifizierung des Ausmasses der Abszesse und der Spondylodiszitis mittels MRT (Magnetresonanstomographie) führten wir eine Hemilaminektomie von L2 (2. Lumbalsegment) mit mikrochirurgischer Abszessdrainage sowie eine CT-gesteuerte (Computertomographie) Abszessdrainage in beiden Psoasmuskeln durch. Es gab keine Anzeichen einer Endokarditis in der transösophagealen Echokardiographie, die Blutkulturen bliebeb nach der Infektsanierung in Abständen von 2 Tagen repetitiv negativ.
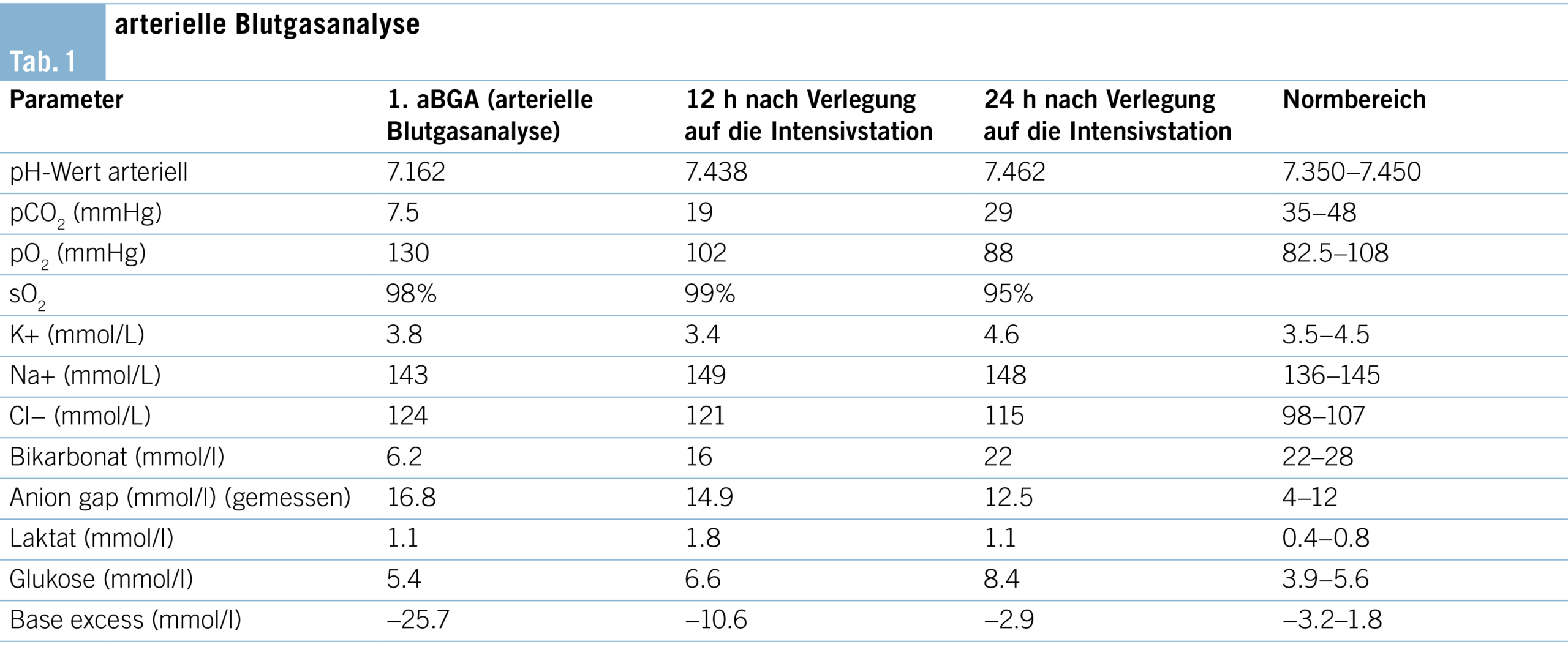
Die starken Schmerzen behandelten wir mit Metamizol (4x500mg p.o. täglich), Paraceta-mol (4×500 mg p.o. täglich), Oxycodon und Ketamin. Drei Wochen nach der Aufnahme präsentierte sich der Patient mit akut aufgetretener Tachypnoe (Atemfrequenz >40/min), Sprechdyspnoe jedoch normalem Lungenauskultationsbefund. Die periphere Sättigung unter Raumluft war normal. Es gab keine Marmorierung der Haut, der Patient war hämo-dynamisch stabil (Blutdruck 170/95 mmHg, Herzfrequenz 112/min., rhythmisch), afebril (37 °C), die Halsvenen waren nicht gestaut, periphere Ödeme bestanden nicht. Die Darm-geräusche waren über allen vier Quadranten normal, der Bauch war weich und ohne Druckempfindlichkeit. Das EKG (Elektrokardiogramm) und die Laboruntersuchungen zeig-ten keine Anzeichen eines akuten Koronarsyndroms. Die Blutgasanalyse zeigte eine schwere metabolische Azidose (pH 7,162, pCO2 7.5 mmHg) mit erhöhter Anionenlücke (16,8 mmol/l), erniedrigtem Bikarbonat (6 mmol/L), normalem Laktat (1,1 mmol/l) und normalem Blutzucker (Tab. 1).
Differenzialdiagnostische Überlegungen
Die Bewertung von Säure-Basen-Störungen sollte die einfache Berechnung der Anionenlücke einschliessen. Sie wird wie folgt berechnet: Anionenlücke = Na+ – (Cl- + HCO3-) und liegt normalerweise bei 10 bis 12 mmol/l. Eine Vergrösserung der Anionenlücke ist in der Regel auf eine Zunahme ungemessener Anionen in der extrazellulären Flüssigkeit zurückzuführen (Additionsazidose) und seltener auf eine Abnahme ungemessener Kationen (Calcium, Magnesium, Kalium). Die ungemessenen Anionen umfassen Phosphat, Sulfat und organische Anionen. Darüber hinaus nimmt die Anionenlücke zu mit einer Zunahme des anionischen Albumins (Serumalbumin minus 10 g/L vom Normalwert (45 g/L) verringert die Anionenlücke um 2,5 mmol/l).
Bei normalem Serumalbumin wird eine Anionenlücke-Azidose also durch nicht-chloridhaltige Säuren verursacht: anorganische (Phosphat, Sulfat), organische (Ketonkör-per, Laktat, urämische organische Anionen), exogene (Salicylat oder aufgenommene Toxine mit Produktion von organischen Säuren) oder nicht identifizierte Anionen.
Weitere Abklärungsschritte und Verlauf
Bei dem Patienten lag eine schwere akute metabolische Azidose vor. Eine Laktatazidose lag nicht vor und die Nierenfunktion war normal (Messung der Cystatin C Clearance). Der Blutzucker war nicht entgleist, Ketonkörper konnten initial im Urin (mittels Streifentest) nicht nachgewiesen werden. Aufgrund der gleichzeitigen Therapie mit Flucloxacillin und Paracetamol bei einem Patienten in einem mangelernährten Zustand (Gewichtsabnahme von 10 kg im letzten Monat) wurde eine Akkumulation von 5-Oxoprolin vermutet.
Die Bestimmung des 5-Oxoprolin-Spiegels im Urin mit einem Wert von 21000 mmol/mol Kreatinin bestätigte die Diagnose (Normbereich bis 200 mmol/mol Kreatinin), was aber eine Anionenlücke von 16mmol/L erwarten lässt (1). Eine mögliche Erklärung für diese Diskrepanz ist die schwere Hypoalbuminämie des Patienten (20 g/L) und eine hyperchlorämische Azidose (Chlorid 124 mmol/L). Die Ursache für diese Komponente war initial unklar. Während der Bestimmung von Oxoprolin im Urin wurden zusätzlich erhöhte Ketonkörper (3-Keto-Butyrat von 700 mmol/mol Kreatinin, Normwert <60; 3-Hydroxybutyrat von 2560 mmol/mol Kreatinin, Normwert <130) nachgewiesen.
Kurz nach Auftreten der ersten Symptome und der Blutgasanalyse erschöpfte sich der Patient respiratorisch und entsättigte bis 60%, weshalb die rasche Verlegung auf die Intensivstation erfolgte. Es wurde eine Therapie mit N-Acetylcystein durchgeführt mit dem Ziel das Glutathion auf-zufüllen. Natriumbicarbonat wurde verabreicht sowie eine kontinuierliche Hämofiltration eingeleitet zwecks Normalisierung der Stoffwechsellage. Die Hämofiltration inklusive Adsorption mittels Cytosorb diente zusätzlich der Clearance des Flucloxacillin. Im Verlauf konnte die Azidose innerhalb von 24 Stunden vollständig korrigiert werden. Nach weiteren 4 Wochen Antibiotikatherapie mit Cefazolin und Clindamycin wurde der Patient zuerst in eine Rehabilitationsklinik verlegt und er konnte diese schliesslich nach weiteren vier Wochen in gebessertem Zustand nach Hause verlassen.
Diagnose
Folgende primäre Ursachen führten zu dieser schweren gemischten metabolischen Azidose. Einerseits bestand eine Ketonurie, andererseits eine 5-Oxoprolinakkumulation nach einem Monat gleichzeitiger Therapie von Flucloxacillin und Paracetamol (Tab. 2). 5-Oxoprolin ist ein Metabolit des Gamma-Glutamyl-Zyklus. Es handelt sich um eine organische Säure, die bei Akkumulation eine metabolische Azidose mit vergrösserter Anionenlü-cke auslösen kann.

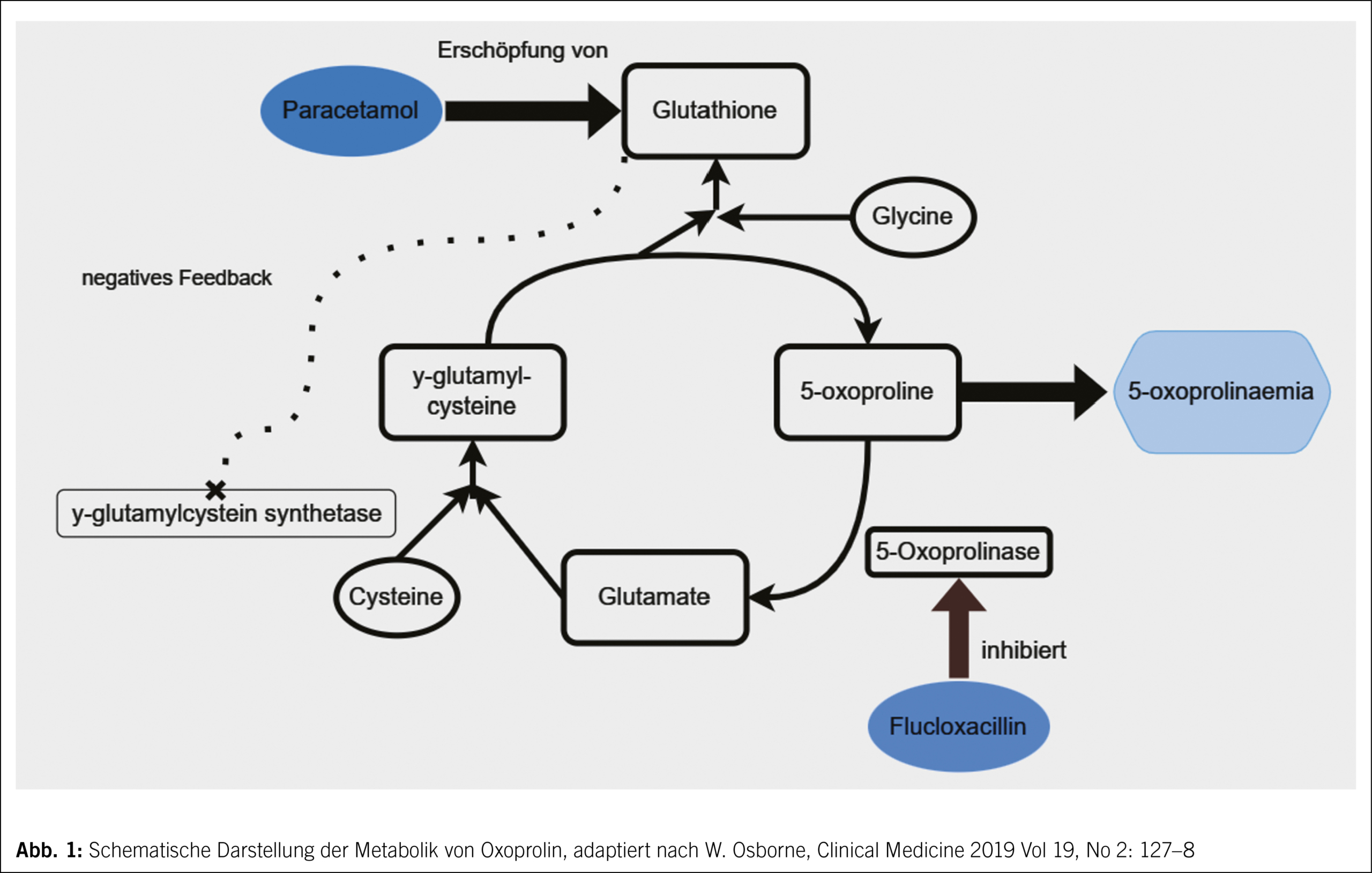
Im Gamma-Glutamyl-Zyklus kann 5-Oxoprolin durch die 5-Oxoprolinase zu Glutamat umgewandelt werden. Glutamat und Cystein bilden gemeinsam γ-Glutamylcystein, aus dem Glutathion und 5-Oxoprolin gebildet werden. Paracetamol verursacht einen Verbrauch von Glutathion durch seinen Metaboliten N-Acetylpbenzoquinonimin (3). Niedrige Glutathionspiegel lösen wiederum durch einen Rückkopplungsmechanismus einen Anstieg von γ-Glutamylcystein aus. Flucloxacillin hemmt die 5-Oxoprolinase (4). Dies führt zu einem Anstieg des 5-Oxoprolin-Spiegels und somit zu einer 5-Oxoprolinämie (Grafik 1). Das Risiko eines Gluthationmangels steigt bei Mangelernährung, Alkoholüberkonsum, fortgeschrittenem Alter sowie chronischen Erkrankungen.
Die Hyperchloridämie ist durch eine erhöhte renale Chloridreabsorption bedingt. Diese dient zur Kompensation der erhöhten Bikarbonatexkretion im Rahmen der Ketonkörper und Flucloxacillin-Ausscheidung (Flucloxacillin liegt als Kation, gebunden an Bikarbonat, im Urin vor). Eine renal-tubuläre Azidose vom Typ 1 im Rahmen der rheumatoiden Arthritis kam differentialdiagnostisch als Ursache der Hyperchloridämie ebenfalls in Frage, wurde aber bei einem Urin pH-Wert von 5 vor und mehrere Wochen nach dem Ereignis bei nor-malisiertem Säure-Base-Haushalt ausgeschlossen.
Die Ketoaziodse wurde im Rahmen der Malnutrition während des protrahierten Infektes gewertet. Während einer akuten Azidose verändert sich das Redox-Gleichgewicht im Kör-per erheblich. Das führt zu einer Verschiebung des Verhältnisses von Beta-Hydroxybutyrat (BHB) und Acetoacetat (AcAc) zugunsten von BHB. Dies geschieht, weil das erhöhte Verhältnis von NADH zu NAD+ die Umwandlung von Acetoacetat in Beta-Hydroxybutyrat begünstigt und die Umkehrung dieser Reaktion hemmt. Infolgedessen wird während einer solchen Krise praktisch nur Beta-Hydroxybutyrat ausgeschieden, während Acetoacetat in geringeren Mengen vorliegt und im Urintest nicht nachweisbar ist. Der Urinstreifentest wird häufig erst im Verlauf positiv, was nicht ein Zeichen der Verschlechterung, sondern eine antizipierbare Folge der Besserung ist. Es ist wichtig zu wissen ist, dass im Urinstreifentest nur Acetoacetat nachgewiesen wird.
Kommentar
Bei einer schweren metabolischen Azidose mit ausgeprägter Hyperventilation als Kompensationsmechanismus droht jederzeit eine respiratorische Erschöpfung. Diese Patienten müssen unverzüglich auf eine Intensivstation verlegt werden. Wichtig zu wissen ist, dass die Gabe von Natriumbikarbonat bei akuten Azidosen schädlich sein kann. Durch die exogene Gabe wird die Produktion vom Kohlendioxid erhöht, was die Hyperventilation ver-stärken und zur respiratorischen Erschöpfung führen kann. (2) Ist eine künstliche Beatmung unumgänglich, muss die Hyperventilation auch nach der Intubation fortgeführt werden, damit die Azidose nicht schwerwiegender wird. Eine metabolische Azidose kann durch mehrere Ursachen gleichzeitig entstehen und für die richtige Diagnosestellung und Therapie braucht es ein systematisches Vorgehen.
Im Gegensatz zum deutschen Merkspruch «Kussmaul» ist im englischsprachigen Mnemonic «GOLD MARK» (5) Oxoprolin als Ursache für eine metabolische Azidose mit vergrösserter Anionenlücke aufgeführt. Die Verwendung des Mnemonic ermöglicht einen systematischen analytischen Ansatz zur Identifizierung der Ursachen der Additionsazidosen.
• Glycol (Ethylenglykol, Propylenglykol)
• Oxoprolin (Pyroglutaminsäure, das toxische Stoffwechselprodukt von übermässigem Paracetamol)
• L-Lactat (Standardlaktat, das bei Laktatazidose auftritt)
• D-Lactat (exogenes Lactat, das von Darmbakterien produziert wird)
• Methanol (dies umfasst allgemein Alkohole)
• Aspirin (Salicylsäure)
• Renal Failure (urämische Azidose)
• Ketone (diabetische, alkoholische und Hungerketose)
In der Fachliteratur werden neben Flucloxacillin weitere Arzneimittel als mögliche Ursachen einer Oxoprolinakkumluation genannt. Hierzu zählen Ciprofloxacin, Netilmicin und Vigabatrin. Der Nutzen von N-Acetylcystein bei akuter Paracetamol-Toxizität ist bekannt. Es wurde postuliert, dass N-Acetylcystein bei Fällen von erworbener 5-Oxoprolinämie eine positive Wirkung zeigt. Es erhöht die Glutathion- und Cystein-Spiegel bei Patienten mit erblichem Mangel an Glutathion-Synthetase. Theoretisch sollte die Auffüllung der Gluta-thion-Speicher die Rückkopplungsinhibition der γ-Glutamylcystein-Synthetase wiederher-stellen, was die Umwandlung von γ-Glutamylcystein in 5-Oxoproline verringert. Die Wiederherstellung der Cystein-Speicher sollte die Umwandlung von γ-Glutamylphosphat in γ-Glutamylcystein ermöglichen, was die Umwandlung von γ-Glutamylphosphat in 5-Oxoproline verhindert und den nutzlosen ATP-verbrauchenden Zyklus unterbricht. Die Literatur bezüglich N-Acetylcystein-Verabreichung bei 5-Oxoprolinämie ist begrenzt (6).
Es gibt nicht genügend Literatur über die Verwendung von Hämoadsorption zur Clearance von Flucloxacillin. Es gibt eine einzige Studie an Schweinen, die zeigt, dass die Hämoad-sorption mit CytoSorb mit einer vernachlässigbaren erhöhten Clearance für Flucloxacillin verbunden war (15% zusätzliche Clearance durch den Absorber) (7). Die Datenlage, ob eine Hämodiafiltration Einfluss auf die Heilung hat, ist begrenzt.
Abkürzungen
aBGA arterielle Blutgasanalyse
CT Computertomographie
EKG Elektrokardiogramm
i.v. intravenös
L2 2. Lumbalsegment
MRT Magnetresonanztomographie
p.o. per os
Klinik und Poliklinik für Innere Medizin
Universitätsspital Zürich
Rämistrasse 100
8091 Zürich
nikolay.todorov@usz.ch
Klinik und Poliklinik für Innere Medizin
Universitätsspital Zürich
Schweiz
Die Autoren haben keine Interessenkonflikte im Zusammenhang mit diesem Artikel deklariert.
• Eine metabolische Azidose kann durch mehrere Ursachen gleichzeitig entstehen. Für die richtige Diagnosestellung und Therapie braucht es ein systematisches Vorgehen.
• GOLD MARK ist eine nützliche Eselsbrücke bei einer Azidose mit vergrösserter Anionenlücke.
• Die Kombination aus Flucloxacillin und Paracetamol kann insbesondere in Anwesenheit von Risikofaktoren zur Oxoprolin-Akkumulation führen.
• Risikofaktoren für die Entwicklung einer metabolischen Azidose aufgrund von 5-Oxoprolin-Akkumulation, neben der Einnahme von Flucloxacillin, Ciprofloxacin, Netilmicin, Vigabatrin und Paracetamol, umfassen: fortgeschrittenes Alter, weibliches Geschlecht, Mangelernährung, Niereninsuffizienz, chronische Leberinsuffizienz, Alkoholmissbrauch und Sepsis.
• Für die Behandlung einer metabolischen Azidose aufgrund von 5-Oxoprolin-Akkumulation gibt es keine Richtlinien. Neben dem Absetzen des auslösenden Medikaments kann eine unterstützende Behandlung mit N-Acetylcystein erfolgen.
• Eine schwere metabolische Azidose kann rasch zu einer respiratorischen Erschöpfung führen, was antizipiert werden muss.
1. Liss DB, Paden MS, Schwarz ES, Mullins ME. What is the clinical significance of 5-oxoproline (pyroglutamic acid) in high anion gap metabolic acidosis following paracetamol (acet-aminophen) exposure? Clin Toxicol (Phila). 2013;51(9):817-27.
2. Wilson R. F., Spencer A. R., Tyburski J. G., Dolman H., Zimmerman L. H. Bicarbonate ther-apy in severely acidotic trauma patients increases mortality. Journal of Trauma and Acute Care Surgery. 2013;74(1):45–50.
3. Weiler S, Bellmann R, Kullak-Ublick GA. [5-0xoproline (pyroglutamic acid) acidosis and acetaminophen- a differential diagnosis in high anion gap metabolic acidosis]. Ther Umsch. 2015;72(11-12):737-41.
4. Lenz JE, Alt V, Dienemann T. Severe acidosis due to 5-oxoprolinase inhibition by flucloxacillin in a patient with shoulder prosthesis joint infection. J Bone Jt Infect. 2022;7(2):71-4.
5. Mehta AN, Emmett JB, Emmett M. GOLD MARK: an anion gap mnemonic for the 21st century. Lancet. 2008;372(9642):892.
6. Hundemer GL, Fenves AZ. Acquired 5-oxoproline acidemia successfully treated with N-acetylcysteine. Proc (Bayl Univ Med Cent). 2017;30(2):169-70.
7. Schneider AG, André P, Scheier J, Schmidt M, Ziervogel H, Buclin T, Kindgen-Milles D. Pharmacokinetics of anti-infective agents during CytoSorb hemoadsorption. Sci Rep. 2021;11(1):10493.w
PRAXIS
- Vol. 113
- Ausgabe 11-12
- Dezember 2024