- Arbeitsplatzassoziiertes Fieber oder wenn es doch das Zebra ist…
Einleitung
Febrile Körpertemperaturen kombiniert mit Grippesymptomatik (Kopf- und Gliederschmerzen, Malaise) sind oftmals angetroffene Beschwerden. Zumeist ist die Ursache in einer viralen oder bakteriellen Infektion zu suchen. Nebst der infektiösen Genese kommen aber auch zahlreiche weitere Krankheiten als Auslöser des Fiebers infrage [1].
Wie immer steht auch hier der Anamnese eine herausragende Bedeutung zu. Es soll u.a. nach der Häufigkeit und Dauer der Fieberschübe, den Begleitsymptomen (inklusive B-Symptomatik), der Umgebungsanamnese, Medikamenteneinnahme, Reisen mit entsprechendem Risikoverhalten und besonderen Freizeitbeschäftigungen gefragt werden.
Die Berufsanamnese soll dabei nicht vergessen werden, denn auch der Arbeitsplatz kann Fieberzustände auslösen. Sind zum Beispiel andere Mitarbeiter ebenfalls von ähnlichen Symptomen betroffen und/oder verschwinden die Beschwerden während des Wochenendes, respektive Urlaubs, lohnt es sich, einen detaillierten Tätigkeitsbericht zu verlangen. Eine Arbeitsplatzbegehung kann weitere Informationen betreffend Tätigkeit und Expositionen am Arbeitsplatz liefern.
Hauptaufnahmeweg von Noxen in der Arbeitswelt ist oft die Inhalation und so tritt häufig begleitend auch eine pulmonale Symptomatik (z.B. Husten, Dyspnoe) auf.
Bereits 1992 gab es Diskussionen bezüglich des Begriffs «Inhalationsfieber» [2], allerdings wurde bis heute kein Konsens bezüglich einheitlicher Nomenklatur gefunden. Gemäss Hendrick et al. werden unter dem Begriff «Inhalationsfieber» [3] eine Gruppe von grippeartigen Syndromen wie z.B. das Metalldampffieber, das Polymerrauchfieber und das organic dust toxic syndrom (ODTS) zusammengefasst. Die Hypersensitivitätspneumonitis (HP), traditionell auch exogen allergische Alveolitis (EAA) genannt [4], welche immunbedingt ebenfalls zu Fieber führt und oft ihren Trigger in der Arbeitswelt findet, wird in der Literatur nicht unter dem Begriff der «Inhalationsfieber» subsumiert.
Bei den Expositionen kann eine Unterscheidung und somit vereinfachende Einteilung in «organische Stäube » und «anorganische Substanzen» gemacht werden. Bei detaillierter Betrachtung der Einteilung gibt es aber Ausnahmen bezüglich der Zuordnung in die Bereiche «organisch» versus «anorganisch».
Durch die Inhalation von organischen Stäuben können die Krankheitsbilder der Hypersensitivitätspneumonitis (HP) und des organic dust toxic syndromes (ODTS) entstehen. Anorganische Substanzen, z.B. in Form von Dampf oder Rauch, verursachen u.a. das Metalldampffieber.
Berufsbedingte Lungenerkrankungen können toxisch oder immunvermittelt sein. Die toxische Wirkung ist abhängig von der Eigenschaft, der Dosis und der Einwirkungszeit der Substanz. Ab einer bestimmten Expositionshöhe kommt es immer zu einer Manifestation von Symptomen. Im Gegensatz dazu ist die immunvermittelte Reaktion eine individuelle Überempfindlichkeitsreaktion.
Je nach Berufsbild und somit Arbeitsort, respektive Inhalationsexposition lässt sich an verschiedene Krankheiten denken. In der Folge werden wir uns auf fieberhafte Zustände in Zusammenhang mit typischen Berufsbildern und deren potentielle Ursache konzentrieren.
Organische Stäube
Ein Landwirt stellt sich mit Fieber vor…
Bei der Arbeit im Landwirtschaftsbereich besteht in der Regel eine hohe Exposition gegenüber organischen Stäuben, dies z.B. in Form von Heu, Getreide, Silage etc. Durch Feuchtigkeitsbelastung kann Schimmel (Aspergillus spp [5], Saccharomycetes spp., termophile Aktinomyzeten) entstehen, dessen Bestandteile dann als Antigene fungieren. Nach Inhalation der genannten Antigene kann sich eine Hypersensitivitätspneumonitis (HP) entwickeln. Bei einem Landwirt wird die Erkrankung treffenderweise auch «Farmerlunge» genannt, wobei diese mit einer saisonalen und geographischen Häufung auftritt [6].
Zusammenfassend stammen die Antigene von folgenden Klassen: Mikroorganismen (Bakterien, Mykobakterien, Pilze), tierischen und pflanzlichen Proteinen (organisch), und auch von Chemikalien (Ausnahme: teilweise anorganisch). Die Autoren Raghu et al. [7]. und auch die Homepage www.hplung.com liefern eine umfassende Übersicht bezüglich HP-auslösenden Antigenen. So ist als bekannteres Beispiel der HP die Taubenzüchterlunge und die Befeuchterlunge zu nennen, exotischer ist dabei die Käsewäscherlunge oder die Federduvetlunge.
Patienten strukturiert zu befragen und an alle möglichen, teils seltenen Expositionen (z.B. Dampfbügeleisen, Blasinstrumente oder Bettfedern) zu denken kann schwierig sein. Hilfestellung liefert ein übersichtlicher Fragebogen, welcher von den Autoren Kreuter et al. [8] erstellt wurde und frei erhältlich ist. Um organisiert vorzugehen, kann man sich vom Patienten auch den detaillierten Tagesablauf schildern lassen.
Die Pathogenese der HP ist nicht abschliessend geklärt; man geht davon aus, dass es nach Inhalation der alveolengängigen Antigenen zu einer Infiltration durch mononukleäre Zellen und Neutrophile im Bereich der Bronchiolen, Alveolen und Interstitium mit folglicher Granulombildung kommt [9].
Da für die Krankheitsauslösung eine Sensibilisierungsphase benötigt wird, gibt es kein Auftreten nach einem Erstkontakt. Ob die Krankheit schliesslich ausbricht, ist abhängig von der Dauer der Exposition, der Staubkonzentration und der genetischen Prädisposition des Patienten [4].
Die HP ist eine seltene Erkrankung und die Inzidenz ist abhängig z.B. von geographischen und klimatischen Bedingungen [10].
Unterschieden wird eine akute, subakute und chronische Form der HP [11]. Die akute Form äussert sich mit Fieber, Schüttelfrost, Gliederschmerzen und pulmonaler Symptomatik (Husten und Dyspnoe) vier bis zwölf Stunden nach massiver Antigenexposition (Bsp. Reinigung eines Taubenschlages) und klingt nach 24 bis 48 Stunden spontan wieder ab. Oft heilt eine akute Form ohne Spätschäden aus. Hingegen braucht es für die chronische Form der HP Kontakt mit kleineren Antigenmengen über einen längeren Zeitraum. Die Symptome sind dann unspezifischer; es zeigen sich trockener Husten, Abgeschlagenheit, Gewichtsverlust und sind assoziiert mit einer schlechteren Prognose.
In der klinischen Untersuchung findet man beim Vorliegen einer bereits fibrotischen (respektive chronischen) Manifestation zumeist ein Knisterrasseln (Sklerosiphonie, velcro rales). Lungenfunktionell zeigt sich eine Restriktion. Eine Diffusionsstörung mit Abfall der Sauerstoffsättigung unter Belastung sind typisch bei fortgeschrittener Erkrankung.
Erhöhte Entzündungsparameter (Leukozyten, CRP) und teils positive antigen-spezifische Immunglobuline G Werte (Präzipitine) sind in der laborchemischen Untersuchung zu detektieren. Durch positive, spezifische IgG kann die Diagnose nicht bestätigt werden, ebenso wenig können negative IgG die Krankheit ausschliessen [10].
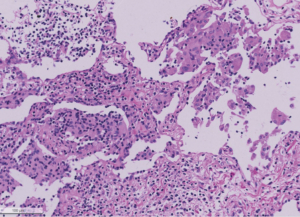
Die bronchoalveoläre Lavage (BAL) zeigt häufig eine relevante Lymphozytose und histopathologisch wird eine bronchiolozentrische Entzündung mit kleinen, histiozytären Granulomen nachgewiesen [7].
![]()
![]()
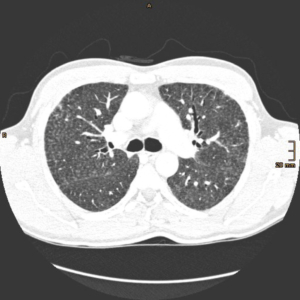
Richtungsweisend ist sicherlich die radiologische Bildgebung (HRCT) mit den typischen Befunden der Akutphase wie zentrilobuläre Noduli, Milchglasopazitäten, Airtrapping in Exspiration und in der chronischen Phase zusätzlich Retikulationen und Traktionsbronchiektasen [7].
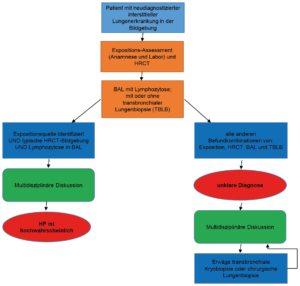
Da die Diagnosestellung knifflig sein kann, liefern die Autoren Raghu et al. [7] ein Flussdiagramm, welches die Kriterien der passenden Anamnese, HRCT- Bildgebung, Labor, BAL und Histopathologie inkludiert.
![]()
Die Expositionskarenz, d.h. Urlaub an einem anderen Ort oder die Expositionstestung, welche direkt am Arbeitsplatz oder auch arbeitsplatzsimulierend vorgenommen werden kann, komplettieren schliesslich die Verdachtsdiagnose. Besonders aussagekräftig ist der Karenztest, wenn die abgeschwächten oder bereits ganz verschwundenen Symptome bei erneuter Exposition, z. B. nach einem Urlaub, wieder auftreten (Karenz−Reexpositionstest).
Nebst der Expositionskarenz, welche entscheidend ist, sind je nach Krankheitsstadien unterschiedliche Medikationsansätze möglich (Glukokortikoide, z.B. Prednison 0.5-1mg/kgKG [12], Immunsuppressiva, Antifibrotika). In einem terminalen Stadium bleibt -bei geeigneten Betroffenen- schliesslich nur die Lungentransplantation.
Betroffene Landwirte erhalten bei der Beratungsstelle für Unfallverhütung in der Landwirtschaft (www.bul.ch) weitere, praxisorientierte Informationen.
Es stellt sich noch ein Landwirt mit Fieber vor…
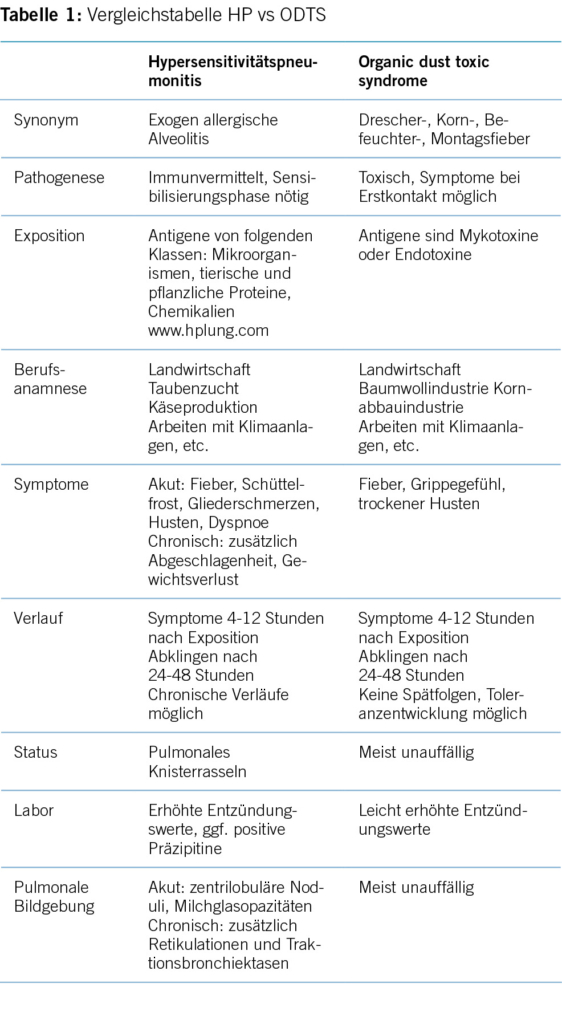
Als Differentialdiagnose zur HP ist das organic dust toxic syndrome (ODTS) [13] zu nennen. Hierbei handelt es sich um eine toxische Alveolitis, welche vier bis zwölf Stunden nach Inhalation von organischem Staub auftritt. Antigene sind dabei Mykotoxine oder Endotoxine, herkommend von u.a. schimmligem Getreide, Heu, Zellwandbestandteile von gramnegativen Bakterien und Pilzsporen. Folgedessen sind Arbeitsumgebungen in der Landwirtschaft (speziell Geflügel- und Schweinezucht), aber auch beispielsweise Baumwoll- oder Kornabbauindustrie [3] und Arbeiten mit/bei (schimmligen) Klimaanlagen/Befeuchtungssystemen betroffen. Klinische Erkrankungen sind u.a. das Drescher-, Korn- und Befeuchterfieber und das Siloentladesyndrom, welche alle deutlich häufiger in den Sommermonaten auftreten [3].
Bei regelmässigem Kontakt mit der auslösenden Substanz kann es einerseits zu einer Toleranzentwicklung beim ODTS kommen, andererseits klingen die Symptome nach 24 bis 48 Stunden spontan wieder ab und Spätfolgen werden nicht gesehen. Aufgrund der genannten Toleranzentwicklung kommt es typischerweise am Montag nach einem arbeitsfreien Wochenende/Urlaub wieder zu Beschwerden (sogenanntes «Montagsfieber»). Oft tritt ein ODTS auf, nachdem eine grosse Antigenmenge freigesetzt wurde, dies in Folge z.B. einer Siloreinigung, einer Be-/Entladung grosser Heumengen oder einer Kompostleerung. Die Krankheit tritt mit einer Inzidenz von 20-190/10000 häufiger als die HP auf. Wie es der Name sagt, handelt es sich um eine toxisch ausgelöste Erkrankung, d.h. liegt die Staub Exposition über einem gewissen Schwellenwert, erleiden ganze Menschengruppen, sogenannte Cluster, ähnliche Symptome [14]. Eine Sensibilisierung ist nicht nötig und Beschwerden können bereits bei der ersten Exposition auftreten. Interessanterweise sind sowohl bei der HP als auch beim ODTS mehr Nichtraucher als Raucher betroffen [12, 15].
Die Patienten klagen über einen trockenen Husten und ein akutes, febriles Krankheitsgefühl (inklusive Myalgien, Kopfschmerzen). In der laborchemischen Untersuchung zeigt sich eine milde Leukozytose. Im Gegensatz zur HP sind der Auskultationsbefund und die radiologische Bildgebung zumeist unauffällig und in der bronchoalveolären Lavage (BAL) finden sich vorherrschend Neutrophile.
Aufgrund der raschen Selbstlimitierung stellen sich wenige Patienten mit ODTS ärztlich vor. Die Therapie ist symptomatisch, Steroide werden nicht empfohlen. Generell soll
auf den Nutzen einer adäquaten, persönlichen Schutzausrüstung hingewiesen werden.
Anorganische Substanzen
Hat ein Schweisser am Montag Fieber…
Der Sektor der Maschinen-, Elektro- und Metallindustrie ist mit 320’000 Beschäftigten der grösste industrielle Arbeitgeber und eine der grössten Exportbranchen der Schweiz [16]. Im Gegensatz zu früheren Zeiten ist das Metalldampffieber, für welches zahlreiche Synonyme (Gelbgiesserfieber, Zinkfieber, Montagsfieber) existieren, heutzutage deutlich weniger bekannt, respektive beachtet.
Bei diversen Metallarbeiten wie z.B. dem Schweissen wird unter Anwendung von grosser Hitze und/oder Druck eine unlösbare Verbindung von Bauteilen (u.a. Stahl, Aluminium) eingegangen. Zusatzwerkstoffe in Form von Stäben und Drähten können zugeführt und abgeschmolzen werden und erstarren schliesslich in der Fuge. Für einen besseren Korrosionsschutz wird Stahl teils verzinkt. Zink verdampft ab 907°C und es entsteht in Kombination mit Sauerstoff Zinkoxid (ZnO).
Durch die hohe Hitzeanwendung beim Schweissen werden bei weitem nicht nur Zinkoxid, sondern je nach involvierten Materialien auch andere aerosolisierte Partikel (u.a. Mangan, Chrom, Eisen, Nickel) mit einer Grösse von ca 0.1 μm Durchmesser generiert.
Vier bis zehn Stunden nach direkter Inhalationsexposition mit metallhaltigem Rauch können grippeartige Beschwerden wie Fieber, Schüttelfrost, Kopfschmerzen und Myalgien und respiratorischen Beschwerden (Husten, Dyspnoe) beklagt werden. Manchmal wird auch über einen süsslich-metallischen Geschmack im Mund berichtet. Über die Arbeitswoche wird eine Toleranzentwicklung [17] beobachtet, hingegen sind die Beschwerden am Montagmorgen nach arbeitsfreien Wochenenden besonders intensiv. Ein zyklisch auftretendes Fieber sollte somit Anlass zur genaueren Nachforschung geben.
Die Pathogenese ist nicht schlüssig geklärt; man geht von einer immunologisch-entzündlichen sowie direkt toxischen Wirkung im Bereich der Atemwege aus [18].
Sowohl die klinische als auch radiologische Untersuchung fallen meistens unauffällig aus. Nur selten und bei schwerwiegenderen Fällen werden bilaterale Infiltrate beschrieben. Laboranalytisch können erhöhte Entzündungsparameter gemessen werden. Im Allgemeinen sind die Beschwerden zwölf bis 48 Stunden nach Exposition selbstlimitierend; eine allfällig benötigte Therapie ist symptomatisch.
Durch Absaugvorrichtungen und dem Tragen von Atemschutzmasken wird das Metalldampffieber heute deutlich seltener gesehen, nichtsdestotrotz gibt es auch viele do-it-yourself Hobbyschweisser, welche nicht unter betrieblichen Schutzmassnahmen stehen und sich dann mit den genannten akuten Beschwerden notfallmässig vorstellen.
Ergänzend sei auf das Polymerrauchfieber hingewiesen, welches sowohl in der Pathogenese als auch den Symptomen, der Therapie und dem Verlauf mit dem Metalldampffieber vergleichbar ist. Erstmals tritt es in der Literatur 1951, kurz nach dem Entdecken von Polytetrafluorethylen (PTFE) bzw. Teflon® [19] auf. PTFE ist ein thermoplastischer Kunststoff, welcher in der Industrie vielfältig als Antihaft- respektive Schmiermittel eingesetzt wird. Die bekannteste Anwendung ist sicherlich die Antihaftbeschichtung in Pfannen und Töpfen. Es wurde beobachtet, dass beim Überhitzen von Teflon® über 300°C ein Dampf/Rauch respektive giftige Fluorverbindungen entstehen. Eine Unterscheidung zwischen Metalldampffieber und Polymerrauchfieber ist nur anhand der Anamnese mit entsprechender Exposition möglich.
Abkürzungen
BAL: Bronchoalveoläre Lavage
DLCO: Diffusionskapazität von Kohlenmonoxid
EAA: Exogen allergische Alveolitis
HP: Hypersensitivitätspneumonitis
HRCT: high resolution Computertomographie
IgG: Immunglobuline G
ILD: interstitielle Lungenerkrankung (interstitial lung disease)
ODTS: organic dust toxic syndrome
TBLB: transbronchiale Lungenbiopsie
Interessenskonflikte
Es bestehen keine Interessenskonflikte.
Dr. med. Celine Schumacher, celine.schumacher@usz.ch
Universität Zürich
Arbeits- und Umweltmedizin
Hirschengraben 84
8001 Zürich
Universität Zürich
Arbeits- und Umweltmedizin
Hirschengraben 84
8001 Zürich
Key messages
• Die Hypersensitivitätspneumonitis (HP) ist eine immunvermittelte Reaktion auf Antigene und tritt nach einer Sensibilisierungsphase auf. Sie äussert sich durch Fieber, Husten und Grippegefühl, sowie einem pulmonalen Knisterrasseln. Bei fortbestehender Exposition kann diese Krankheit verheerende Folgen haben.
• Als Differentialdiagnose zur HP muss an das organic dust toxic syndrome (ODTS) gedacht werden. Diese selbstlimitierende Krankheit tritt häufiger auf und nicht selten präsentiert sich eine Menschengruppe (sogenannte Cluster) mit den gleichen Symptomen.
• Das Metalldampffieber ist eine gutartige, in der Regel selbstlimitierende Erkrankung, welche typischerweise durch Inhalation von Zinkoxidrauch infolge Schweissarbeiten auftritt.
• Treten Fiebersymptome zyklisch auf und haben einen Zusammenhang mit Arbeitsplatz, Haushalt oder Hobby, lohnt es sich, eine diesbezüglich detaillierte Anamnese zu erheben. Strukturierte Fragebögen können hilfreich sein. Bei komplexen Fällen kann stets die Expertise der Arbeitsmedizin zu Rate gezogen werden.
Literatur
1. Battegay, E., Differenzialdiagnose Innerer Krankheiten. Vol. 21. 2017: Georg Thieme Verlag KG Stuttgart.
2. Rask-Andersen, A. and D.S. Pratt, Inhalation fever: a proposed unifying term for febrile reactions to inhalation of noxious substances. Br J Ind Med, 1992. 49(1): p. 40.
3. Hendrick, D., et al., Occupational Disorders of the Lung: Recognition, Management, and Prevention. 2002: Saunders.
4. Quirce, S., et al., Occupational hypersensitivity pneumonitis: an EAACI position paper. Allergy, 2016. 71(6): p. 765-79.
5. Al-Alawi, A., et al., Aspergillus-related lung disease. Can Respir J, 2005. 12(7): p. 377-87.
6. Terho, E.O., et al., Incidence of clinically confirmed farmer‘s lung in Finland and its relation to meteorological factors. Eur J Respir Dis Suppl, 1987. 152: p. 47-56.
7. Raghu, G., et al., Diagnosis of Hypersensitivity Pneumonitis in Adults. An Official ATS/JRS/ALAT Clinical Practice Guideline. Am J Respir Crit Care Med, 2020. 202(3): p. e36-e69.
8. Kreuter, M., et al., [DGP Interstitial Lung Disease Patient Questionnaire]. Pneumologie, 2018. 72(6): p. 446-457.
9. Ismail, T., C. McSharry, and G. Boyd, Extrinsic allergic alveolitis. Respirology, 2006. 11(3): p. 262-8.
10. Barnes, H., et al., Hypersensitivity pneumonitis: Current concepts in pathogenesis, diagnosis, and treatment. Allergy, 2022. 77(2): p. 442-453.
11. Richerson, H.B., et al., Guidelines for the clinical evaluation of hypersensitivity pneumonitis. Report of the Subcommittee on Hypersensitivity Pneumonitis. J Allergy Clin Immunol, 1989. 84(5 Pt 2): p. 839-44.
12. Spagnolo, P., et al., Hypersensitivity Pneumonitis: A Comprehensive Review. J Investig Allergol Clin Immunol, 2015. 25(4): p. 237-50; quiz follow 250.
13. Widmeier, S. and P. Hotz, [Organic dust toxic syndrome (ODTS)]. Praxis (Bern 1994), 2007. 96(22): p. 887-92; quiz 892.
14. Brinton, W.T., et al., An outbreak of organic dust toxic syndrome in a college fraternity. JAMA, 1987. 258(9): p. 1210-2.
15. Warren, C.P., Extrinsic allergic alveolitis: a disease commoner in non-smokers. Thorax, 1977. 32(5): p. 567-9.
16. EDA. Maschinen-, Elektro- und Metallindustrie. 2017; Available from: https://www.eda.admin.ch/aboutswitzerland/de/home/wirtschaft/taetigkeitsgebiete/maschinen—elektro–und-metallindustrie.html.
17. El-Zein, M., et al., Prevalence and association of welding related systemic and respiratory symptoms in welders. Occup Environ Med, 2003. 60(9): p. 655-61.
18. Greenberg, M.I. and D. Vearrier, Metal fume fever and polymer fume fever. Clin Toxicol (Phila), 2015. 53(4): p. 195-203.
19. Harris, D.K., Polymer-fume fever. Lancet, 1951. 2(6692): p. 1008-11.
Therapeutische Umschau
- Vol. 81
- Ausgabe 1
- Februar 2024