- Stellenwert der Knochenumbau-parameter im Management der Osteoporose
Einleitung
Die Messung der Knochenumbauparameter im klinischen Alltag ist eine etablierte Säule des modernen Osteoporose-managements und heute sowohl in der Diagnostik als auch im Krankheitsverlauf nicht mehr wegzudenken. Dieser Artikel soll einen Überblick über die wichtigsten Parameter und deren Relevanz und Bedeutung im klinischen Alltag geben.
Die Osteoporose ist eine chronische Erkrankung des Skelettapparates, welche durch eine verringerte Knochendichte und eine Störung der Knochenarchitektur gekennzeichnet ist. Aufgrund dieser Veränderungen kommt es zu einer erhöhten Frakturgefährdung, was insbesondere bei älteren Personen mit erhöhter Morbidität und Mortalität assoziiert ist.
Der Knochen wird zeitlebens umgebaut, damit er sich an die Belastung anpassen und seine mechanische Kompetenz erhalten kann (1, 2). Der Knochenumbau erfolgt durch zwei gegensätzliche Prozesse: den Knochenabbau und den Knochenanbau. Der Knochenumbau erfolgt geordnet mit Koppelung («coupling») zwischen Knochenabbau und Knochenanbau (1, 2). Diese beschriebene Knochenstoffwechselaktivität kann durch die Messung der Knochenumbauparameter («bone turnover markers») erfasst werden und liefert wichtige Informationen sowohl in der initialen Diagnostik von metabolischen Knochenerkrankungen als auch zur Überprüfung der Wirksamkeit von spezifischen Therapien.
Funktion der Knochenumbauparameter
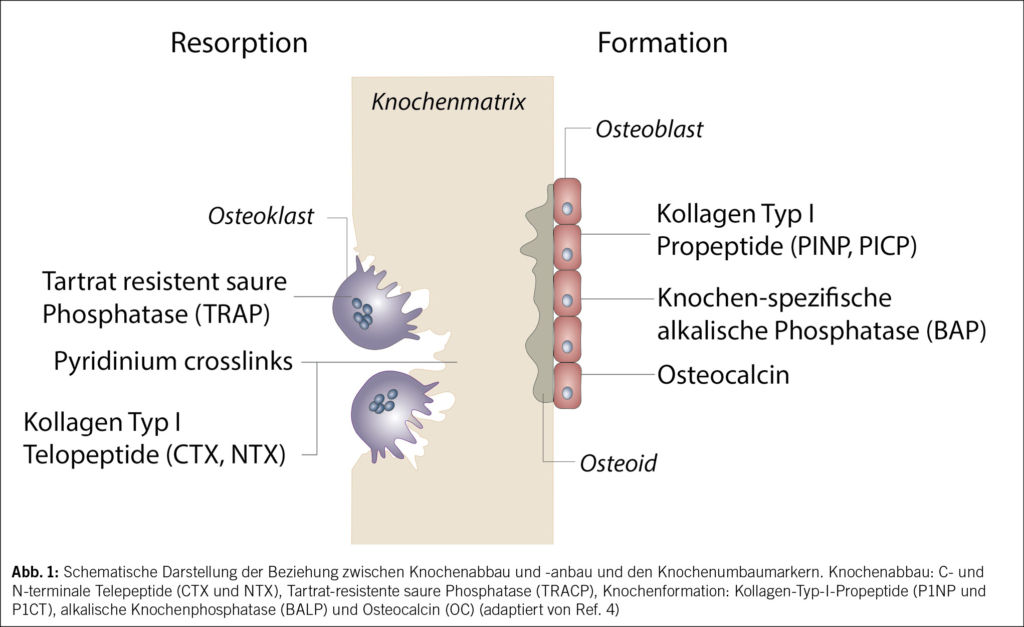
Die Knochenumbaumarker widerspiegeln die Aktivität der Osteoblasten und Osteoklasten. Die Osteoidbildung durch die Osteoblasten wird durch Bildung der knochenspezifischen alkalischen Phosphatase, Osteocalcin und Prokollagen N-Propeptide reflektiert (Abb. 1 und Tab. 1). Beim Knochenabbau werden Fragmente des Kollagens (N- und C-terminale Telopeptide, Pyridinoline) und Tartrat-resistente saure Phosphatase freigesetzt (2–4). Diese Marker ermöglichen eine dynamische Beurteilung des Knochenumbaus.
Prokollagen Typ 1 N-terminales Propeptid (P1NP)
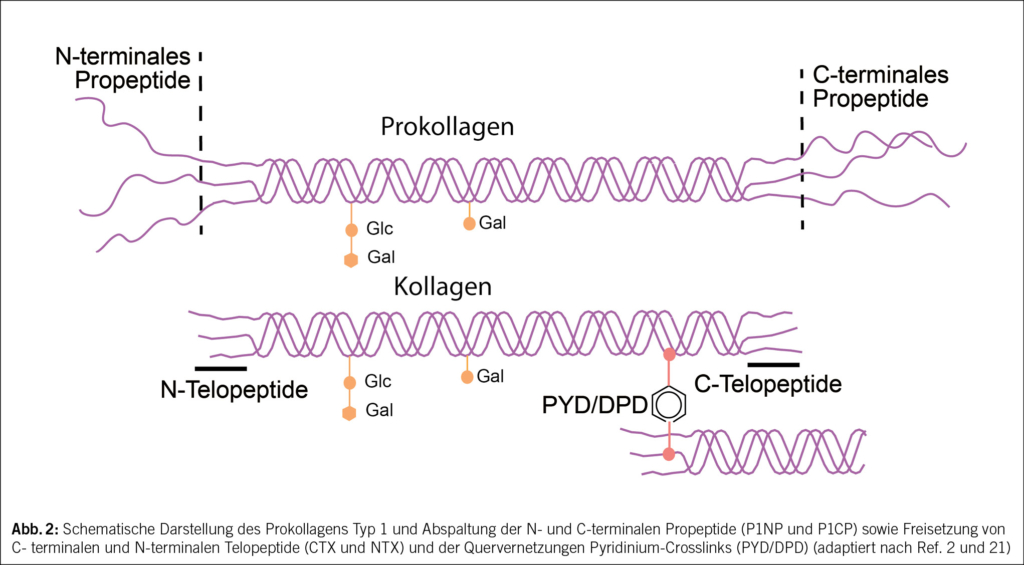
Das Kollagen wird von den Osteoblasten als Prokollagen sezerniert. Durch Abspaltung der C-terminalen und N-terminalen Endigungen entstehen die C-terminalen (P1CP) und N-terminalen Propeptide (P1NP) und das Kollagenmolekül, Hauptbestandteil (90 % des Proteinanteils) der Knochenmatrix (Abb. 2) (2, 5). Untersuchungen der letzten Jahre haben gezeigt, dass vor allem das P1NP zur Beurteilung der Knochenformation am geeignetsten ist, und wird deshalb als Referenzmarker empfohlen (6–8).
P1NP wird in der Leber abgebaut. Es kann aber auch zur Freisetzung einer monomeren Form von P1NP kommen, das über die Niere ausgeschieden wird und damit bei der Niereninsuffizienz retiniert wird (2, 9). Es gibt also zwei Formen von P1NP im Serum: das «intakte» oder trimere Molekül und das Monomer (10, 11). Derzeit verfügbare Assays messen entweder nur die trimere Form (intaktes P1NP) oder beide Formen (Gesamt-P1NP). Der Gesamt-P1NP-Assay (automatisiert) ist auf Elecsys (Roche Diagnostics) erhältlich. Der automatisierte Assay für intaktes P1NP ist auf IDS-iSYS, Immunodiagnostic Systems, erhältlich. Ausser bei Niereninsuffizienz korrelieren diese beiden Assays gut (12).
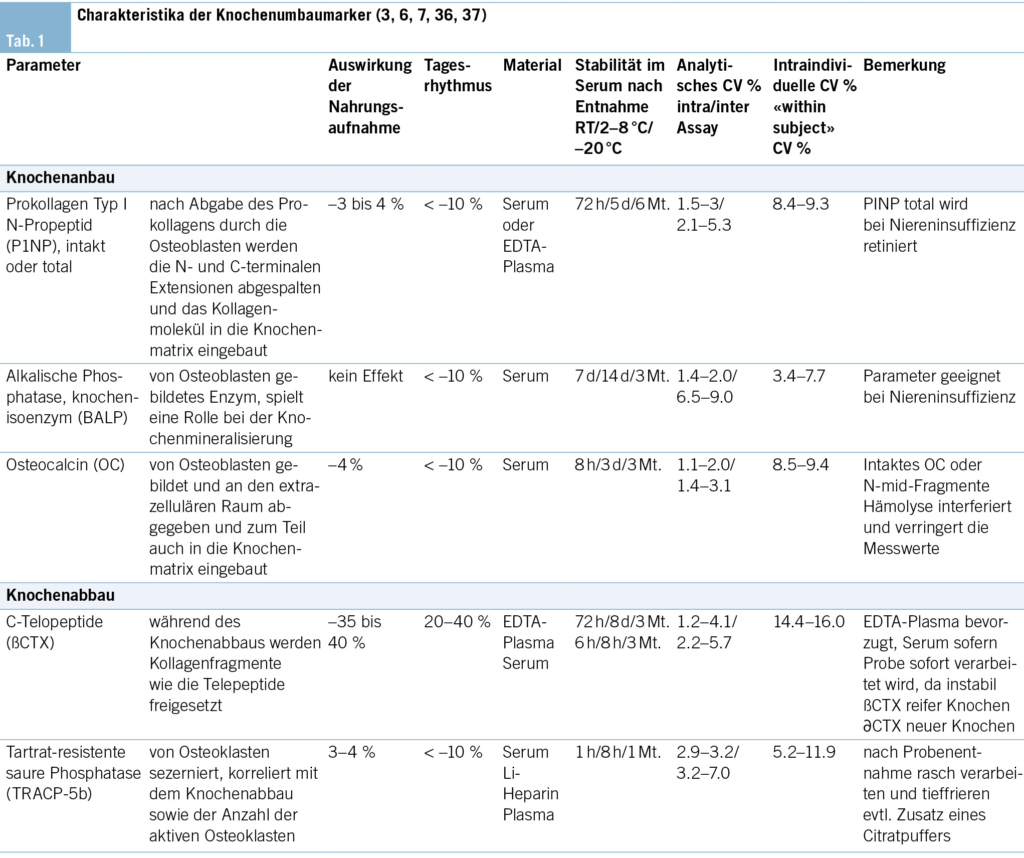
Das PINP weist nur einen schwachen Tagesrhythmus auf (< 10 %) und wird nur wenig durch Nahrungsaufnahme beeinflusst (3–4 %) (2).
P1NP ist besonders sensitiv gegenüber der Aktivität der Osteoblasten, die für den Knochenaufbau verantwortlich sind. Ein hoher P1NP-Spiegel zeigt den vermehrten Aufbau neuer Knochensubstanz an, was z. B. beim Heilungsprozess nach Frakturen, in den Wachstumsphasen oder bei der Wirkung anaboler Osteoporosetherapien (wie z. B. Teriparatid) typisch ist (13, 14).
Osteocalcin (OC)
Osteocalcin ist ein Nichtkollagenprotein, das von Osteoblasten produziert wird. Mittels Bindung an Kalzium und die Knochenmatrix hat es eine wichtige Rolle in der Knochenneubildung inne und zeigt die Aktivität der Osteoblasten an. OC enthält Glutamatreste, die unter dem Einfluss von Vitamin K carboxyliert und durch Warfarin gehemmt werden (2, 5). Das in Osteoblasten neu gebildete OC wird in den Extrazellulärraum abgegeben und zum Teil aber auch in die Knochenmatrix eingebaut. Osteocalcin wird in vivo und in vitro rasch abgebaut, und sowohl das intakte Molekül als auch Fragmente finden sich in der Zirkulation (5). Es wird über die Niere ausgeschieden und kann bei Niereninsuffizienz akkumulieren. OC zeigt einen geringen Tagesrhythmus (< 10 %), es wird nicht durch Nahrungsaufnahme beeinflusst (5). Nach der Blutentnahme ist das Osteocalcin instabil, und die Probe muss deshalb rasch verarbeitet und analysiert werden. Damit ist dieser Parameter zur Anwendung im klinischen Alltag ungeeignet. In hämolysierten Serumproben nimmt die Immunoreaktivität bis zu 90 % ab (2).
Obwohl nur ein kleiner Anteil des neu synthetisierten OC in den Extrazellulärraum gelangt, ist es ein guter Paramater zur Beurteilung der Knochenformation. Die aus dem Knochenabbau freigesetzten Fragmente finden sich in nur sehr geringer Konzentration im Blut.
Es gibt Hinweise, dass die «untercarboxylierte» Form des OC während des Knochenabbaus freigesetzt wird und den Energie- und Glukosestoffwechsel beeinflusst (2, 15).
Assays für OC basieren hauptsächlich auf Gesamt-OC oder N-MID-OC und sind manuelle ELISA oder Immunoassays auf Autoanalyzern (2).
Knochenspezifische alkalische Phosphatase (BALP)
BALP wird von den Osteoblasten sezerniert und spielt eine Rolle bei der Knochenmineralisierung und trägt bis zur Hälfte der Gesamtaktivität der alkalischen Phosphatase im Serum von Erwachsenen bei, aber einen grösseren Anteil während des Wachstums bei Kindern. Da BALP von der Leber eliminiert wird und nicht über die Nieren ausgeschieden wird, wird seine Konzentration nicht direkt von der Nierenfunktion beeinflusst (2, 5). Damit ist die BALP auch ein wichtiger Parameter bei der Beurteilung des Knochenstoffwechsels bei Niereninsuffizienz.
Es gibt mehrere Methoden zur Messung der BALP-Masse und -Aktivität, wie z. B. Hitzeinaktivierung, Elektrophorese, Weizenkeim-Lektin-Fällung, HPLC und Immunoassays (114–118). Die Immunoassays sind am geeignetsten für den klinischen Einsatz, da sie monoklonale Antikörper verwenden, die spezifisch für die BALP sind. Die Knochen-isoform ist seit Kurzem auch auf einer automatisierten Plattform verfügbar (IDS-iSYS, Immunodiagnostic Systems) (16). Die alkalische Phosphatase der Leber zeigt eine Kreuzreaktivität von etwa 10–20 % in der Bestimmung mit der BALP.
Die Serumkonzentrationen der BALP weisen keinen zirkadianen Rhythmus auf und werden nicht durch Nahrungsaufnahme beeinflusst und können damit zu jeder Tageszeit abgenommen werden (2, 17).
C-terminales Telopeptid (ßCTX)
Im Kollagenmolekül gibt es einen N-Telopeptid- (NTX) und C-Telopeptid-Bereich (CTX) (Abb. 2) Beim Kollagenabbau werden NTX und CTX freigesetzt und können im Serum oder Urin gemessen werden. Auch bei diesen Abbaumarkern hat sich gezeigt, dass die Bestimmung des CTX am geeignetsten ist, die Knochenabbauaktivität zu beurteilen, weswegen CTX als Referenzmarker empfohlen wird (6).
Beim CTX findet nach einigen Monaten eine Beta-Isomerisierung statt. Diese Isomerisierung findet sich nicht bei NTX. Die Alpha- und Beta-Formen von CTX können beide im Urin mittels ELISA gemessen werden (18). Die Alpha-Form spiegelt die Neusynthese von Kollagen wider, wie sie bei hohem Knochenumsatz wie der Paget-Krankheit, malignen Knochenerkrankungen oder physiologischerweise bei Kindern vorkommt. Die Beta-Form spiegelt reiferes Kollagen wider und ist bei Erkrankungen wie Osteoporose oder bei gesunden Erwachsenen häufiger anzutreffen (19).
CTX wird in der Regel (in der Beta-Form: ßCTX) im Plasma (oder Serum) gemessen, da es im Urin eine sehr grosse Variabilität von Tag zu Tag aufweist. NTX wird in der Regel im Urin bestimmt. Die Bestimmung von NTX im Serum zeigt nur geringe Veränderungen unter einer antiresorptiven Therapie bei Osteoporose und hat sich daher nicht durchgesetzt.
CTX im Serum kann mit ELISA und seit Längerem mit Immunoassays auf zwei automatisierten Plattformen (Roche Diagnostics und IDS-iSYS, Immunodiagnostic Systems) gemessen werden. Beide Systeme benutzen den gleichen monoklonalen Antikörper. Es besteht aber ein Bedarf einer Standardisierung und Harmonisierung dieser beiden Assays, da bei Vergleichsstudien unterschiedliche Resultate gefunden wurden (2, 20). Eine Anpassung der beiden Assays hat vor Kurzem stattgefunden.
CTX kann entweder im Serum oder Plasma analysiert werden. Im Serum ist das CTX nur ca. 8 Stunden stabil, im EDTA über mehrere Tage. CTX unterliegt tageszeitlichen Schwankungen: die Werte sind morgens am höchsten und nehmen im Tagesverlauf ab. Aus diesem Grund wird empfohlen, die Blutproben immer zur gleichen Tageszeit morgens zu entnehmen.
Tartrat-resistente saure Phosphatase (TRACP)
Die Tartrat-resistente saure Phosphatase (TRACP) wird von verschiedenen Zellen der Monozyten-/Makrophagenlinie wie Osteoklasten, aktivierte Makrophagen oder dendritische Zellen exprimiert (21–23). Im Serum finden sich die Isoformen TRACP-5a und -5b. Diese unterscheiden sich durch eine posttranslationale Modifikation. Erhöhte TRACP-5a-Werte finden sich bei entzündlichen rheumatologischen Erkrankungen wie die Polyarthritis (22, 23). Die TRACP-5b wird hauptsächlich von Osteoklasten sezerniert, korreliert mit dem Knochenabbau sowie der Anzahl der aktiven Osteoklasten und wird im Allgemeinen als zytochemischer Marker verwendet, um Osteoklasten von anderen Knochenzellen zu unterscheiden (21, 22). Nach der Freisetzung in den Extrazellulärraum wird die TRACP-5b inaktiviert und zerfällt in Fragmente, welche von der Leber abgebaut werden. Damit ist die TRACP-5b zur Beurteilung der Osteoklastenaktivität auch bei Niereninsuffizienz geeignet.
Im Serum kann TRACP-5b entweder mit spektrophotometrischen Verfahren oder mit Immunoassays gemessen werden (22–25). Eine Adaptation eines Immunoassays an eine automatisierte Plattform wurde kürzlich vorgenommen (IDS-iSYS, Immunodiagnostic Systems).
Die Serumkonzentration von TRACP-5b weist einen nur sehr geringen Tagesrhythmus (10–12 %) auf und wird nicht durch die Nahrungsaufnahme beeinflusst (23, 26).
Nach der Blutentnahme wird die TRACP rasch abgebaut und muss deshalb innert einer Stunde zentrifugiert und eingefroren werden. Die Zugabe eines Citratpuffers ins Blutentnahmegefäss kann die Stabilität verlängern.
Insgesamt ist TRACP-5b im Serum ein Marker für die Anzahl Osteoklasten und die Knochenresorption. Sie hat den Vorteil, dass sie die Osteoklasten, d. h. die eigentliche zelluläre Aktivität, widerspiegelt und nicht nur den Kollagenabbau, der dieser Aktivität untergeordnet ist.
Pyridinium-Crosslinks
Die 3-Hydroxypyridinium-Quervernetzungen von Kollagen, Pyridinolin (PYD) und Deoxypyridinolin (DPD) werden während der extrazellulären Reifung von Kollagenen gebildet. Sie überbrücken als Querverbindungen mehrere Kollagenpeptide und stabilisieren das Kollagenmolekül (21). Sie sind nur in reifen, aber nicht in unreifen oder neu synthetisierten Kollagenen vom Typ I, II und III zu finden. Während PYD in Knorpel, Knochen, Bändern und Gefässen vorkommt, ist DPD fast ausschliesslich in Knochen und Dentin zu finden. Da Knochen einen viel höheren Umsatz haben als Knorpel, Bänder, Gefässe oder Sehnen, stammen die gemessenen Mengen an PYD und DPD im Serum oder Urin hauptsächlich aus dem Knochenumbau. Beim Kollagenabbau werden die Pyridinolin-Crosslinks freigesetzt und über die Nieren ausgeschieden.
Die Methoden für die Messung der Pyridinolin-Crosslink-Konzentration im Urin sind HPLC-Analysen mit oder ohne Hydrolyse des Urins und Immunoassays (27). Obwohl die HPLC-Analyse als Referenzmethode gilt, ist sie umständlich und arbeitsintensiv. Gleichzeitig weisen die im Urin gemessenen Knochenumbaumarker eine deutlich höhere biologische Variabilität auf als die im Serum gemessenen Marker (siehe unten), sodass heute die letzteren bevorzugt werden.
Praktische Aspekte
Beim Einsatz und dann vor allem auch bei der Interpretation der Resultate der biochemischen Marker gilt es, die verschiedenen Quellen der Variabilität dieser Marker zu berücksichtigen. Einerseits werden die Resultate durch die analytische Präzision, die bei den verschiedenen zur Verfügung stehenden Assays sehr unterschiedlich ist, beeinflusst. Andererseits wird das Resultat durch präanalytische Bedingungen wie Tagesschwankungen, Tag-zu-Tag-Schwankungen, Nahrungsaufnahme und dann auch die Stabilität des Markers nach der Blutentnahme mitbestimmt.
Die analytische Variabilität konnte durch Applikation dieser Messungen auf Autoanalyzer deutlich verringert und damit auch standardisiert werden (Tab. 1).
Die biochemischen Marker des Knochenstoffwechsels, v. a. die Knochenabbaumarker ßCTX und PYD, zeigen eine mehr oder weniger ausgeprägte zirkadiane Rhythmik mit den höchsten Werten in den frühen Morgenstunden und den tiefsten Werten während des Nachmittags und der Nacht. Der Einfluss der Nahrungsaufnahme ist ebenfalls variabel. Diese kann für ßCTX 20–40 % betragen. Die Knochenanbaumarker (BALP, PINP) weisen in der Regel einen geringeren Tagesrhythmus auf (< 10 %) und sind weniger durch Nahrungsaufnahme beeinflusst. Dies bedeutet, dass die Probenentnahme in der Regel am Morgen nüchtern zwischen 7.30 h und 10 h erfolgen sollte. Die Probe für die Knochenanbaumarker BALP und P1NP können auch im Laufe des Tages und nach Nahrungsaufnahme entnommen werden. Die Probenstabilität nach der Entnahme sollte beachtet werden (Serum versus EDTA-Plasma) (Tab. 1).
Die biochemischen Marker zeigen eine intraindividuelle Tag-zu-Tag-Variabilität, in der Regel beträgt diese Variabilität 5–10 % für die Knochenanbaumarker und 10– 15 % für die Knochenabbaumarker (Tab. 1).
Bei der Interpretation der Messresultate müssen auch die nicht kontrollierbaren Aspekte, welche zur Variabilität beitragen, berücksichtigt werden (Alter, Geschlecht, kürzlich erlittene Fraktur, bereits eingeleitete Behandlung der Osteoporose und Komorbiditäten, wie z. B. Niereninsuffizienz). Bei einer Fraktur steigen die PINP- und ßCTX-I-Spiegel im Serum in den ersten Wochen nach der Fraktur steil an (um bis zu 150 %) (2, 3, 8). ßCTX erreicht 4 Wochen nach der Fraktur und PINP 12 Wochen nach der Fraktur einen Spitzenwert; danach nehmen die Werte ab, können aber noch mehr als 1 Jahr nach der Fraktur erhöht bleiben. Eine intensive sportliche Aktivität kann die Knochenumbaumarker ebenfalls verändern (leichter Anstieg von ßCTX und leichter Abfall von PINP), damit sollte eine solche idealerweise am Tag vor und am Tag der Probenentnahme vermieden werden (8).
Klinische Bedeutung der Knochenumbaumarker
Vorhersage des Knochensubstanzverlustes
Die Knochenumbaumarker ermöglichen eine dynamische Bewertung des Knochenumbaus, da sie die Aktivität der Knochenzellen widerspiegeln. Sie helfen, mögliche Ursachen einer sekundären Osteoporose zu ermitteln, indem Patienten mit hohem Knochenumsatz und schnellem Knochenverlust identifiziert werden.
Die hauptsächlichen Ursachen für den Knochensubstanzverlust in der zweiten Lebenshälfte, und damit für die Entstehung der postmenopausalen Osteoporose, ist der Östrogenmangel in der Menopause, bei beiden Geschlechtern Alterungsprozesse, Lebensstil und Umweltfaktoren sowie Krankheiten, die zu einem vermehrten Knochensubstanzverlust führen.
Der Östrogenmangel nach Beginn der Menopause führt zu einer Zunahme des Knochenumbaus und damit zu einem Anstieg der Knochenumbaumarker. Dieser Anstieg wurde in mehreren Studien mit einem schnelleren Knochenverlust in Verbindung gebracht (3, 5, 28). Höhere Werte für alle Marker korrelierten signifikant (wenn auch mässig) mit der Geschwindigkeit des Knochenverlustes. Die Vorhersage des Knochenverlustes auf individueller Basis ist jedoch schwach, da für einen gegebenen Wert eines Markers eine grosse Streuung der individuellen Werte des nachfolgenden Knochenverlustes besteht. Eine einzelne Messung eines Knochenumbaumarkers kann also das Ausmass des individuellen Knochensubstanzverlustes nicht vorhersagen. Erhöhte Knochenumbaumarker können allenfalls als Risikofaktoren für einen schnellen Knochenabbau angesehen werden.
Evaluation des Frakturrisikos
Prospektive Studien über den Zusammenhang zwischen Knochenumbaumarker und Frakturen bei postmenopausalen Frauen zeigten, dass je höher die Werte für die Umbaumarker sind, desto höher das Frakturrisiko ist (18). Die Assoziation mit dem Frakturrisiko zeigte sich v. a. mit den Knochenabbaumarkern und der alkalischen Knochenphosphatase und weniger mit anderen Knochenanbaumarkern (2, 3, 14). Eine Assoziation zwischen erhöhten Knochenumbauwerten und den Frakturen besteht vor allem für Wirbel- und Hüftfrakturen bei postmenopausalen und älteren Frauen und zum Teil auch bei Männern (2, 3, 29).
Interessanterweise sind erhöhte Knochenumbaumarker unabhängig von der gemessenen Knochendichte mit dem Frakturrisiko assoziiert. In einer Metaanalyse von sechs prospektiven Kohorten mit Frauen und Männern, bei denen ßCTX und PINP untersucht wurden, war das Risiko einer Fraktur um 23 % und 18 % pro Standard-Deviation- Erhöhung von PINP oder ßCTX erhöht (2, 3, 14, 30). Die prädiktive Wertigkeit der Knochenumbaumarker wurde vorwiegend für kürzere Zeitintervalle (bis 5–7 Jahre) gezeigt. Dies beschränkt ihren Nutzen für die langfristige Vorhersage von Frakturen in Risikorechnern wie FRAX, macht sie aber für die kurzfristige Vorhersage des Frakturrisikos in populationsbasierten Studien attraktiv (2, 3, 14).
Komorbiditäten können die Beziehung zwischen den Knochenumbaumarkern zur Vorhersage des Frakturrisikos beeinflussen. Beispielsweise zeigte sich, dass bei Patienten mit einem Diabetes mellitus Typ 2 die Knochendichtemessungen das Frakturrisiko unterschätzen (31, 32). Daher ist die Frage, wie BTMs am besten zur Abschätzung des Frakturrisikos bei Patienten mit Typ 2 Diabetes eingesetzt werden können, noch offen.
Therapiemonitoring
Kontrollen unter Therapie
Der wichtigste Bereich für den klinischen Einsatz von Knochenumbaumarkern ist das Monitoring antiresorptiver oder knochenanaboler Osteoporosetherapien. Das oberste Ziel bei der Behandlung von Patienten mit Osteoporose ist die Verringerung ihres Frakturrisikos. Die kurzfristige Inzidenz osteoporotischer Frakturen ist jedoch gering, und das Ausbleiben von Frakturen während der Behandlung bedeutet nicht zwingend, dass eine Behandlung wirksam ist. Daher werden zur Überwachung der Osteoporosetherapie serielle Messungen von Veränderungen der Knochendichte als Surrogatmarker für die therapeutische Wirksamkeit eingesetzt. Veränderungen der Knochendichte treten jedoch langsam auf, sodass therapeutische Wirkungen in der Regel erst nach mindestens 1–2 Jahren der Behandlung nachweisbar werden. Im Gegensatz dazu ändern sich die Knochenumbaumarkerwerte als Reaktion auf anabole und antiresorptive Behandlungen kurzfristig.
Die Änderung der Knochenumbaumarker unter Therapie können einerseits mit dem «least significant change» (kleinste signifikante Änderung, LSC; neuerdings auch «reference change value», RCV, genannt) oder andererseits gemäss dem «Referenzmittelwert»-Ansatz beurteilt werden. Der LSC wird unter Berücksichtigung der analytischen Variabilität und der intraindividuellen Variabiltät (LSC = 2.77 x intraindividelle Variabilität für eine 95 %- Wahrscheinlichkeit einer signifikanten Änderung) berechnet. Das Problem mit dem LSC-Ansatz ist, dass zwei Messungen erforderlich sind, was in der klinischen Praxis nicht immer möglich ist. Aus diesem Grund wird ein zweiter Ansatz vorgeschlagen, der den Durchschnittswert für junge prämenopausale Frauen verwendet («Referenzmittelwert»-Ansatz). Bei diesem Ansatz wird die individuelle Veränderung im Vergleich zu den prämenopausalen Referenzbereichen festgelegt. Unter einer antiresorptiven Therapie sollte als Therapieerfolg eine Abnahme erhöhter Resorptionsmarker wie ßCTX in die mittlere bis untere Hälfte des Referenzbereiches erreicht werden (13, 14).
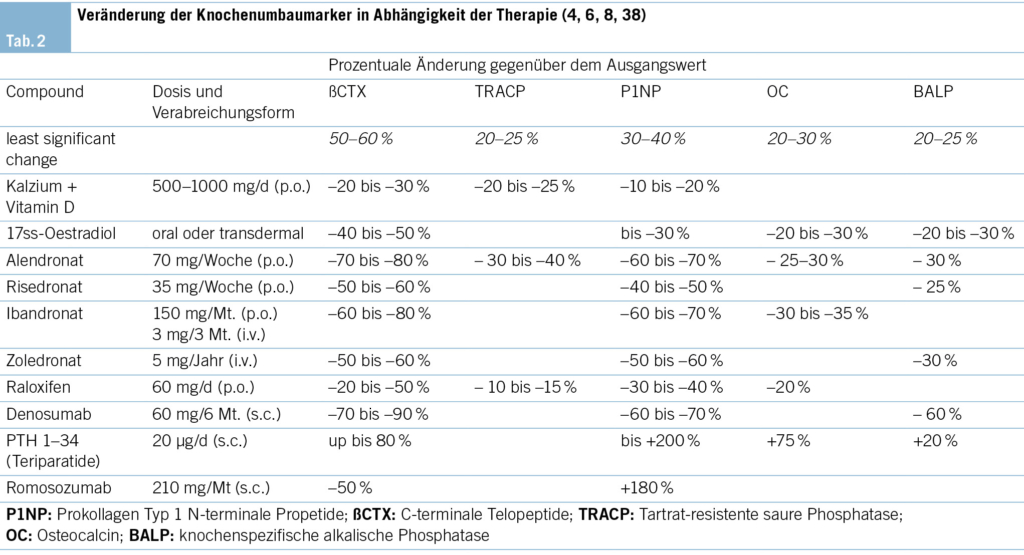
Die Veränderung der Marker hängt vom eingesetzten Therapeutikum und dem gemessenen Marker ab (Tab. 2). Findet eine zu geringe Veränderung statt, kann dies ein Hinweis auf eine schlechte Compliance des Patienten oder eine unsachgemässe Verabreichung des Medikaments sein.
Antiresorptive Therapie
Eine antiresorptive Behandlung bewirkt eine rasche Abnahme der Knochenresorptionsmarker nach bereits 2–4 Wochen und mit einem Nadir nach 3–6 Monaten. Die Abnahme der Knochenanbaumarker, infolge der physiologischen Kopplung von Anbau und Abbau, ist verzögert und erreicht nach 6–12 Monaten ein Plateau. Mehrere Studien haben gezeigt, dass eine kurzfristige Abnahme des Knochenumbaus bei Frauen, die mit Hormonersatztherapie Raloxifen, Risedronat und Alendronat behandelt wurden, mit der Zunahme der Knochendichte nach 1–2 Jahren und einer Abnahme des Risikos von Wirbelkörper- und/oder anderen Frakturen einhergeht (7, 13, 14).
Es wird empfohlen, bei einer oralen Bisphosphonattherapie die Knochenumbaumarker zur Beurteilung der Compliance und der Behandlung einzusetzen unter Verwendung von ßCTX und PINP. Eine Messung vor Beginn der Behandlung und eine Wiederholung nach 3 Monaten erlaubt eine Beurteilung mit gewünschter Abnahme der Knochenumbaumarker über den «least significant change»-Wert (LSC) hinaus (siehe oben und Tab. 2).
Bei einer parenteralen Behandlung mit Zoledronat kommt es bereits nach 2 Wochen zu einer deutlichen Abnahme von ßCTX, und bei kontinuierlicher Therapie bleibt die Suppression von ßCTX und PINP bestehen. Es gibt Hinweise, dass zur Beurteilung der klinischen Wirksamkeit (Frakturen) und «Responders» PINP geeigneter ist als ßCTX (oder die Knochendichte). Ähnlich wie bei einer oralen Bisphosphonattherapie zeigt sich auch bei der Zoledronat-Therapie eine positive Korrelation zwischen einer Abnahme von PINP und der Verringerung des Risikos vertebraler Frakturen (13).
Denosumab ist ein monoklonaler Antikörper gegen RANKL, der subkutan verabreicht wird und den Knochenabbau rasch hemmt, was sich in einem sehr schnellen Abfall der Knochenresorptionswerte auf nahezu nicht nachweisbare Werte des Markers ßCTX innerhalb weniger Tage nach der Verabreichung äussert. Auch das Serum-PINP wird durch die Denosumab-Behandlung supprimiert, aber die Abnahme ist nicht so ausgeprägt wie bei ßCTX und kommt mit einer Verzögerung von 3–6 Monaten zustande.
Beim Absetzen der Denosumab-Behandlung kommt es, im Gegensatz zu den Bisphosphonaten, zu einem ausgeprägten Wiederanstieg der Knochenumbaumarker, und zwar über die Werte vor der Behandlung. Dieser sog. Rebound-Effekt ist mit einem beschleunigten Knochenmassenverlust und einem erhöhten Risiko für vertebrale Frakturen assoziiert. Das Monitoring mithilfe der Knochenumbaumarker hilft bei der Beurteilung des Zeitpunktes einer sequenziellen Bisphosphonattherapie (14, 33).
Anabole Therapie
Die Behandlung mit dem Parathormon-Analogon Teriparatid bewirkt einen schnellen, innerhalb von Tagen eintretenden Anstieg des Knochenanbaumarkers PINP mit einem Maximum nach 3–4 Monaten. Die Knochenabbaumarker zeigen einen verzögerten und weniger ausgeprägten Anstieg als die Knochenanbaumarker. Die Knochenanbaumarker, insbesondere PINP, korrelieren mit dem Anstieg der Knochenmineralgehaltswerten. Die Frakturrisikoreduktion unter der Teriparatid-Therapie ist unabhängig vom Ausgangswert von P1NP (3). Es gibt keine Studien, die den Zusammenhang zwischen Veränderung der Knochenanbaumarker und der Frakturrisikoreduktion untersucht haben.
Für die Überwachung von Patienten, welche mit Teriparatid behandelt werden, wurde ein Algorithmus mit Knochenumbaumarkern vorgeschlagen. Das PINP sollte vor der Behandlung und dann 1 und 3 Monate nach Beginn der Behandlung überprüft werden. Ein Anstieg des PINP um mehr als den LSC von 10 μg/l und ein Anstieg über den Referenzbereich gilt als gutes Ansprechen auf die Behandlung (2, 3, 14). Nach zweijähriger Behandlung und vor einer sequenziellen antiresorptiven Behandlung sind Messungen von PINP und der Knochendichte zu empfehlen (2, 13).
Romosozumab ist ein monoklonaler Antikörper, der Sklerostin bindet und dessen Wirkung blockiert. Die einzigartige Wirkungsweise besteht darin, dass der Knochenanbau angeregt und gleichzeitig der Knochenabbau gehemmt wird (34). Unter der Behandlung kommt es zu einem vorübergehenden Anstieg von PINP mit einem Peak nach ca. 2 Wochen und einer Abnahme auf den Ausgangswert nach ca. 9 Monaten (2). OC und BALP verhalten sich ähnlich. Die Werte für ßCTX nehmen rasch ab (Nadir nach ca. 2 Wochen) und kehren 3–6 Wochen nach der letzten Dosis zum Ausgangswert zurück (2, 34). Romosozumab wurde vor Kurzem in einigen Ländern zugelassen, doch gibt es noch keine offiziellen Empfehlungen für den Einsatz von Knochenumbaumarkern für das Therapiemonitoring.
Kontrollen bei Therapiepause («drug holiday»)
Die Knochenumbaumarker können auch zur Beurteilung des Nachlassens des Therapieeffektes und Notwendigkeit einer Wiederaufnahme der Therapie eingesetzt werden.
Im Allgemeinen wird empfohlen, bei moderat erhöhtem Frakturrisiko eine Bisphosphonattherapie nach 3–5 Jahren zu pausieren, um das Risiko für die seltenen unerwünschten Wirkungen einer Langzeittherapie wie atypische Femurfrakturen zu minimieren. Bisphosphonate binden sich an den Knochen und verbleiben über längere Zeit im Skelett (2, 5, 13, 35). Damit persistiert auch nach dem Absetzen der Bisphosphonate eine residuelle Wirkung, im Gegensatz zu anderen antiresorptiven Therapien, bei denen die Wirkung nach Absetzen schnell nachlässt (d. h. bei Denosumab, Östrogenen oder Raloxifen). Eine generelle Empfehlung, in welchen Abständen eine Bestimmung der Knochenumbaumarker angezeigt ist, gibt es nicht. Es scheint sinnvoll, eine Bestimmung in ein- bis zweijährlichen Intervallen vorzunehmen. Bei der Beurteilung, ob eine Wiederaufnahme der Behandlung zu erwägen ist, kann, wie bei der Verlaufskontrolle unter Therapie, der LSC-Ansatz oder ein Anstieg der Werte über den Mittelwert prämenopausaler Frauen herangezogen werden.
Die Beendigung der Denosumab-Therapie führt zu einem erneuten ausgeprägten Anstieg des Knochenumbaus etwa 8–9 Monate nach der letzten Dosis. Die Knochenumbaumarker können bei der Identifikation von Patienten mit einem erhöhten Risiko für diese Komplikation und um die Bisphosphonatbehandlung in Dosierung und Applikationsfrequenz zu leiten, eingesetzt werden. Die European Calcified Tissue Society (ECTS) hat eine Leitlinie veröffentlicht: Darin wird empfohlen, die Knochenumbaumarker nach 3 und 6 Monaten nach Absetzen von Denosumab zu bestimmen. Steigen die Werte über den prämenopausalen Referenzwert an, ist der Einsatz bzw. eine Wiederholung einer Bisphosphonattherapie (idealerweise mit Zoledronat) angezeigt (2, 14, 33).
Speziallabor Hormone und Knochenstoffwechsel
Aeschenvorstadt 57
4051 Basel
marius.kraenzlin@unibas.ch
Die Autorenschaft hat keine Interessenkonflikte im Zusammenhang mit diesem Artikel deklariert.
1. Seeman E. Bone quality: the material and structural basis of bone strength. J Bone Miner Metab 2008;26(1):1-8.
2. Schini M, Vilaca T, Gossiel F, Salam S, Eastell R. Bone Turnover Markers: Basic Biology to Clinical Applications. Endocr Rev 2023 May 8;44(3):417-73.
3. Eastell R, Szulc P. Use of bone turnover markers in postmenopausal osteoporosis. Lancet Diabetes Endocrinol 2017 Nov;5(11):908-23.
4. Bonjour JP, Kohrt W, Levasseur R, Warren M, Whiting S, Kraenzlin M. Biochemical markers for assessment of calcium economy and bone metabolism: application in clinical trials from pharmaceutical agents to nutritional products. Nutr Res Rev 2014 Nov 14;1-16.
5. Brown JP, Don-Wauchope A, Douville P, Albert C, Vasikaran SD. Current use of bone turnover markers in the management of osteoporosis. Clin Biochem 2022 Nov;109-110:1-10.
6. Vasikaran S, Cooper C, Eastell R, Griesmacher A, Morris HA, Trenti T, et al. International Osteoporosis Foundation and International Federation of Clinical Chemistry and Laboratory Medicine position on bone marker standards in osteoporosis. Clin Chem Lab Med 2011 Aug;49(8):1271-4.
7. Vasikaran SD, Miura M, Pikner R, Bhattoa HP, Cavalier E. Practical Considerations for the Clinical Application of Bone Turnover Markers in Osteoporosis. Calcif Tissue Int 2023 Feb;112(2):148-57.
8. Szulc P, Naylor K, Hoyle NR, Eastell R, Leary ET. Use of CTX-I and PINP as bone turnover markers: National Bone Health Alliance recommendations to standardize sample handling and patient preparation to reduce pre-analytical variability. Osteoporos Int 2017 Sep;28(9):2541-56.
9. Cavalier E, Lukas P, Carlisi A, Gadisseur R, Delanaye P. Aminoterminal propeptide of type I procollagen (PINP) in chronic kidney disease patients: the assay matters. Clin Chim Acta 2013 Oct 21;425:117-8.
10. Lee J, Vasikaran S. Current recommendations for laboratory testing and use of bone turnover markers in management of osteoporosis. Ann Lab Med 2012 Mar;32(2):105-12.
11. Brown JP, Albert C, Nassar BA, Adachi JD, Cole D, Davison KS, et al. Bone turnover markers in the management of postmenopausal osteoporosis. Clin Biochem 2009 Jul;42(10-11):929-42.
12. Cavalier E, Eastell R, Rye JrN, Makris K, Tournis S, Vasikaran S, et al. A multicenter study to evaluate harmonization of assays for N-terminal propeptide of type I procollagen (PINP): a report from the IFCC-IOF Joint Committee for Bone Metabolism. Clin Chem Lab Med 2019 Sep 25;57(10):1546-55.
13. Eastell R, Pigott T, Gossiel F, Naylor KE, Walsh JS, Peel NFA. Bone turnover markers: are they clinically useful? Eur J Endocrinol 2018 Jan;178(1):R19-R31.
14. Lorentzon M, Branco J, Brandi ML, Bruyere O, Chapurlat R, Cooper C, et al. Algorithm for the Use of Biochemical Markers of Bone Turnover in the Diagnosis, Assessment and Follow-Up of Treatment for Osteoporosis. Adv Ther 2019 Oct;36(10):2811-24.
15. Moser SC, van der Eerden BCJ. Osteocalcin-A Versatile Bone-Derived Hormone. Front Endocrinol (Lausanne) 2018;9:794.
16. Diemar SS, Mollehave LT, Quardon N, Lylloff L, Thuesen BH, Linneberg A, et al. Effects of age and sex on osteocalcin and bone-specific alkaline phosphatase-reference intervals and confounders for two bone formation markers. Arch Osteoporos 2020 Feb 24;15(1):26.
17. Diemar SS, Dahl SS, West AS, Simonsen SA, Iversen HK, Jørgensen NR. A Systematic Review of the Circadian Rhythm of Bone Markers in Blood. Calcif Tissue Int 2023 Feb;112(2):126-47.
18. Gineyts E, Cloos P, Borel O, Grimaud L, Delmas P, Garnero P. Racemization and isomerizatin of type I collagen c-telopeptides in human bone and soft tissue: assessment of tissue turnover. Biochem J 2000;345:481-5.
19. Cloos PA, Fledelius C, Christgau S, Christiansen C, Engsig M, Delmas P, et al. Investigation of bone disease using isomerized and racemized fragments of type I collagen. Calcif Tissue Int 2003 Jan;72(1):8-17.
20. Cavalier E, Eastell R, Jorgensen NR, Makris K, Tournis S, Vasikaran S, et al. A Multicenter Study to Evaluate Harmonization of Assays for C-Terminal Telopeptides of Type I Collagen (beta-CTX): A Report from the IFCC-IOF Committee for Bone Metabolism (C-BM). Calcif Tissue Int 2021 Jun;108(6):785-97.
21. Kraenzlin ME, Seibel M. Measurement of biochemical markers of bone resorption. In: Seibel M, Robins S, Bilezikian J, editors. Dynamics in bone and cartilage metabolism. 2 ed. Academic Press; 2006. p. 541-64.
22. Cavalier E, Lukas P, Delanaye P. Analytical evaluation of the Nittobo Medical tartrate resistant acid phosphatase isoform 5b (TRACP-5b) EIA and comparison with IDS iSYS in different clinically defined populations. Clin Chem Lab Med 2022 Feb 23;60(3):394-400.
23. Hannon RA, Clowes JA, Eagleton AC, Al HA, Eastell R, Blumsohn A. Clinical performance of immunoreactive tartrate-resistant acid phosphatase isoform 5b as a marker of bone resorption. Bone 2004 Jan;34(1):187-94.
24. Kraenzlin ME, Lau K-HW, Liang L, Freeman TK, Singer FR, Stepan J, et al. Development of an immunoassay for human serum osteoclastic tartrate-resistant acid phosphates. J Clin Endocrinol Metab 1990;71:442-51.
25. Halleen J, Alatalo SL, Janckila AJ, Woitge H, Seibel MJ, Väänänen HK. Serum tartrate-resistant acid phosphatase 5b is a specific and sensitive marker of bone resorption. Clin Chem 2001;47:597-600.
26. Gossiel F, Ugur A, Peel NFA, Walsh JS, Eastell R. The clinical utility of TRACP-5b to monitor anti-resorptive treatments of osteoporosis. Osteoporos Int 2022 Jun;33(6):1357-63.
27. Kraenzlin ME, Kraenzlin CA, Meier C, Giunta C, Steinmann B. Automated HPLC assay for urinary collagen cross-links: effect of age, menopause, and metabolic bone diseases. Clin Chem 2008 Sep;54(9):1546-53.
28. Szulc P. Bone turnover: Biology and assessment tools. Best Pract Res Clin Endocrinol Metab 2018 Oct;32(5):725-38.
29. Meier C, Nguyen TV, Center JR, Seibel MJ, Eisman JA. Bone resorption and osteoporotic fractures in elderly men: the dubbo osteoporosis epidemiology study. J Bone Miner Res 2005;20(4):579-87.
30. Johansson H, Odén A, Kanis JA, McCloskey EV, Morris HA, Cooper C, et al. A meta-analysis of reference markers of bone turnover for prediction of fracture. Calcif Tissue Int 2014 May;94(5):560-7.
31. Meier C, Eastell R, Pierroz DD, Lane NE, Al-Daghri N, Suzuki A, et al. Biochemical Markers of Bone Fragility in Patients With Diabetes. J Clin Endocrinol Metab 2023 May 8.
32. Vestergaard P, Rejnmark L, Mosekilde L. Diabetes and its complications and their relationship with risk of fractures in type 1 and 2 diabetes. Calcif Tissue Int 2009 Jan;84(1):45-55.
33. Tsourdi E, Langdahl B, Cohen-Solal M, Aubry-Rozier B, Eriksen EF, Guanabens N, et al. Discontinuation of Denosumab therapy for osteoporosis: A systematic review and position statement by ECTS. Bone 2017 Dec;105:11-7.
34. Mäkinen VN, Solling AS, McClung M, Langdahl BL. Romosozumab for the treatment of osteoporosis – a systematic review. J Endocrinol Invest 2024 Nov 2.
35. Naylor KE, McCloskey EV, Jacques RM, Peel NFA, Paggiosi MA, Gossiel F, et al. Clinical utility of bone turnover markers in monitoring the withdrawal of treatment with oral bisphosphonates in postmenopausal osteoporosis. Osteoporos Int 2019 Apr;30(4):917-22.
36. Cavalier E, Lukas P, Bottani M, Aarsand AK, Ceriotti F, Coşkun A, et al. European Biological Variation Study (EuBIVAS): within- and between-subject biological variation estimates of β-isomerized C-terminal telopeptide of type I collagen (β-CTX), N-terminal propeptide of type I collagen (PINP), osteocalcin, intact fibroblast growth factor 23 and uncarboxylated-unphosphorylated matrix-Gla protein-a cooperation between the EFLM Working Group on Biological Variation and the International Osteoporosis Foundation-International Federation of Clinical Chemistry Committee on Bone Metabolism. Osteoporos Int 2020 Aug;31(8):1461-70.
37. Christensen GL, Halgreen JR, Milenkovski M, Kose A, Quardon N, Jorgensen NR. Bone turnover markers are differentially affected by pre-analytical handling. Osteoporos Int 2019 May;30(5):1137-41.
38. Henriksen K, Leeming DJ, Christiansen C, Karsdal MA. Use of bone turnover markers in clinical osteoporosis assessment in women: current issues and future options. Womens Health (Lond Engl ) 2011 Nov;7(6):689-98.
Therapeutische Umschau
- Vol. 82
- Ausgabe 1
- Februar 2025