- Fokusthema Dyspnoe – eine Einführung
Definition, Epidemiologie und Prognose
Gemäss der American Thoracic Society leidet jede vierte Patientin in der hausärztlichen Praxis und jeder zweite hospitalisierte Patient in irgendeiner Weise an Dyspnoe. Diese Zahlen greifen vermutlich etwas hoch. Die Erfahrung von vermutlich uns allen bestätigt aber: Dyspnoe ist eines der häufigsten und zugleich eines der kompliziertesten Symptome. Die breit gefasste Definition – als Dyspnoe wird jede Form einer unangenehm empfundenen Atmung bezeichnet (1) – macht Atemnot in besonderem Masse zu einem sehr subjektiven Symptom: „dyspnea per se can only be perceived by the person experiencing it“. Dyspnoe muss daher in der Anamnese immer auch ganz konkret erfragt werden.
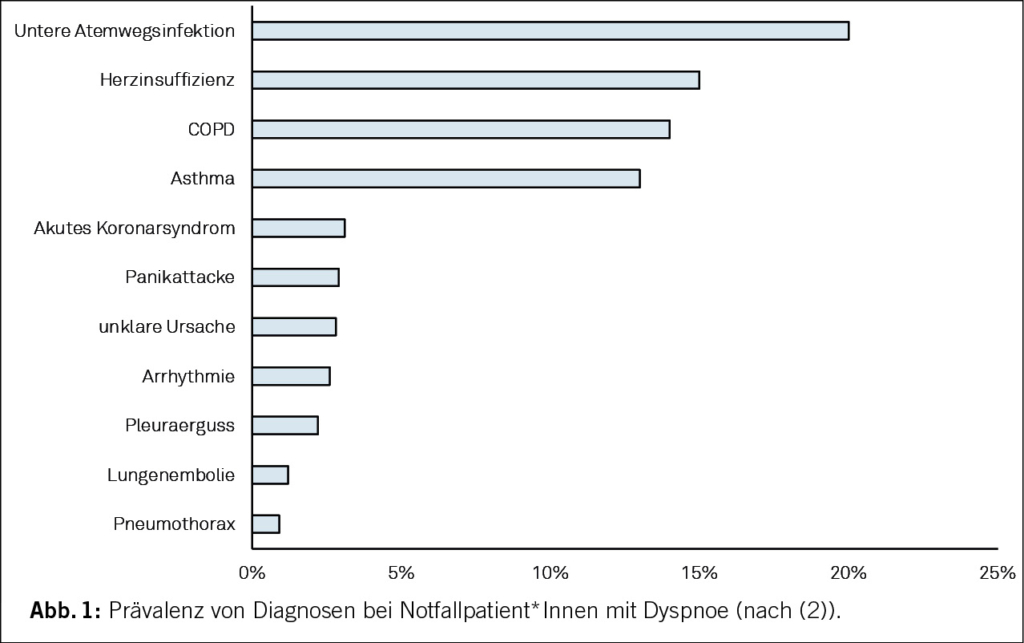
Abbildung 1 gibt eine Übersicht über die Häufigkeit von Diagnosen, die bei Patient*Innen mit Dyspnoe auf der Notfallstation gestellt werden: Ätiologisch stehen im klinischen Alltag kardiale und pulmonale Ursachen klar im Vordergrund. Unklare Fälle sind die Ausnahme. Bei Patient*Innen > 50 Jahre ist zudem die Schnittmenge zwischen kardiorespiratorischen Krankheiten, Angst- und depressiven Erkrankungen und Adipositas gross: in zwei Dritteln aller Fälle findet sich dann mehr als nur eine Ursache der Dyspnoe (3). Dies wird auch durch die folgenden Zusammenhänge anschaulich illustriert: Ältere Patient*Innen haben eine hohe Prävalenz von Herzinsuffizienz mit erhaltener Auswurffraktion (HFpEF). Dieses Syndrom – früher auch als «diastolische» Herzinsuffizienz bezeichnet – beinhaltet eine Vielzahl von Mechanismen, die zu Dyspnoe führen können: Neben der erwähnten diastolischen Dysfunktion spielen dabei eine reduzierte systolische oder diastolische funktionelle Reserve, eine chronotrope Inkompetenz, ein erhöhter pulmonaler Widerstand, eine erniedrigte periphere Sauerstoffverwertung, Dekonditionierung, Übergewicht, u.v.m. eine relevante Rolle (4).
Atemnot ist aber auch ein Surrogatmarker für die Mortalität und damit ein prognostischer Marker: Patient*Innen, die mit Dyspnoe ins Krankenhaus eintreten, haben ein deutlich höheres Risiko, zu versterben, als Patienten ohne Atemnot (5). Bei Patient*Innen mit einer chronisch-obstruktiven Lungenkrankheit ist das subjektive Ausmass der Atemnot sogar der bessere Prädiktor für die Mortalität als die objektivierbare lungenfunktionelle Einschränkung (6).
Zur Diagnose kommen
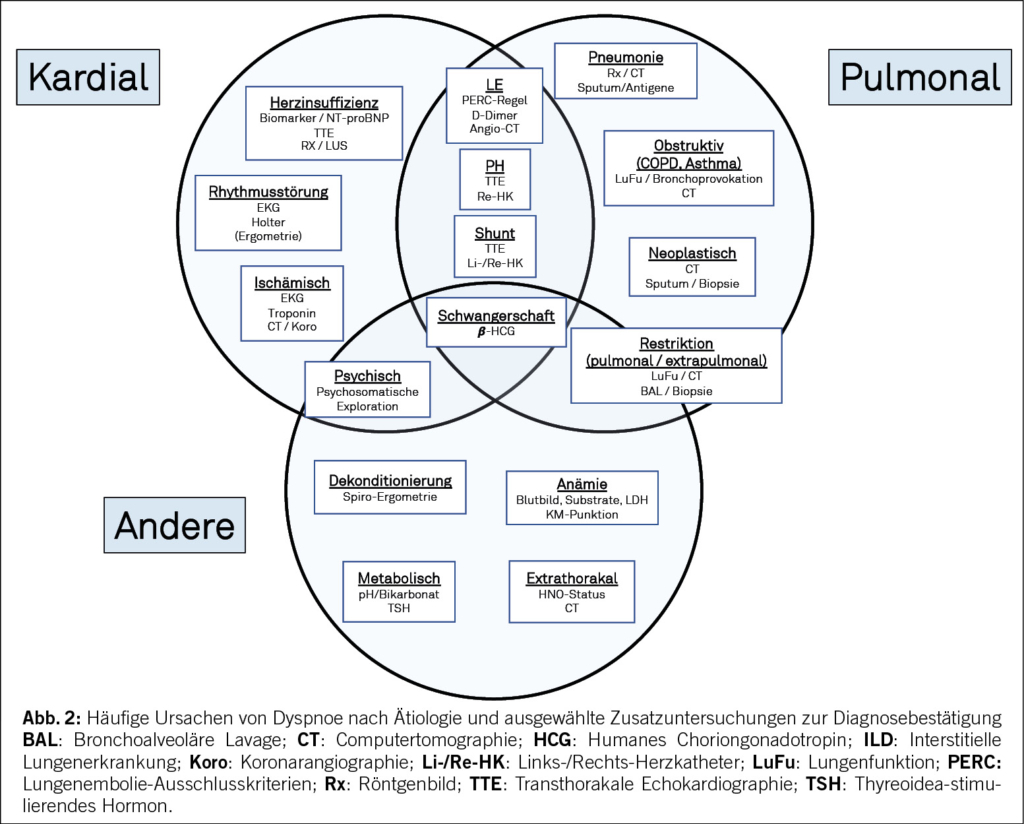
Auch wenn sich alleine aus der Qualität der Dyspnoe – z.B. Engegefühl, Lufthunger, Erstickungsangst – keine guten Rückschlüsse auf die Ursache ziehen lassen (7), so hat die Synthese aus genauer Anamnese und fokussierter klinischer Untersuchung einen herausragenden Stellenwert. Nach wie vor kann damit die überwiegende Mehrheit aller Diagnosen gestellt werden – dies gilt auch für Patient*Innen mit Dyspnoe (8-10). Spezifische apparative Tests und ausgewählte Zusatzmodalitäten unterstützen dabei: Mit der Beurteilung der Resultate aus Blutbild, Labor und Bildgebung werden dann die initial gestellten Arbeitshypothesen im Diagnoseprozess bestätigt oder verworfen (11).
Der umgekehrte Ansatz ist hingegen bedeutungslos: mit isolierten Laboruntersuchungen zum Beispiel werden keine Diagnosen gestellt. Wie bereits andernorts erwähnt (12, 13), kann das Resultat jedes medizinischen Tests ohne Berücksichtigung der Vortestwahrscheinlichkeit nicht korrekt interpretiert werden: Bei sehr hoher Vortestwahrscheinlichkeit für das Vorliegen einer Krankheit handelt es sich so selbst bei einem sehr guten (d.h. sehr sensitiven) Test im Falle eines negativen Resultates um ein falsch-negatives Resultat: Liegt klinisch eine hohe Vortestwahrscheinlichkeit für eine akute Herzinsuffizienz vor, ist der zusätzliche diagnostische Wert von natriuretischen Peptiden von limitierter Bedeutung. Auch tiefe Werte sind dann mit Vorsicht zu interpretieren (14, 15). Ganz generell kann damit gesagt werden, dass die Wertigkeit apparativer Untersuchungen für die Bestätigung bzw. den Ausschluss einer Diagnose im probabilistischen Prozess der klinischen Entscheidungsfindung überschätzt wird (16).
Eine entscheidende Rolle im Diagnoseprozess spielen zudem kognitive Fehler und Fallstricke (engl. Bias). Auf eine breite Abhandlung dieser Prozesse verzichten wir hier mit Verweis auf die einschlägige Literatur (17).
Erwähnen, da für den diagnostischen Prozess entscheidend, möchten wir aber kurz die folgenden Fallstricke:
i) der Anker (engl. anchoring), der durch das selektive Hervorheben gewisser Charakteristika gesetzt wird, exemplarisch bei der Patientenvorstellung: Der 80-jährige Raucher mit Dyspnoe löst andere Assoziationen und diagnostische Überlegungen aus als die 35-jährige Schwangere; ii) der ascertainment bias, der uns dazu verleitet, aus Anamnese, Untersuchungsbefunden und Testresultaten diejenigen Befunde herauszusuchen, welche unsere Hypothese bestätigen (kurz: wir sehen das, was wir sehen möchten); iii) der availability bias, aufgrund dessen wir die Wahrscheinlichkeit einer Krankheit höher schätzen, wenn sie uns schneller in den Sinn kommt («Verfügbarkeitsheuristik») und schliesslich iv) das premature closure, also das vorzeitige Stoppen des diagnostischen Prozesses ohne
Berücksichtigung weiterer Diagnosen. Das letzte Phänomen wird v.a. unter Zeitdruck, z.B. bei der Arbeit auf der Notfallstation beobachtet. Anhand des Beispiels einer Patientin, die sich während der COVID-Pandemie mit Dyspnoe, Fieber und pulmonalen Groundglass-Opazitäten vorstellt, können diese Fallstricke eindrücklich veranschaulicht werden (11). Die Patientin wird – vermutlich vorschnell – mit einer SARS-CoV2-Pneumonie diagnostiziert. Das wichtige Engramm dazu lautet: Es gibt immer eine Differentialdiagnose.
Dyspnoe: ein weites Feld
Der Dyspnoe und ihrer breiten Differentialdiagnose ist diese Umschau gewidmet. Expert*Innen beleuchten das Thema Atemnot aus ganz unterschiedlichen Blickwinkeln. Die zehn Artikel dieses Monographs haben dabei ein gemeinsames Ziel: die Vermittlung von möglichst praxisrelevanten Aspekten im Zusammenhang mit Atemnot. Die Artikel beginnen deshalb mit einer kurzen Zusammenfassung oder einer klinischen
Vignette. Engramme, Algorithmen und konkrete Empfehlungen für Diagnostik und Therapie stehen bewusst vor komplexen pathophysiologischen Grundlagen. Die Evidenz aus der publizierten Literatur wird dabei persönlich gefärbt und ergänzt durch die Expertenmeinung der Autor*Innen. Damit gibt sich ein buntes Kaleidoskop der Dyspnoe, ihrer Ursachen, von differentialdiagnostischen Überlegungen und therapeutischen Optionen. Diskutiert werden die wichtigsten Organsysteme, rehabilitativmedizinische Ansätze und palliative Konzepte.
Allen Autor*Innen möchten wir unseren herzlichen Dank für die aufgewendete Zeit beim Erstellen der einzelnen Beiträge und das Teilen ihrer Expertise aussprechen. Das erfolgreiche Gelingen dieses Themenheftes wäre ohne das grosse Engagement nicht möglich gewesen. Ihnen, geschätzte Leser*Innen, wünschen wir viel Vergnügen und eine anregende Lektüre!
Klinik Innere Medizin
Stadtspital Zürich Triemli
Birmensdorferstrasse 497
8063 Zürich, Schweiz
lars.huber@stadtspital.ch
Klinik Innere Medizin
Stadtspital Zürich Triemli
Birmensdorferstrasse 497
8063 Zürich, Schweiz
mattia.arrigo@uzh.ch
1. Parshall MB, Schwartzstein RM, Adams L, Banzett RB, Manning HL, Bourbeau J, et al. An official American Thoracic Society statement: update on the mechanisms, assessment, and management of dyspnea. Am J Respir Crit Care Med. 2012;185(4):435-52.
2. Kelly AM, Keijzers G, Klim S, Graham CA, Craig S, Kuan WS, et al. An Observational Study of Dyspnea in Emergency Departments: The Asia, Australia, and New Zealand Dyspnea in Emergency Departments Study (AANZDEM). Acad Emerg Med. 2017;24(3):328-36.
3. Sandberg J, Ekstrom M, Borjesson M, Bergstrom G, Rosengren A, Angeras O, et al. Underlying contributing conditions to breathlessness among middle-aged individuals in the general population: a cross-sectional study. BMJ Open Respir Res. 2020;7(1).
4. Shah AM, Pfeffer MA. The many faces of heart failure with preserved ejection fraction. Nat Rev Cardiol. 2012;9(10):555-6.
5. Stevens JP, Dechen T, Schwartzstein RM, O‘Donnell CR, Baker K, Banzett RB. Association of dyspnoea, mortality and resource use in hospitalised patients. Eur Respir J. 2021;58(3).
6. Nishimura K, Izumi T, Tsukino M, Oga T. Dyspnea is a better predictor of 5-year survival than airway obstruction in patients with COPD. Chest. 2002;121(5):1434-40.
7. Simon PM, Schwartzstein RM, Weiss JW, Fencl V, Teghtsoonian M, Weinberger SE. Distinguishable types of dyspnea in patients with shortness of breath. Am Rev Respir Dis. 1990;142(5):1009-14.
8. Hampton JR, Harrison MJ, Mitchell JR, Prichard JS, Seymour C. Relative contributions of history-taking, physical examination, and laboratory investigation to diagnosis and management of medical outpatients. Br Med J. 1975;2(5969):486-9.
9. Mulrow CD, Lucey CR, Farnett LE. Discriminating causes of dyspnea through clinical examination. J Gen Intern Med. 1993;8(7):383-92.
10. Paley L, Zornitzki T, Cohen J, Friedman J, Kozak N, Schattner A. Utility of clinical examination in the diagnosis of emergency department patients admitted to the department of medicine of an academic hospital. Arch Intern Med. 2011;171(15):1394-6.
11. Vyas JM, Castle AC, Bourgouin PP, Turbett SE. Case 9-2022: A 56-Year-Old Woman with Fever, Myalgias, Diarrhea, and Cough. N Engl J Med. 2022;386(12):1166-74.
12. Speich R. [Diagnostic process in internal medicine: decision analysis or intuition?]. Schweiz Med Wochenschr. 1997;127(31-32):1263-79.
13. Stussi-Helbling M, Arrigo M, Huber LC. Pearls and Myths in the Evaluation of Patients with Suspected Acute Pulmonary Embolism. Am J Med. 2019;132(6):685-91.
14. Steinhart B, Thorpe KE, Bayoumi AM, Moe G, Januzzi JL, Jr., Mazer CD. Improving the diagnosis of acute heart failure using a validated prediction model. J Am Coll Cardiol. 2009;54(16):1515-21.
15. Simel DL, Rennie D. Heart Failure. The Rational Clinical Examination: Evidence-Based Clinical Diagnosis. New York, NY: McGraw-Hill Education; 2016.
16. Morgan DJ, Pineles L, Owczarzak J, Magder L, Scherer L, Brown JP, et al. Accuracy of Practitioner Estimates of Probability of Diagnosis Before and After Testing. Jama Intern Med. 2021;181(6):747-55.
17. Kahneman D. Thinking, Fast and Slow. London, UK: Penguin; 2012.
Therapeutische Umschau
- Vol. 80
- Ausgabe 6
- August 2023