- Kryobiopsien zur Differenzierung interstitieller Pneumopathien
Einleitung
Bei der interstitiellen Pneumopathie (ILD) handelt es sich um eine heterogene Gruppe von pulmonalen Erkrankungen, die sich aufgrund einer ähnlichen klinischen, radiologischen oder pathologischen Manifestation zusammenfassen lassen. Es handelt sich um entzündliche und/ oder fibrosierende Prozesse im Lungeninterstitium, welche zu irreversiblen Vernarbungen des Lungengewebes führen können. Als Initialsymptome bestehen meist eine langsam progrediente Dyspnoe und/oder ein unproduktiver Husten. Lungenfunktionell ist das Korrelat der Dyspnoe letztlich die Ausbildung einer Restriktion und die Einschränkung der Diffusionskapazität durch eine Verbreiterung der Blut-Gas-Schranke im Alveolarraum. Assoziationen mit zugrundeliegenden Erkrankungen (z.B. aus dem rheumatologischen Formenkreis die rheumatoide Arthritis oder Sklerodermie) sowie eine familiäre Prädisposition als Risikofaktor sind wichtig zu differenzieren. Die affirmative Diagnosesicherung kann richtungsweisend sein für die Etablierung der optimalen Therapie.
Zur Eingrenzung der Ätiologie sind neben einer umfassenden Anamnese bezüglich familiärer Disposition, Berufsanamnese (z.B. Asbest-, Steinstaubexposition), Noxenexpositionen in der Freizeit (Höhlenbesuche, Kontakt mit Holzstäuben etc.) auch Laboruntersuchungen zum Screening für rheumatologische Erkrankungen, chronische Infektionen (HIV) oder andere chronische Lungenerkrankungen wie z.B. Sarkoidose notwendig. Bei auffälligem Rheuma-Screening und/oder Rheumaassoziierten Beschwerden ist die Vorstellung bei einem Spezialisten zur näheren Eingrenzung bezüglich einer Rheuma-assoziierten-ILD indiziert. Weitere Differentialdiagnosen für interstitielle Pneumopathien sind Raucher-assoziierten Erkrankungen wie die RB-ILD (respiratorische Bronchiolitis) und die desquamative interstitielle Pneumonie (DIP), welche bei langfristigem Nicotinkonsum auftreten können.
Das CT-graphische Muster einer ILD ist entscheidend bezüglich der Wahl des weiteren diagnostischen Vorgehens respektive dessen Invasivität. Bei klinischem Verdacht auf eine idiopathische pulmonale Fibrose (IPF) und der CT-radiologischen Diagnose eines klassisches UIP (usual interstitial pneumonia)-Musters besteht eine sehr hohe Wahrscheinlichkeit (>90%), dass auch histologisch ein UIP-Muster vorliegt. Gemäss der American Thoracic Society (ATS) und der European Respiratory Society (ERS) sprechen wir von einem UIP-Muster bei subpleuralen Retikulationen mit einem basoapikalen Gradienten (Zunahme der Veränderungen in den unteren Anteilen der Lunge) und Nachweis von Honigwaben (honey combing) +/- Traktionsbronchiektasen. Finden sich zwar der basoapikale Gradient und Traktionsbronchiektasen, fehlen aber die typischen subpleuralen mehrreihig angeordneten kleinzystischern Veränderungen (=Honigwaben), spricht man von einem möglichen UIP-Muster. Bei Vorliegen von Mikronoduli, ausgedehnten Infiltrationen und Milchglasinfiltraten sowie einer peribronchovaskulären Verteilung spricht man CT-radiologisch von einem «alternative diagnosis» Muster und eine histologische UIP ist unwahrscheinlich.
Interventionelle Diagnosesicherung
1. Liegt CT-radiologisch ein typisches UIP-Muster vor, wird per internationalem Konsens keine bioptische Sicherung benötigt.
2. Ähnliches gilt, sofern eine kausale rheumatologische Grunderkrankung für die Pneumopathie gefunden wurde.
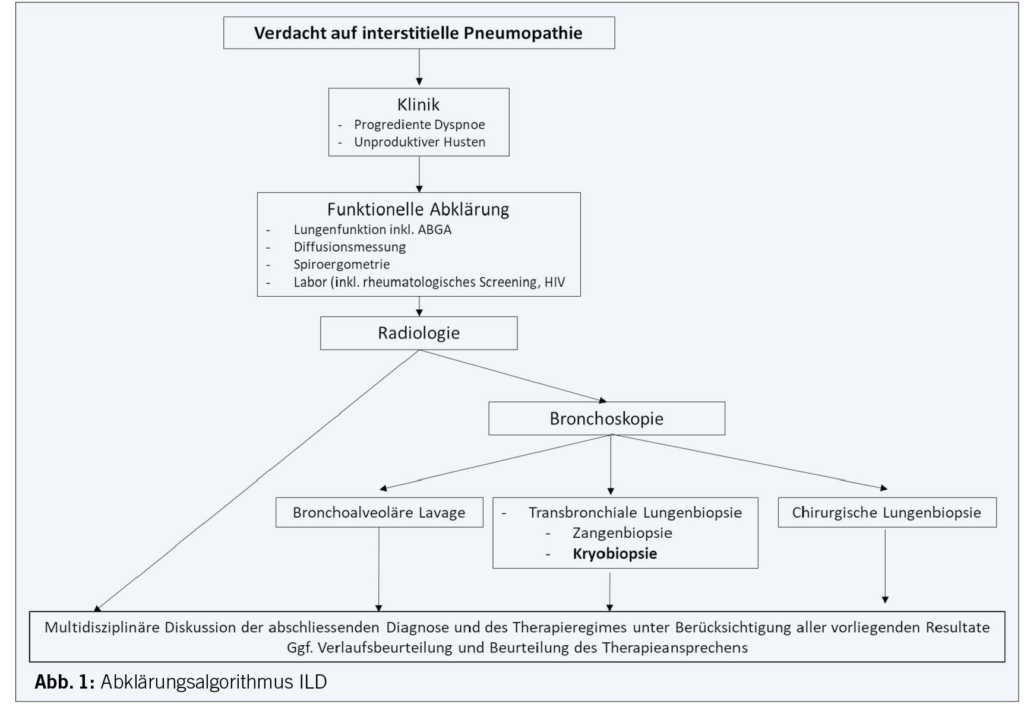
Sofern im Rahmen einer interdisziplinären Besprechung keine affirmative Diagnose unter Berücksichtigung der Klinik, des Labors und der Bildgebung zu stellen ist, wäre als nächster Schritt eine Lungenspiegelung vorgesehen (Abbildung 1).
Die Bronchoskopie erfolgt meist in Analgosedation mit z.B. Disoprivan und einem antitussiv wirkenden Hydrocodon. Diese Intervention kann ambulant erfolgen.
Die sicherste Materialentnahme erfolgt in Form einer bronchoalevolären Lavage (BAL). Hierbei wird der Alveolarraum des mittels CT vordefinierten repräsentativen Areals durch Intubation des zuführenden Subsegmentbronchus mit physiologischer Kochsalzlösung gespült (1-3x 50ml) und die Spülflüssigkeit unter direkter Absaugung asserviert. In diesem Material kann eine Zelldifferenzierung durchgeführt werden. Als Nebenwirkungen können einerseits Husten durch Reizung der Stimmbänder und des Tracheobronchialbaums sowie Fieber innert 24 Stunden nach der Intervention auftreten. Beides ist fast immer selbstlimitierend. Die definitive Diagnosestellung einer ILD ist in bestimmten Fällen, wie z.B. der eosinophilen Pneumonie möglich, und relevante Differentialdiagnosen wie ein Infekt oder eine alveoläre Hämorrhagie lassen sich ausschliessen.
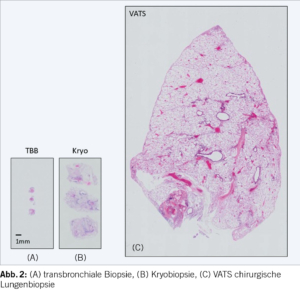
Eine Aussagekraft über strukturelle Veränderungen lässt sich mit einer transbronchialen Zangenbiopsie (TBB) erzielen. In etwa 30-40% aller unklaren ILD wird eine Histologie zur Festlegung des therapeutischen Vorgehens erforderlich. Die TBB wird unter Durchleuchtung mit einer Zange durchgeführt. Hierbei wird v.a. der zentrilobuläre Lungenbereich erreicht. Die Biopsien haben eine Kantenlänge von ca. 1x1x1mm (Abbildung 2) und es lassen sich relativ zuverlässig homogene Veränderungen detektieren, wie z.B. eine Sarkoidose, eine organisierende Pneumonie oder einen diffusen Lungenschaden im Sinne einer DAD (diffuse alveolar damage) oder einer Lymphangiosis carcinomatosa. Häufig unterliegen die Biopsien jedoch einem «sampling error» oder sind aufgrund von Quetschartefakten nur eingeschränkt aussagekräftig. Vor der Biopsieentnahme ist es notwendig, eine bestehende orale Antikoagulation leitlinienkonform aufzuheben und eine Thrombozytenzahl >50×10*9/l zu garantieren. Für Aspirin liegen bisher keine umfassenden Daten in prospektiven Studien vor, aber unter konsequenter Einnahme ergibt sich im klinischen Setting kein erhöhtes Blutungsrisiko, ähnlich wie bei den EBUS gesteuerten transbronchialen Lymphknotenbiopsien. Des Weiteren muss vor Biopsieentnahme eine relevante Druckerhöhung im kleinen «Lungen»kreislauf mit einer transthorakalen Echokardiographie ausgeschlossen werden, da dies eine absolute Kontraindikation aufgrund des hohen Blutungsrisikos darstellt. Im Rahmen der Zangenbiospien besteht ein höheres Blutungsrisiko im Vergleich zur BAL und ein geringes Pneumothoraxrisiko (1-5%), wobei dieser meist ohne weitere Interventionen vollständig regredient ist.
Als Goldstandard zur Diagnosesicherung einer ILD ist weiterhin die chirurgische Lungenbiopsie zu nennen. Damit kann repräsentatives Lungengewebe bis auf die Ebene der sekundären Lobuli analysiert werden (Abbildung 2). Die Gewebeproben können aufgrund ihrer Grösse und der fehlenden Quetschartefakte die diagnostische Sicherheit auf bis zu 95% erhöhen. Jedoch besteht ein deutlich höheres periinterventionelles Risiko bei teils schwer kranken Patienten sowie der Notwendigkeit einer mehrtätigen Hospitalisierung, was deutlich höhere Kosten nach sich zieht. Vor allem bei ILD-Patienten besteht ein hohes Risiko einer Exazerbation der Pneumopathie postoperativ. Die Inzidenz für postoperative Komplikationen wird mit 3-19% deklariert.
Als vielversprechenden semiinvasiven Kompromiss zwischen einer TBB und der chirurgischen Lungenbiopsie hat sich die transbronchiale Kryobiopsie etabliert. Diese Untersuchung kann in flexibler oder starrer Endoskopie am intubierten Patienten durchgeführt werden und liefert parenchymatöse Biopsien von mehreren Millimetern Kantenlänge (ca. 3x3x3mm) (Abbildung 2). Unter tiefer Sedierung oder in Allgemeinanästhesie wird ein Metalltip, mit einem Durchmesser von 1.9 oder 2.4mm, mit einem Guidewire über ein therapeutisches Endoskop mit grossem Arbeitskanal unter Durchleuchtung in das Zielgebiet geführt. Hierbei sollte mit einem Abstand von ca. 1-2 cm zur Pleura die Sonde positioniert werden. Je weiter peripher man sich befindet, desto grösser ist das Pneumothoraxrisiko und je weiter zentral der zu biopsierende Ort liegt, erhöht sich das Blutungsrisiko erheblich. Nach Platzierung der Sonde wird durch das Kryogas (z.B. Stickstoffdioxid, Kohlendioxid) für 5 bis 7 Sekunden Kälte appliziert. Dabei friert das Lungengewebe um die Metallspitze. Nachfolgend wird die Sonde zurückgezogen und das gefrorene Material geborgen und für die Analyse direkt in Formalin fixiert und kann dann in Paraffin eingebettet und für weitere Färbungen verarbeitet werden. Immunhistochemische Untersuchungen und molekulare Analysen können wie bei der chirurgischen Biopsie durchgeführt werden. Die Diagnosestellung kann durch die minimal invasive Methode der Kryobiopsie von 65% auf 93% gesteigert werden, wie Ravagalia an einer Kohorte von 699 Patienten nachweisen konnte. Zur Minimierung der Blutungskomplikationen durch Gefässläsionen im Kryobereich wird endobronchial ein Ballon (z.B. Fogarty) vorgelegt, welcher direkt nach der Kryobiopsie aufgeblasen wird, um das Segment zu verschliessen und eine lokale Blutstillung zu ermöglichen. Der Anteil an «sampling error» wird auf ca. 20% geschätzt, wobei es sich hierbei vor allem um Material mit unzureichendem alveolären Parenchymanteil oder ausschliesslich um Bronchialwandanteile handelt. Daher wird in den aktuellen Leitlinien eine Entnahme von drei (bis max. fünf) Kryobiopsien empfohlen. Die transbronchiale Kryobiopsie sollte an Zentren mit Expertise in dieser Technik und mit intensivmedizinischem Background erfolgen.
Als Komplikationen bei der transbronchialer Kryobiopsie treten gehäuft Blutungen und Pneumothoraces auf. Als milde Blutung wird ein Ereignis angesehen, welches allein durch Absaugen behoben werden kann. Eine moderate Blutung liegt vor, wenn die zusätzliche Nutzung von vasopressiver Substanzen endobronchial (Glypressin, Adrenalin, Terlipressin etc.) oder eine manuelle Subsegmentbronchusobstruktion durch einen Ballon/ Bronchusblocker erforderlich wird. Schwere Blutungskomplikationen werden in weniger als 1% aller Interventionen beschrieben und bedürfen dann einer intensivpflichtigen Überwachung.
Zum Ausschluss eines Pneumothorax erfolgt innert 3-12 Std. postinterventionell ein Röntgen Thorax. Prinzipiell ist das Pneumothorax-Risiko mit 20-30% deutlich höher als bei den regulären transbronchialen Zangenbiopsien (in der Literatur grosse Spannbreite von 1-30%). Das Risiko steigt mit Schweregrad der Fibrose und mit zunehmender Restriktion.
Bei pulmonalen endstage Patienten mit sehr fortgeschrittener Grunderkrankung, bei einer bestehenden pulmonalen Hypertonie oder einer zwingenden Indikation zur Fortführung einer konsequenten Antikoagulation stellt die Kryobiopsie keine Alternative dar.
Als Kontraindikationen sind neben Gerinnungsstörungen, eine Thrombozytenzahl <50×10*9/l und die kontinuierliche Einnahme von Plättchenaggregationshemmern/ Antikoagulantien (z.B. Clopidogrel, NOAK, Marcoumar etc.) zu erwähnen. Kontrainduziert sind ein systolischer pulmonal-arterieller Druck von 50mmHg, eine Diffusion <35% Soll, eine FVC von <50% und eine schwere Hypoxämie <55mmHg unter 2 lpm Sauerstoffgabe.
Konklusion:
Das Spektrum der interventionellen Möglichkeiten der Abklärung einer unklaren interstitiellen Pneumopathie hat sich um die Kryobiopsie erweitert, womit eine rasche histologische Diagnosesicherung ermöglicht wird.
Prinzipiell ist bei einer intraalveolären oder zentrilobulären Distribution der auffälligen Befunde weiterhin die BAL oder die TBB der erste diagnostische Schritt, da es sich hierbei eher um homogen verteilte Pathologien handelt, bei denen die Treffsicherheit hoch ist, wie z.B. bei akuten/ chronischen Infekten, eosinophiler Pneumonie, Sarkoidose, alveolärer Hämorrhagie, organisierende Pneumonie etc.
Befinden sich die Befunde eher peripher oder im Bereich der Sekundärlobuli ist als initialer Abklärungsschritt die transbronchiale Kryobiopsie indiziert. Prinzipiell bestehen die gleichen Indikationen zur Durchführung wie bei einer chirurgischen Lungenbiopsie. V.a. bei diffusen Lungenparenchymerkrankungen ist eine Kryobiopsie eine risikoärmere Möglichkeit der Gewebesicherung.
Zusammenfassend kann durch die Etablierung der Kryobiopsie zusätzlich zur klassischen bronchoalveolären Lavage in der invasiven endoskopischen Diagnostik die diagnostische Treffsicherheit auf bis zu 80% gesteigert werden. In einer retrospektiven Analyse von Hostettler et al. konnte gezeigt werden, dass die Kryobiopsie die Notwendigkeit der chirurgischen Lungenbiopsie vermindern konnte. Dabei ergab sich, dass in 45% der Fälle durch die Histologie allein eine Diagnose gestellt werden konnte und in weiteren 25% wurden die histologischen Befunde durch Wertung eines multidisziplinären Gremiums aus Pathologen, Pneumologen, Radiologen und Rheumatologen zu einer affirmativen Diagnose geleitet und auf eine chirurgische Intervention konnte verzichtet werden.
Die Interdisziplinarität ist ein wichtiger Bestandteil der Konsensfindung bezüglich definitiver Diagnose und Therapieetablierung. Neben der klinischen Beurteilung benötigt es die umfassende fachkompetente Beurteilung der radiologischen und pathologischen Seite sowie der Rheumatologen und ggf. anderer Fachspezialisten wie Immunologen oder Hämatologen. Solche Gremien sind feste Bestandteile an den Zentrumsspitälern für ILD-Erkrankungen und können direkt für eine Beurteilung von externen Zuweisern angefragt werden und stehen für Networking gern zur Verfügung.
Dr. Kathleen Jahn, kathleen.jahn@usb.ch
Kaderärztin
Universitätsspital Basel
Klinik für Pneumologie
Petersgraben 4
4031 Basel
Interessenskonflikte: Die Autorin hat keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
Universitätsspital Basel
Klinik für Pneumologie
Petersgraben 4
4031 Basel
Die Autorin hat keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
Literatur:
1. Hetzel J., Monaldo F., Ravaglia C. et al. Transbronchial Cryobiopsies for the Diagnosis of Diffuse Parenchymal Lung Disease: Expert Statement from the Cryobiopsy Working Group on Safety and Utility and a Call for Standardization of the Procedure. Respiration 2018.2018;95(3):188-200.
2. Korevaar D.A., Colella S., Fally M. et al. European Respiratory Society Guidelines on Transbronchial Cryobiopsy in the Diagnosis of Interstital Lung Diseases. Eur Respir J 2022; 60:2200425
3. Richeldi L., Du Bois R.M., Rhagu G et al. Efficacy and Safety of Nintedanib in idiopathic Pulmonary Fibrosis. N Engl J Med 2014;370:2071-82.
4. Hetzel J., Eberhardt R., Petermann C. et al. Bleeding Risk of Transbronchial Cryobiopsy compared to Transbronchial Forceps Biopsy in Interstitial Lung Disease – a Prospective, Randomized, Multicentre Cross-over Trial. Respir Res. 2019;20:140.
5. Ravaglia C., Athol W., Tomassetti S. et al. Diagnostic Yield and Risk/ Benefit analysis of Transbronchial Lung cryobiopsy in Diffuse Parenchymal Lung Disease: a Large Cohort of 699 Patients. BMC Pulm Med 2019;19:16.
6. Rodrigues I., Gomes R.E., Coutinho L.M. et al. Diagnostic Yield and Safety of Transbronchial Lung Cryobiopsy and Surgical Lung Biopsy in Interstitial Lung Disease: A Systematic Review and Meta-Analysis. Eur Respir Rev. 2022 Dec 31;31(166):210280.
7. Hostettler K.E., Tamm M., Bubendorf L. et al. Integration of Transbronchial Cryobiopsy into Multidisciplinary Board Decision: A Single Center Analysis of one hundred Consecutive Patients With Interstitial Lung Disease. Respir Res. 2021; 22: 228.
8. Troy LK., Grainge C., Corte T. et al. Cryobiopsy versus Open Lung Biopsy in the Diagnosis of Interstitial Lung Disease (COLDICE): Protocol of a Multicentre Study. BMJ Open Respir Res. 2019; 6(1):e000443
Therapeutische Umschau
- Vol. 81
- Ausgabe 1
- Februar 2024