- Nebenwirkungen von Onkologika bei älteren Patienten
Krebs ist eine Erkrankung des Alters mit ungefähr 50 % der neuen Krebsfälle die beim Menschen im Alter von 65 Jahren oder älter auftreten, und diese Zahl wird voraussichtlich bis 2030 auf 58 % steigen. Die Chemotherapie ist nach wie vor ein Standardbestandteil der Krebsbehandlung, neben den neuen Therapien wie Immuntherapie und gezielten Therapien. Allerdings besteht bei älteren Patienten im Vergleich zu jüngeren Erwachsenen ein erhöhtes Risiko für eine Chemotherapieinduzierte-Toxizität. Verschiedene pharmakologische Parametern müssen berücksichtigt werden bei der onkologischen Behandlung von älteren Patienten.
Die Beurteilung von Altersbedingten Veränderungen durch eine geriatrische Untersuchung ist vor Behandlungsbeginn einer
Chemotherapie sehr wichtig. Mehrere Studien haben gezeigt, dass mit Hilfe von Geriatric Assessment-Variablen, ältere Erwachsene identifiziert werden können, bei denen das Risiko einer schweren Toxizität durch die Chemotherapie am höchsten ist.
Orale onkologische Therapien stellen mehrere Vorteile dar. Sie enthalten aber auch Nachteile, vor allem beim älteren Patienten, die zu einer schlechteren Effizienz oder früherem Therapieabbruch führen können.
Trotz der physiologischen Phänomene der Immunoseneszenz und des Inflammaging, die Daten, die aus Subgruppenanlaysen von Metaanalysen hauptsächlich kommen, zeigen tendenziell, dass eine Immuntherapie auch bei älteren Patienten wirksam und gut verträglich ist.
Einleitung
Krebs ist eine Erkrankung des Alters mit ungefähr 50 % der neuen Krebsfälle die beim Menschen im Alter von 65 Jahren oder älter auftreten, und diese Zahl wird voraussichtlich bis 2030 auf 58 % steigen.(1) Obwohl die meisten Krebserkrankungen bei älteren Menschen auftreten, werden neue Krebsmedikamente hauptsächlich zugelassen auf der Grundlage von Daten die bei jüngeren Menschen oder einer Auswahl gesunder älterer Menschen ohne Komorbiditäten oder geriatrische Beeinträchtigungen untersucht werden.
Die Chemotherapie ist nach wie vor ein Standardbestandteil der Krebsbehandlung, neben den neuen Therapien wie Immuntherapie und gezielten Therapien. Allerdings besteht bei älteren Patienten im Vergleich zu jüngeren Erwachsenen ein erhöhtes Risiko für eine Chemotherapieinduzierte-Toxizität.(2) Darüber hinaus wird älteren Erwachsenen seltener eine Chemotherapie angeboten, da sie Bedenken hinsichtlich ihrer Fähigkeit haben, die Behandlung zu überstehen.(3)
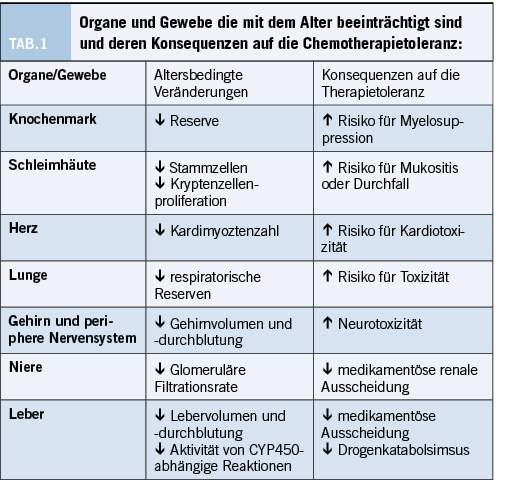
Wichtig ist, dass sich die Pharmakologie von Krebsmedikamenten bei jüngeren und älteren Menschen aufgrund von Veränderungen in der Zusammensetzung der Körperflüssigkeiten, dem Leberstoffwechsel, der renalen und hepatischen Ausscheidung und der Pharmakodynamik unterscheiden kann. (4)
Pharmakokinetik bei älteren Leuten
Verschiedene pharmakologische Parametern müssen berücksichtigt werden bei der onkologischen Behandlung von älteren Patienten.
Die folgenden gelisteten Parametern können einen Einfluss in der onkologischen Behandlung haben:
– Orale Absorption
– Verteilungsvolumen
– Körperzusammensetzung
– Serum Albumin
– Hemoglobin
– Lebermetabolismus
– Renale Ausscheidung
– Biliäre Ausscheidung
– Medikamentöse Interaktionen
– Pharmakodynamik auf die zelluläre Ebene
(5) Das Verteilungsvolumen (Vv) ist Funktion der Körperzusammensetzung, des Serumproteinprofils und der Blutzellen (z. B. Erythrozyten). Bis zum Alter von 85 Jahren kommt es in der Regel zu einem fortschreitenden Anstieg des Körperfetts und einem Rückgang des Körperwassers. Es wird geschätzt, dass der Fettgehalt im Alter zwischen 25 und 75 Jahren von 15 % auf 30 % des Körpergewichts ansteigt und der intrazelluläre Wassergehalt von 42 % auf 33 % abnimmt.[4] Diese Veränderungen neigen dazu, das Verteilungsvolumen von wasserlöslichen Arzneimitteln wie Anthrazyklinen zu verringern und dem Verteilungsvolumen von fettlöslichen Verbindungen wie Carmustin (BCNU) zu erhöhen. Auch die Leberfunktion wird durch das Alter verändert: Es wurde über eine Abnahme der Lebergrösse (um 18–44 %), des Blutflusses, der Albuminproduktion und der CYP-Funktion berichtet. Die abnehmende renale Ausscheidung von Arzneimitteln ist wegen der glomerulären Veränderung die am besten vorhersehbare pharmakokinetische Veränderung. Die Filtrationsrate (GFR) nimmt ab einem Alter von 40 Jahren kontinuierlich mit dem Alter um etwa 1 ml/min pro Jahr ab.
Geriatrische Evaluation
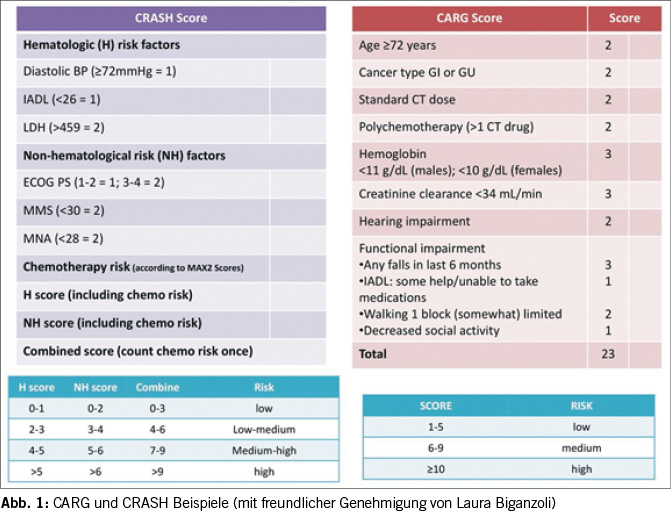
Chemotherapie-Toxizität Prädiktoren
Uebersicht verschiedener Chemotherapien bei betagen Karzinompatienten (9)
Alkylanzien
Intravenöse Fluoropyrimidine
Platine
Anthrazykline
Antimikrotubuli
Mehrere Studien haben die Toxizität von Docetaxel bei älteren Patienten untersucht (19). Schlussendlich gibt es keine klaren Daten um Dosismodifikationen rein auf dem Alter basierend zu unterstützen; allerdings mit dem Wissen, dass die 3-wöchentliche Verabreichung mehr hämatotoxisch istund dass bei älteren Patienten die Knochenmarksreserve physiologisch reduziert ist.
Zytidine Analoga
– Gemcitabine zeigt generell als Monotherapie minimale Toxizität bei älteren Patienten. (20)
Antimetaboliten
– Pemetrexed soll mit Vorsicht bei älteren Patienten mit beeinträchtigter Nierenfunktion verabreicht werden da das Riskio einer Hämatotoxizität erhöht sein kann.
Adhärenz zu oralen Medikamenten
Orale onkologische Therapien stellen mehrere Vorteile dar. Sie ermöglichen weniger klinische Termine, sind weniger invasiv und verbessern die Patientenautonomie. Sie enthalten aber auch Nachteile, vor allem beim älteren Patienten, die zu einer schlechteren Effizienz oder früherem Therapieabbruch führen können.
Es existieren verschiedene Faktoren die die Adhärenz zu oralen Therapien bei älteren Patienten beeinflussen(21):
– Patientenbezogene Faktoren: Alter, Gender, Gesundheitsstatus
– Alterspezifische Faktoren: kognitive Defizite, visuelle oder auditive Beeinträchtigungen, Komorbiditäten, Polypharmazie
– Sozioökonomische Situation: soziale Situation, caregiver-Qualität, familiäre Unterstützung
– Krankheitsbedingte Faktoren: Krankheitschwere, unkontrollierte Beschwerden, psychologische Komponente
– Therapiebezogene Faktoren: Toxizität der Therapie, Therapiedauer, Wirksamkeit
– Health-care Team Faktoren: Medikamentenverfügbarkeit und –versorgung, Patient-Anbieter Beziehung, Kommunikationsbarriere, unzureichende oder unklare Arzneimittelinformation
Bei schlechterer Effizienz, früherem Abbruch oder erhöhter Toxizität ist Non-Adherenz mit einer erhöhten Mortalität assoziiert.
Verschiedene Interventionen wie Patientenanweisungen mit klaren und schriftlichen Instruktionen, Caregiverimplikation, soziale Unterstützung, kontinuierliche Überwachung und Bewertung durch das medizinische Betreuungsteam ermöglichen die Therapieadhärenz zu verbessern.
Toxizität der Immuntherapie bei älteren Patienten (22)
Immunbedingte Nebenwirkungen können bei älteren Menschen eine grössere Herausforderung darstellen aufgrund verminderter Funktionsreserve und altersbedingten Komorbiditäten.(23)
Trotz der physiologischen Phänomene der Immunoseneszenz und des Inflammaging, die Daten, die aus Subgruppenanlaysen von Metaanalysen hauptsächlich kommen, zeigen tendenziell, dass eine Immuntherapie auch bei älteren Patienten wirksam und gut verträglich ist.
In der klinischen Praxis sind Checkpoint-Inhibitoren daher eine gute Behandlungsmöglichkeit, auch für ältere Patienten. (24)
HFR Freiburg – Kantonsspital
Chemin des Pensionnats 2-6
1752 Villars-sur-Glâne
verene.dogoud-chauvin@h-fr.ch
Dr. med. Dougoud-Chauvin hat Travel Grants von Amgen erhalten.
1. Pilleron S, Sarfati D, Janssen-Heijnen M, Vignat J, Ferlay J, Bray F, et al. Global cancer incidence in older adults, 2012 and 2035: A population-based study. International Journal of Cancer. 2019;144(1):49‑58.
2. Hurria A, Mohile S, Gajra A, Klepin H, Muss H, Chapman A, et al. Validation of a Prediction Tool for Chemotherapy Toxicity in Older Adults With Cancer. J Clin Oncol. 2016;34(20):2366‑71.
3. Hurria A, Wong FL, Villaluna D, Bhatia S, Chung CT, Mortimer J, et al. Role of Age and Health in Treatment Recommendations for Older Adults With Breast Cancer: The Perspective of Oncologists and Primary Care Providers. JCO. 2008;26(33):5386‑92.
4. Wildiers H, de Glas NA. Anticancer drugs are not well tolerated in all older patients with cancer. The Lancet Healthy Longevity. 2020;1(1):e43‑7.
5. Pharmacology of Anticancer Drugs in the Elderly Population | SpringerLink [Internet]. [2023]. Disponible sur: https://link.springer.com/article/10.2165/ 00003088-200342140-00003
6. Flannery MA, Culakova E, Canin BE, Peppone L, Ramsdale E, Mohile SG. Understanding Treatment Tolerability in Older Adults With Cancer. JCO. 2021;39(19):2150‑63.
7. Adjei A, Buckner JC, Cathcart-Rake E, Chen H, Cohen HJ, Dao D, et al. Arti Hurria, M.D.: A tribute to her shining legacy in the Alliance for Clinical Trials in Oncology. J Geriatr Oncol. 2020;11(2):179‑83.
8. Extermann M, Boler I, Reich RR, Lyman GH, Brown RH, DeFelice J, et al. Predicting the risk of chemotherapy toxicity in older patients: the Chemotherapy Risk Assessment Scale for High-Age Patients (CRASH) score. Cancer. 2012;118(13):3377‑86.
9. Lichtman SM, Wildiers H, Chatelut E, Steer C, Budman D, Morrison VA, et al. International Society of Geriatric Oncology Chemotherapy Taskforce: Evaluation of Chemotherapy in Older Patients—An Analysis of the Medical Literature. JCO. 2007;25(14):1832‑43.
10. Wildiers H, Highley MS, de Bruijn EA, van Oosterom AT. Pharmacology of anticancer drugs in the elderly population. Clin Pharmacokinet. ;42(14):1213‑42.
11. Grem JL, Takimoto CH, Multani P, Chu E, Ryan D, Chabner BA, et al. Antimetabolites. Cancer Chemother Biol Response Modif.;18:1‑38.
12. Cassidy J, Twelves C, Cameron D, Steward W, O’Byrne K, Jodrell D, et al. Bioequivalence of two tablet formulations of capecitabine and exploration of age, gender, body surface area, and creatinine clearance as factors influencing systemic exposure in cancer patients. Cancer Chemother Pharmacol.;44(6):453‑60.
13. Feliu J, Salud A, Escudero P, Lopez-Gómez L, Bolaños M, Galán A, et al. XELOX (capecitabine plus oxaliplatin) as first-line treatment for elderly patients over 70 years of age with advanced colorectal cancer. Br J Cancer. 2006;94(7):969‑75.
14. Yamamoto N, Tamura T, Maeda M, Ando M, Shinkai T, Eguchi K, et al. The influence of ageing on cisplatin pharmacokinetics in lung cancer patients with normal organ function. Cancer Chemother Pharmacol. 1995;36(2):102‑6.
15. Donahue A, McCune JS, Faucette S, Gillenwater HH, Kowalski RJ, Socinski MA, et al. Measured versus estimated glomerular filtration rate in the Calvert equation: influence on carboplatin dosing. Cancer Chemother Pharmacol. 2001;47(5):373‑9.
16. Pinder MC, Duan Z, Goodwin JS, Hortobagyi GN, Giordano SH. Congestive heart failure in older women treated with adjuvant anthracycline chemotherapy for breast cancer. J Clin Oncol. 2007;25(25):3808‑15.
17. Loadman PM, Bibby MC. Pharmacokinetic drug interactions with anticancer drugs. Clin Pharmacokinet. 1994;26(6):486‑500.
18. Green MC, Buzdar AU, Smith T, Ibrahim NK, Valero V, Rosales MF, et al. Weekly paclitaxel improves pathologic complete remission in operable breast cancer when compared with paclitaxel once every 3 weeks. J Clin Oncol. 2005;23(25):5983‑92.
19. Massacesi C, Marcucci F, Boccetti T, Battelli N, Pilone A, Rocchi MBL, et al. Low dose-intensity docetaxel in the treatment of pre-treated elderly patients with metastatic breast cancer. J Exp Clin Cancer Res. 2005;24(1):43‑8.
20. Shepherd FA, Abratt RP, Anderson H, Gatzemeier U, Anglin G, Iglesias J. Gemcitabine in the treatment of elderly patients with advanced non-small cell lung cancer. Semin Oncol. avr 1997;24(2 Suppl 7):S7-50-S7-55.
21. Mislang AR, Wildes TM, Kanesvaran R, Baldini C, Holmes HM, Nightingale G, et al. Adherence to oral cancer therapy in older adults: The International Society of Geriatric Oncology (SIOG) taskforce recommendations. Cancer Treat Rev. 2017;57:58‑66.
22. Rhyner Agocs G, Dougoud-Chauvin V, Betticher D. Immunothérapie: aussi chez le patient âgé ? Rev Med Suisse. 2019;660:1512‑5.
23. Extermann M. Interaction between comorbidity and cancer. Cancer Control. 2007;14(1):13‑22.
24. Haanen J, Obeid M, Spain L, Carbonnel F, Wang Y, Robert C, et al. Management of toxicities from immunotherapy: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-upI. Annals of Oncology. 2022;33(12):1217‑38.
Therapeutische Umschau
- Vol. 80
- Ausgabe 8
- Oktober 2023