- Osteoporosetherapie – Update 2025, Teil 2: Sequenzielle Osteoporosetherapie
Einführung
Durch die Verfügbarkeit verschiedener, durch unterschiedliche Wirkmechanismen gekennzeichnete Präparate zur Osteoporosetherapie haben sich die Behandlungsstrategien in den letzten Jahren wesentlich verändert. Aufgrund potenzieller Behandlungsrisiken unter langjähriger Monotherapie und der Tatsache, dass die bei Patientinnen mit hohem Frakturrisiko eingesetzten osteoanabolen Therapien zeitlich limitiert sind (12–24 Monate), kommen heute vermehrt sequenzielle Therapiestrategien zum Einsatz.
Um die möglichen Auswirkungen bestimmter Behandlungssequenzen zu verstehen (Tab. 1 und Tab. 2), ist es entscheidend, die Folgen des Absetzens von Medikamenten zu vergleichen. Bedingt durch deren hohe Knochenaffinität und damit einhergehenden residuellen Wirkung kann nach Absetzen von Bisphosphonaten der antiresorptive Behandlungseffekt (inkl. der Frakturrisikoreduktion) zumindest über einige Jahre bestehen bleiben (1, 2). Im Gegensatz dazu führt ein Absetzen von Denosumab, welches als monoklonaler Antikörper für die Dauer der Behandlung wirksam bleibt, zu einem raschen Wirkverlust bzw. zu einer raschen Stimulation der Osteoklasten-vermittelten Knochenresorption (3). Dieses sog. Rebound-Phänomen geht mit einem akzelerierten Knochenmassenverlust einher und kann zum Auftreten multipler vertebraler Frakturen führen (4–6).
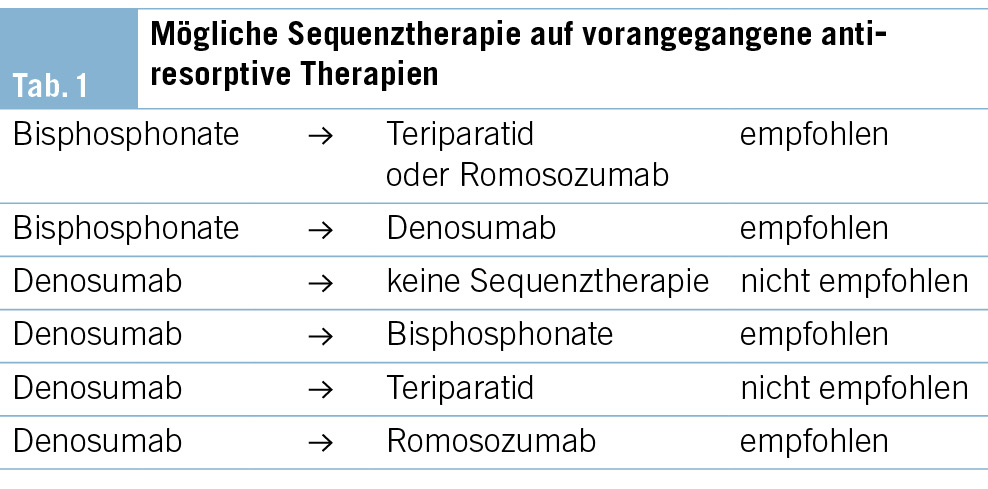
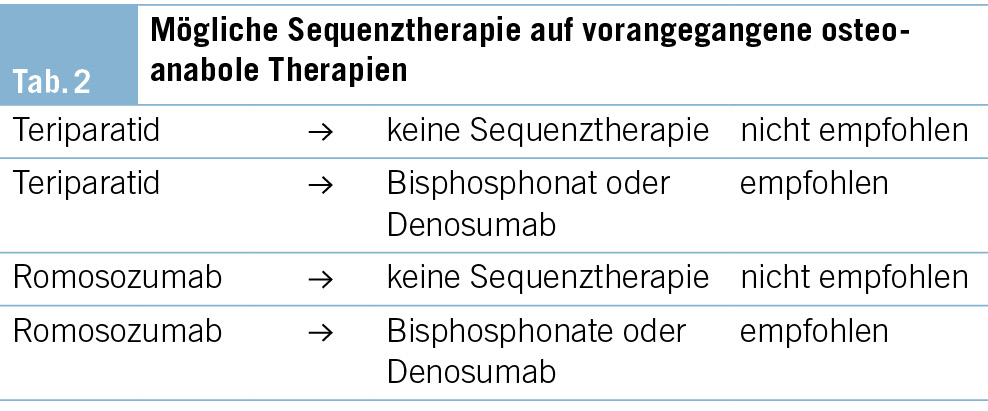
Nach Absetzen knochenanaboler Therapien geht der neu gewonnene Knochen (v.a. Osteoid) ohne eine Folgetherapie durch Ausbleiben einer genügenden Mineralisation wieder verloren. Um eine sekundäre Mineralisation zu fördern, ist daher eine sequenzielle antiresorptive Behandlung notwendig (7).
Im vorangegangenen Artikel haben wir die Wirkmechanismen und die klinische Wirksamkeit antiresorptiv und osteoanabol wirkender Präparate zusammengefasst. In diesem Übersichtsartikel soll auf den Stellenwert der verschiedenen Behandlungssequenzen in der Osteoporosetherapie eingegangen werden.
Sequenzieller Einsatz von antiresorptiven Präparaten nach antiresorptiver Therapie
Unter fortgesetzter Behandlung mit Östrogenen kann ein knochenerhaltender und frakturreduzierender Effekt beobachtet werden. Werden Östrogene abgesetzt, nimmt der Knochenumsatz zu, die Knochendichte sinkt, und der Frakturschutz nimmt ab. Ist ein antiresorptiver Effekt weiterhin notwendig, können Patientinnen entweder auf Raloxifen oder Bisphosphonate umgestellt werden. Wie eingehend erläutert, stellt Raloxifen ein ideales Präparat zur Verhinderung des Mineralgehaltsverlustes insbesondere bei jüngeren postmenopausalen Frauen mit einem familiären Mammakarzinomrisiko dar (8). Es bleibt zu beachten, dass gemäss Studienlage Raloxifen v.a. das vertebrale Frakturrisiko senkt. Ist eine sequenzielle Therapie bei Frauen über 60 Jahren notwendig, insbesondere wenn auch nicht vertebrale Frakturen verhindert werden sollen, ist eine antiresorptive Behandlung mit einem Bisphosphonat (Alendronat, Zoledronat) zu favorisieren.
Innerhalb der Gruppe der Antiresorptiva ist ein Wechsel von einem oralen auf ein intravenöses Bisphosphonat indiziert, wenn die orale Therapie nicht toleriert wird oder wenn die Adhärenz oder intestinale Absorption ungenügend ist (9, 10). Dies kann u.a. mit der Bestimmung der Knochenumbauparameter im Serum (CTX oder P1NP) eruiert werden. Wenn mit oralen oder parenteralen Bisphosphonaten eine Therapiedauer von 5–6 Jahren erreicht ist, kann bei Personen mit mässig erhöhtem Frakturrisiko eine Therapiepause («drug holiday») erwogen werden, da dann keine weitere Zunahme der Knochendichte bzw. keine zusätzliche Frakturreduktion erwartet werden kann.
Ausserdem führen Bisphosphonate in der Langzeitanwendung (> 5–7 Jahre) zu seltenen, aber schweren Nebenwirkungen wie atypischen Femurfrakturen (11, 12). Bei Personen mit hohem Frakturrisiko sollte die Therapie weitergeführt oder ein Wechsel auf eine osteoanabole Therapie bzw. auf Denosumab erwogen werden.
Nach Denosumab ist zwingend eine sequenzielle Bisphosphonattherapie angezeigt. Aufgrund der reversiblen Wirkung und des oben erwähnten Rebound-Effektes sollte Denosumab nicht ohne Nachbehandlung abgesetzt werden. Zur Verhinderung oder zumindest Abschwächung dieses Rebounds nach Absetzen von Denosumab wird der Einsatz von Bisphosphonaten empfohlen, und Zoledronat (erste Infusion 6 Monate nach der letzten Denosumab-Spritze) ist aktuell das am besten untersuchte Medikament in dieser Situation (6, 13). Möglicherweise kann auch Alendronat als Anschlusstherapie verwendet werden, sofern die Adhärenz gegeben ist. In diesem Fall empfehlen wir den Beginn bereits 5 Monate nach der letzten Denosumab-Injektion. Es gelingt nicht bei allen Personen mit Denosumab, diesen Rebound mit einer einzelnen Zoledronat-Infusion zu verhindern. Insbesondere bei einer Langzeitbehandlung von über 3 Jahren wird nach Absetzen von Denosumab und Umstellung auf eine Bisphosphonattherapie ein erhöhtes Risiko für einen Knochendichteverlust und, wenn auch seltener, für Wirbelfrakturen beobachtet (14, 15). Im klinischen Alltag versucht man, mit dreimonatlicher Bestimmung der Knochenumbauparameter (CTX oder P1NP) den Rebound frühzeitig zu erkennen und diesem mit allenfalls mehreren Zoledronat-Infusionen innerhalb eines Jahres entgegenzuwirken (14, 16). Bei betagten Personen oder bei denjenigen, bei denen eine Umstellung auf eine Bisphosphonattherapie nicht möglich ist (z.B. schwere Niereninsuffizienz), kann Denosumab bis ans Lebensende eingesetzt werden, wobei auf eine strikte Therapieadhärenz geachtet werden muss.
Sequenzieller Einsatz von antiresorptiven Präparaten nach osteoanaboler Therapie
Wie vorangehend erwähnte «head-to-head»-Studien bei Patienten mit hohem Frakturrisiko zeigen, reduzieren osteoanabole Präparate (VERO, Teriparatid; ARCH, Romosozumab) das Risiko vertebraler und z.T. nicht vertebraler Frakturen stärker als Risedronat bzw. Alendronat (17, 18). Entsprechend sollten osteoanabol wirkende Medikamente als Erstlinientherapie bei Patienten mit sehr hohem Risiko eingesetzt werden (19). Einschränkend ist festzuhalten, dass in der Schweiz Teriparatid nur als Zweitlinientherapie bei Patienten mit inzidenten Wirbelkörperfrakturen unter mindestens 6-monatiger antiresorptiver Vortherapie kassenpflichtig ist. Eine Erstlinienbehandlung mit Teriparatid wird bei klinischer Begründung im Einzelfall jedoch ebenfalls vergütet. Im Gegensatz dazu ist Romosozumab in der Schweiz bei Patientinnen mit imminentem bzw. sehr hohem Frakturrisiko zur Erstlinienbehandlung zugelassen.
Weil osteoanabole Präparate entsprechend der Limitatio in der Regel nur für 12 bis 24 Monate eingesetzt werden und das Potenzial osteoanaboler Medikamente auf den Mineralgehaltsgewinn und die Frakturrisikoreduktion mit einer anschliessenden antiresorptiven Therapie aufrechterhalten werden kann, gehören antiresorptive Folgetherapien (Bisphosphonate, Denosumab) zum integralen Behandlungskonzept bei osteoanabol vorbehandelten Patienten. Beispielsweise konnten Black et al. den Nutzen einer sequenziellen Alendronat-Therapie nach vorangegangener Parathormontherapie aufzeigen: Während der Mineralgehalt nach Umstellung einer 12-monatigen Behandlung mit Parathormon auf Placebo abnahm, konnte dieser Verlust durch eine Folgetherapie mit Alendronat verhindert werden bzw. der Mineralgehalt über die folgenden 12 Monate noch weiter verbessert werden (20). In ähnlicher Weise zeigte sich in der DATA-Switch-Studie ein günstiger mineralgehaltsaufbauender Effekt einer Folgetherapie mit Denosumab nach vorangegangener 24-monatiger Therapie mit Teriparatid (21).
In der FRAME-Studie, in der postmenopausale Frauen mit fortgeschrittener Osteoporose ein Jahr lang Romosozumab und dann ein weiteres Jahr Denosumab erhielten, war das vertebrale und nicht vertebrale Frakturrisiko gegenüber Placebo reduziert. Die Reduzierung des Frakturrisikos wurde während des zweiten Folgejahres mit Denosumab nachhaltig fortgesetzt (22). Die Folgetherapie mit dem antiresorptiv wirkenden Denosumab verhinderte den zu erwartenden Mineralgehaltsverlust, was auch in einer anderen Studie mit einer Bisphosphonatsequenztherapie (Zoledronat) gezeigt werden konnte (23). In der ARCH-Studie wurde dieser nachhaltige Effekt auch auf die Reduktion des Frakturrisikos in Patientinnen, welche nach einer Behandlung mit Romosozumab eine Folgetherapie mit Alendronat erhielten, bestätigt (18).
Sequenzieller Einsatz von osteoanabolen Präparaten nach antiresorptiver Therapie
Die meisten Studien, welche die Wirkung von osteoanabolen Präparaten nach vorangegangener antiresorptiver Therapie untersucht haben, sind durch kleine Untersuchungsgruppen und Bestimmung des Mineralgehaltsverlaufes ohne Frakturdaten charakterisiert.
Im klinischen Alltag ist dies eine nicht seltene Konstellation, beispielsweise wenn Patientinnen unter einer Bisphosphonattherapie neue Frakturen erleiden. Im Falle inzidenter vertebraler Frakturen entspricht diese Konstellation in der Schweiz einer Zweitlinientherapie mit Teriparatid.
Interessanterweise ist die Wirkung von osteoanabolen Medikamenten von den spezifischen Eigenschaften des zuvor verwendeten antiresorptiv wirkenden Medikamentes abhängig. Bei Patientinnen, die mit Raloxifen (24) oder Risedronat (25) vorbehandelt wurden, führte Teriparatid zu einem Mineralgehaltsanstieg, der mit dem für therapienaive Patienten vergleichbar war. Im Gegensatz dazu war eine Vorbehandlung mit Alendronat mit einem geringeren Anstieg der Knochendichte assoziiert (26). Gemäss der DATA-Switch-Studie kam es bei Patienten, welche im Gegensatz dazu mit Denosumab vorbehandelt waren, unter der nachfolgenden Sequenztherapie mit Teriparatid zu einem vorübergehenden Mineralgehaltsverlust, vorwiegend am Schenkelhals (21).
Ebenfalls scheint eine Vorbehandlung mit antiresorptiv wirkenden Präparaten den Effekt von Romosozumab abzuschwächen. Verglichen zu therapienaiven Patienten führte eine Vorbehandlung mit Alendronat oder Denosumab bei postmenopausalen Frauen mit Osteoporose zu einem geringeren Mineralgehaltsanstieg unter Romosozumab (27, 28).
Dennoch kann gefolgert werden, dass für Hochrisikopatienten, die unter einer antiresorptiven Therapie eine vertebrale oder nicht vertebrale Fraktur erleiden oder eine anhaltend niedrige Knochendichte aufweisen, die Umstellung auf Romosozumab zu einer Verbesserung der skelettalen Widerstandskraft führt, was für eine Folgetherapie mit Teriparatid nicht vollumfänglich gezeigt ist.
Kombinationstherapien
Studien zur Untersuchung der Wirkung einer kombinierten Behandlung mit antiresorptiv und osteoanabol wirkenden Präparaten haben inkonklusive Resultate ergeben. Beispielsweise konnte in der Behandlung von rhPTH(1–84) in Kombination mit Alendronat kein stärkerer Effekt auf den Knochenmineralgehalt beobachtet werden als mit den entsprechenden Monotherapien (20).
Im Gegensatz dazu führte bei Frauen mit postmenopausaler Osteoporose eine Kombinationsbehandlung von Zoledronat und Teriparatid zu einem grösseren und rascheren Mineralgehaltszuwachs als die jeweiligen Monotherapien, wenn sowohl die Wirbelsäule als auch die Hüfte berücksichtigt wurde (29). Leder et al. konnten in einer randomisierten Studie den superioren Effekt einer Kombinationsbehandlung von Teriparatid mit Denosumab bei postmenopausalen Frauen mit hohem Frakturrisiko nachweisen. Der Mineralgehaltsgewinn nach einer 12-monatigen Behandlung war stärker als die jeweilige Therapie mit Teriparatid bzw. Denosumab (30).
Es bleibt aber festzuhalten, dass die genannten Studien den Knochenmineralgehalt als Surrogatmarker der Knochenwiderstandsfähigkeit untersucht haben. Studien zur Beurteilung der Wirksamkeit einer kombinierten antiresorptiven und osteoanabolen Therapie auf das Frakturrisiko liegen nicht vor (31). Entsprechend ist der Einsatz einer Kombinationsbehandlung im Sinne einer Einzelfallentscheidung für Patienten mit sehr hohem Frakturrisiko reserviert.
Klinik für Endokrinologie, Diabetologie und Metabolismus
Universitätsspital Basel
Endonet Praxis und Osteologisches Universitätsforschungszentrum DVO
Aeschenvorstadt 57
4051 Basel
christian.meier@unibas.ch
Die Autorenschaft hat keine Interessenkonflikte im Zusammenhang mit diesem Artikel deklariert.
1. Reid IR, Horne AM, Mihov B, Bava U, Stewart A, Gamble GD. Duration of fracture prevention after zoledronate treatment in women with osteopenia: observational follow-up of a 6-year randomised controlled trial to 10 years. The lancet Diabetes & endocrinology. 2024;12(4):247-56.
2. Dennison EM, Cooper C, Kanis JA, Bruyere O, Silverman S, McCloskey E, et al. Fracture risk following intermission of osteoporosis therapy. Osteoporos Int. 2019;30(9):1733-43.
3. Ferrari S, Langdahl B. Mechanisms underlying the long-term and withdrawal effects of denosumab therapy on bone. Nat Rev Rheumatol. 2023;19(5):307-17.
4. Burckhardt P, Faouzi M, Buclin T, Lamy O, The Swiss Denosumab Study G. Fractures After Denosumab Discontinuation: A Retrospective Study of 797 Cases. J Bone Miner Res. 2021;36(9):1717-28.
5. Cummings SR, Ferrari S, Eastell R, Gilchrist N, Jensen JB, McClung M, et al. Vertebral Fractures After Discontinuation of Denosumab: A Post Hoc Analysis of the Randomized Placebo-Controlled FREEDOM Trial and Its Extension. J Bone Miner Res. 2018;33(2):190-8.
6. Anastasilakis AD, Papapoulos SE, Polyzos SA, Appelman-Dijkstra NM, Makras P. Zoledronate for the Prevention of Bone Loss in Women Discontinuing Denosumab Treatment. A Prospective 2-Year Clinical Trial. J Bone Miner Res. 2019;34(12):2220-8.
7. Meier C, Uebelhart B, Aubry-Rozier B, Birkhaeuser M, Bischoff-Ferrari H, Frey D, et al. Osteoporosis drug treatment: duration and management after discontinuation Swiss Med Wkly. 2017;in press.
8. Cosman F, Langdahl B, Leder BZ. Treatment Sequence for Osteoporosis. Endocr Pract. 2024;30(5):490-6.
9. Hamel ME, Sebaldt RJ, Siminoski K, Adachi JD, Papadimitropoulos E, Petrie A, et al. Influence of fracture history and bone mineral density testing on the treatment of osteoporosis in two non-academic community centers. Osteoporos Int. 2005;16(2):208-15.
10. Dempster DW, Zhou H, Recker RR, Brown JP, Recknor CP, Lewiecki EM, et al. Differential Effects of Teriparatide and Denosumab on Intact PTH and Bone Formation Indices: AVA Osteoporosis Study. J Clin Endocrinol Metab. 2016;101(4):1353-63.
11. Black DM, Eastell R, Adams AL. Atypical Femur Fracture Risk versus Fragility Fracture Prevention with Bisphosphonates. Reply. N Engl J Med. 2020;383(22):2189-90.
12. Bauer DC, Black DM, Dell R, Fan B, Smith CD, Ernst MT, et al. Bisphosphonate Use and Risk of Atypical Femoral Fractures: A Danish Case Cohort Study with Blinded Radiographic Review. J Clin Endocrinol Metab. 2024.
13. Everts-Graber J, Reichenbach S, Ziswiler HR, Studer U, Lehmann T. A Single Infusion of Zoledronate in Postmenopausal Women Following Denosumab Discontinuation Results in Partial Conservation of Bone Mass Gains. J Bone Miner Res. 2020;35(7):1207-15.
14. Solling AS, Harslof T, Langdahl B. Treatment with Zoledronate Subsequent to Denosumab in Osteoporosis: a Randomized Trial. J Bone Miner Res. 2020;35(10):1858-70.
15. Cosman F, Huang S, McDermott M, Cummings SR. Multiple Vertebral Fractures After Denosumab Discontinuation: FREEDOM and FREEDOM Extension Trials Additional Post Hoc Analyses. J Bone Miner Res. 2022;37(11):2112-20.
16. Tsourdi E, Zillikens MC, Meier C, Body JJ, Gonzalez Rodriguez E, Anastasilakis AD, et al. Fracture risk and management of discontinuation of denosumab therapy: a systematic review and position statement by ECTS. J Clin Endocrinol Metab. 2020.
17. Kendler DL, Marin F, Zerbini CAF, Russo LA, Greenspan SL, Zikan V, et al. Effects of teriparatide and risedronate on new fractures in post-menopausal women with severe osteoporosis (VERO): a multicentre, double-blind, double-dummy, randomised controlled trial. Lancet. 2018;391(10117):230-40.
18. Saag KG, Petersen J, Brandi ML, Karaplis AC, Lorentzon M, Thomas T, et al. Romosozumab or Alendronate for Fracture Prevention in Women with Osteoporosis. N Engl J Med. 2017;377(15):1417-27.
19. Ferrari S, Lippuner K, Lamy O, Meier C. 2020 recommendations for osteoporosis treatment according to fracture risk from the Swiss Association against Osteoporosis (SVGO). Swiss Med Wkly. 2020;150:w20352.
20. Black DM, Greenspan SL, Ensrud KE, Palermo L, McGowan JA, Lang TF, et al. The effects of parathyroid hormone and alendronate alone or in combination in postmenopausal osteoporosis. N Engl J Med. 2003;349(13):1207-15.
21. Leder BZ, Tsai JN, Uihlein AV, Wallace PM, Lee H, Neer RM, et al. Denosumab and teriparatide transitions in postmenopausal osteoporosis (the DATA-Switch study): extension of a randomised controlled trial. Lancet. 2015;386(9999):1147-55.
22. Lewiecki EM, Dinavahi RV, Lazaretti-Castro M, Ebeling PR, Adachi JD, Miyauchi A, et al. One Year of Romosozumab Followed by Two Years of Denosumab Maintains Fracture Risk Reductions: Results of the FRAME Extension Study. J Bone Miner Res. 2019;34(3):419-28.
23. McClung MR, Bolognese MA, Brown JP, Reginster JY, Langdahl BL, Maddox J, et al. A single dose of zoledronate preserves bone mineral density for up to 2 years after a second course of romosozumab. Osteoporos Int. 2020;31(11):2231-41.
24. Ettinger B, San Martin J, Crans G, Pavo I. Differential effects of teriparatide on BMD after treatment with raloxifene or alendronate. J Bone Miner Res. 2004;19(5):745-51.
25. Boonen S, Marin F, Obermayer-Pietsch B, Simoes ME, Barker C, Glass EV, et al. Effects of previous antiresorptive therapy on the bone mineral density response to two years of teriparatide treatment in postmenopausal women with osteoporosis. J Clin Endocrinol Metab. 2008;93(3):852-60.
26. Miller PD, Delmas PD, Lindsay R, Watts NB, Luckey M, Adachi J, et al. Early Responsiveness of Women with Osteoporosis to Teriparatide Following Therapy with Alendronate or Risedronate. J Clin Endocrinol Metab. 2008.
27. Ebina K, Hirao M, Tsuboi H, Nagayama Y, Kashii M, Kaneshiro S, et al. Effects of prior osteoporosis treatment on early treatment response of romosozumab in patients with postmenopausal osteoporosis. Bone. 2020;140:115574.
28. Cosman F, Kendler DL, Langdahl BL, Leder BZ, Lewiecki EM, Miyauchi A, et al. Romosozumab and antiresorptive treatment: the importance of treatment sequence. Osteoporos Int. 2022;33(6):1243-56.
29. Cosman F, Eriksen EF, Recknor C, Miller PD, Guanabens N, Kasperk C, et al. Effects of intravenous zoledronic acid plus subcutaneous teriparatide [rhPTH(1-34)] in postmenopausal osteoporosis. J Bone Miner Res. 2011;26(3):503-11.
30. Tsai JN, Uihlein AV, Lee H, Kumbhani R, Siwila-Sackman E, McKay EA, et al. Teriparatide and denosumab, alone or combined, in women with postmenopausal osteoporosis: the DATA study randomised trial. Lancet. 2013;382(9886):50-6.
31. Foessl I, Dimai HP, Obermayer-Pietsch B. Long-term and sequential treatment for osteoporosis. Nat Rev Endocrinol. 2023;19(9):520-33.
Therapeutische Umschau
- Vol. 82
- Ausgabe 1
- Februar 2025






