- Pulmonale Dyspnoe
Eine 59-jährige Patientin stellt sich mit zunehmender Anstrengungsdyspnoe seit einigen Monaten vor, sobald sie schnell gehen oder bergaufsteigen müsse, komme sie schnell ausser Atem. Vor mehr als 10 Jahren sei ein Asthma von ihrem damaligen Hausarzt diagnostiziert worden, Vorbefunde liegen keine vor. Die inhalative Therapie mit einem Kortisonpräparat habe sie nur unregelmässig bei störender Heiserkeit (Beruf: Sängerin) angewendet. Husten, Auswurf und rhinokonjunktivitische Beschwerden werden verneint. Geraucht habe sie gelegentlich, allerdings wird eine regelmässige Passivrauch-Exposition beschrieben. Als Jugendliche habe sie Neurodermitis gehabt, bekannte Allergien: Pollen (Gräser, Hausstaubmilben, Hundepithelien). Lungenfunktionell imponiert eine schwere obstruktive Ventilationsstörung ohne vollständige Reversibilität nach Bronchodilatation.
Einleitung
Dyspnoe ist eines der häufigsten Symptome bei Patienten mit akuten und chronischen Lungenerkrankungen. Aufgrund des subjektiven Charakters der Atembeschwerden kann sich die Diagnosestellung als sehr herausfordernd darstellen, dennoch lässt eine genauere «Sprachanalyse» der Dyspnoe Rückschlüsse auf die zugrundliegende Erkrankung des Atmungsorgans zu (2). Erschwerend kann eine multifaktorielle und überlappende Ätiologie auch mit extrapulmonalen Grunderkrankungen hinzukommen. Ähnlich wie beim Schmerz existieren keine wahren objektiven Messparameter der Dyspnoe: Sowohl Atemnot als auch Schmerz werden nur von derjenigen Person wahrgenommen, die sie empfindet. Das Vorliegen von Atemnot hat sich nicht nur bei chronischen pulmonalen Erkrankungen als Mortalitätsprädiktor erwiesen (3), sondern auch bei hospitalisierten Patienten unabhängig von der zugrundliegenden Erkrankung, je ausgeprägter die Atemnot, desto höher das Mortalitätsrisiko (4). Im Gegensatz zur Dyspnoe zeigten Schmerzen, die bei hospitalisierten Patienten standardisiert erhoben werden, in dieser grossangelegten Studie interessanterweise jedoch keinen Zusammenhang mit einem schlechten Outcome. Meistens liegen Dyspnoe kardiale oder pulmonale Ätiologien zu Grunde. Häufige ursächliche pulmonale Erkrankungen sind neben broncho-pulmonalen Infekten: Asthma bronchiale, chronisch obstruktive Pneumopathie (COPD) und interstitielle Lungenerkrankungen. Das Symptom «Dyspnoe» sollte nicht nur im medizinischen Kontext der pulmonalen Grunderkrankung gewertet werden, sondern ganzheitlich mit seinen Auswirkungen auf die Funktionalität im privaten sowie beruflichen Leben. Folgeerscheinungen wie die Abnahme der körperlichen Aktivität mit konsekutiver Dekonditionierung, Depressionen und Angstzustände sowie eine etwaige Arbeitsunfähigkeit gilt es frühzeitig zu erkennen und im therapeutischen Management zu berücksichtigen.
Definition
Dyspnoe (von altgriechisch δυσ dys ‚schwierig‘ und πνοή pnoe ‚Atmung‘) wird umgangssprachlich auch als Atem- oder Luftnot bezeichnet, ferner werden die Begriffe Atemlosigkeit, Luftnötigkeit, Kurzatmigkeit oder Lufthunger verwendet. In einem Konsensus Statement der American Thoracic Society wurde Dyspnoe als eine «subjektive Wahrnehmung von Atembeschwerden, die sich aus qualitativ unterschiedlichen Empfindungen unterschiedlicher Intensität zusammensetzen» definiert (5). Dabei wurde postuliert, dass dieses subjektive Empfinden «durch das Zusammenspiel mehrerer physiologischer, psychologischer, sozialer und umweltbedingter Faktoren entsteht und sekundäre physiologische und verhaltensbezogene Reaktionen hervorrufen kann». Dyspnoe stellt damit als Sammelbegriff für subjektive, multifaktorielle Atembeschwerden ein komplexes Leitsymptom dar. Zusätzlich besteht eine zeitliche Definition: Akute Dyspnoe entwickelt sich innerhalb von wenigen Minuten bis Stunden, chronische Dyspnoe entsteht über mindestens mehrere Wochen. Des Weiteren muss eine akute Verschlechterung von einer chronischen Dyspnoe («acute-on-chronic») unterschieden werden.
Grundlagen
Pulmonale Dyspnoe kann im Wesentlichen auf Störungen im Gasaustausch und Störungen der Atemmuskelpumpe zurückgeführt werden. Die genaue Pathophysiologie und insbesondere neurophysiologische Zusammenhänge der Dyspnoe sind bis dato nicht abschliessend geklärt, komplexe Interaktionen von multiplen afferenten und efferenten Signalen des zentralen und autonomen Nervensystems führen zu einer Stimulation des zentralen Atemzentrums mit konsekutiver Steigerung der Ventilation sowie resultierenden Atembeschwerden und «Lufthunger» (6). Es wird vermutet, dass Atembeschwerden bei chronischen Lungenerkrankungen durch eine individuelle Anpassung des Grund-Atemmusters durch die zentrale Atemregulation reduziert werden: Patienten mit schwerer obstruktiver Ventilationsstörung atmen tendenziell langsam und tief, wohingegen Patienten mit restriktiven Ventilationsstörungen eine schnelle, flache Atmung aufweisen (7).
Störungen im Gasaustausch
Der pulmonale Gasaustausch findet zwischen den Alveolen und dem Kapillarbett statt und beruht auf einem optimalen Zusammenspiel von Ventilation, Perfusion und Diffusion. Störungen des Gasaustauschs resultieren in einer Hypoxämie (Respiratorische Insuffizienz Typ I, früher Partialinsuffizienz) mit begleitender Normo- oder Hypokapnie. Wichtigste Ursachen sind Verteilungsstörungen mit Ventilations-Perfusions-Inhomogenitäten (z.B. bei obstruktiven Atemwegserkrankungen, Atelektasen), Diffusionsstörungen (z.B. pulmonal-parenchymatöse Erkrankungen, Lungenemphysem) oder pulmonale Rechts-Links-Shunts (z.B. ausgedehnte Pneumonie, Acute Respiratory Distress Syndrom (ARDS), pulmonale AV-Malformationen). CO2 weist eine 25-fach bessere Diffundierbarkeit als O2 auf, daher gibt es keine klinisch relevante diffusionsbedingte CO2-Retention. Sowohl eine Verteilungsstörung als auch eine Diffusionsstörung lassen sich durch Sauerstoffgabe ad hoc verbessern, bei einem signifikanten Rechts-Links-Shunt führt Sauerstoff jedoch nicht zu einer vollständigen Oxygenierung des Bluts. Fortgeschrittene Erkrankungen des Lungenparenchyms führen nicht nur zu einer Verminderung der alveolären Gasaustauschfläche, sondern auch zu einer Abnahme der pulmonalen Perfusion aufgrund einer lokoregionären hypoxischen pulmonalen Vasokonstriktion (Euler-Liljestrand-Reflex). Diese zeigt sich in den frühen Stadien unter Sauerstoffsupplementation noch reversibel, in späteren Stadien zeigt sich keine Vasoreagibilität mehr. Die Verminderung des gesamten Lungengefässquerschnittes führt zu einem Anstieg des pulmonalen Gefässwiderstands (Verweis Kapitel Pulmonale Hypertonie) mit Verstärkung das Ventilations-Perfusions-Mismatches.
Störungen der Atemmuskelpumpe
Die Atemmuskelpumpe ist ein komplexes Konstrukt bestehend aus der Atemmuskulatur, dem knöchernen Thorax, der Pleura und den entsprechenden peripheren Nerven. Störungen der Atemmuskelpumpe können zu einer alveolären Hypoventilation und im weiteren Verlauf zu einem hyperkapnischen Pumpversagen führen (respiratorische Insuffizienz Typ II, früher Globalinsuffizienz). Akute oder anhaltende Gasaustauschstörungen z.B. Ventilationsstörungen können infolge der erhöhten Atemarbeit in ein Atempumpenversagen münden. In Ruhe beträgt der Sauerstoffbedarf der Atemmuskulatur ca. 1-2 % der gesamten Sauerstoffaufnahme (VO2), unter körperlicher Belastung kann dieser bei Gesunden auf bis zu 10% ansteigen, bei Patienten mit fortgeschrittener COPD werden diese Werte aufgrund der erhöhten Atemarbeit bereits in Ruhe überschritten (8). Die Berechnung des arterio-alveolären Gradienten (A-a Gradient) kann zur Differenzierung einer Hypoxämie bei begleitender Hyperkapnie beitragen. Ein normwertiger A-a Gradient liegt bei prädominierender Hypoventilation vor, ein erhöhter Quotient zeigt sich bei Diffusionsstörungen oder Verteilungsstörungen, Normalwerte unter Raumluft können anhand des Alters geschätzt werden (siehe Abb.1) (9). Häufig bestehen allerdings Mischformen einer kombinierten Gasaustauschstörung mit begleitender alveolärer Hypoventilation, ein normwertiger A-a Gradient kann jedoch eine relevante Diffusions- und Verteilungsstörung ausschliessen. Klassische Ursachen, die Störungen der Atemmuskelpumpe bedingen, sind neuromuskuläre Erkrankungen, z.B. Myopathien/Muskeldystrophien und anatomische Deformationen mit Einschränkungen der Atemmechanik, z.B. Kyphoskoliose, Zwerchfellhochstand.
Diagnostik
Anamnese und klinische Untersuchung
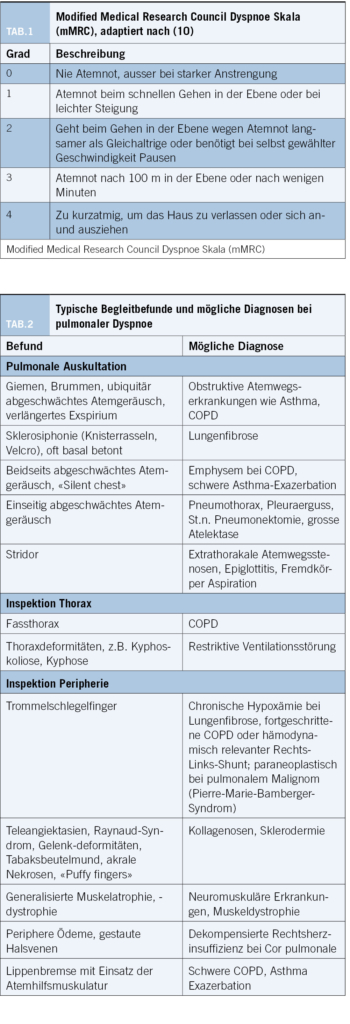
Im Rahmen der Erstvorstellung bei Dyspnoe müssen zunächst der Schweregrad und der Verlauf der Symptomatik erhoben werden. In einem ersten Schritt sollte eine potentiell lebensbedrohliche Symptomatik mit drohender respiratorischer Erschöpfung von nicht akut vital gefährdenden Beschwerden unterschieden und bei Bedarf medizinische Sofortmassnahmen eingeleitet werden. Kardiale Ursachen und Lungenarterienembolien müssen differentialdiagnostisch immer bei Dyspnoe, jedoch insbesondere bei akutem Beschwerdebild, in Betracht gezogen werden. In einem zweiten Schritt empfiehlt es sich, die zeitliche Entwicklung zu erfassen: Sind die Atembeschwerden akut oder chronisch? Zeigt sich ein schleichend progredienter oder ein chronischer Verlauf mit aktuell akuter Verschlechterung? Somit kann besser differenziert werden, ob es sich um die Erstmanifestation einer neuen bzw. einer bis dato noch nicht diagnostizierten Erkrankung (z.B. Asthma bronchiale) oder um eine Verschlechterung einer vorbekannten Grunderkrankung handelt (z.B. Infektexazerbation einer interstitiellen oder obstruktiven Pneumopathie). In einem dritten Schritt schliesst sich die ausführliche pulmonale Anamnese an, die «Sprache der Dyspnoe» und respiratorische Begleitsymptome lassen mitunter Rückschlüsse auf die zugrundeliegende Erkrankung zu (siehe Tabelle 2). Zur besseren Einschätzung der Intensität der Dyspnoe können die Borg-Skala (Von 0 keine Beschwerden bis 10 maximale Beschwerden) oder modified medical Research Council (mMRC) Skala (10) eingesetzt werden (siehe Tabelle 1), letztere erleichtert eine semiquantitative Einordnung der Alltagsbeeinträchtigung der Patienten. Anschliessend sollte eine extrapulmonale Systemanamnese mit Erfassung der inhalativen Noxen, Berufs- und Freizeitanamnese, Familienanamnese und die aktuelle Medikation erfasst werden.
Die körperliche Untersuchung und die Erfassung der Vitalparameter (Herzfrequenz, Atemfrequenz, Blutdruck, Puls, periphere Sauerstoffsättigung, Körpertemperatur) stellen einen weiteren wichtigen Baustein der initialen Diagnostik dar. Die subjektive Empfindung «Dyspnoe» kann zusätzlich anhand von klinischen Zeichen objektiviert werden: z.B. Tachypnoe, Sprechdyspnoe, Stridor, paradoxe Atmung, Einsatz der Atemhilfsmuskulatur, Lippenbremse, respiratorische Einziehungen der Interkostalräume. Neben dem kardiopulmonalen Auskultationsbefund tragen Beurteilung der Thoraxkonfiguration, Volumenstatus, Trommelschlegelfinger, Hautkolorit, Gewicht, Hautveränderungen, Gelenkbeschwerden, Schluckbeschwerden, Muskelatrophie wesentlich zur differentialdiagnostischen Einordnung bei (siehe Schema). Dennoch korrelieren die klinischen Befunde häufig nur unzureichend mit der Symptomatik und mit dem Schweregrad der pulmonalen sowie globalen Funktionseinschränkung, sodass weitere Untersuchungen notwendig werden.
Basisdiagnostik
Je nach klinischem Bild empfiehlt sich eine Blutentnahme (Anämie als Ursache der Dyspnoe?, Polyglobulie als Hinweis für eine bereits länger andauernde Hypoxämie?, Leukozytose als Hinweis für eine Entzündung?) inkl. Differentialblutbild (Granulozytose als Hinweis für eine bakterielle Entzündung? Lymphozytose als Hinweis für eine virale/autoimmune Entzündung?, Eosinophilie als Hinweis für ein eosinophiles Asthma bronchiale oder eosinophile pulmonale Erkrankung?) sowie des CRP, der Elektrolyte, der Nieren- und Leberfunktionswerte. Zusätzlich können bei klinisch nicht eindeutiger pulmonaler Genese der Beschwerden die Bestimmung des Troponin, des NT-proBNP und die D-Dimere zur weiteren differentialdiagnostischen Aufarbeitung beitragen. Eine aktuelle prospektive Studie konnte beispielsweise aufzeigen, dass bei COPD-Patienten mit einer akuten hospitalisations-bedürftigen respiratorischen Verschlechterung anhand einer systematischen Diagnostik bei bis zu 5% der Fälle eine Lungenarterienembolie diagnostiziert werden konnte, bestand klinisch der Verdacht auf eine Lungenembolie, lag die Prävalenz sogar bei 10% (11).
Im EKG können sich nicht nur Hinweise für eine myokardiale Ischämie oder Linksherzpathologie ergeben, sondern auch indirekte Zeichen einer akuten Rechtsherzbelastung (SIQIII-Typ bei Lungenarterienembolie) oder einer chronischen Rechtsherzbelastung im Sinne eines Cor pulmonale auffällig werden (Sokolow Index, Rechtsschenkelblock,
p Pulmonale, Rechtslagetyp). Grundsätzlich sollte bei jedem Patienten mit Dyspnoe eine konventionelle Röntgen-Thorax-Untersuchung in zwei Ebenen erfolgen, Ausnahmen sind beispielsweise junge Patientinnen mit klassischen Befunden eines Asthmas und gutem Therapieansprechen auf Inhalativa. Bei fehlendem Therapieansprechen oder uneindeutigen Befunden sollte die Diagnose eines Asthmas jedoch immer kritisch hinterfragt und um eine Bilddiagnostik erweitert werden (GINA Guidelines 2022).
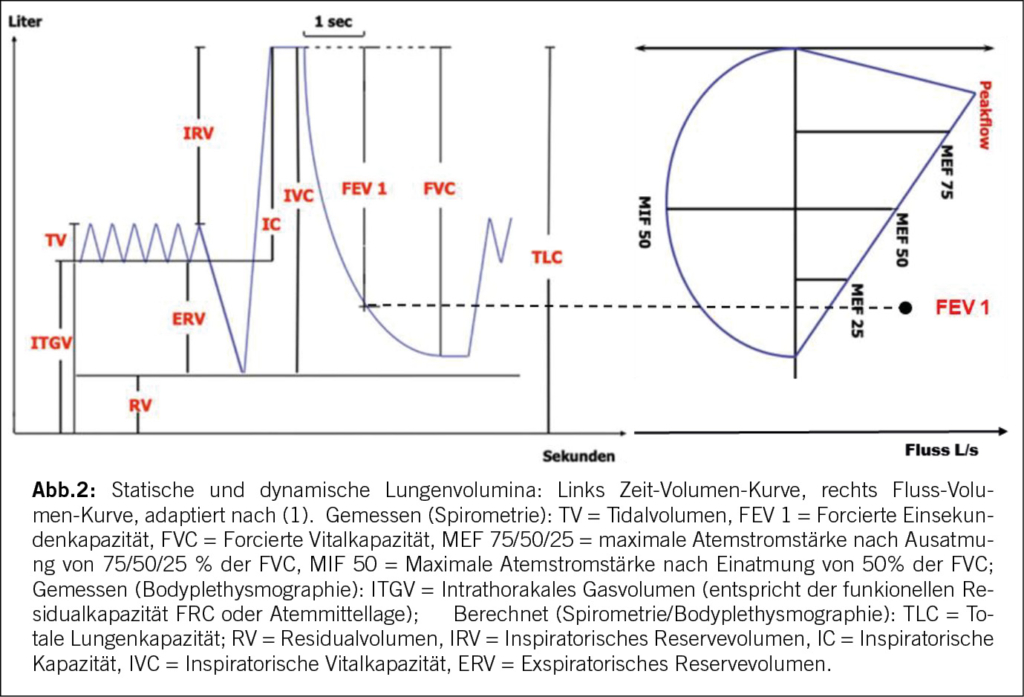
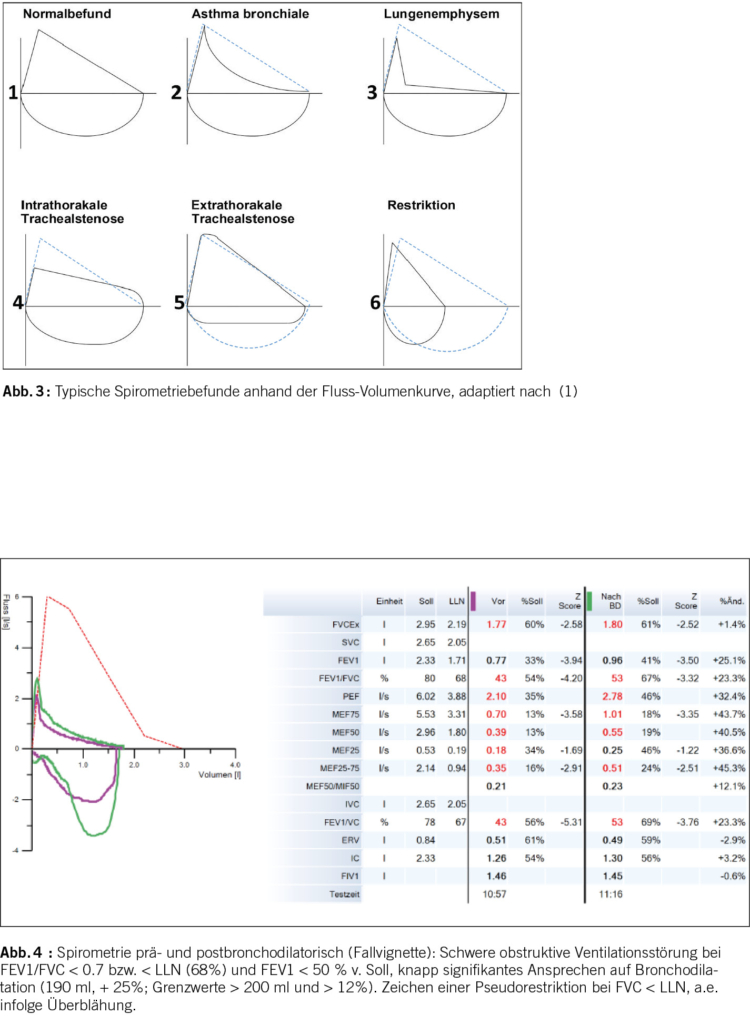
Zu einer ersten Standortbestimmung hinsichtlich einer Ventilationsstörung (Obstruktion, Restriktion) eignet sich die Spirometrie. Sie dient zur Erfassung der dynamischen Atemvolumina und des Tiffeneau-Index (Forcierte Einsekunden-Kapazität FEV1/Forcierte Vitalkapazität FVC), zudem kann der Spitzenfluss (Peak Exspiratory Flow, PEF) bestimmt werden (Abb. 2). Die diagnostische Aussagekraft hängt jedoch entscheidend von der Untersuchungsqualität ab, da die Atemmanöver stark mitarbeitsabhängig sind und eine entsprechende Expertise des Untersuchers benötigt wird. In den aktualisierten Leitlinien zu Standardisierung der Spirometrie wurden neben den technischen Kriterien für Akzeptabilität und Reproduzierbarkeit, auch neu Kriterien zur klinischen Verwendbarkeit (Usability) definiert (12). Untersuchungen, die formal die Akzeptabilitätskriterien nicht erfüllen, können sich trotzdem als klinisch brauchbar erweisen. Die Spirometrie ist der Goldstandard zur Diagnose einer obstruktiven Ventilationsstörung, zudem kann der Schweregrad der Obstruktion erhoben und ein Therapieansprechen mittels konsekutiver Messungen beurteilt werden. Der Kurvenverlauf im Fluss-Volumen-Diagramm kann zudem Hinweise für intra- oder extrathorakale Stenosen als weitere Ursache von Dyspnoe ergeben (Abb. 3). Eine restriktive Ventilationsstörung hingegen darf spirometrisch bei verminderten dynamischen Atemvolumina nur vermutet werden. Für die Diagnose einer restriktiven Ventilationsstörung wird die Messung der totalen Lungenkapazität (TLC) gefordert, sollten sich in der Spirometrie Hinweise für eine restriktive oder gemischt restriktive-obstruktive Ventilationsstörung ergeben, wird deswegen eine weiterführende pneumologische Diagnostik mittels Bodyplethysmographie und Messung der Diffusionskapazität empfohlen. Bis dato wurde ein pathologischer Grenzwert anhand fester Prozentangaben bezogen auf den Sollwert definiert. Dabei wurde jedoch die Streubreite der Normalwerte nicht berücksichtigt. Die Lungenfunktionswerte gesunder Probanden weisen eine Normalverteilung auf, mittels Perzentilen kann ein Untersuchungsresultat in Bezug zur statistischen Verteilung des Parameters auf der Normalverteilungskurve gesetzt werden (Abb. 5). Als unterer Grenzwert (Lower Limit of Normal, LLN) wurde die 5. Perzentile definiert, entsprechend 1,645 Standardabweichungen vom Sollmittelwert (= Z-Score) (13). Mit zunehmendem Alter nimmt die natürliche Streuung der Messwerte zu und die LLN entsprechend ab. Fixe Grenzwerte führen damit in höherem Alter zu einer Überdiagnose von Ventilationsstörungen, in jüngerem Alter zu einer Unterdiagnose. Generell gilt es jedoch zu beachten, dass die erhobenen Messparameter immer individuell und im Rahmen des klinischen Kontexts zu werten sind, formal noch normale Werte können für den Einzelnen bereits pathologisch sein. Wichtiger als der Vergleich mit der Normalpopulation, sind somit intraindividuelle Verlaufsmessungen.
Erweiterte Diagnostik
Bildgebung
Bei auffälligem Röntgen-Thorax mit z.B. interstitieller Zeichnungsvermehrung, malignomsuspekten Befunden, unklaren oder persistierenden Infiltraten, Emphysemaspekt oder Mediastinalverbreitung sollte eine Computertomographie des Thorax erfolgen. Bei diskonkordanten Befunden von Klinik und unauffälligem Röntgen-Thorax kann eine CT-Untersuchung eine konventionell-radiologisch nicht detektierte interstitielle Lungenerkrankung aufdecken bzw. Hinweise für eine anderweitige Ursache der Dyspnoe geben z.B. indirekte Zeichen einer pulmonalen Hypertonie. Besteht konventionell röntgenologisch bereits der Verdacht auf eine interstitielle Pneumopathie sollte eine native hoch auflösende (High-Resolution, HR) CT-Thorax-Untersuchung angefordert werden, da eine i.v. Kontrastmittelgabe die Bildmorphologie des Lungenparenchyms verändern und damit z.B. die radiologische Beurteilung von Milchglasinfiltraten (Ground Glass Infiltrate) erschweren kann (14). Bei Verdacht auf ein Malignom ist die Kontrastmittelgabe allerdings zur Einordnung der pulmonalen Raumforderung und Beurteilung der Lymphadenopathie obligat. Sollte sich die Frage nach einer Beteiligung der kleinen Atemwege («Small Airway Disease», z.B. bei Bronchiolitis, Hypersensitivitätspneumonitis) stellen, ist es hilfreich In- und Exspirationsaufnahmen durchführen zu lassen. Ein Vergleich der Bildmorphologie in In- und Exspiration kann gefangene Luft (Air Trapping) bei in Exspiration zunehmend hypodensen Lungenarealen zur Darstellung bringen. Generell gilt, je mehr klinischen Angaben und je dezidierter die Fragestellung an die KollegInnen der Radiologie, desto aussagekräftiger die radiologische Befundung.
Die Thoraxsonographie hat insbesondere «bedside» bei akuter Dyspnoe ihren Stellenwert als schnell verfügbare, nicht-strahlenbelastende und in geübten Händen sehr differenzierte Bildgebung erwiesen. Sie stellt die Methode der Wahl zur Detektion von Pleuraergüssen dar und eignet sich zur Darstellung von Pneumothoraces, pulmonalen Infiltraten, Lungeninfarkten und eines Lungenödems (15). Sonographisch können bereits 5 bis 10 ml Pleuraerguss detektiert werden, wohingegen konventionell radiologisch Ergussmengen erst ab 200 ml dargestellt werden können (16). Beurteilt werden können zusätzlich die Echogenität der pleuralen Flüssigkeit incl. die Darstellung von Septen, angrenzende pleurale Verdickungen. Begleitend kann eine Einschränkung der Zwerchfellbeweglichkeit als weitere Differentialdiagnose von Atembeschwerden erhoben werden. Zudem können als erweiterte Diagnostik bei Atembeschwerden grob orientierend die kardiale Pumpfunktion incl. der Volumenstatus anhand der Darstellung der Vena Cava inferior eingeschätzt sowie ein hämodynamisch relevanter Perikarderguss untersucht werden.
Funktionelle Diagnostik
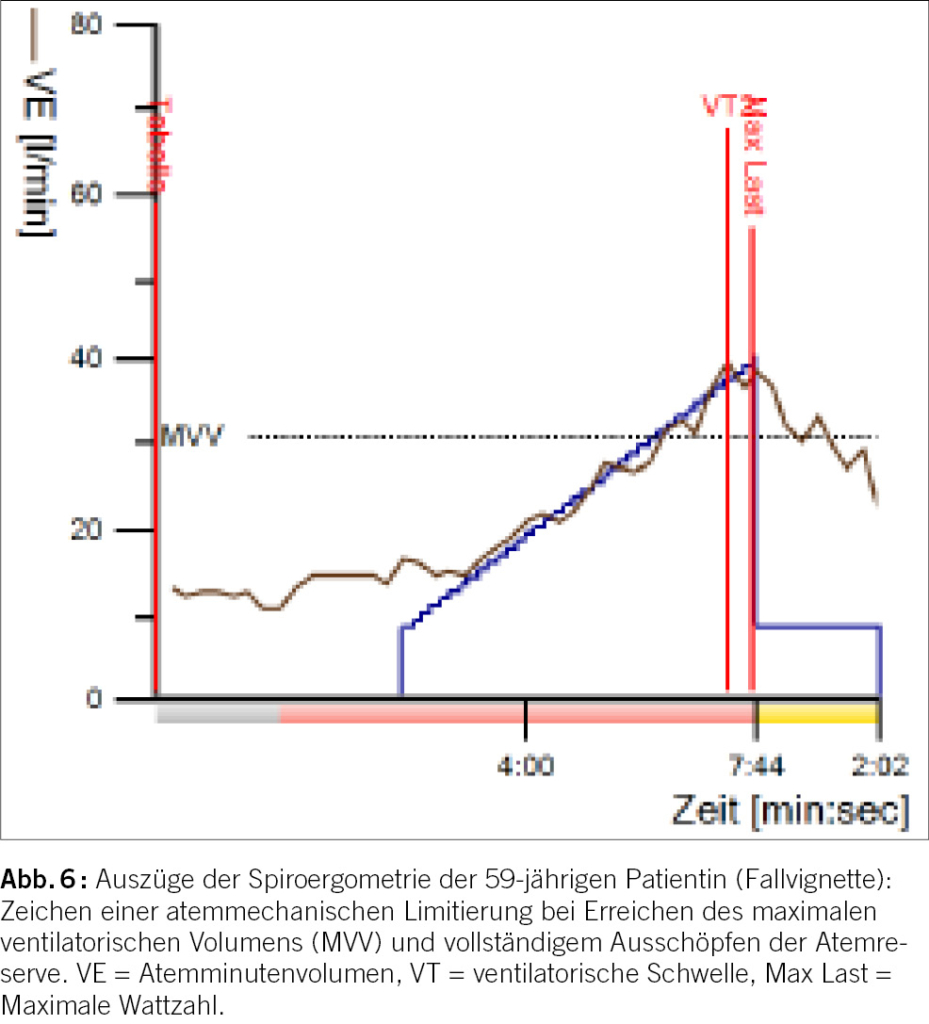
Die Spiroergometrie eignet sich nicht nur zur Objektivierung der kardiopulmonalen Leistungsfähigkeit, sondern stellt auch ein hervorragendes Instrument zur Differenzierung hinsichtlich ventilatorischer, pulmonalvaskulärer und kardialer Limitierungen der Leistungsfähigkeit dar.
(Abb. 6, Auszüge der Spiroergometrie der 59-jährigen Patientin (Fallvignette)). Neben der klassischen Leistungsdiagnostik, sind Dyspnoe und Leistungsintoleranz die klassischen Indikationen zur Durchführung einer Spiroergometrie. Zur Beurteilung pulmonaler Grunderkrankungen sind neben der Messung der maximalen Sauerstoffaufnahme (VO2max) insbesondere die Messung der Ventilation, der arteriellen Blutgase, der Atemäquivalente und der dynamischen Lungenvolumina unter Belastung relevant. Ferner kann die Diagnose eines Anstrengungsasthmas mittels Spirometrien nach der Belastungsphase gestellt werden (Statement Exercise Induced Asthma). Weitere Indikationen sind die Beurteilung der Operabilität vor pulmonalen Resektionen und die Beurteilung der Ateminvalidität im Rahmen der pneumologischen Arbeitsmedizin.
Erweiterte Labordiagnostik
Bei begleitenden Hinweisen für eine rheumatologische Systemerkrankung im Rahmen der Abklärungen der Dyspnoe kann eine erweiterte serologische Diagnostik zur differentialdiagnostischen Einordnung beitragen. Interstitielle Pneumopathien können bereits vor der rheumatologischen Grunderkrankung manifest werden. So wird in der Schweiz, entsprechend den internationalen Leitlinien, bei Erstdiagnose einer ILD sowie erneut im Verlauf bei neuen klinischen Aspekten, die Bestimmung von antinukleären Antikörpern (ANA), Rheumafaktoren (RF), anti-zyklisches citrulliniertes Peptid (anti-ccP) empfohlen. Stellen sich bei Erstdiagnose einer Pneumopathie bereits Hinweise für eine Autoimmunerkrankung, sollte das serologische Screening ausgeweitet werden (17).
Schlafdiagnostik
Schlafbezogene Atemstörungen sind weitere Differentialdiagnosen der Dyspnoe bzw. können diese verstärken. Ergeben sich klinisch, lungenfunktionell und bildmorphologisch keine Hinweise für eine pulmonale Ursache der Dyspnoe, kann die Durchführung einer nächtlichen Pulsoxymetrie oder Polygraphie erwogen werden. Neben der obstruktiven Schlafapnoe gilt es auch eine nächtliche Hypoventilation auszuschliessen, insbesondere bei Nachweis einer Hyperkapnie oder eines erhöhten Bikarbonats
(≥ 27 mmol/l) am Tag nach Ausschluss anderer Ursachen der Hypoventilation (18).
Ausgewählte Krankheitsbilder
In den folgenden Abschnitten werden ausgewählte Krankheitsbilder vorgestellt, die sich klassischerweise mit Dyspnoe äussern können. Schwerpunktmässig werden dabei die klinische Präsentation der Dyspnoe sowie deren Ursachen ausgeführt und orientierende Grundzüge der Diagnostik und Therapie dargelegt. Auf Atembeschwerden im Rahmen broncho-pulmonaler Infekte, infolge pulmonaler Malignome oder Atemwegsstenosen wird explizit nicht eingegangen und auf die entsprechende Literatur verwiesen.
Asthma und COPD
Sowohl Asthma als auch COPD können sich primär mit Dyspnoe äussern. Beide Erkrankungen zeichnen sich durch eine Atemwegsobstruktion aus. Dyspnoe bei Asthma variiert definitionsgemäss in Intensität und Häufigkeit, wohingegen sich die Symptomatik bei COPD typischerweise durch eine Persistenz mit Progredienz auszeichnet. Dyspnoe bei COPD wird klassischerweise als Empfindung einer vermehrten Atemarbeit, eines Schweregefühls im Brustkorb, eines Lufthungers oder als Keuchen beschrieben (19). Asthma äussert sich selten mit isolierter Dyspnoe, häufige begleitende respiratorische Symptome sind ein thorakales Engegefühl, Giemen, Husten und die Symptome zeigen häufig eine nächtliche/frühmorgendliche Verschlechterung. Zudem werden meist Auslöser der Atembeschwerden beschrieben (z.B. Allergene, Kälte, Sport, virale Infekte, Stress). Das Alter bei Erstmanifestation und Expositionsanamnese können zusätzlich zur Differenzierung der beiden Erkrankungen beitragen. Die charakteristische variable Atemwegsobstruktion bei Asthma kann im späteren Verlauf der Erkrankung persistieren («fixierte Obstruktion»), insbesondere bei älteren Patienten und Rauchern wird damit eine Unterscheidung zur chronisch obstruktiven Pneumopathie (COPD) erschwert. Ein überlappendes Vorliegen von Asthma und COPD (Asthma-COPD Overlap) zeichnet sich durch eine persistierende Atemwegsobstruktion mit klinischen Merkmalen eines Asthmas und einer COPD aus (siehe Fallvignette). Normale Alterungsprozesse der Atemwege und des Lungenparenchyms weisen einige strukturelle Gemeinsamkeiten mit der COPD auf, eine Abnahme der FEV1 und des Tiffeneau-Index im Alter sind per se nicht pathologisch und sollten immer im klinischen Kontext gewertet werden (siehe Kapitel Basisdiagnostik). Sowohl die Diagnose eines Asthmas als auch der COPD erfordern neben der passenden Klinik den lungenfunktionellen Nachweis einer Atemwegsobstruktion. Zusätzlich wird beim Asthma der Nachweis einer signifikanten lungenfunktionellen Reversibilität in der Spirometrie (FEV1 > 12% und 200 ml) bzw. tägliche Variabilität im Peak-Flow (PEF > 10%) gefordert, eine positive Reversibilitätstestung oder bronchiale Hyperreagibilität schliessen eine COPD jedoch nicht aus. Eine Beteiligung des Lungenparenchyms liegt beim Asthma klassischerweise nicht vor, sodass eine Einschränkung der Diffusionskapazität auf eine COPD mit begleitenden emphysematösen Veränderungen hinweist.
Die Therapie des Asthmas ist primär antiinflammatorisch, wohingegen die Therapie der COPD zunächst auf eine
Bronchodilatation mit Verminderung der gefangenen Luft und Steigerung der inspiratorischen Kapazität abzielt. Doch auch bei Patienten mit COPD kann eine antiinflammatorische Therapie insbesondere bei rezidivierenden Exazerbationen als Korrelat einer chronischen Atemwegsentzündung indiziert sein. Dennoch bestehen noch viele offene Fragen hinsichtlich der optimalen Therapie. Eine individualisierte Therapie, angepasst an die funktionelle Einschränkung, prädominierende Symptomatik, Komorbiditäten sowie Biomarker (z.B. Eosinophilenzahl) wird sich zukünftig bei beiden Erkrankungen noch etablieren müssen.
Interstitielle Pneumopathien
Dyspnoe infolge Lungenparenchymerkrankungen äussert sich primär unter körperlicher Belastung, häufig besteht ein begleitender trockener Husten. Interstitielle Pneumopathien stellen ein sehr heterogenes Krankheitsbild dar. Der zeitliche Verlauf der Atembeschwerden und die Begleitsymptomatik helfen bei der differentialdiagnostischen Einordnung. So wird beispielsweise zwischen akuten (organisierende Pneumonie (OP), akute interstitielle Pneumopathien wie der Respiratorischen Bronchiolitis-ILD (RB-ILD), der desquamativen interstitiellen Pneumopathie (DIP) und der pulmonalen Langerhanshistiozytose kann die Diagnose allein anhand der Raucheranamnese und der CT-graphischen Bildmorphologie gestellt werden. Pulmonale Parenchymveränderungen führen zu einer verminderten Lungen-Compliance mit Einschränkung der inspiratorischen Kapazität und zu einer Einschränkung des alveolo-arteriellen Gasaustauschs, die Veränderungen äussern sich meist zunächst nur unter Belastung. Eine belastungsinduzierte Desaturation im Rahmen eines 6-Minuten-Gehtests kann somit frühzeitige Hinweise für eine interstitielle Pneumopathie geben.
Die Therapie der ILD richtet sich prinzipiell nach der Klassifikation, kausale Therapien bestehen bei den meisten Formen jedoch nicht und neue antifibrotische Therapien sind nur bei ausgewählten Entitäten indiziert. Die korrekte Diagnose ist von zentraler Bedeutung, eine interdisziplinäre Herangehensweise ist dabei erforderlich.
Fazit
Dyspnoe ist eines der häufigsten Symptome bei Lungenerkrankungen, eine genaue Charakterisierung der Atembeschwerden sowie Erhebung der Begleitsymptomatik sind essentiell und wegweisend. Die Spirometrie eignet sich zur initialen Standortbestimmung und Schweregradeinteilung, dabei korreliert der Schweregrad der pulmonalen Funktionseinschränkung häufig nicht mit dem klinischen Bild. Eine erweiterte Diagnostik und insbesondere bildgebende Verfahren helfen bei der differentialdiagnostischen Einordnung. Eine multifaktorielle Genese der Dyspnoe ist häufig. Eine ganzheitliche Therapie zur Erhaltung der körperlichen Aktivität sowie der Funktionalität im Alltag sollte angestrebt werden.
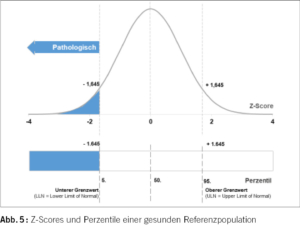
Fallvignette: Im Rahmen der erweiterten Diagnostik zur Abklärung der schweren obstruktiven Ventilationsstörung (Abb. 4) zeigten sich sowohl das Gesamt-IgE als auch die Eosinophilen normwertig, die Diffusionskapazität war leichtgradig eingeschränkt. CT-graphisch kamen Zeichen einer milden chronischen Bronchitis mit leichtgradigem Air-Trapping sowie geringgradigen emphysematischen Veränderungen zur Darstellung. Ein Asthma-COPD-Overlap wurde diagnostiziert und eine inhalative Kombinationstherapie (ICS/LABA + LAMA) begonnen. Im Rahmen einer Spiroergometrie zur Objektivierung der Leistungseinschränkung zeigte sich eine noch leichtgradige Einschränkung der globalen Leistungsfähigkeit bei schwerer atemmechanischer Limitation (maximale Sauerstoffaufnahme 69% v. Soll), zur Verbesserung der Funktionalität wurde eine ambulante pulmonale Rehabilitation initiiert.
Oberärztin
Klinik für Pneumologie, Universitätsspital Zürich
Rämistrasse 100
8091 Zürich
Laura.Mayer@usz.ch
1. Rothe T. [Spirometry in the Medical Practice – Part 1: Measuring]. Praxis (Bern 1994). 2021;110(11):629-36.
2. Scano G, Stendardi L, Grazzini M. Understanding dyspnoea by its language. Eur Respir J. 2005;25(2):380-5.
3. Celli BR, Cote CG, Marin JM, Casanova C, Montes de Oca M, Mendez RA, et al. The body-mass index, airflow obstruction, dyspnea, and exercise capacity index in chronic obstructive pulmonary disease. N Engl J Med. 2004;350(10):1005-12.
4. Stevens JP, Dechen T, Schwartzstein RM, O’Donnell CR, Baker K, Banzett RB. Association of dyspnoea, mortality and resource use in hospitalised patients. Eur Respir J. 2021;58(3).
5. Dyspnea. Mechanisms, assessment, and management: a consensus statement. American Thoracic Society. Am J Respir Crit Care Med. 1999;159(1):321-40.
6. Manning HL, Schwartzstein RM. Pathophysiology of dyspnea. N Engl J Med. 1995;333(23):1547-53.
7. Banzett RB, Pedersen SH, Schwartzstein RM, Lansing RW. The affective dimension of laboratory dyspnea: air hunger is more unpleasant than work/effort. Am J Respir Crit Care Med. 2008;177(12):1384-90.
8. Donahoe M, Rogers RM, Wilson DO, Pennock BE. Oxygen consumption of the respiratory muscles in normal and in malnourished patients with chronic obstructive pulmonary disease. Am Rev Respir Dis. 1989;140(2):385-91.
9. Mellemgaard K. The alveolar-arterial oxygen difference: its size and components in normal man. Acta Physiol Scand. 1966;67(1):10-20.
10. Fletcher CM, Elmes PC, Fairbairn AS, Wood CH. The significance of respiratory symptoms and the diagnosis of chronic bronchitis in a working population. Br Med J. 1959;2(5147):257-66.
11. Couturaud F, Bertoletti L, Pastre J, Roy PM, Le Mao R, Gagnadoux F, et al. Prevalence of Pulmonary Embolism Among Patients With COPD Hospitalized With Acutely Worsening Respiratory Symptoms. JAMA. 2021;325(1):59-68.
12. Graham BL, Steenbruggen I, Miller MR, Barjaktarevic IZ, Cooper BG, Hall GL, et al. Standardization of Spirometry 2019 Update. An Official American Thoracic Society and European Respiratory Society Technical Statement. Am J Respir Crit Care Med. 2019;200(8):e70-e88.
13. Quanjer PH, Stanojevic S, Cole TJ, Baur X, Hall GL, Culver BH, et al. Multi-ethnic reference values for spirometry for the 3-95-yr age range: the global lung function 2012 equations. Eur Respir J. 2012;40(6):1324-43.
14. Raghu G, Remy-Jardin M, Myers JL, Richeldi L, Ryerson CJ, Lederer DJ, et al. Diagnosis of Idiopathic Pulmonary Fibrosis. An Official ATS/ERS/JRS/ALAT Clinical Practice Guideline. Am J Respir Crit Care Med. 2018;198(5):e44-e68.
15. Lichtenstein DA. BLUE-protocol and FALLS-protocol: two applications of lung ultrasound in the critically ill. Chest. 2015;147(6):1659-70.
16. Eibenberger KL, Dock WI, Ammann ME, Dorffner R, Hormann MF, Grabenwoger F. Quantification of pleural effusions: sonography versus radiography. Radiology. 1994;191(3):681-4.
17. Funke-Chambour M, Azzola A, Adler D, Barazzone-Argiroffo C, Benden C, Boehler A, et al. Idiopathic Pulmonary Fibrosis in Switzerland: Diagnosis and Treatment. Respiration. 2017;93(5):363-78.
18. Randerath W, Verbraecken J, Andreas S, Arzt M, Bloch KE, Brack T, et al. Definition, discrimination, diagnosis and treatment of central breathing disturbances during sleep. Eur Respir J. 2017;49(1).
19. Elliott MW, Adams L, Cockcroft A, MacRae KD, Murphy K, Guz A. The language of breathlessness. Use of verbal descriptors by patients with cardiopulmonary disease. Am Rev Respir Dis. 1991;144(4):826-32.
Zusätzlich:
Global Initiative for Asthma. Global Strategy for Asthma Management and
Prevention, 2022. www.ginasthma.org
Global Strategy for the diagnosis, management, and prevention of chronic
obstructive pulmonary disease, 2022. www.goldcopd.org
Therapeutische Umschau
- Vol. 80
- Ausgabe 6
- August 2023